Микроклональное размножение Gladiolus х hybridus сорта ‘пермский сувенир’ селекции Учебного ботанического сада ПГНИУ
Автор: Шибанова Н.Л., Черткова М.А., Чемарова Т.Д.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Ботаника
Статья в выпуске: 2, 2020 года.
Бесплатный доступ
Представлены результаты микроклонального размножения нового сорта гладиолуса гибридного ‘Пермский Сувенир’. Установлено, что для стерилизации эксплантов оптимальным является следующий порядок использования стерилизующих агентов: 7%-ный раствор гипохлорита натрия с экспозицией 15 или 20-25 мин. и 96%-ный этанол с экспозицией 30 или 60 сек. соответственно для клубнепочек и клубнелуковиц. Выход стерильной культуры при этом составил более 56% для клубнелуковиц и 76% для клубнепочек. На этапе микроразмножения хорошие результаты получены при добавлении к питательной среде Мурасиге и Скуга витаминов (0.1 мг/л тиамина, 0.5 мг/л пиридоксина, 0.5 мг/л никотиновой кислоты) и р-индолилуксусной кислоты (0.1-1 мг/л). Коэффициент размножения составил для клубнепочек - 2-3; для фрагментов клубнелуковиц с апикальной или пазушной почкой - 2-4. Приживаемость растений, переведенных из условий in vitro в in vivo, составила 70%. Диаметр полученных ювенильных клубнелуковиц из культуры in vitro и количество сформированных на них клубнепочек не имели статистически значимых отличий от посаженных in vivo (t = [1.16; 1.22] 05 = 1.96).
Микроклональное размножение, клубнепочки, клубнелуковицы, Gladiolus х hybridus hort., 'Пермский Сувенир'
Короткий адрес: https://sciup.org/147229649
IDR: 147229649 | УДК: 581.143.6: | DOI: 10.17072/1994-9952-2020-2-97-102
Micropropagation of Gladiolus x hybridus hort. ‘пермский сувенир’, which was bred in Botanical garden of PSU
The article presents data on micropropagation of new Gladiolus x hybridus cultivar ‘Пермский Сувенир’. It is found that for the sterilization of corms and cormels better use the 7% sodium hypochlorite solution (15 min or 20-25 min) and then 96% ethanol (30 sec or 60 sec). Sterile culture was more than 56% for corms and 76% for cormels. At the micropropagation good results were obtained when vitamins (0.1 mg/l thiamine, 0.5 mg/l pyridoxine, 0.5 mg/l nicotinic acid) and p-indolylacetic acid (0.1-1 mg/l) were added to the Murashige and Skoog medium. The breeding rate for cormels was 2-3, for corm fragments was 2-4. The survival rate of plants transferred from in vitro to in vivo conditions was 70%. The diameter of the obtained juvenile corms from in vitro culture and the number of cormels formed on them did not have statistically significant differences from those planted in vivo (t = [1.16; 1.22] 05 = 1.96).
Текст научной статьи Микроклональное размножение Gladiolus х hybridus сорта ‘пермский сувенир’ селекции Учебного ботанического сада ПГНИУ
Одним из современных методов размножения растений является клональное микроразмножение, позволяющее круглогодично и в короткие сроки получать большое количество посадочного материала. Кроме того, метод in vitro позволяет с высокой эффективностью размножать редкие и плохо поддающиеся размножению в обычных условиях виды растений, а также единично полученные уникальные мутанты и гибридные экземпляры [Бабикова, Горпеченко, Журавлев, 2007].
Активная селекционная работа с гладиолусами ведется уже более ста лет и интерес к этим растениям неизменно растет. Появляются новые сорта, которые особенно нуждаются в массовом размножении. Методы клонального микроразмножения позволяют значительно сократить селекционный процесс [Шипунова, 2003]. Исследования последних лет направлены на изучение биологических особенностей различных типов эксплантов, оптимизацию минерального и органического состава питательных сред, повышение коэффициента размножения в культуре in vitro, получение здорового
посадочного материала [Ахмед, 2000; Мокшин, 2005; Prasad, Gupta, 2006; Осипова, 2008; Ruffoni, 2008].
Цель данной работы – оптимизация этапов микроклонального размножения новых сортов Gladiolus × hybridus селекции Учебного ботанического сада Пермского государственного национального исследовательского университета (ПГНИУ) на примере сорта ‘Пермский Сувенир’ (365-ОР-18 Черткова, Шумихин).
Материалы и методы исследований
Исследования проводились в 2018 г. в лаборатории микроклонального размножения кафедры ботаники и генетики растений и в Учебном ботаническом саду ПГНИУ. Сорт ‘Пермский сувенир’ был получен в результате скрещивания сортов ‘Si Foam’ (500-РС-80) и ‘Медовый Спас’ (327-С-97). Высота растений в период массового цветения составляет 105‒120 см, длина соцветия – 58‒61 см. Цветок светло-сиреневый с ярким желтомалиновым пятном на нижних долях околоцветника, имеет ровный с небольшими защипами край. Соцветие плотное, содержит 14‒17 цветков, из которых одновременно раскрыты 7–8. Оценка декоративных признаков составляет 97 баллов, оценка хозяйственно-ценных качеств – 44 балла [Пат. РФ …, 2018].
В качестве первичных эксплантов использованы клубнепочки и апикальные или пазушные почки клубнелуковиц. Всего было высажено 130 клубнепочек и 126 фрагментов клубнелуковиц. Стерилизацию материала проводили несколькими способами. Для клубнепочек применяли один режим стерилизации: раствор нейтрального детергента – 40 мин.; промывка проточной водой – 10
Таблица 1
Варианты питательной среды Мурасиге и Скуга для микроклонального размножения сорта гладиолуса ‘Пермский Сувенир’
|
Номер |
Витамины, мг/л |
Фитогормоны |
|
|
Ауксины, мг/л |
Цитокинины, мг/л |
||
|
1 |
+ |
ИУК – 0.5 |
– |
|
2 |
– |
– |
– |
|
3 |
0.1 – тиамин |
– |
– |
|
4 |
+ |
ИУК – 1 |
6-БАП – 0.5 |
|
5 |
+ |
НУК – 1 |
6-БАП – 2 |
|
6 |
+ |
ИУК – 0.1 |
– |
|
7 |
+ |
НУК – 1 |
6-БАП – 2 |
|
8 |
+ |
– |
– |
|
9 |
+ |
НУК – 10 |
6-БАП – 0.5 |
Примечание. + витамины по Р.Г. Бутенко 0.1 мг/л тиамин, 0.5 мг/л пиридоксин, 0.5 мг/л никотиновая кислота; прочерк означает отсутствие витаминов и/или регуляторов роста.
Клубнепочки высаживали на первые пять вариантов питательной среды MS, фрагменты клубнелуковиц – на все варианты. Клубнепочки брали самой мелкой категории (менее 4 мм), не рекомендуемые для посадки в открытый грунт [Громов, мин.; 7%-ный раствор гипохлорита натрия – 15 мин., 96%-ный этанол – 30 сек., с последующей промывкой в трех порциях стерилизованной дистиллированной воды по 5 мин. в каждой.
Для клубнелуковиц применяли 4 режима стерилизации, отличающиеся по времени нахождения в нейтральном детергенте и стерилизующем агенте, особенностям выделения почек. Стерилизация клубнепочек и I режим стерилизации клубнелуковиц были аналогичными. II и III режимы стерилизации: раствор нейтрального детергента – 50 мин.; промывка проточной водой – 15 мин.; 7%-ный раствор гипохлорита натрия – 20 мин., 96%-ный этанол – 60 сек.; IV режим стерилизации: раствор нейтрального детергента – 60 мин.; промывка проточной водой – 15 мин.; 7%-ный раствор гипохлорита натрия – 25 мин., 96%-ный этанол – 60 сек. Разделение клубнелуковиц на фрагменты и вычленение почек при I и II режимах проводили после стерилизации, при III и IV – до стерилизации.
Простерилизованный материал и экспланты, полученные при последующих пассажах, высаживали в пробирки на наиболее часто используемую для культуры растительных тканей твердую питательную среду с минеральной основой по Т. Murashige и F. Skoog (MS) [1962], 3%-ной сахарозой, 0.7%-ным агар-агаром. Исследовали влияние на культуру гладиолуса витаминов по Р.Г. Бутенко [1964], а также регуляторов роста: β-индолилуксусной кислоты (ИУК) в концентрациях 0.1; 0.5; 1 мг/л; α-нафтилуксусной кислоты (НУК) в концентрациях 1 и 10 мг/л; 6-бензиламинопурина (6-БАП) в концентрациях 0.5 и 2 мг/л. Всего использовано 9 вариантов среды с разным соотношением витаминов и фитогормонов (табл. 1).
Ардабьевская, 2002].
Питательную среду стерилизовали паром при температуре +120°С под давлением 1.1 атм. в течение 15 мин. Стерилизацию культуральных сосудов, инструментов и оборудования осуществляли согласно общепринятым методикам [Бутенко, 1964]. Процесс высадки эксплантов на питательную среду производили в ламинар-боксе в соответствии с правилами работы со стерильным материалом. Экспланты содержали в климатической камере Binder KBF LQC 240 с фотопериодом 14/10, при температуре +20±2°С.
Через 10‒14 дней после очередного пассажа выбраковывали материал, имевший признаки инфицирования. Одновременно вычисляли отношение числа стерильных объектов к общему числу эксплантов, подвергнутых стерилизации. Жизнеспособность стерильного материала определяли в процентах как число стерильных объектов с признаками регенерации. Часть растений, полученных в культуре in vitro , переносили в Учебный ботанический сад ПГНИУ, где выращивали в условиях открытого грунта. Почва экспериментального участка имеет искусственное происхождение, темно-гумусовая, влагоемкая, хорошо структурированная. Агрофон участка является выровненным. Реакция рН приближается к нейтральной (6.6‒7.2). Содержание органических веществ высокое (17.2– 23.8 мг на 100 г почвы).
Статистическую обработку результатов проводили с использованием стандартного пакета анализа Statistica 5.5. Для сравнения средних значений количественных признаков применяли t-критерий Стьюдента, для сравнения качественных показателей – критерий χ2.
Результаты и их обсуждение
Микроклональное размножение гладиолусов проводится в три этапа, выделение которых является общепринятым [Высоцкий, 1986]. Первый этап включал стерилизацию эксплантов и их посадку на твердую питательную среду MS. В дальнейшем проводилось микроразмножение. Заклю- чительный этап состоял в укоренении растений in vitro и перевод их in vivo.
Определяющую роль на первом этапе микро-клонального размножения играет стерильность культуры, которая для клубнепочек при выбранном режиме была 76.92%. В исследовании Н.Л. Шибановой, М.А. Чертковой, Т.В. Мельниковой [2017] по микроклональному размножению некоторых сортов гладиолуса гибридного клубне-почками с применением аналогичного режима стерилизации, выход стерильной культуры составил более 87%. Клубнелуковицы по-разному реагировали на стерилизацию. Наименьший процент стерильной культуры наблюдался при применении I режима (17.14%), а наибольший – при III (81.25%). II и IV режимы показали средние результаты (68.75 и 56.25% соответственно).
В результате анализа данных по выходу стерильной культуры можно сделать заключение, что клубнелуковицы и клубнепочки сорта ‘Пермский Сувенир’ по-разному реагируют на выбранный режим стерилизации. Стерильность культуры при использовании одинакового способа стерилизации для клубнепочек и клубнелуковиц (I режим) достоверно выше для первого типа экспланта (χ2 = 69.91, р<0.001). Выход стерильной культуры клубнелуковиц после применения I режима стерилизации достоверно ниже, чем при других способах (χ2 = [14.02; 42.71], р<0.001). Разница между II, III, IV режимами стерилизации клубнелуковиц и режимом стерилизации клубнепочек оказалась недостоверной (χ2 = [0.28; 3.38], р>0.001).
Развитие эксплантов начинается через 7 дней после посадки на твердую питательную среду MS, что представлено на рисунке. Результаты по развитию апикальных и пазушных почек клубнелуковиц гладиолуса на твердой питательной среде MS представлены в табл. 2.
Клубнепочки

а б
Клубнелуковицы
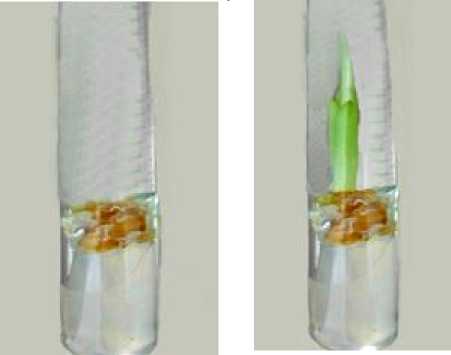
б
Развитие клубнепочек и клубнелуковиц гладиолуса на питательной среде MS: а – на момент посадки, б – через 21 день после посадки
Таблица 2
Развитие почек клубнелуковиц сорта ‘Пермский Сувенир’ на твердой питательной среде Мурасиге и Скуга
|
№ варианта среды |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
|
Выживаемость, % |
66.67 |
50.00 |
0.00 |
100.00 |
0.00 |
81.82 |
16.67 |
33.33 |
21.43 |
|
Коэффициент размножения, M±m |
3.00±0.00 |
3.00±0.00 |
- |
2.00±0.71 |
- |
2.00±0.35 |
3.00±1.00 |
1.50±0.50 |
2.00±0.47 |
Примечания: 1 - с витаминами и ИУК (0.5 мг/л), 2 - без витаминов и фитогормонов, 3 - с тиамином (0.1 мг/л), без фитогормонов, 4 - витаминами, 6-БАП (0.5 мг/л) и ИУК (1 мг/л), 5 - с витаминами, 6-БАП (2 мг/л) и НУК (1 мг/л), 6 - с витаминами, ИУК (0.1 мг/л), 7 - с витаминами, 6-БАП (2 мг/л) и НУК (1 мг/л), 8 - с витаминами, без фитогормонов, 9 - с витаминами, 6-БАП (0.5 мг/л) и НУК (10 мг/л).
Анализ данных по развитию апикальных и пазушных почек клубнелуковиц на твердой питательной среде MS показал, что состав среды влияет на выживаемость эксплантов. Установлена достоверная разница между выходом жизнеспособного материала и составом среды. По критерию х2 экспланты на 4 и 6 вариантах среды были более жизнеспособны, чем на 7, 8 и 9 (х2 = [4.00; 9.76], р<0.05). Между 1-, 2-, 4- и 6-й средами достоверной разницы не обнаружено (х2 = [0.32; 1.88], р>0.05), так же как между 7-, 8- и 9-м вариантами среды (х2 = [0.32; 1.88], р>0.05). Возможно, это связано с тем, что в 1-, 4- и 6-м вариантах пита тельной среды из фитогормонов применили ИУК, более естественный для растений, чем НУК. Между формированием побегов на всех использованных питательных средах статистически достоверной разницы не наблюдалось (t = [0.00; 1.34] Результаты по развитию эксплантов клубнепо-чек гладиолуса на твердой питательной среде MS представлены в табл. 3. Таблица 3 Развитие эксплантов клубнепочек сорта ‘Пермский Сувенир’ на твердой питательной среде Мурасиге и Скуга № варианта среды 1 2 3 4 5 Выживаемость, % 92.31 95.65 100.00 95.24 82.35 Количество побегов, M±m 2.04±0.07 1.09±0.06 1.00±0.00 1.00±0.00 1.86±0.18 Количество корней, M±m 3.25±0.35 2.91±0.21 3.29±0.26 1.80±0.35 2.57±0.21 Примечания: 1 - с витаминами и ИУК (0.5 мг/л), 2 - без витаминов и фитогормонов, 3 - с тиамином (0.1 мг/л), без фитогормонов, 4 - с витаминами, 6-БАП (0.5 мг/л) и ИУК (1 мг/л), 5 - с витаминами, 6-БАП (2 мг/л) и НУК (1 мг/л). Анализ данных по развитию клубнепочек гладиолуса на твердой питательной среде MS показал, что состав среды не влияет на выживаемость эксплантов. Статистически достоверной разницы между выходом жизнеспособного материала и составом среды по критерию х2 не выявлено (х2 = [0.01; 3.29], р>0.05). Возможно, это связано с изначальным выбором типа экспланта - клубнепоч-кой, которая в своем составе содержит все вещества, необходимые для прорастания. Однако количество побегов, образовавшихся на клубнепочках на 1 варианте среды, было достоверно больше, чем на других вариантах (t = [4.68; 186.27] >t05 = 1.96). По количеству корней, образовавшихся на клубне-почках, наблюдается похожая картина (t = [2.00; 13.94] >t05 = 1.96), только с 3-м вариантом среды нет достоверной разницы (t = 0.23 В мае-июне 2018 г. 75 растений, выращенных in vitro, и 100 клубнепочек, рекомендуемых для посадки размером более 4 мм, полученных in vivo, были перенесены в условия открытого грунта Учебного ботанического сада ПГНИУ. Приживаемость растений из культуры in vitro в условиях открытого грунта составила 70%, «всхожесть» клубнепочек in vivo - 90%. В конце вегетационного периода 2018 г. был определен диаметр ювенильных клубнелуковиц, который для растений из культуры in vitro составил 2.26±0.38 см и незначительно уступал клубнепочкам, посаженным in vivo - 2.44±0.08 см. Разница по этому показателю оказалась статистически незначимой (t = 1.22 Среднее количество образовавшихся клубнепо-чек на одно растение, полученное в культуре in vitro, составило 5.25±1.77, что согласуется с литературными данными [Калинин, Кушнир, Сарнац- кая, 1992], в которых отмечается, что растения, перенесенные с корнями из пробирок в открытый грунт, через 4‒6 месяцев формировали клубнелуковицы с клубнепочками. У растений in vivo образовалось 9.22±0.56 клубнепочек на клубнелуковицу. Однако достоверной разницы между ними не обнаружено (t = 1.16 Заключение В качестве первичных эксплантов рекомендуется использовать как клубнепочки, так и фрагменты клубнелуковиц, содержащие апикальные и пазушные почки. Для получения хорошо растущей стерильной культуры клубнелуковиц необходимо увеличить время нахождения в нейтральном детергенте с 40 до 50 мин. и в стерилизующем агенте ‒ с 15 до 20 мин. (7%-ный раствор гипохлорита натрия) и с 30 до 60 сек. (96%-ный этанол). Для изученных эксплантов на этапе микроразмножения рекомендуется использовать вариант твердой питательной среды MS с добавлением ИУК в концентрации 0.1–1 мг/л и витаминов – 0.1 мг/л тиамин, 0.5 мг/л пиридоксин, 0.5 мг/л никотиновая кислота. Выход адаптированных растений к условиям открытого грунта составляет 70%.
Список литературы Микроклональное размножение Gladiolus х hybridus сорта ‘пермский сувенир’ селекции Учебного ботанического сада ПГНИУ
- Ахмед А.К. Создание высокоэффективной системы микроклонального размножения генетически стабильных растений гладиолуса: автореф. дис. ... канд. биол. наук. М., 2000. 16 с.
- Бабикова А.В., Горпеченко Т.Ю., Журавлев Ю.Н. Растение как объект биотехнологий // Комаров-ские чтения. 2007. Вып. 4. С. 184-211.
- Бутенко Р.Г. Культура изолированных тканей и физиология морфогенеза растений. М., 1964. 272 с.
- Высоцкий В.А. Клональное микроразмножение растений // Культура клеток растений и биотехнология. М., 1986. С. 91-102.
- Громов А.Н., Ардабьевская Т.В. Гладиолусы. М.: ОЛМА-ПРЕСС Звездный мир, 2002. 176 с.
- Калинин Ф.Л., Кушнир Г.П., Сарнацкая В.В. Технология микроклонального размножения растений. Киев, 1992. 232 с.
- Мокшин Е.В. Морфо-физиологические особенности клонального микроразмножения in vitro различных сортов лилий и гладиолусов: автореф. дис. ... канд. биол. наук. Саранск, 2005. 20 с.
- Осипова Е.Ю. Технология размножения гладиолуса in vitro // Генетика, селекция и биотехнология: 61-я студ. науч. конф. / РГАУ-МСХА им. К. А. Тимирязева. М., 2008. С. 54-55. Пат. РФ № 9425. Селекционное достижение Гладиолус (Gladiolus L.) ПЕРМСКИЙ СУВЕНИР, 2018.
- Шибанова Н.Л., Черткова М.А., Мельникова Т.В. Использование клубнепочек в качестве первичных эксплантов при микроклональном размножении видов рода Gladiolus L. // Пермский аграрный вестник, 2017. №1 (17). С. 98-103.
- Шипунова А.А. Клональное микроразмножение садовых растений: автореф. дис. ... канд. с-х. наук. М., 2003. 24 с.
- Murashige T., Skoog F. A revised medium for rapid growth and bio assays with tobacco tissued cultures // Physiol. plant. 1962. Vol. 15. P. 473-497.
- Prasad V.S.S., Dutta Gupta S. In vitro shoot regeneration of gladiolus in semi-solid agar versus liquid cultures with support systems // Plant Cell Tiss Organ Cult. 2006. № 87. Р. 263-271.
- Ruffoni B. et al. Gladiolus micropropagation in temporary immersion system // Propagation of Ornamental Plants, 2008. Vol. 8, № 2. Р. 102-104.


