Минеральный обмен и микробное разнообразие слепого отдела кишечника у цыплят-бройлеров (Gallus gallus L.) при включении в полусинтетический рацион пищевых волокон
Автор: Кван О.В., Сизова Е.А., Вершинина И.А., Камирова А.М.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Метаболизм, микробиота, кормление
Статья в выпуске: 4 т.58, 2023 года.
Бесплатный доступ
Кормовые добавки могут изменять минеральный статус сельскохозяйственной птицы. Например, пищевые волокна долгое время относили к антипитательным факторам, так как считалось, что они снижают усвояемость питательных веществ и неблагоприятно сказываются на потреблении корма. Однако позднее было доказано положительное влияние пищевых волокон на переваривание корма, ферментацию и процессы всасывания у домашней птицы. В настоящей работе впервые продемонстрировано снижение накопления токсичных микроэлементов и изменение в микробном сообществе слепого отдела кишечника у цыплят-бройлеров при добавлении в корм микрокристаллической целлюлозы, лактулозы и хитозана. Цель исследования - изучить влияние пищевых волокон на минеральный обмен и микробиоценоз слепого отдела кишечника у цыплят-бройлеров, содержащихся на полусинтетической диете. Эксперименты на цыплятах-бройлерах (Gallus gallus L.) кросса Arbor Acres были проведены в условиях вивария ФНЦ БСТ РАН. Отобрали 150 цыплят-бройлеров в возрасте 1 нед, которых разделили на 5 групп ( n = 30) методом пар-аналогов. Продолжительность эксперимента составила 35 сут, подготовительного и учетного периодов - соответственно 7 и 28 сут. В течение учетного периода первая контрольная группа (К1) находилась на полусинтетическом рационе (ПР), вторая контрольная (К2) - на ПР, дефицитном по микроэлементам (ПДР), I опытная группа получала ПДР c дополнительным введением микрокристаллической целлюлозы (Е460) в дозе 0,25 г/кг корма, II опытная - ПДР с лактулозой в дозе 1 г/кг корма, III опытная - ПДР с пищевым хитозаном в дозе 0,5 г/кг корма. Анализ элементного состава кормов и биосубстратов бройлеров включал определение 25 химических элементов: Ca, Cu, Fe, Li, Mg, Mn, Ni, As, Cr, K, Na, P, Zn, I, V, Co, Se, Ti, Al, Be, Cd, Pb, Hg, Sn, Sr. Исследование элементного состава кормов и биоматериалов проводили атомно-эмиссионным и масс-спектральным методами. Микробное биоразнообразие слепого отдела кишечника птицы оценивали на 42-е сут. NGS-секвенирование выполняли на платформе MiSeq («Illumina, Inc.», США). Включение пищевых волокон в состав полусинтетических рационов привело в I опытной группе к статистически значимому увеличению содержания кальция на 23,4 % (р ≤ 0,05) относительно К2, в III опытной группе - к снижению показателя в 1,50 раза (р ≤ 0,05) в сравнении с К1 и на 26,3 % (р ≤ 0,05) относительно К2. Введение хитозана в полусинтетический рацион, дефицитный по микроэлементам, способствовало увеличению содержания лития в 1,70 раза (р ≤ 0,05) относительно К1. Концентрация марганца и кобальта достоверно (р ≤ 0,05) снижалась во всех опытных группах относительно К1. В I группе наблюдали повышение количества селена в 2,35 раза (р ≤ 0,05) в сравнении с К1, а также его снижение (р ≤ 0,05) в 1,74 раза по сравнению с К2. В этой же группе выявили увеличение количества йода в 1,74 и 1,50 раза (р ≤ 0,05) относительно обеих контрольных групп. Во II и III опытных группах мы отмечали снижение накопления селена в 4,64 и 4,55 раза (р ≤ 0,05) по сравнению с К2. Концентрация мышьяка во II группе превысила К1 в 1,63 раза (р ≤ 0,05), а в III группе его концентрация, напротив, снизилась в 1,58 и 2,00 раза (р ≤ 0,05) по отношению к К1 и К2. Добавление пищевых волокон способствовало активному выведению токсичных элементов. Содержание стронция в I и в III опытных группах снизилось соответственно на 25,7 и 45,9 % (р ≤ 0,05) относительно К1 и на 22,2 и 43,4 % (р ≤ 0,05) по сравнению с К2. Выполненное нами определение микробного профиля содержимого слепой кишки бройлеров показало, что в I группе численность Rikenellaceae увеличилась в 6,3 и 6,8 раза, Lachnospiraceae - в 12,0 и 4,9 раза, Ruminococcaceae - в 2,1 раза и 3,9 раза по сравнению соответственно с К1 и К2. Во II группе отмечали снижение содержания Lactobicallaceae в 6 раз, численность Rikenellaceae увеличилась в 6,20 раза, Lachnospiraceae - в 9,57 раза, Ruminococcaceae - в 3,10 раза относительно К1. В III группе произошло снижение содержания Lactobicallaceae в 13,30 и 1,55 раза по сравнению с К1 и К2. Численность Rikenellaceae увеличилась в 5,5 раза, Lachnospiraceae - в 11,8 раза, Ruminococcaceae - в 3,5 раза по сравнению с К1. Таким образом, введение пищевых волокон в полусинтетический рацион цыплят-бройлеров кросса Arbor Acres приводило к снижению содержания макроэлементов в организме, элиминации токсичных элементов, увеличению численности таксонов Rikenellaceae и Lachnospiraceae с одновременным снижением численности Lactobacillaceae в кишечнике.
Полусинтетическая диета, пищевые волокна, обмен веществ, минеральный обмен, микробиом, слепой отдел кишечника
Короткий адрес: https://sciup.org/142239846
IDR: 142239846 | УДК: 636.5.033:636.084:579 | DOI: 10.15389/agrobiology.2023.4.700rus
Effects of dietary fiber on mineral metabolism and caecal microbial diversity in broiler chickens (Gallus gallus L.) fed a semi-synthetic diet
Various additives used in poultry diets can change the mineral status of the body. Dietary fiber has long been considered an anti-nutritional factor due to adverse effects on feed intake and nutrient absorption. However, with increasing evidence, it has been found that dietary fiber has a positive effect on nutrient digestion, fermentation, and absorption processes in poultry. In this work, for the first time, data were obtained on the influence of dietary fibers, the microcrystalline cellulose, lactulose and chitosan on mineral metabolism and caecal microbiocenosis of broiler chickens fed a semi-synthetic diet. A decrease in the accuulation of toxic microelements in the body of a bird was demonstrated, as well as a change in the microbial community of the caecum. Experiments on the Arbor Acres cross broiler chickens (Gallus gallus L.) were carried out in the vivarium (the FSC BSA RAS). A total of 150 of week-old broiler chickens were divided into 5 groups of analogues (n = 30 each). The duration of the experiment was 35 days. The first control group C1 was fed with a semi-synthetic diet (SS). The second control group C2 received a semi-synthetic diet deficient in trace elements (DSS). For dietary fibers, test group I was fed with dietary microcrystalline cellulose (E460, 0.25 g/kg feed), test group II with dietary lactulose (1 g/kg feed), and test group III with dietary chitosan (0.5 g/kg feed). In feed and biomaterial of broilers, 25 chemical elements were assayed: Ca, Cu, Fe, Li, Mg, Mn, Ni, As, Cr, K, Na, P, Zn, I, V, Co, Se, Ti, Al, Be, Cd, Pb, Hg, Sn, Sr by atomic emission spectrometry and mass spectrometry techniques. Microbial biodiversity of the caecum was assessed on day 42. NGS sequencing was performed using a MiSeq platform (Illumina, Inc., USA). In test group I, the dietary fiber led to a statistically significant increase in the calcium (by 23,4 %. p ≤ 0.05) vs. C2. In test group III, there was a 1.5-forl decrease in the indicator (p ≤ 0.05) vs. C1 and a 26.3 % decrease (p ≤ 0.05) vs. C2. The lithium content increased 1.7 times (p ≤ 0.05) vs. C1 when chitosan was added to a semi-synthetic diet deficient in trace elements. The concentration of manganese and cobalt significantly (p ≤ 0.05) decreased in all test groups vs. C1. In group I, the amount of selenium increased 2.35 times (p ≤ 0.05) vs. C1 it decreased 1.74 times (p ≤ 0.05) vs, C2. In the same group, the iodine level increased 1.74 times and 1.5 times (p ≤ 0.05) vs. control groups. In test groups II and III, selenium decrease 4.64 times and 4.55 times (p ≤ 0.05) vs. C2. The concentration of arsenic in group II exceeded C1 1.63 times (p ≤ 0.05), and in group III, its concentration, on the contrary, decreased 1.58 times and 2.0 times (p ≤ 0.05) vs. C1 and C2. The dietary fiber scontributed to the removal of toxic elements. In test group I and group III, the concetration of strontium decreased (p ≤ 0.05) by 25.7 and 45.9 %, respectively, vs. C1. For C2, a decrease in the amount of strontium by 22.2 and 43.4 % was similarly revealed (p ≤ 0.05). In group I, the counts of Rikenellaceae increased 6.3 and 6.8 times, Lachnospiraceae 12 and 4.9 times, Ruminococcaceae 2.1 times and 3. 9 times compared to C1 and C2, respectively. In group II, the abundance of Lactobicallaceae decreased 6 times, the number of Rikenellaceae increased 6.2 times, Lachnospiraceae 9.57 times, Ruminococcaceae 3.1 times compared to C1. In group III, there was a decrease in the content of Lactobicallaceae by 13.3 and 1.55 times compared to C1 and C2. The number of Rikenellaceae increased 5.5 times, Lachnospiraceae 11.8 times, Ruminococcaceae 3.5 times compared to C1. Thus, dietary fibers added to a semi-synthetic diet led to a decrease in the content of macroelements in the body of Arbor Aikres cross broiler chickens, the elimination of toxic elements, and increased the counts of Rikenellaceae and Lachnospiraceae taxa with a simultaneous decrease in the number of Lactobacillaceae in the intestine.
Текст научной статьи Минеральный обмен и микробное разнообразие слепого отдела кишечника у цыплят-бройлеров (Gallus gallus L.) при включении в полусинтетический рацион пищевых волокон
За несколько последних десятилетий концепции кормления сельскохозяйственной птицы претерпели существенные изменения, что обусловлено переходом от домашнего хозяйства к промышленному производству рационов (1). Это стало возможным благодаря определению потребности животных в питательных веществах и установления метаболической роли последних.
С 1950-х годов проводятся многочисленные эксперименты по выяснению потребностей птицы в белках и незаменимых аминокислотах (2, 3) и идеального соотношения белков в рационах (4). В настоящее время, когда доступны пять синтезированных незаменимых аминокислот, можно создать сбалансированный полусинтетический рацион, в котором содержание сырого протеина будет определяться наиболее ограничивающей аминокислотой, поступающей из кормовых белков (5). Кроме того, применение полу-синтетического рациона, возможно, станет одним из приемов, обеспечивающих сбалансированное кормление за счет компенсации дефицита по некоторым питательным веществам (6). Использование полусинтетического рациона позволит более полно оценить влияние кормовых добавок или других составляющих рациона на минеральный обмен и микробное разнообразие кишечника птицы, а также будет полезно при изучении генетических и экологических вариаций в популяции.
При составлении полусинтетических рационов необходимо учитывать, что микроэлементный статус организма определяется экзогенным поступлением микроэлементов с пищей в процессе нормализации внутрики-шечного состава химуса (7). В результате этого, а также вследствие стремления организма к постоянству внутренней среды изменяются процессы всасывания, что приводит либо к нормализации содержание тех или иных элементов, либо к микроэлементному дефициту (8). В свою очередь, интенсивность всасывания зависит от множества условий, среди которых важное место занимает нормальное функционирование кишечной микрофлоры, способной модифицировать биодоступность микроэлементов через их аккумуляцию внутри микробных клеток и изменение значений внутрикишеч-ного рН (9).
Различные добавки, применяемые в рационах сельскохозяйственной птицы, могут изменять минеральный статус организма. Например, пищевые волокна долгое время считались антипитательным фактором из-за их неблагоприятного воздействия на потребление корма и усвояемость питательных веществ. Однако впоследствии ученые обнаружили, что пищевые волокна оказывает положительное влияние на переваривание питательных веществ, ферментацию и процессы всасывания у домашней птицы (10). Включение клетчатки в умеренном количестве в рационы также изменяет показатели роста и улучшает здоровье кишечника, модулируя полезную микробиоту в толстой кишке и усиливая иммунные функции (11).
В настоящей работе при введении микрокристаллической целлюлозы, лактулозы и хитозана в рацион цыплят-бройлеров, содержащихся на полусинтетической диете, впервые продемонстрировано снижение содержание токсичных микроэлементов у птицы, а также изменение в микробном сообщество слепого отдела кишечника.
Цель исследования — изучить влияние пищевых волокон на минеральный обмен и микробиоценоз слепого отдела кишечника у цыплят-бройлеров, содержащихся на полусинтетической диете.
Методика. Эксперименты на цыплятах-бройлерах (Gallus gallus L.) кросса Arbor Acres проводили в условиях экспериментально-биологической клиники (вивария) ФНЦ БСТ РАН . Методом пар аналогов отобрали 150 цыплят-бройлеров в возрасте 1 нед, которых разделили на 5 групп (по n = 30).
Во время эксперимента вся птица находилась в одинаковых условиях содержания. Обслуживание животных и экспериментальные исследования выполняли в соответствии с инструкциями и рекомендациями Russian Regulations, 1987 (Order No. 755 on 12.08.1977 the USSR Ministry of Health) и The Guide for the Care and Use of Laboratory Animals (National Academy Press, Washington, D.C., 1996). При проведении исследований были предприняты усилия, чтобы свести к минимуму страдания животных и уменьшить количество используемых образцов (Протокол ¹ 1 от 21.05.2021 года).
Продолжительность эксперимента составила 35 сут, подготовительного и учетного периодов — соответственно 7 и 28 сут. В течение учетного периода первая контрольная группа (К 1 ) находилась на полусинтетическом рационе (ПР), вторая контрольная (К 2 ) — на ПР, дефицитном по микроэлементам (ПДР), I опытная группа получала ПДР c дополнительным введением микрокристаллической целлюлозы (Е460) в дозе 0,25 г/кг корма, II опытная — ПДР с лактулозой в дозе 1 г/кг корма, III опытная — ПДР с пищевым хитозаном в дозе 0,5 г/кг корма. Цыплят поили дистиллированной водой без ограничения. Использовали полусинтетический рацион, рекомендованный M.L. Scott с соавт. (12) (К 1 ) и полусинтетический рацион, дефицитный по микроэлементам, в нашей модификации (К 2 ). Образцы готовили ступенчатым смешиванием.
Птицу декапитировали под нембуталовым эфиром на 42-е сут. Тушки цыплят-бройлеров измельчали целиком, после чего отбирали среднюю пробу и проводили ее элементный анализ.
Элементный анализ включал определение 25 химических элементов: Ca, Cu, Fe, Li, Mg, Mn, Ni, As, Cr, K, Na, P, Zn, I, V, Co, Se, Ti, Al, Be, Cd, Pb, Hg, Sn, Sr. Исследование элементного состава проводили атомно-эмиссионным и масс-спектральным методами. Озоление биоматериала проводили в микроволновой системе разложения MD-2000 («PerkinElmer, Inc.», США). Содержание элементов в золе определяли на масс-спектрометре Elan 9000 («PerkinElmer, Inc.», США) и атомно-эмиссионном спектрометре Optima 2000 V («PerkinElmer, Inc.», США).
Микробное биоразнообразие слепого отдела кишечника птицы оценивали на 42-е сут (работы проводили на базе Института клеточного и внутриклеточного симбиоза УрО РАН, г. Оренбург; цкп/). При выделении ДНК пробы инкубировали при 37 °С в течение 30 мин в 300 мкл стерильного буфера для лизиса (20 мM EDTA, 1400 мM NaCl, 100 мM Tris-HCl, pH 7,5; 50 мкл раствора лизоцима в концентрации 100 мг/мл). Чистоту полученных препаратов ДНК проверяли электрофорезом в 1,5 % агарозном геле с фотометрией (NanoDrop 8000, «Thermo Fisher Scientific, Inc.», США). Концентрацию ДНК измеряли флуориметрическим методом (прибор Qubit 2.0 с высокой чувствительностью определения dsDNA, «Life Technologies», США).
ДНК-библиотеки для секвенирования были созданы по протоколу «Illumina, Inc.» (США) с праймерами S-D-Bact-0341-b-S-17 и S-D-Bact-0785-a-A-21 к вариабельному участку V3-V4 гена 16S рРНК (24). NGS-секвенирование выполняли на платформе MiSeq («Illumina, Inc.», США) с набором реактивов MiSeq Reagent Kit V3 PE600 («Illumina, Inc.», США) в Центре коллективного пользования научным оборудованием «Персистенция микроорганизмов» (Институт клеточного и внутриклеточного симбиоза УрО РАН, г. Оренбург). Полученные операционные таксономические единицы (ОТЕ) классифицировали с использованием интерактивного инструмента VAMPS и базы данных RDP . Некоторые ОТЕ выравнивали, используя алгоритм BLAST , базы данных нуклеотидных последовательностей nr/nt (National Center for Biotechnological Information, NCBI, и выравненных последовательностей генов рибосомальной РНК SILVA .
Статистическую обработку данных проводили в программе Statis-tica 10.0 («StatSoft, Inc.», США). Результаты представлены в виде средних арифметических значений (M) и стандартных ошибок среднего (±SEM). Различия считали статистически значимыми при р ≤ 0,05 (t-критерий Стьюдента). При биоинформатической обработке результатов секвенирования применяли комплекс программ USEARCH v8.0.1623_win32 . Обработка включала слияние парных ридов в операционных таксономических единицах, фильтрацию ридов по качеству и длине (минимальный размер — 300 п.н.), удаление химер, даблтонов и синглтонов, кластеризацию ридов в ОТЕ на уровне сходства 97 % (26).
Результаты. Состав рационов, которые использовали для кормления цыплят-бройлеров, представлен в таблице 1.
1. Состав (г/100 г корма) полусинтетического рациона (ПР) и дефицитного по микроэлементам полусинтетического рациона (ПДР) цыплят-бройлеров ( Gallus gallus L.) кросса Arbor Acres (виварий ФНЦ биологических систем и агротехнологий РАН)
|
Ингредиент |
1 ПР 1 |
ПДР |
|
Казеин |
20 |
20 |
|
Желатин |
5 |
5 |
|
Целлюлоза |
3 |
3 |
|
Растительное масло |
3 |
3 |
|
Холин-хлорид |
0,2 |
0,2 |
|
Глюкоза |
1,25 |
1,25 |
|
Рис |
61,38 |
61,38 |
|
Метионин |
0,1 |
0,1 |
|
Цистин |
0,2 |
0,2 |
|
CaHPO 4 •H 2 O |
1,8 |
1,8 |
|
CaCO 3 |
1,45 |
1,45 |
|
KH 2 PO 4 |
1,013 |
1,013 |
|
KCl |
0,21 |
0,21 |
|
Na 2 CO 3 |
0,555 |
0,555 |
|
MnCl•4H 2 O |
0,04 |
- |
|
FeSO 4 •7H 2 O |
0,05 |
- |
|
MgSO 4 •7H 2 O |
0,615 |
0,615 |
|
KJ |
0,001 |
0,001 |
|
CuSO 4 •5H 2 O |
0,001 |
- |
|
ZnCl 2 |
0,016 |
- |
|
CoCl 2 |
0,0002 |
- |
|
NaMoO 4 •2H 2 O |
0,0008 |
- |
|
Na 2 SeO 3 |
0,000015 |
- |
|
Витаминная смесь |
0,052 |
0,052 |
|
Примечани е. Состав витаминной смеси (мг/100 г корма): B 1 — 2,5, B 2 |
— 1,5, B 6 — 0,6, B 12 — 0,002, |
|
|
Са-пантотенат — 2,0, биотин — |
0,06, фолиевая кислота — 0,4, К 3 — 0,5, С — |
25,0, РР — 15,0, А — 1000 ИЕ, |
|
D 3 — 360 ИЕ, Е — 0,5 ИЕ. Прочерки означают, что ингредиент отсутствовал в составе рациона. |
||
При выявлении химических веществ в биологических субстратах прежде всего было необходимо изучить их накопление в теле цыплят, чтобы сделать выводы о кумуляции макро- и микроэлементов.
Включение в рацион цыплят-бройлеров пищевых волокон привело к статистически значимому увеличению содержания кальция в I опытной группе на 23,4 % (р ≤ 0,05) относительно К 2 . В III группе, напротив, мы отмечали его снижение в 1,5 раза (р ≤ 0,05) по сравнению с К 1 и на 26,3 %
(р ≤ 0,05) относительно К 2 . В целом следует отметить тенденцию к снижению содержания всех макроэлементов в группе, дополнительно получавшей хитозан, в том числе статистически значимое снижение количества фосфора на 17,5 % (р ≤ 0,05) по отношению к К 1 (табл. 2).
2. Содержание (г/гол.) макроэлементов, эссенциальных, условно-эссенциальных микроэлементов и токсичных элементов в теле цыплят-бройлеров ( Gallus gallus L.) кросса Arbor Acres, получавших полусинтетический рацион с добавлением различных пищевых волокон ( n = 30, M ±SEM; виварий ФНЦ биологических систем и агротехнологий РА)
|
Элемент |
Группа |
||||
|
К 1 |
К 2 1 |
I опытная |
II опытная |
III опытная |
|
|
Макроэл |
ементы |
||||
|
Na |
12,9±1,03 |
12,7±1,01 |
13,4±1,21 |
13,3±1,23 |
11,7±1,07 |
|
P |
63,3±3,12 |
60,6±2,86 |
69,6±3,21 |
68,5±3,68 |
52,2±2,69a |
|
K |
35,2±1,89 |
35,8±2,11 |
35,3±1,58 |
35,3±2,11 |
32,8±3,11 |
|
Ca |
91,9±5,42 |
80,7±2,31 |
99,6±3,14b |
89,3±2,89 |
59,5±3,11ab |
|
Mg |
4,1±0,65 |
3,9±0,72 |
4,1±0,81 |
4,3±0,78 |
3,6±0,98 |
|
Микроэл |
ементы |
||||
|
Li |
0,2±0,02 |
0,2±0,01 |
0,2±0,03 |
0,1±0,02 |
0,3±0,01a |
|
B |
0,9±0,03 |
1,3±0,04 |
1,1±0,02 |
0,9±0,01 |
0,4±0,03ab |
|
Si |
488,3±23,12 |
458,9±31,83 |
454,1±34,17 |
545,8±24,61 |
398,6±31,64 |
|
V |
0,7±0,03 |
0,7±0,04 |
0,7±0,02 |
0,9±0,02 |
0,5±0,03 |
|
Cr |
4,4±1,11 |
4,4±1,09 |
4,6±1,23 |
6,0±2,11 |
5,3±3,12 |
|
Mn |
16,9±1,32 |
8,8±2,11 |
9,1±2,36a |
11,2±3,12a |
9,5±4,17a |
|
Fe |
916,6±30,10 |
883,4±29,86 |
960,5±35,44 |
956,2±41,2 |
852,6±34,97 |
|
Co |
4,1±1,45 |
0,4±0,02 |
0,5±0,03a |
0,3±0,03a |
0,2±0,04a |
|
Ni |
6,1±1,21 |
5,6±1,45 |
5,2±1,24 |
4,5±2,11 |
5,1±2,45 |
|
Cu |
24,6±2,36 |
21,5±2,45 |
20,5±3,11 |
29,2±2,58 |
17,8±3,12 |
|
Zn |
383,4±25,64 |
339,9±18,95 |
376,7±21,37 |
377,5±31,20 |
283,6±29,34 |
|
As |
0,19±0,00 |
0,24±0,001 |
0,20±0,001 |
0,31±0,002a |
0,12±0,001ab |
|
Se |
4,7±1,24 |
19,5±2,36 |
11,2±3,12ab |
4,2±2,86b |
4,3±3,14b |
|
I |
3,3±1,32 |
3,9±1,45 |
5,8±2,11ab |
4,7±3,11 |
3,7±2,87 |
|
Токсичные |
элементы |
||||
|
Sr |
29,2±1,31 |
27,9±1,87 |
21,7±2,23ab |
23,9±3,11 |
15,8±2,89ab |
|
Cd |
0,12±0,001 |
0,14±0,001 |
0,13±0,001 |
0,13±0,001 |
0,12±0,001 |
|
Sn |
0,03±0,001 |
0,12±0,001 |
0,03±0,001b |
0,03±0,001b |
0,03±0,001b |
|
Hg |
0,03±0,001 |
0,03±0,001 |
0,03±0,001 |
0,03±0,001 |
0,03±0,001 |
|
Pb |
1,2±0,63 |
0,6±0,03 |
0,6±0,02a |
0,6±0,03a |
0,6±0,04a |
|
Al |
1,6±0,74 |
1,1±0,68 |
0,5±0,02ab |
0,7±0,01ab |
0,7±0,03ab |
Примечани е. Описание групп см. в разделе «Методика».
a, b Различия соответственно с K 1 и K 2 статистически значимы при р ≤ 0,05.
Введение хитозана в ПДР способствовало увеличению количества лития в 1,7 раза (р ≤ 0,05) относительно К 1 . Содержание бора в III опытной группе уменьшилось соответственно в 2,19 раза (р ≤ 0,05) и в 3,15 раза (р ≤ 0,05) по отношению к двум контрольным группам (см. табл. 2). Содержание марганца снижалось во всех опытных группах (р ≤ 0,05) относительно К 1 : в I опытной группе — в 1,86 раза, во II — в 1,50 раза, в III — в 1,77 раза. Аналогичная тенденция наблюдалась по кобальту: его количество статистически значимо уменьшалось в опытных группах соответственно в 7,98; 12,70 и 16,90 раза по сравнению с К 1 .
В I опытной группе было зарегистрировано повышение количества селена (р ≤ 0,05) в 2,35 раза относительно К 1 , а также его снижение (р ≤ 0,05) в 1,74 раза по отношению к К 2 . В этой же группе выявили достоверное (р ≤ 0,05) увеличение содержания йода (в 1,74 раза и в 1,50 раза относительно обеих контрольных групп). Во II и III группах количество селена снижалось в 4,64 и 4,55 раза (р ≤ 0,05) по сравнению к К 2 . Концентрация As во II группе превысила К 1 в 1,63 раза (р ≤ 0,05), а в III, напротив, снизилась в 1,58 раза и 2,00 раза (р ≤ 0,05) по отношению к К 1 и К 2 .
Скорость всасывания соединений тяжелых металлов, их распределение и токсичность зависит не только от биологических особенностей органов пищеварения, но и от физико-химических свойств всасываемых веществ, их взаимодействия с компонентами пищи и от присутствия в кормах различных добавок. Как известно, содержание протеина в рационе влияет на всасывание токсичных элементов в организме животных. В нашем случае добавление пищевых волокон способствовало активному выведению токсичных элементов (см. табл. 2). Содержание стронция у птицы в I и III опытных группах снизилось соответственно на 25,7 и 45,9 % (р ≤ 0,05) относительно К1. По сравнению с К2 показатель уменьшился на 22,2 и 43,4 % (р ≤ 0,05). Количество олова у птицы из опытных групп оказалось снижено в 4,0 раза (р ≤ 0,05) относительно К2, свинца — в 2,0 раза (р ≤ 0,05) по сравнению с К1. Аналогичные данные были получены по алюминию. Статистически значимое (р ≤ 0,05) снижение его содержания отмечали во всех опытных группах: в I группе соответственно в 3,19 и в 2,22 раза (р ≤ 0,05) по сравнении с К1 и К2, во II — в 2,51 и в 1,74 раза (р ≤ 0,05), в III — в 2,23 и 1,55 раза (р ≤ 0,05).
В микробном профиле содержимого слепой кишки цыплят-бройлеров в К 1 и III опытной группах мы выявили доминирование представителей филума Firmicutes , в то время как в I и II группах их обилие составило соответственно 39,7 и 39,8 %. Численность Bacteroidetes в К 1 составила 30,5 %, что было на 16,8; 28,9; 28,9 и 16,6 % меньше, чем соответственно в K 2 , I, II и III опытных группах. Численность остальных таксонов не превышала 3 % (рис. 1).
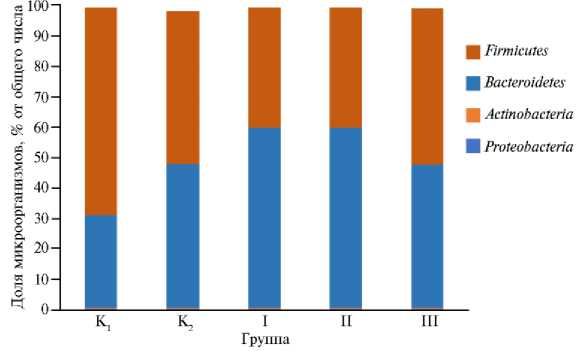
Рис. 1. Микробный профиль слепого отдела кишечника у цыплят-бройлеров ( Gallus gallus L.) кросса Arbor Acres, получавших полусинтетический рацион с добавлением различных пищевых волокон ( n = 30, виварий ФНЦ биологических систем и агротехнологий РАН). Описание групп см. в разделе «Методика».
На более низком таксономическом уровне в группе К 1 доминировало семейство Lactobicallaceae (61,6 %), также были представлены Bactero-daceae (26,2 %), Ruminococcaceae (4,5 %), Rikenellaceae (4,2 %). В группе К 2 наибольшую численность имели бактерии семейств Rikenellaceae (26,5 %), Lactobicallaceae (22,7 %), Bacterodaceae (20,6 %) и Lachnospiraceae (16,8 %). В группе К 2 по сравнению с группой К 1 численность Lactobicallaceae уменьшилась в 2,71 раза, в то время как численность Rikenellaceae увеличилась в 6,30 раза, Lachnospiraceae — в 12 раз, Ruminococcaceae — в 2,10 раза, Entero-bacteriaceae — в 5,60 раза.
В I опытной группе численность Lactobicallaceae уменьшилась в 4,5 раза, Bacterodaceae — увеличилась на 3,8 и 9,4 %, Rikenellaceae — в 6,3 и 6,8 раза, Lachnospiraceae — в 12 и 4,9 раза, Ruminococcaceae — в 2,1 и 3,9 раза по сравнению с К1 и К2. Во II опытной группе при внесении в рацион лактулозы обилие Lactobicallaceae снизилось в 6 раз, а численность представителей Bacterodaceae увеличилась на 6,5 и 12,1 % по сравнению с К1 и К2. Численность Rikenellaceae возросла в 6,20 раза, Lachnospiraceae — в 9,57 раза, Ru-minococcaceae — в 3,10 раза относительно группы К1. В III опытной группе при добавлении к рациону хитозана отмечали снижение обилия Lactobical-laceae соответственно в 13,30 и 1,55 раза по сравнению с К1 и К2. Численность Rikenellaceae увеличилась в 5,5 раза, Lachnospiraceae — в 11,8 раза, Ruminococcaceae — в 3,5 раза относительно К1 (рис. 2).
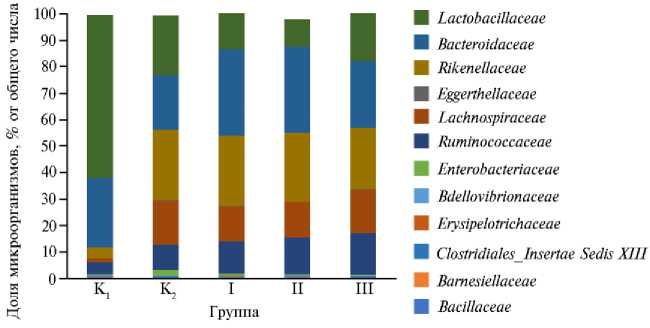
Рис. 2. Бактериальные семейства, обнаруженные в слепом отделе кишечника у цыплят-бройлеров ( Gallus gallus L.) кросса Arbor Acres, получавших полусинтетический рацион с добавлением различных пищевых волокон ( n = 30, виварий ФНЦ биологических систем и агротехнологий РАН). Описание групп см. в разделе «Методика».
Результаты NGS-секвенирования показали, что в содержимом слепой кишки цыплят-бройлеров из группы, получавшей ПР, на 42-е сут эксперимента на уровне родов большинство составляли представители Lactobacillus (59,8 %), Bacteroidetes (25,9 %), Alistipes (4,2 %) (рис. 3, А). В группе К 2 , которая получала рацион, дефицитный по минеральным веществам, доминировали представители рода Alistipes (26,5 %, или на 22,3 % выше, чем в К 1 ). Численность Lactobacillus была ниже на 39,5 %, Bacteroidetes — на 8,5 %, чем в группе К 1 . На неклассифицированных представителей микробного сообщества приходилось 11,2 %. Также в группе К 2 присутствовали роды Mediterraneibacter (7 %), Merdimonas (5,6 %), Limasilactobacillus (2,1 %), Intestinomonas (1,9 %) (см. рис. 3, Б).
В I опытной группе по результатам метагеномного секвенирования в содержимом слепой кишки доминировали представители рода Alistipes (28,9 %, или соответственно на 24,7 и 2,4 % выше по сравнению с К 1 и К 2 ). Бактерии рода Bacteroidetes составили 27,5 %, что на 10,1 % выше, чем в группе К 2 , неклассифицированные микроорганизмы — 9,4 %. Доля Lactobacillus была на 47,6 и 8,1 % ниже, чем соответственно в группах К 1 и К 2 . Число бактерий рода Intestinomonas (10 %) оказалось на 9,8 и 8,1 % выше, чем в К 1 и К 2 (см. рис. 3, В).
Во II опытной группе наиболее многочисленными таксонами были Bacteroidetes и Alistipes . Численность Bacteroidetes оказалась на 10,5 % выше, чем в группе К 2 . Доля бактерий Alistipes была на 22,2 % выше по сравнению с К 1 . Неклассифицированные микроорганизмы составили 14,5 % от общего числа. Обиие Lactobacillus было на 50,1 и 10,6 % ниже, чем соответственно в группах К 1 и К 2 , Mediterraneibacter — на 7,3 % выше, чем в К 1 . Бактерии рода Merdimonas составили 2,7 %, Subdoligranulum — 1,9 %, Intestinmonas —
1,5 %. На бактерии других родов приходилось не более 1 % от общей численности (см рис. 3, Г).
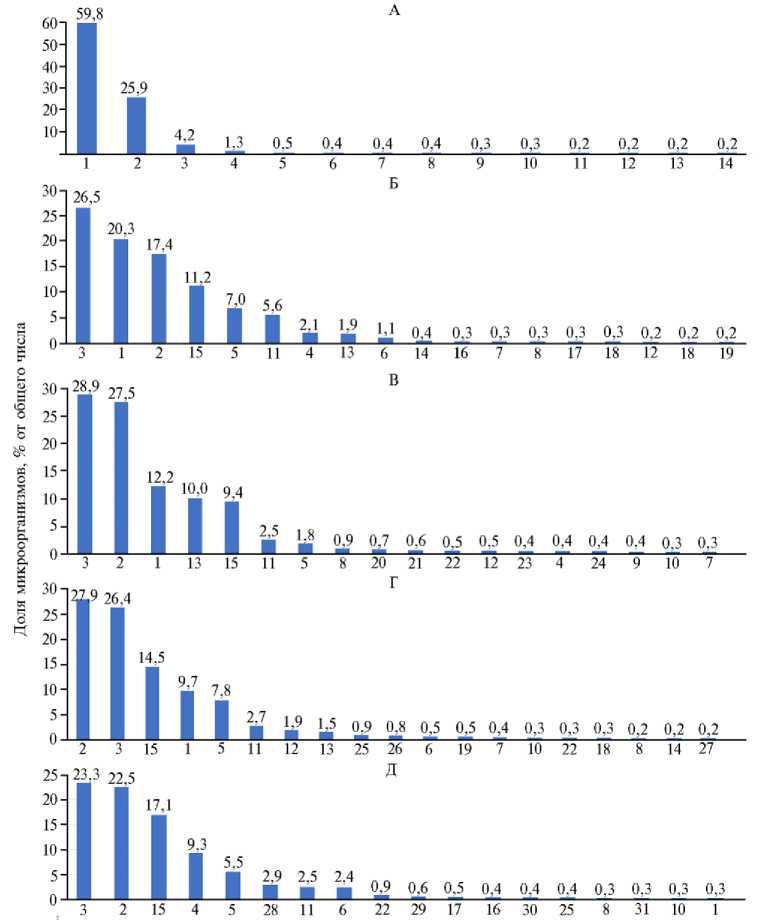
Род бактерий
Рис. 3. Состав микробиома на уровне родов в слепом отделе кишечника у цыплят-бройлеров ( Gallus gallus L.) кросса Arbor Acres, получавших полусинтетический рацион с добавлением различных пищевых волокон: 1 — Lactobacillus , 2 — Bacteroides , 3 — Alistipes , 4 — Limosilactobacillus , 5 — Mediterraneibacter , 6 — Faecalibacterium , 7 — Pseudoflavonifractor , 8 — Ligilactobacillus , 9 — Enterobacter , 10 — Rubneribacter , 11 — Merdimonas , 12 — Subdoligranulum , 13 — Intestinimonas , 14 — Neglecta , 15 — unclassified, 16 — Frisingicoccus , 17 — Eisenbergiella , 18 — Lachnospiraceae incertae sedis , 19 — Monoglobus , 20 — Fournierella , 21 — Ruthenibacterium , 22 — Coprobacter , 23 — Dysosmobacter , 24 — Catabacter , 25 — Anaerotignum , 26 — Clostridium XVIII , 27 — Anaero-masillibacillus , 28 — Weisella , 29 — Blautia , 30 — Bacillus , 31 — Ihubacter ; А — первая контрольная группа (К 1 ), Б — вторая контрольная группа (К 2 ), В — I опытная группа, Г — II опытная группа, Д — III опытная группа ( n = 30, виварий ФНЦ биологических систем и агротехнологий РАН). Описание групп см. в разделе «Методика».
В III опытной группе наиболее многочисленными были бактерии рода Alistipes (23,3 %, или на 19,1 % выше, чем в группе К 1 ) и Bacteroidetes
(22,5 %, или на 5,1 % выше, чем в К 2 ). В этой группе мы выявили 17,1 % неидентифицированных представителей бактериального сообщества. Доля бактерий Limosilactobacillus составила 9,3 %, что на 8,0 и 7,2 % выше по сравнению соответственно с группами К 1 и К 2 . Также в этой группе, получавшей дополнительно хитозан, были идентифицированы представители родов Weisella (2,9 %), Merdimonas (2,5 %), Faecalibacterium (2,4 %). На бактерии других родов приходилось менее 1 % (см. рис. 3, Д).
В целом мы показали, что добавление пищевых волокон в рацион цыплят-бройлеров приводило к уменьшению накопления в тканях тяжелых металлов, что также может быть связано с их выведением из организма с пищевыми волокнами и уменьшением всасывания в кишечнике. Это наблюдение делает перспективным разработку добавок на основе пищевых волокон для оздоровления сельскохозяйственных животных в условиях постоянно возрастающей антропогенной нагрузки на окружающую среду.
Известно, что клетчатка снижает абсорбцию минералов. Металлы, связанные непереваримыми веществами, в основном клетчаткой, остаются недоступными для абсорбции. Бактериями толстого кишечника клетчатка может быть гидролизована с выделением металлов, но абсорбции не произойдет и металлы будут выводиться с фекалиями. Поэтому именно содержание клетчатки в кормах во многом может определять доступность минеральных веществ (13). В современных условиях из-за удорожания традиционных компонентов комбикормов необходимы новые ингредиенты, которые позволят удешевить корма для сельскохозяйственной птицы. В качестве возможного решения рассматривается использовании в рационе пищевых волокон (14).
Эффективность новых кормовых субстратов необходимо не только оценивать по общепринятым параметрам, но и уделять внимание обмену химических элементов в организме. Пищевые волокна оказывают существенное влияние на минеральный обмен, изменения в котором могут привести к разнообразным нарушениям (1), и, наоборот, сбалансированность по химическим элементам обеспечивает повышение продуктивности животных и птицы (15). Ферментированные пищевые волокна способствуют снижению интоксикации, поскольку укрепляют барьерную стенку кишечника, нормализуют его двигательную активность, восстанавливают микрофлору (6). При анализе микробного профиля содержимого слепой кишки обращает на себя внимание то, что численность Lactobacillaceae значительно уменьшилась в группе К 2 и опытных группах, что может быть связано с недостатком минеральных веществ, необходимых для роста. Одновременно с этим не зафиксировано значимого увеличения обилия условно-патогенной микрофлоры. В то же время повышалась численность целлюлозолитических бактерий из таксонов Rikenellaceae и Lachnospiraceae . Это связано с увеличением содержания трудноразлагаемых компонентов в рационе бройлеров.
Наши данные согласуются с сообщениями, подтверждающими тенденцию к использованию клетчатки в качестве альтернативы антибиотикам как стимуляторам роста. Ранее антибиотики широко применяли в кормах для домашней птицы с целью профилактики и лечения болезней. Однако неизбирательное использование антибиотиков может привести к их остаточному содержанию в мясе и селекции антибиотикорезистентных форм микроорганизмов. С запретом или строгим регулированием использования антибиотиков в кормах в качестве стимуляторов роста в мировом птицеводстве регистрируется повышение частоты кишечных расстройств у домашней птицы (25). Поэтому ведется поиск альтернатив антибиотикам, разрабатываются рецептуры кормов с легкоусвояемыми ингредиентами, добавками ферментов, рассматривается применение различных методов обработки корма, чтобы в конечном итоге повысить показатели роста птицы.
Умеренное количество клетчатки в рационе рассматривалось как одна из альтернатив для улучшения усвояемости питательных веществ и показателей роста. Так, Y.P. Li с соавт. (26) установили, что диеты с низким содержанием клетчатки не позволяют в полной мере использовать протеин, содержащийся в корме, и птица получает меньше энергии по сравнению с диетами с высоким содержанием клетчатки. В дополнение к кормовым добавкам, таким как пробиотики, пребиотики и растительные экстракты, кормовые ингредиенты или их компоненты, например клетчатка, перспективны для разработки стратегий питания, позволяющих снижать заболеваемость ЖКТ и повышать продуктивность сельскохозяйственной птицы (23). Однако отметим, что имеющиеся данные об улучшения усвоения питательных веществ при скармливании пищевых волокон противоречивы. Например, M. Houshmand с соавт. (27) исследовали способность волокон компенсировать дефицит кальция в рационах домашней птицы. При использовании рациона с низким содержанием кальция и рациона с добавлением волокон во второй группе не наблюдалось дефицита. То есть было показано преимущество волокон в качестве пищевых добавок для улучшения показателей роста птицы и использования питательных веществ. Вместе с тем добавление клетчатки не всегда улучшает показатели роста и усвоение питательных веществ. В экспериментах, проведенных A. Sadeghi с соавт. (28), авторы обнаружили, что длина кишечных ворсинок уменьшалась у птицы, получавшей пищевые волокна. Это вызывало снижение всасывания питательных веществ в тощей кишке и увеличение их экскреции, что согласуется с нашими результатами.
На основании полученных нами данных могут быть разработаны способы модуляции микробного профиля кишечника птицы, чтобы исполь- зовать недорогие корма, содержащие трудноразлагаемую клетчатку. Важно отметить, что при введении пищевых волокон в дефицитный по минеральным веществам рацион мы не отмечали у птицы тяжелых дисбиотических процессов.
Таким образом, введение пищевых волокон (микрокристаллической целлюлозы, лактулозы, пищевого хитозана) в полусинтетический рацион цыплят-бройлеров кросса Арбор Айкрес приводит к снижению накопления макроэлементов в организме птицы, способствует элиминации токсичных химических элементов, а также увеличению численности таксонов Rikenel-laceae и Lachnospiraceae с одновременным снижением численности Lactoba-cillaceae в кишечнике птицы. Содержание стронция у птицы в группах, потреблявших целлюлозу и пищевой хитозан, снизилось соответственно на 25,7 и 45,9 % (р ≤ 0,05) относительно контрольной группы, получавшей полусинтетическом рацион (К 1 ). Уменьшение показателя на 22,2 и 43,4 % (р ≤ 0,05) было выявлено по отношению к контрольной группе, потреблявшей полусинтетическом рацион, дефицитный по микроэлементам (К 2 ). Количество олова в опытных группах оказалось снижено в 4,0 раза (р ≤ 0,05) относительно К 2 , свинца — в 2,0 раза в опытных группах (р ≤ 0,05) по сравнению с К 1 . Во всех опытных группах статистически значимо (р ≤ 0,05) снижалось содержание алюминия. В I группе, получавшей целлюлозу, численность Lactobicallaceae уменьшилась на 4,5 %, в то время как численность Bacterodaceae увеличилась на 3,8 и 9,4 %, Rikenellaceae — в 6,3 и 6,8 раза, Lachnospiraceae — в 12,0 и 4,9 раза, Ruminococcaceae — в 2,1 и 3,9 раза по сравнению с К 1 и К 2 . Во II группе при внесении в корм лактулозы численность Lactobicallaceae снижалась в 6 раз, а количество Bacterodaceae увеличилось на 6,5 и 12,1 % по сравнению с К 1 и К 2 . Численность Rikenellaceae увеличилась в 6,2 раза, Lachnospiraceae — в 9,57 раза, Ruminococcaceae — в 3,1 раза относительно К 1 . В III опытной группе при скармливании цыплятам-бройлерам хитозана численность Rikenellaceae увеличилась в 5,5 раза, Lachnospiraceae — в 11,8 раза, Ruminococcaceae — в 3,5 раза относительно К 1 . В целом выявлена способность пищевых волокон влиять на состав микробиома слепого отростка кишечника, что, как мы полагаем, позволит, используя биотические взаимоотношения между бактериями, изменять показатели продуктивности птицы в желаемую сторону.
Список литературы Минеральный обмен и микробное разнообразие слепого отдела кишечника у цыплят-бройлеров (Gallus gallus L.) при включении в полусинтетический рацион пищевых волокон
- Zhou C., Xu D., Lin K., Sun C., Yang X. Intelligent feeding control methods in aquaculture with an emphasis on fish: a review. Reviews in Aquaculture, 2018, 10(4): 975-993 (doi: 10.1111/raq.12218).
- Sklan D. Development of the digestive tract of poultry. World’s Poultry Science Journal, 2001, 57(4): 425-428 (doi: 10.1079/wps20010030).
- Stein H.H., Sève B., Fuller M.F., Moughan P.J., de Lange C.F.M. Invited review: Amino acid bioavailability and digestibility in pig feed ingredients: Terminology and application. Journal of Animal Science, 2007, 85(1): 172-180 (doi: 10.2527/jas.2005-742).
- Nahm K.H., Carlson C.W., Halverson A.W., Thiex N. Effects of cellulase supplementation and wheat bran on mineral utilization in broilers. South Dakota Poultry Field Day Proceedings and Research Reports, 1983: 12.
- Kvan O., Duskaev G., Rakhmatullin S., Kosyan D. Changes in the content of chemical ele-ments in the muscle tissue of broilers on the background of plant extract and tetracyclines. International Journal of Environmental Science and Development, 2019, 10(12): 419-423 (doi: 10.18178/ijesd.2019.10.12.1209).
- Anwar M.N., Ravindran V. Influence of methodology on the measurement of ileal endogenous calcium losses in broiler chickens. Journal of Applied Animal Research, 2020, 48(1): 264-267 (doi: 10.1080/09712119.2020.1781133).
- Иванов А.А., Полякова Е.П., Ксенофонтов Д.А. Общебиологический феномен депонирования катионов структурами химуса и его значение для создания смесей энтерального питания. Экспериментальная и клиническая гастроэнтерология, 2012, 2: 71-75.
- Bassi L.S., Teixeira L.V., Sens R.F., Almeida L., Zavelinski V.A.B., Maiorka A. High doses of phytase on growth performance, bone mineralization, diet utilization, and plasmatic myo-inositol of turkey poults. Poultry Science, 2021, 100(5): 101050 (doi: 10.1016/j.psj.2021.101050).
- Yaqoob M.U., Abd El-Hack M.E., Hassan F., El-Saadony M.T., Khafaga A.F., Batiha G.E., Yehia N., Elnesr S.S., Alagawany M., El-Tarabily K.A., Wang M. The potential mechanistic insights and future implications for the effect of prebiotics on poultry performance, gut microbiome, and intestinal morphology. Poultry Science, 2021, 100(7): 101143 (doi: 10.1016/j.psj.2021.101143).
- Jiménez-Moreno E., de Coca-Sinova A., González-Alvarado J.M., Mateos G.G. Inclusion of insoluble fiber sources in mash or pellet diets for young broilers. 1. Effects on growth performance and water intake. Poultry Science, 2016, 95(1): 41-52 (doi: 10.3382/ps/pev309).
- Tejeda O.J., Kim W.K. Role of dietary fiber in poultry nutrition. Animals, 2021, 11(2): 461 (doi: 10.3390/ani11020461).
- Scott M.L., Nesheim M.C., Young R.J. Nutrition of the chicken. M.L. Scott & Assoc, Ithaca, NY, 1969.
- Short F.J., Gorton P., Wiseman J., Boorman K.N. Determination of titanium dioxide added as an inert marker in chicken digestibility studies. Animal Feed Science and Technology, 1996, 59(4): 215-221 (doi: 10.1016/0377-8401(95)00916-7).
- Ansia I., Stein H.H., Vermeire D.A., Brøkner C., Drackley J.K. Ileal digestibility and endogenous protein losses of milk replacers based on whey proteins alone or with an enzyme-treated soybean meal in young dairy calves. Journal of Dairy Science, 2020, 103(5): 4390-4407 (doi: 10.3168/jds.2019-17699).
- Blaut M. Relationship of prebiotics and food to intestinal microflora. European Journal of Nutri-tion, 2002, 41(Suppl. 1): i11-i16 (doi: 10.1007/s00394-002-1102-7).
- Jha R., Woyengo T.A., Li J., Bedford M.R., Vasanthan T., Zijlstra R.T. Enzymes enhance deg-radation of the fiber—starch—protein matrix of distillers dried grains with solubles as revealed by a porcine in vitro fermentation model and microscopy. Journal of Animal Science, 2015, 93(3): 1039-1051 (doi: 10.2527/jas.2014-7910).
- Williams B.A., Grant L.J., Gidley M.J., Mikkelsen D. Gut fermentation of dietary fibres: physico-chemistry of plant cell walls and implications for health. International Journal of Molecular Sci-ences, 2017, 18(10): 2203 (doi: 10.3390/ijms18102203).
- JøRgensen H., Zhao X.Q., Knudsen K.E.B., Eggum B.O. The influence of dietary fibre source and level on the development of the gastrointestinal tract, digestibility and energy metabolism in broiler chickens. British Journal of Nutrition, 1996, 75(3): 379-395 (doi: 10.1079/BJN19960141).
- Sadeghi A., Toghyani M., Tabeidian S.A., Foroozandeh A.D., Ghalamkari G. Efficacy of die-tary supplemental insoluble fibrous materials in ameliorating adverse effects of coccidial chal-lenge in broiler chickens. Archives of Animal Nutrition, 2020, 74(5), 362-379 (doi: 10.1080/1745039X.2020.1764811).
- Kheravii S.K., Morgan N.K., Swick R.A., Choct M., Wu S.B. Roles of dietary fibre and ingredient particle size in broiler nutrition. World’s Poultry Science Journal, 2018, 74(2): 301-316 (doi: 10.1017/S0043933918000259).
- Sozcu A. Growth performance, pH value of gizzard, hepatic enzyme activity, immunologic indi-cators, intestinal histomorphology, and cecal microflora of broilers fed diets supplemented with processed lignocellulose. Poultry Science, 2019, 98(12): 6880-6887 (doi: 10.3382/ps/pez449).
- Mahmood T., Guo Y. Dietary fiber and chicken microbiome interaction: where will it lead to? Animal Nutrition, 2020, 6(1): 1-8 (doi: 10.1016/j.aninu.2019.11.004).
- Mateos G.G., Jiménez-Moreno E., Serrano M., Lázaro R. Poultry response to high levels of dietary fiber sources varying in physical and chemical characteristics. Journal of Applied Poultry Research, 2012, 21(1): 156-174 (doi: 10.3382/JAPR.2011-00477).
- Jha R., Fouhse J.M., Tiwari U.P., Li L., Willing B.P. Dietary fiber and intestinal health of mo-nogastric animals. Frontiers in Veterinary Science, 2019, 6: 48 (doi: 1010.3389/fvets.2019.00048).
- Adhikari P., Kiess A., Adhikari R., Jha R. An approach to alternative strategies to control avian coccidiosis and necrotic enteritis. Journal of Applied Poultry Research, 2020, 29(2): 515-534 (doi: 10.1016/j.japr.2019.11.005).
- Li Y.P., Wang Z.Y., Yang H.M., Xu L., Xie Y.J., Jin S.L., Sheng D.F. Effects of dietary fiber on growth performance, slaughter performance, serum biochemical parameters, and nutrient utiliza-tion in geese. Poultry Science, 2017, 96(5): 1250-1256 (doi: 10.3382/ps/pew385).
- Houshmand M., Azhar K., Zulkifli I., Bejo M.H., Meimandipour A., Kamyab A. Effects of non-antibiotic feed additives on performance, tibial dyschondroplasia incidence and tibia characteris-tics of broilers fed low-calcium diets. Journal of Animal Physiology and Animal Nutrition, 2011, 95(3): 351-358 (doi: 10.1111/j.1439-0396.2010.01061.x).
- Sadeghi A., Toghyani M., Gheisari A. Effect of various fiber types and choice feeding of fiber on performance, gut development, humoral immunity, and fiber preference in broiler chicks. Poultry Science, 2015, 94(11): 2734-2743 (doi: 10.3382/ps/pev292).


