Миниинвазивная торакоскопическая техника стимуляции экстракардиальной васкуляризации миокарда методом ЮрЛеон при диффузном поражении коронарного русла при ИБС
Автор: Шевченко Ю.Л., Байков В.Ю., Борщев Г.Г., Аблицов А.Ю.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Клинические наблюдения
Статья в выпуске: 2 т.17, 2022 года.
Бесплатный доступ
Представлено клиническое наблюдение пациента 67 лет, длительно страдающего ИБС и в разное время в течение 8 лет дважды (2011, 2014 гг.) перенесшего эндоваскулярное вмешательство на сердце - стентирование коронарных артерий. Однако в 2021 г. наступил рецидив стенокардии. При обследовании в клинике выявлено тяжелое диффузное поражение коронарного русла. При этом консервативная терапия неэффективна, а повторное вмешательство в виде стентирования или АКШ невыполнимо. Поэтому выполнена изолированная процедура ЮрЛеон - стимуляция экстракардиальной васкуляризации миокарда методом торакоскопического вмешательства.
Видеоторакоскопия, стентирование коронарных артерий, неоангиогенез
Короткий адрес: https://sciup.org/140294378
IDR: 140294378 | DOI: 10.25881/20728255_2022_17_2_103
Minimally invasive thoracoscopic technique for stimulating extracardiac myocardial vascularization using the YurLeon method for diffuse coronary disease in coronary heart disease
The article presents a clinical case of a 67-year-old patient suffering from coronary artery disease for a long time and at different times during 8 years twice (2011, 2014) underwent endovascular intervention on the heart - stenting of the coronary arteries. However, in 2021, angina pectoris relapsed. Clinical examination revealed a severe diffuse lesion of the coronary bed. At the same time, conservative therapy is not effective, and re-intervention in the form of stenting or CABG is not feasible. An isolated YurLeon procedure was undertaken - stimulation of extracardiac myocardial vascularization using a minimally invasive thoracoscopic intervention technique.
Текст научной статьи Миниинвазивная торакоскопическая техника стимуляции экстракардиальной васкуляризации миокарда методом ЮрЛеон при диффузном поражении коронарного русла при ИБС
Современные возможности кардиохирургии позволяют помочь большинству пациентов с различными формами ИБС. Однако существует группа больных возвратной стенокардией после проведенных ранее реваскуляризирующих операций — стентирование либо АКШ [1–3].
При этом значительному количеству больных, которым стандартное оперативное лечение невыполнимо в виду ряда причин: выраженное диффузное дистальное поражение коронарных артерий; чрезвычайно высокий риск операции в виду крайне тяжёлого общего состояния, а так же технических трудностей [4; 5].
Для лечения этой группы сложных пациентов была разработана специальная хирургическая процедура стимуляции экстракардиального ангиогенеза (ЮрЛеон) [6; 8], предложенная академиком РАН Ю.Л. Шевченко в 2007 г. (патент на изобретение № 2758024). Методика применена более чем у двух тысяч пациентов как дополнение к АКШ и показала свою клиническую эффективность и безопасность [7; 8].
В последнее время у таких больных метод применяется как самостоятельная процедура из миниинвазивного доступа — переднебоковой левосторонней миниторакотомии или из видеоторакоскопи-ческого доступа.
Представляем клиническое наблюдение успешного хирургического лечения пациента после ранее перенесенных в разные сроки стентирований коронарных артерий с последующим развитием диффузной и дистальной формы поражением коронарного русла.
Больной О. 67 лет в 2021 г. поступил в клинику грудной и сердечнососудистой хирургии им. Св.Георгия НМХЦ им. Н.И. Пирогова с жалобами на боли давящего характера за грудиной с иррадиацией в левую лопаточную область, возникающие при незначительной физической нагрузке (ходьба на расстояние 200–250 м).
Из анамнеза известно: с 2011 г. беспокоили ангинозные боли.
При коронарографии: ПМЖА — стенозы проксимальной, средней трети до 75–80%, ДА — без гемодинамически значимых стенозов, ОА — стенозы проксимальной и средней трети до 40–50%, ВТК — стеноз проксимально трети до 40%, ПКА — стеноз проксимальной трети до 50%.
Пациенту выполнена операция — стентирование ПМЖА стентом Endeavor Sprint 4,0 x 15 мм.
Послеоперационный период протекал без осложнений, пациент выписан в удовлетворительном состоянии.
С 2014 г. — возврат стенокардии на уровне 3 функционального класса.
При контрольной коронарографии: ствол ЛКА — без гемодинамически значимых стенозов, ПМЖА — неровности контуров, стентированный участок средней трети без признаков тромбоза и рестеноза, ОА — стенозы проксимальной и средней трети до 50–60%. ВТК — стеноз проксимально трети до 50%, ПКА — стеноз проксимальной трети до 50%, в средней трети субокклюзия с признаками

оформленного пристеночного тромба, отделы дистальнее субокклюзии слабо контрастируются антеградно, атеросклеротически изменены, кровоток TIMI I–II.
Пациенту выполнено стентирование ПКА стентом Endeavor Sprint 4,0 x 18 мм, Endeavor Sprint 4,0 x 15 мм.
Послеоперационный период протекал без осложнений, пациент выписан в удовлетворительном состоянии.
В 2021 г. вновь возврат стенокардии. Пациент госпитализирован в клинику для обследования и определения дальнейшей тактики лечения.
При коронарографии: ствол ЛКА стенозирован до 50% в устье. Передняя межжелудочковая артерия диффузно изменена, рестеноз в стенте до 60%, ок-клюзирована в среднем сегменте с постокклюзионным слабым контрастированием по внутрисистемным перетокам, постокклюзионное русло диффузно изменено со стенозированием до 70%. Диагональная артерия стенозирована до 50% в проксимальном сегменте. Огибающая артерия — стеноз устья до 40%, окклюзи-рована на границе проксимального и дистального сегментов; постокклюзионные отделы диффузно изменены и контрастируются по межсистемным перетокам. Артерия тупого края I порядка диффузно стенозирована до 90% в проксимальном сегменте. Артерия тупого края II порядка окклюзирована, заполняется ретроградно по внутрисистемным перетокам, диффузно стенозирована до 90% в проксимальном сегменте. Правая коронарная артерия — диффузно изменена на всём протяжении, устьевой стеноз 80%, кальциноз и стенозирование проксимального и среднего сегментов до 70%, стеноз дистального сегмента до 50–60%. ЗМЖА окклюзия (Рис. 1; 2).
При эхокардиографии: фракция выброса левого желудочка 32%. Региональная систолическая функция ЛЖ нарушена: гипокинез боковой стенки ЛЖ, гипокинез задней стенки ЛЖ.
Данные синхро-ОФЭКТ с99mTc-технет-рилом: сцинтиграфические признаки рубцовых изменений с гибернированным миокардом (17%) в области передней, передне-боковой стенок (частично верхушечные и средние сегменты). Зона рубцового поражения более 15%.
Клинический диагноз
Основной: ИБС; Стенокардия напряжения III ФК; состояние после стентирования ПМЖА 2011 г, ПКА в 2014 г.; стенозирующий атеросклероз коронарных
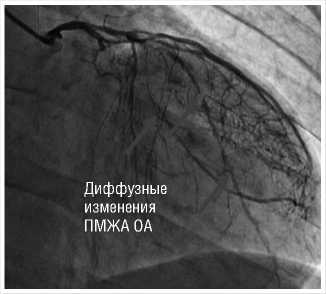
Рис. 1. Данные коронарографии, бассейн ЛКА.
артерий: ствол ЛКА стенозирован до 50% в устье. ПМЖА — диффузно изменена, с рестенозом в стенте до 60%, окклюзи-рована в среднем сегменте с постокклюзионным слабым контрастированием по внутрисистемным перетокам; постокклюзионное русло диффузно изменено со стенозированием до 70%; ДА — стенозирована до 50% в проксимальном сегменте; ОА — стеноз устья до 40%, окклю-зирована на границе проксимального и дистального сегментов, постокклюзионные отделы диффузно изменены и слабо контрастируются по межсистемным перетокам. ВТК I порядка — диффузно стенозирована до 90% в проксимальном сегменте. ВТК II порядка — окклюзирована, заполняются рентроградно по внутрисистемным перетокам, диффузно стенозирована до 90% в проксимальном сегменте. ПКА — диффузно изменена на всём протяжении, устьевой стеноз 80%, кальциноз и стенозирование проксимального и среднего сегмента до 70%, стеноз дистального сегмента до 50–60%. ЗМЖА окклюзирована.
Фон: Гипертоническая болезнь III стадии, артериальная гипертензия 2 степени, риск IV.
Осложнения: ХСН I. ФК II.
Сопутствующий: стенозирующий атеросклероз брахиоцефальных артерий (стеноз ВСА слева до 30–40%). Стенозирующий атеросклероз артерий нижних конечностей (ПБА справа стеноз до 30%, ПБА справа стеноз до 40%, ПБА слева стеноз до 40–50%). Хронический гастрит.
После предоперационной подготовки выполнена операция — видео-торакоскопическая перикардэктомия, липокардиопексия и стимуляция экс-тракардиального ангиогенеза .
Положение пациента на правом боку (Рис. 3).
Под многокомпонентной интубационной анестезией с раздельной вен-
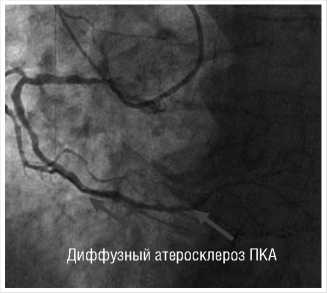
Рис. 2. Данные коронарографии, бассейн ПКА.
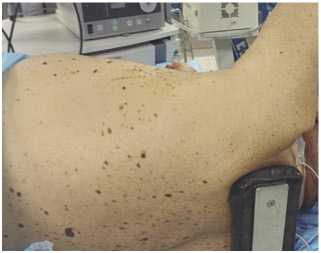
Рис. 3. Положение пациента на операционном столе.

Рис. 4. Видеоторакоскопический доступ в IV и V межреберьях.
тиляцией легких сформирован 10-мм видеоторакоскопический доступ в V-м межреберье по передней подмышечной линии, 10-мм в V-м межреберье по срединно-ключичной, 5-мм в IV-м по передней подмышечной (Рис. 4).
После отсепарирования паракарди-альной жировой ткани выше на 2 см от n. phrenicus вскрыт перикард (Рис. 5).
С помощью аппарата Harmonic выполнено удаление части перикарда в области левого желудочка сердца (Рис. 6).
В дальнейшем выполняли механическую обработку эпикарда и остаточной части перикарда (Рис. 7). Механиче-
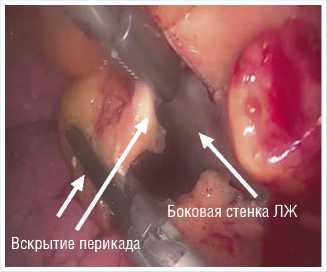
Рис. 5. Вскрытие перикарда.
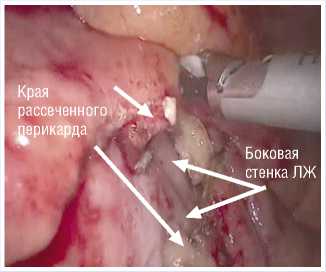
Рис. 6. Перикардэктомия.
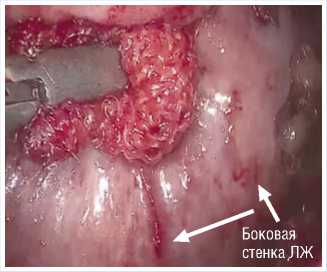
Рис. 7. Механическая обработка эпикарда.
ская десквамация мезотелия перикарда и эпикарда способствует асептическому воспалению, основополагающей частью которого является образование новых сосудов (неоангиогенез) в послеоперационном периоде.
Методика индукции асептического перикардита осуществлялась путем воздействия на большую часть перикарда (боковая, задняя его поверхности) и эпикарда (задняя и боковая стенки ЛЖ) с помощью специальных приспособлений для скарификации перикарда и эпикарда (Рис. 8).
В дальнейшем выполнили карди-олипопексию — мобилизованый жир укладывается непосредственно на миокард и фиксируется в области удаленного перикарда (Рис. 9). Жировая ткань — это самообновляющаяся структура, богатая кровеносными сосудами. Обоснованием для использования клеток жировой ткани для стимуляции ангиогенеза являются: осуществление неоангиогенеза за счёт дифференцировки в эндотелиальные клетки, влияние на модуляцию местных воспалительных реакций, значительная секреторная активность [8].
Плевральная полость дренирована одной силиконовой трубкой, подключена к дренажной системе по Бюлау. Также установлен тонкий дренаж в оставшуюся полость перикарда под заднюю поверхность сердца.
Установленные дренажи подключали к стерильному резервуару и налаживали систему активной аспирации. На вторые сутки полученное дренажное отделяемое центрифугировали для отделения разрушившихся форменных элементов крови и обработанную суспензию хранили в холодильнике при температуре 4 °C. На 3–4 сутки через тонкий дренаж в остаточную полость перикарда вводили обработанную суспензию с факторами роста.
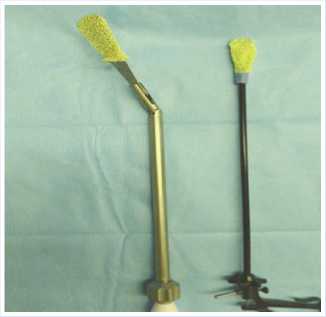
Рис. 8. Видеоторакоскопические инструменты для механической обработки перикарда и эпикарда.
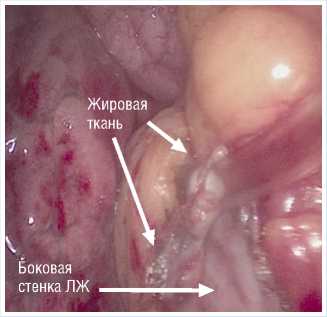
Рис. 9. Кардиолипопексия.
Послеоперационный период протекал без осложнений.
Данные Эхо-КГ, выполненной на 2 сутки после операции, прежние. Рана зажила первичным натяжением.
Пациент выписан на 7 сутки после операции с рекомендациями амбулаторного кардиологического лечения.
Через 6 месяцев после операции пациент обследован в клинике. Отмечена явная положительная динамика — отсутствие приступов стенокардии, увеличилась толерантность к физическим нагрузкам. Проведен тест с 6-ти минутной ходьбой. На дооперационном этапе дистанция составила 250 метров, через 6 месяцев после операции — до 500 м.
При Эхо-КГ улучшение показателей сократимости миокарда ЛЖ: фракция выброса ЛЖ увеличилась с 32 до 50%, улучшилась сократимость ЛЖ — выявленный ранее гипокинез боковой стенки ЛЖ регрессировал.
По данным сцинтиграфии миокарда отмечается улучшение перфузии по передне-боковой стенке ЛЖ (Рис. 10, 11): зона рубцового поражения 15%, нормальный миокард — 85%.
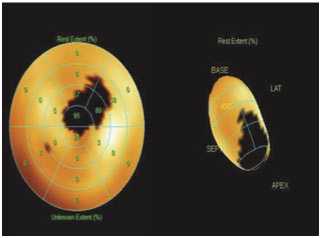
Рис. 10. Синхро-ОФЭКТ с 99mTc-технетрилом до оперативного лечения
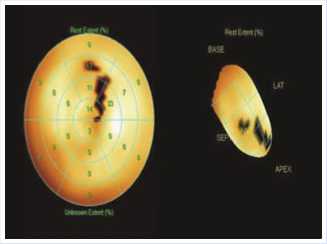
Рис. 11. Синхро-ОФЭКТ с 99mTc-технетрилом после оперативного лечения.

Обсуждение
Хирургическое лечение пациентов с ИБС с диффузным поражением коронарных артерий и после проведённых ранее операций связано с различными сложностями. У данных пациентов выполнение классической операции в объеме повторного стентирования коронарных артерий или аортокоронарного шунтирования, как правило, не дает результатов. Процедура ЮрЛеон из видеоторакоскопи-ческого доступа является эффективным и безопасным методом хирургического лечения подобных пациентов и обеспечивает дополнительное кровоснабжение миокарда, улучшая его сократительную функцию в отдаленные сроки после операции (начиная с 3-х месяцев после вмешательства).
Выводы
Пациенты, ранее перенесшие операцию по реваскуляризации миокарда и с последующим прогрессированием в диффузную дистальную форму коронарного атеросклероза из-за высокого риска повторного вмешательства зачастую признаются неоперабельными.
В приведенном клиническом наблюдении продемонстрирован возможный тактический и методический подход для хирургического лечения подобного больного — выполнение операции стимуляции экстракардиальной реваскуляризации миокарда из видеоторакоскопи-ческого доступа. Вмешательство полностью себя оправдало, что доказывается как данными лабораторных и инструментальных исследований, так и, прежде всего, хорошим клиническим эффектом в отдаленном периоде.
Этот метод применим для пациентов, которым невозможно выполнить операцию ни стентирования, ни коронарного шунтирования. Эта операция показана пациентам и со сниженной фракцией выброса (30–40%), и пациентам с исходно тяжелым состоянием, для которых любая хирургическая агрессия сопряжена с крайне высоким риском осложнений. Поэтому, благодаря сочетанию метода ЮрЛеон с минимальным хирургическим воздействием, непродолжительным временем операции и наркоза, и последующей интенсивной комплексной кардиологической терапией, удастся достичь хороших результатов в лечении этой категории сложных больных высокого риска.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Миниинвазивная торакоскопическая техника стимуляции экстракардиальной васкуляризации миокарда методом ЮрЛеон при диффузном поражении коронарного русла при ИБС
- Шевченко Ю.Л., Симоненко В.Б., Борщев Г.Г. Экстракардиальная реваскуляризация миокарда при диффузном поражении коронарного русла, как компонент комплексного лечения больных ИБС // Клиническая медицина. - 2018. - Т.96. - № 11. - С.10-18.
- Хубулава Г.Г., Пайвин А.А., Волков А.М. и др. Особенности хирургического лечения рецидива ишемии миокарда у пациентов после коронарного шунтирования // Вестник Северо-Западного государственного медицинского университета. - 2009. - Т.1. - №3. - С.21-28.
- Fuchs S., Dib N., Cohen BM et al. A randomized, double-blind, placebocontrolled, multicenter, pilot study of the safety and feasibility of catheterbased intramyocardial injection of Ad-VEGF121 in patients with refractory advanced coronary artery diseasе. Catheter Cardiovasc Interv. 2006; 68(3): 372-8.
- Шевченко Ю.Л., Пинаев Г.П., Матвеев С.А. и др. Первый опыт имплантации эмбриональных кардиомиоцитов (ЭК) человека в комплексном лечении больных ишемической болезнью сердца // 4-й Всероссийский съезд сердечно-сосудистых хирургов. 1998.
- Шевченко Ю.Л., Попов Л.В., Батрашов В.А. и др. Трудности выбора объема реваскуляризации при лечении ишемической болезни сердца у пациента с высоким риском // Вестник Национального медико-хирургического Центра им. Н.И. Пирогова. - 2015. - Т.10. - № 4. - С.134-136.
- Шевченко Ю.Л., Виллер А.Г. Экстракардиальная реваскуляризация у больных ишемической болезнью сердца после коронарного шунтирования - существующий фактор кровоснабжения миокарда // Вестник Национального медико-хирургического Центра им. Н.И. Пирогова. - 2007. - Т.2. - №2. - С.9-14.
- Борщев Г.Г. Экстравазальная реваскуля-ризация миокарда в комплексном лечении пациентов с ИБС: исторические предпосылки и современные реалии // Медицинский вестник Юга России. - 2015. - Т.2. - С.4-8. 10.21886/2219-8075- 2015-2-4-8.
- DOI: 10.21886/2219-8075-2015-2-4-8 EDN: UHNGGR
- Шевченко Ю.Л., Борщев Г.Г. Экстракардиальная реваскуляризация миокарда у больных ИБС с диффузным поражением коронарного русла. М.: Национальный медико-хирургический центр имени Н.И. Пирогова, 2022.


