Миокардиты. клинические варианты течения и прогноз
Автор: Муркамилов И.Т., Айтбаев К.А., Муркамилова Ж.А., Райимжанов З.Р., Солижонов Ж.И., Гасанов К.А., Закиров О.Т., Хакимов Ш.Ш., Ыманкулов Д.С., Хабибуллаев К.К., Абдибалиев И.А.
Журнал: Бюллетень науки и практики @bulletennauki
Рубрика: Медицинские науки
Статья в выпуске: 4 т.12, 2026 года.
Бесплатный доступ
Миокардит представляет собой очаговое или диффузное воспалительное поражение сердечной мышцы, клинически проявляющееся симптомами и/или признаками сердечной недостаточности (СН). Его этиология включает инфекционные (вирусы, бактерии, паразиты, простейшие) и неинфекционные (токсины, яды, тяжёлые металлы, ожоги, радиация, обменные и метаболические нарушения, аллергены, пестициды, лекарственные средства) агенты, а также системные заболевания соединительной ткани (СЗСТ). По клиническому течению различают молниеносный, подострый, хронический (активный и персистирующий), гигантоклеточный и эозинофильный миокардит. Основные звенья патогенеза включают внедрение возбудителя через входные ворота (дыхательные пути, желудочно-кишечный тракт, мочевыделительная система), проникновение вирусов в кардиомиоциты, их репликацию, нарушение мультибелкового комплекса, активацию инфламмасомного каскада, апоптоз, некробиоз и некроз кардиомиоцитов. Далее формируются воспалительная инфильтрация, выработка хемокинов и цитокинов, а также развивается аутоиммунное повреждение с последующей структурно-функциональной перестройкой миокарда. Диагностика миокардита базируется на анамнестических (острое начало, связь с инфекцией), клинических (одышка, сердцебиение, лихорадка, боли в области сердца), электрокардиографических (нарушения возбудимости и/или проводимости), эхокардиографических (снижение систолической функции, дилатация полостей), лабораторных (лейкоцитоз, лимфопения, ускоренное СОЭ, повышение уровней мозгового натрийуретического пептида, С-реактивного белка, фибриногена, прокальцитонина, ферритина, Д-димера, IgE), а также серологических данных (идентификация вирусов, бактерий и др.). Дополнительно применяются методы определения концентрации тропонинов, лактатдегидрогеназы, КФК-МВ, титров интерлейкина-6 и миокардиальных антител, оценка активности СЗСТ и вирусной нагрузки с помощью ПЦР. При остром миокардите МРТ с контрастированием гадолинием выявляет субэпикардиальное и трансмуральное накопление контраста. Золотым стандартом диагностики остаётся эндомиокардиальная биопсия с последующим проведением световой микроскопии формалин-фиксированных парафиновых срезов, иммуногистохимического исследования, молекулярных тестов (ПЦР) и трансмиссионной электронной микроскопии. Современное лечение миокардита включает этиотропную и патогенетическую терапию. У большинства пациентов, особенно при нетяжёлом течении, миокардит разрешается самостоятельно без активного вмешательства; по мере элиминации возбудителя наступает спонтанное выздоровление. В тяжёлых и крайне тяжёлых случаях заболевание может переходить в постмиокардитический кардиосклероз с развитием дилатационной кардиомиопатии и последующей необходимостью трансплантации сердца. В данной статье представлены результаты клинического наблюдения острого миокардита у 38-летнего пациента с двусторонней пневмонией. Диагноз был установлен на основании данных анамнеза, клинической картины, эхокардиографического исследования, лабораторных и серологических тестов.
Миокардиты, воспаление, вирусы, бактерии, респираторная инфекция, клиническое течение
Короткий адрес: https://sciup.org/14135159
IDR: 14135159 | УДК: 616-002.616.06.616.07 | DOI: 10.33619/2414-2948/125/28
Myocarditis: Clinical Variants and Prognosis
Myocarditis is a focal or diffuse inflammatory lesion of the heart muscle that clinically manifests with symptoms and/or signs of heart failure (HF). It is caused by infectious agents (viruses, bacteria, parasites, protozoa) and non-infectious factors (toxins, poisons, heavy metals, burns, radiation, metabolic disorders, allergens, pesticides, medications), as well as systemic connective tissue diseases (CTDs). Clinically, myocarditis can present in fulminant, subacute, or chronic forms (active or persistent), and also as giant cell or eosinophilic myocarditis. The main pathogenetic mechanisms include the entry of pathogens through portals such as the respiratory tract, gastrointestinal tract, or genitourinary system; viral penetration into cardiomyocytes; viral replication; disruption of the multiprotein complex within the cell; activation of the inflammasome cascade; apoptosis, necrobiosis, and necrosis of cardiomyocytes; formation of inflammatory cellular infiltration; chemokine and cytokine production; and autoimmune damage to cardiomyocytes, leading to structural and functional remodeling of the heart. Diagnosis of myocarditis is based on anamnesis (acute onset, association with infection), clinical symptoms (dyspnea, palpitations, fever, chest pain), electrocardiographic findings (conduction and/or excitability disturbances), echocardiographic findings (reduced systolic function, chamber dilatation), laboratory tests (leukocytosis, lymphopenia, elevated ESR, increased levels of brain natriuretic peptide, C-reactive protein, fibrinogen, procalcitonin, ferritin, D-dimer, immunoglobulin E), and serological tests (identification of viruses, bacteria, etc.). Additional diagnostic tools include measurements of troponins, lactate dehydrogenase, CK-MB, interleukin-6 titers, myocardial autoantibodies, assessment of CTD activity, and viral load quantification via polymerase chain reaction (PCR). In cases of acute myocarditis, cardiac MRI with gadolinium shows subepicardial and transmural contrast enhancement. The gold standard for diagnosis remains endomyocardial biopsy with light microscopy of formalin-fixed paraffin-embedded sections, immunohistochemical analysis, molecular tests (PCR), and transmission electron microscopy. Modern treatment of myocarditis includes etiological and pathogenetic therapy. In the majority of patients, especially in milder cases, myocarditis resolves spontaneously without active intervention, with spontaneous recovery occurring as the infection subsides. Severe and extremely severe cases often progress to post-myocarditic cardiosclerosis, leading to dilated cardiomyopathy and the potential need for heart transplantation. This article presents the results of a clinical case of acute myocarditis in a 38-year-old patient with bilateral pneumonia. The diagnosis of acute myocarditis was established based on medical history, clinical presentation, echocardiographic findings, and laboratory and serological data.
Текст научной статьи Миокардиты. клинические варианты течения и прогноз
Бюллетень науки и практики / Bulletin of Science and Practice
УДК 616-002.616.06.616.07
Миокардит представляет собой очаговое или диффузное воспалительное поражение сердечной мышцы, клинически проявляющееся симптомами и/или признаками сердечной недостаточности (СН). История изучения миокардита как одной из причин СН восходит к 1812 году, когда французский патолог Ж. N. Corvisart выдвинул предположение о том, что воспаление сердечной мышцы может приводить к прогрессирующему развитию СН [1].
Спустя 150 лет, в 1962 году, S. Sakakibara и S. Konno опубликовали в журнале Japanese Heart Journal работу, в которой впервые была представлена роль эндомиокардиальной биопсии в диагностике миокардита [2].
Результаты исследований последних лет подтвердили значимость эндомиокардиальной биопсии как «золотого стандарта» в диагностике воспалительных поражений миокарда [3].
На практике острый миокардит нередко остаётся недооценённым, что приводит к его гиподиагностике. В то же время заболевание может протекать не только остро, но и принимать хроническое течение. По данным аутопсий, частота миокардита составляет 5-7 случаев на 100 умерших. Согласно опубликованным данным, при проведении эндомиокардиальной биопсии миокардит верифицируется в 9-16% случаев у пациентов с необъяснимой дилатацией левого желудочка (ЛЖ) [4].
У большинства детей с дилатационной кардиомиопатией миокардит выявляется в 46% случаев по результатам эндомиокардиальной биопсии. Миокардит может развиваться в любом возрасте, однако наиболее часто встречается у молодых пациентов [5].
Мужчины молодого возраста заболевают миокардитом чаще, чем женщины, что связывают с модулирующим влиянием половых гормонов на силу иммунного ответа у женщин [3].
В литературе описан случай развития острого миокардита у 21-летнего пациента, диагностированного на основании данных магнитно-резонансной томографии (МРТ) сердца [6].
Имеются сведения, что миокардит выявляется до 42% среди случаев внезапной смерти у молодых спортсменов [7, 8].
Наибольшая частота миокардита отмечается при таких заболеваниях, как системная красная волчанка, ревматоидный артрит, системная склеродермия, ВИЧ-инфекция и дифтерия. В работе российских исследователей описан случай гигантоклеточного миокардита у пациента с ВИЧ-инфекцией. Авторы подчеркивают, что ключевым звеном в патогенезе острого миокардита при ВИЧ-инфекции являются нарушения Т-клеточного звена иммунной системы [9].
У лиц пожилого и старческого возраста миокардит может быть одним из клинических проявлений злокачественных новообразований. Кроме того, у пациентов с онкологическими заболеваниями миокардит нередко развивается как осложнение лучевой терапии или агрессивной химиотерапии. Миокардит может развиваться на различных стадиях инфекционного процесса, нередко сочетаясь с патологией внутренних органов [10].
Оценить истинную частоту случаев миокардита затруднительно из-за неспецифичности его клинических проявлений, а также отсутствия рутинного проведения эндомиокардиальной биопсии. Как показано в Таблице, миокардит чаще вызывается инфекционными агентами (вирусы, бактерии, простейшие) и значительно реже — неинфекционными (токсины, вакцины, яды, радиация, гормоны, тяжёлые металлы). В клинической практике также выделяют аутоиммунный, паранеопластический миокардит и миокардит неясной этиологии. В настоящее время наблюдается тенденция к расширению этиологического спектра миокардита. Так, описан случай его развития у 36-летнего пациента после тяжёлого солнечного ожога. По данным авторов, заболевание сопровождалось выраженным болевым синдромом, достоверным повышением уровня высокочувствительного тропонина и изменениями на электрокардиограмме (ЭКГ), что вызвало затруднения при проведении дифференциальной диагностики между острым коронарным синдромом (инфаркт миокарда без поражения коронарного русла) и миокардитом [11].
В литературе также приводятся данные клинических исследований, демонстрирующих роль наследственной предрасположенности в развитии миокардита [12].
Согласно Далласским критериям, принятым в гистологической диагностике, различают достоверный и вероятный миокардит. В соответствии с клиническими рекомендациями Российской Федерации (2025 г), по течению заболевания выделяют следующие формы:
молниеносный (фульминантный), подострый, хронический активный, хронический персистирующий, гигантоклеточный и эозинофильный миокардит [13].
Таблица
ЭТИОЛОГИЯ МИОКАРДИТОВ
|
Вирусы |
Бактерии |
Другие факторы |
|
Парвовирус В19 |
Chlamydia |
Протозойные инфекции |
|
Грипп (вирус гриппа А2) |
Legionella |
Риккетсии |
|
Аденовирус 2-го и 5-го типов |
Brucella |
Спирохеты |
|
Вирус герпеса человека 6 типа |
Mycobacterium tuberculosis complex |
Грибы |
|
Энтеровирус |
Corynebacterium diphtheriae |
Гельминты |
|
Вирус простого герпеса |
Streptococcus pyogenes |
Паразитарная инфекция |
|
Цитомегаловирус |
Corynebacterium diphtheria |
Аутоантигены |
|
Вирус Эпштейн-Барр |
Mycoplasma |
Лекарственные препараты |
|
Коронавирусы |
Staphylococcus |
Тяжелые металлы |
|
Вирус гепатита В |
Haemophilus influenzae |
Аллергены |
|
ЕСНО |
Гормоны |
|
|
ВИЧ-инфекция |
Витамины |
|
|
Энтеровирус Коксаки В |
Яды |
|
|
Вирус Коксаки |
Физические агенты |
|
|
Эпидемический паротит |
Фосфор |
Накопленные научные и клинические данные подтверждают, что острый миокардит представляет собой преимущественно клинический диагноз, ограниченный временными рамками — менее одного месяца от появления первых симптомов до установления диагноза, а при проведении эндомиокардиальной биопсии — наличием морфологических признаков, характерных для активного воспаления миокарда [14].
Диагностические критерии острого миокардита включают: боли в грудной клетке (ассоциированные с сухим перикардитом или имеющие псевдоишемический характер); одышку, возникшую впервые или прогрессирующую как в покое, так и при физической нагрузке; учащённое сердцебиение; необъяснимые аритмии; эпизоды потери сознания или случаи внезапной сердечной смерти; а также необъяснимый кардиогенный шок [15].
Дополнительными клиническими критериями, поддерживающими диагноз острого миокардита, считаются: лихорадка выше 38°C в течение предыдущих 30 дней (с признаками или без признаков ОРВИ либо энтеровирусной инфекции), послеродовый период, а также наличие в анамнезе перенесённого миокардита. Цель работы — представить клиническое наблюдение острого миокардита, развившегося на фоне тяжёлой респираторной инфекции у молодого пациента.
Описание клинического случая. Пациент А., 38 лет, поступил 29.04.2025 г в 18:30 в многопрофильный госпиталь (г. Бишкек) с жалобами на одышку в покое, усиливающуюся при физической нагрузке, кашель с выделением слизисто-гнойной мокроты, повышение температуры тела до 39,8°C, тошноту, рвоту, жидкий стул (5-6 раз в сутки), выраженную мышечную слабость и учащённое сердцебиение. Анамнез заболевания: заболевание началось 25.04.2025 г. с повышения температуры тела до 39,8°C, сердцебиения, одышки и выраженной мышечной слабости. По словам родственников, в течение двух суток пациент находился на домашнем лечении, самостоятельно принимал жаропонижающие препараты без выраженного клинического эффекта. 27.04.2025 г в 20:32 был доставлен родственниками в приёмное отделение терапевтического стационара по месту жительства. После осмотра врачом-терапевтом, с клиникой артериальной гипотонии и диареи, пациент был госпитализирован в отделение реанимации инфекционной больницы, где ему установлен клинический диагноз: бактериальная кишечная инфекция неуточнённая, тяжёлой формы, осложнённая гиповолемическим шоком
Объективный статус на момент осмотра: сознание оглушённое, по шкале комы Глазго (GCS) — 13 баллов.
Проведены клинико-лабораторные исследования: общий анализ крови (ОАК): гемоглобин — 138 г/л, эритроциты — 4,5×10¹²/л, тромбоциты — 150×10⁹/л, лейкоциты — 7,1×10⁹/л, лимфоциты — 31%, моноциты — 6%, СОЭ — 8 мм/ч. Общий анализ мочи (ОАМ): без патологических изменений. ОАК в динамике: гемоглобин — 95 г/л, эритроциты — 3,1×10¹²/л, тромбоциты — 133×10⁹/л, лейкоциты — 13,8×10⁹/л, лимфоциты — 8%, моноциты — 2%, СОЭ — 2 мм/ч. Биохимия крови: глюкоза венозная — 3,0 ммоль/л; С-реактивный белок (СРБ) — 48 мг/л (норма: 0,00-8,00); фибриноген — 3800 мг/л. Активность печёночных ферментов — в пределах референтных значений. У пациента отмечались принаки белкового дефицита: общий белок — 32 г/л; альбумин — 26 г/л. Функция почек: креатинин — 83,0 мкмоль/л (норма: 44,0-84,0); остаточный азот — 19,2 ммоль/л (норма: 10,6-24,4); мочевина — 6,4 ммоль/л (норма: 1,7-8,3); СКФ по формуле CKD-EPI — 103 мл/мин.
Инструментальная диагностика : по данным УЗИ внутренних органов и малого таза патологических изменений не выявлено, за исключением небольшого скопления жидкости в правой плевральной полости объёмом 50 мл.
Микробиологическое исследование : посев на энтеропатогенные микроорганизмы (БП22: дизентерийная и тифо-паратифозная группы) — отрицательный результат. Полученное лечение: цефтриаксон, глюконат кальция, раствор Рингера, альбумин, дофамин, фамотидин. Анамнез жизни: контакта с инфекционными больными не отмечает. Курит на протяжении многих лет.
При поступлении : общее состояние пациента расценено как крайне тяжёлое. Сознание ясное, на вопросы отвечает адекватно, но с некоторым замедлением. Кожные покровы и видимые слизистые оболочки бледные, с незначительным иктеричным оттенком. Отмечается выраженное набухание шейных вен, пастозность голеней и стоп. Частота дыхания — 26 в минуту. Сатурация кислорода на атмосферном воздухе в покое — 87-88%. При аускультации — незвучные влажные хрипы в нижних отделах лёгких. Частота сердечных сокращений (ЧСС) — 86 в минуту, артериальное давление (АД) — 120/80 мм рт. ст. Границы относительной сердечной тупости смещены влево на 1 см от средней ключичной линии. I тон на верхушке сердца ослаблен. Живот мягкий, безболезненный при пальпации. Печень безболезненная, не выступает из-под края рёберной дуги. Селезёнка не увеличена. Почки не пальпируются. Симптом поколачивания по поясничным областям отрицательный. По данным ЭКГ от 29.04.2025 — умеренная синусовая тахикардия, подъём сегмента S-T в отведениях, отражающих переднюю стенку левого желудочка (Рисунок 1).
Инструментальные методы исследования. По данным ультразвукового исследования (УЗИ) органов брюшной полости выявлены сонографические признаки хронического холецистита и кисты левой почки. В плевральных синусах с обеих сторон определяется скопление жидкости: справа — 385-400 мл, слева — 400-450 мл. При УЗИ щитовидной железы патологии не обнаружено. По данным УЗИ предстательной железы — эхографические признаки очагового фиброза в левой доле. Компьютерная томография (КТ) органов грудной клетки выявила признаки правосторонней полисегментарной пневмонии, двустороннего экссудативного плеврита, а также участки фиброзно-пневмосклеротических изменений в проекциях сегментов S9 и S10 правого лёгкого, и S5, S6, S9, S10 левого лёгкого (остаточные изменения после ранее перенесённого воспалительного процесса). Кроме того, отмечаются умеренно выраженная лимфоаденопатия, частичная кальцинация внутригрудных лимфатических узлов паратрахеальной группы центрального средостения, признаки кардиомегалии и кальцинация левой коронарной артерии.
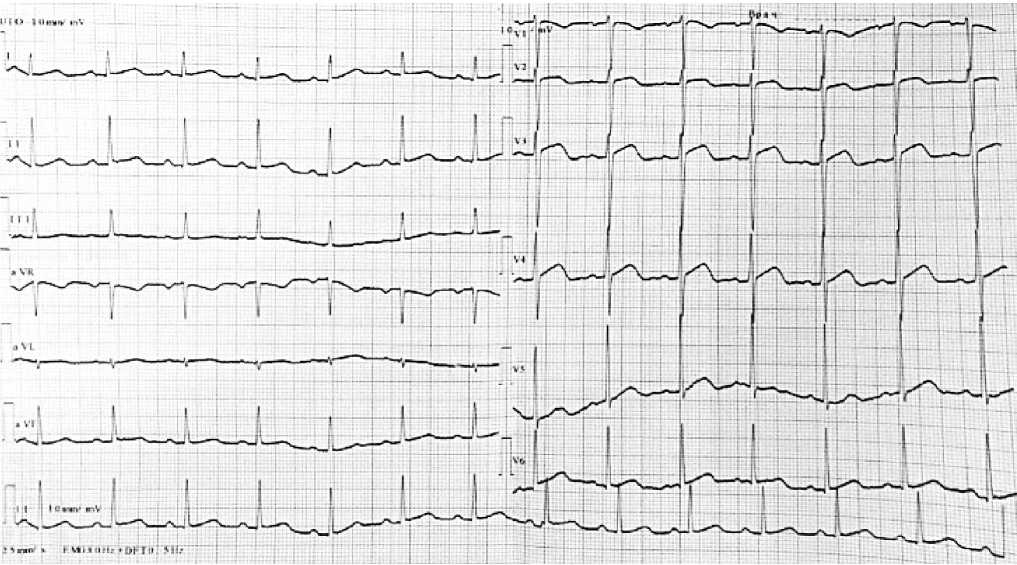
Рисунок. Электрокардиография пациента А., 38 лет
Эхокардиография. По данным ультразвукового исследования сердца у пациента А., 38 лет: толщина межжелудочковой перегородки — 0,9 см, задней стенки левого желудочка (ЛЖ) — 0,9 см. Фракция выброса ЛЖ (по Симпсону) — 38%. Размер левого предсердия — 4,5 см. Конечный систолический размер ЛЖ — 4,2 см, конечный диастолический размер ЛЖ — 6,1 см. Конечный систолический объём ЛЖ — 72 мл (референс: 18–68 мл), конечный диастолический объём ЛЖ — 168 мл (референс: 59–157 мл). Размер правого желудочка — 2,2 см, толщина его передней стенки — 0,4 см. Систолическое давление в лёгочной артерии — 32 мм рт. ст. Выявлены диффузный гипокинез миокарда ЛЖ, снижение систолической функции и нарушение процессов диастолического расслабления. Полости левых отделов сердца расширены. Перикард — без патологических изменений (Рисунок 2, 3, 4). Отмечены признаки атеросклеротического поражения аорты, аортального и митрального клапанов. Допплерографическое ультразвуковое исследование сонных и бедренных артерий: кровоток сохранён, признаков структурных и функциональных нарушений не выявлено. При обследовании венозных сосудов верхних и нижних конечностей тромбоз не диагностирован.
ОАК: гемоглобин — 118 г/л, гематокрит — 33,7%, эритроциты — 3,64×10¹²/л, тромбоциты —150×10⁹/л, лейкоциты — 23,01×10⁹/л, лимфоциты — 2,4%, моноциты — 3,1%, эозинофилы — 0,0%, базофилы — 0,0%. Скорость оседания эритроцитов (СОЭ) — 80 мм/ч.
ОАМ: протеинурия — белок 150 мг/л, лейкоцитурия — 98 лейкоцитов в поле зрения, эритроцитурия — 23 неизменённых и 10 изменённых эритроцитов в поле зрения.
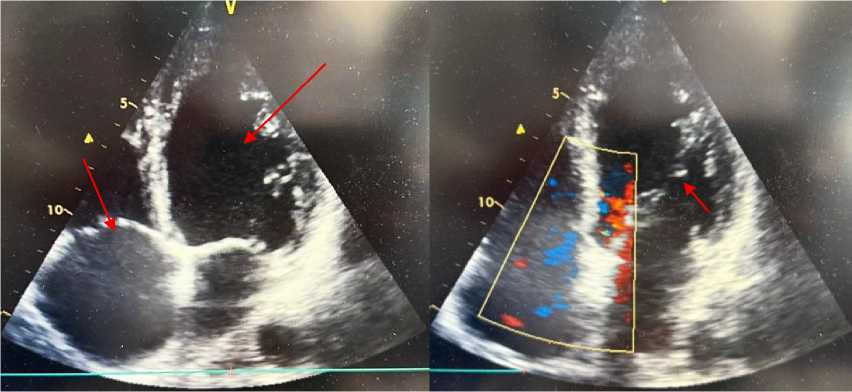
Рисунок 2. Эхокардиографическая картина миокардита у пациента А., 38 лет. Увеличение полости левого желудочка и митральная регургитация
Биохимический анализ крови: углеводный обмен : глюкоза венозной крови натощак — 7,11 ммоль/л. Белковый обмен: альбумин — 34,3 г/л (референс: 35,0-50,0). Ферменты поджелудочной железы: альфа-амилаза — 113 U/L (норма: 20–220), липаза — 96,2 U/L (норма: 13-60). Печёночные пробы: общий билирубин — 6,9 мкмоль/л (норма: 3,4–21,0); гамма-глутамилтрансфераза (ГГТ) — 71 Ед/л (норма: 0–49); аспартатаминотрансфераза (АсТ) — 57,2 Ед/л (норма: 0–49); аланинаминотрансфераза (АлТ) — 88,2 Ед/л (норма: 0–49). Ферритин: 680,2 нг/мл (референс: 30,0-400,0).
Маркеры воспаления: С-реактивный белок (СРБ) — 153,81 мг/л (норма: 0,00-8,00), фибриноген — 6230 мг/л (норма: 2000–4000), прокальцитонин — 21,06 нг/мл (норма: <0,05), D-димер — 4,64 мг FEU/л (норма: 0-0,55).
Показатели липидного обмена: общий холестерин — 3,39 ммоль/л, холестерин липопротеинов высокой плотности (ЛПВП) — 0,74 ммоль/л, холестерин липопротеинов низкой плотности (ЛПНП) — 2,46 ммоль/л, триглицериды — 2,12 ммоль/л.
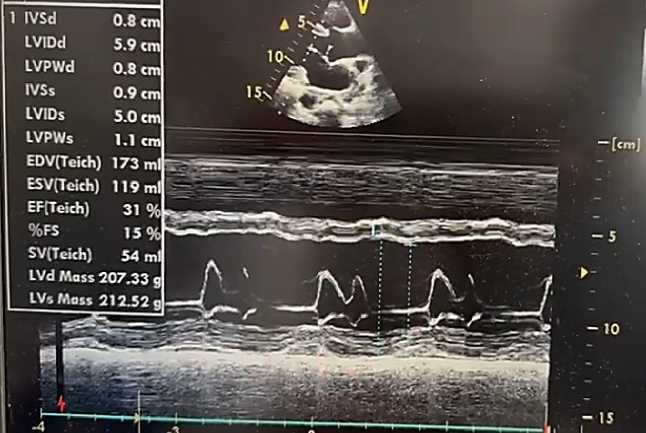
Рисунок 3. Эхокардиография пациента А., 38 лет с миокардитом. В М-режиме графическое движение стенок сердца и створок клапанов во времени / оценка систолической функции желудочков
Свертывающая система крови: протромбиновое время 12,7 сек (норма: 13,00-16,00), тромбиновое время 17,4 сек (норма: до 30 сек), АЧТВ 24,0 сек (норма: 23,50-39,00), РФМК 10,0 мг/100мл (норма: 3,50-4,50). Протромбиновый индекс 100,0% (норма: 80.00-100,0), МНО 1,00 ед. (норма: 1,00-1,40).
Показатели электролитного обмена: уровень калия составил 4,30 ммоль/л (норма: 3,305,50), натрия — 137 ммоль/л (норма: 130,00-155,00), кальция — 2,04 ммоль/л (норма: 2,152,50), магния — 0,96 ммоль/л (норма: 0,75-1,10).
Кардиоспецифические маркеры: тропонин I – 0,166 (норма: 0,40-3,00). Мозговой натрийуретический пептид 530 пг/мл (норма: 0,00-300,0). Лактатдегидрогеназа 212 МЕ/л (норма: 135,00-225,00).
Функция щитовидной железы: Т3 — 0,602 нмоль/л (норма: 1,08-3,14), Т4 — 116 нмоль/л (норма: 59,00-135,00), ТТГ — 1,22 мМЕ/л (норма: 0,40-4,00). Ревматоидный фактор 22,9 МЕ/мл (норма:0,00-14,00). HLA B27 в сыворотке не обнаружен.
Антитела к фосфолипидам : антитела к кардиолипину IgM — 21 Ед/мл (норма до 44 антител нет); антитела к кардиолипину IgG — 6 Ед/мл (норма до 48 антител нет).
Цитокины: интерлейкин 6-7,9 пг/мл (норма: 0,00-10,00), интерлейкин 10-0,01 пг/мл (норма: 0,00-31,00).
Антитела к цитомегаловирусу: антитела класса IgМ — отрицательный. Антитела класса IgG — положительный (2,03 при норме менее 1).
Антитела к вирусу простого герпеса 1 и 2 типы: антитела класса IgМ — отрицательный. Антитела класса IgG — положительный (3,20 у.е/мл при норме менее 2 у.е/мл).
Антитела к вирусу Эпштейн-Барра, VCA (капсадный антиген вируса): антитела класса IgМ — отрицательный. Антитела класса IgG — положительный (28,2 AU/ml при норме 0,002,00).
Функциональный статус почек: креатинин — 84,0 мкмоль/л (норма: 44,0–84,0); остаточный азот — 26,1 ммоль/л (норма: 10,6-24,4); мочевина — 9,1 ммоль/л (норма: 1,7-8,3); цистатин C — 1,03 мг/л (норма: 0,47-1,09); СКФ по формуле CKD-EPI — 100 мл/мин. СКФ по цистатину С — 81 мл/мин.
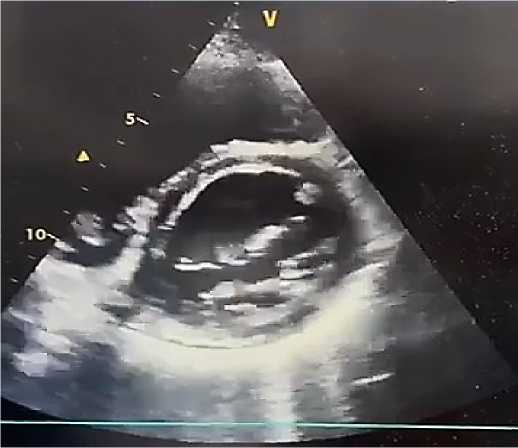
Рисунок 4. Эхокардиография пациента А., 38 лет с миокардитом. Парастернальная позиция, короткая ось на уровне митрального клапана
Клинический диагноз. Основное заболевание: двусторонняя полисегментарная пневмония вирусно-бактериальной этиологии, тяжёлого течения. Острый миокардит. Двусторонний плеврит. Острый респираторный дистресс-синдром (ОРДС), II стадия.
Осложнения: острая дыхательная недостаточность II–III степени. Сердечная недостаточность III функционального класса.
Проводимая терапия: Пациент получал комплексное лечение, включавшее: антибактериальную терапию — цефтриаксон, глюкокортикоиды — дексаметазон, антикоагулянты — гепарин, гепатопротектор — гептрал, диуретик — верошпирон, блокатор H₂-гистаминовых рецепторов — квамател, спазмолитик миотропного действия — дюспаталин, антагонист лейкотриеновых рецепторов — монтелукаст, синбиотик (пробиотик + пребиотик) — нормобакт, противодиарейное средство — лоперамид. На фоне проводимой терапии отмечено улучшение состояния: прекратилась диарея, одышка в покое не наблюдается, исчезло чувство сердцебиения, кашель значительно уменьшился, повысилась толерантность к физическим нагрузкам.
ОАК в динамике: гемоглобин — 148 г/л, гематокрит — 41,9%, эритроциты — 4,62×10¹²/л, тромбоциты — 251×10⁹/л, лейкоциты — 10,79×10⁹/л, лимфоциты — 8,2%, моноциты 5,6%, эозинофилы — 0,0%, базофилы – 0,1%, СОЭ — 38 мм/ч.
ОАК при выписке из стационара: гемоглобин — 144 г/л, гематокрит — 42,0%, эритроциты — 4,57×10¹²/л, тромбоциты — 314×10⁹/л, лейкоциты — 5,61×10⁹/л, лимфоциты — 30,3%, моноциты 6,0%, эозинофилы — 2,4%, базофилы – 0,3%, СОЭ — 12 мм/ч. Ревматоидный фактор 0 МЕ/мл (норма: 0,00-14,00).
На фоне терапии наряду с улучшением общего состояния пациента отмечались положительные сдвиги со стороны биохимии крови: глюкоза венозной крови натощак — 4,78 ммоль/л; альбумин — 33,6 г/л (норма: 35,0-50,0); СРБ 3,34 мг/л (норма: 0,00-8,00), прокальцитонин 0,51 нг/мл (норма: менее 0,05). Д-димер 0,98 мкг/мл (норма: 0-0,55).
Пациент продолжает наблюдаться на клинической базе кафедры факультетской терапии. По данным эхокардиографии от 23.05.2025 г: толщина межжелудочковой перегородки 0,9 см, толщина задней стенки ЛЖ 1,0 см, фракция выброса ЛЖ 63 (Simpson), размер левого предсердия 3,1 см, конечный систолический размер ЛЖ 3,1 см, конечный диастолический размер ЛЖ 5,0 см, конечный систолический объем ЛЖ 72 мл (18-68), конечный диастолический объем ЛЖ 82 мл (59-157), правый желудочек 2,2 см, толщина передней стенки правого желудочка 0,4 см, систолическое легочное давление 38 мм рт. ст., легочная артерия не расширена. Перикард без особенностей. Сократительная функция ЛЖ не нарушена.
Обсуждение
В последние десятилетия клинический интерес исследователей сосредоточен на воспалительно-дистрофических изменениях сердечной мышцы, в частности, миокардитах. Пандемия новой коронавирусной инфекции продемонстрировала значимую роль вирусных агентов в развитии воспалительных поражений миокарда [16, 17].
При миокардите в воспалительный процесс вовлекаются как кардиомиоциты, так и интерстициальная ткань. В одном из клинических наблюдений у молодой пациентки с миокардитом и ВИЧ-инфекцией при аутопсии была выявлена диффузная инфильтрация межмышечной стромы эозинофилами, лимфоцитами, плазмоцитами, множественными гигантскими многоядерными клетками, а также очаги некроза [9].
Острый миокардит, как правило, протекает тяжело и сопровождается неблагоприятным прогнозом. В недавно опубликованной работе описан случай острого миокардита с летальным исходом у 40-летнего мужчины. Согласно данным аутопсии, отмечены увеличение массы сердца, дилатация полостей желудочков, пристеночные тромбы в предсердиях и желудочках. Гистологически диагностирован диффузно-очаговый миокардит с выраженной дистрофией и некрозом кардиомиоцитов [14].
Как следует из данных литературы, поражение сердечной мышцы может быть обусловлено вирусной или бактериальной инвазией [18].
Клиническая симптоматика миокардита варьирует от малосимптомного до злокачественного течения. Тяжесть проявлений зависит от этиологического фактора, возраста пациента и наличия сопутствующих заболеваний. Основные симптомы — одышка, утомляемость и периферические отеки — как правило, развиваются постепенно, в течение от двух недель до трёх месяцев. Важно отметить, что ни один из симптомов не является специфичным для миокардита. Наиболее частыми триггерами миокардита служат острые респираторные вирусные инфекции (ОРВИ), среди которых ключевое значение отводится аденовирусам и энтеровирусам. Диагностика вирусной этиологии требует проведения серологических исследований. У пациента А., 38 лет, с установленным диагнозом острого миокардита, при серологическом исследовании были выявлены антитела класса IgG к цитомегаловирусу, вирусу простого герпеса 1 и 2 типов, а также вирусу Эпштейна–Барр (Epstein-Barr nuclear antigen 1 (EBNA1). Однако следует подчеркнуть, что вирусная серология обладает ограниченной специфичностью, и выявление IgG-антител чаще свидетельствует о предшествующем контакте с возбудителем, а не об активной фазе инфекции. Учитывая высокую распространённость кардиотропных вирусов в популяции, положительные серологические тесты не могут служить единственным основанием для постановки диагноза миокардита. Как уже отмечалось, «золотым стандартом» верификации миокардита остаётся эндомиокардиальная биопсия, однако в рутинной клинической практике данный метод применяется крайне редко. Окончательное подтверждение диагноза «миокардит» возможно только по результатам гистологического исследования [16].
Согласно клиническим рекомендациям и данным наблюдений, проведение эндомиокардиальной биопсии показано при тяжёлом клиническом течении, дилатации полостей сердца, выраженной сердечной недостаточности, тяжёлых нарушениях ритма и/или проводимости [12].
Метод также оправдан при подозрении на гигантоклеточный или эозинофильный миокардит. Эндомиокардиальная биопсия (Endomyocardial biopsy) рекомендуется и при подостром течении миокардита, сопровождающемся острой сердечной недостаточностью, устойчивой к терапии; при её прогрессировании, несмотря на проводимое лечение; при возникновении жизнеугрожающих аритмий, сочетании СН с лихорадкой и эозинофилией; при системных заболеваниях соединительной ткани; а также саркоидозе, амилоидозе и гемохроматозе [18].
В диагностике миокардитов основными ориентирами служат анамнестические сведения, клинико-лабораторные показатели и результаты эхокардиографии. Для уточнения диагноза острого миокардита важное значение имеет проведение магнитно-резонансной томографии (МРТ) сердца. Как подчёркивают исследователи, МРТ с внутривенным контрастированием гадолинием в настоящее время считается одним из наиболее информативных методов визуализации воспалительных изменений миокарда [3, 4].
Это объясняется тем, что комплексы гадолиния обладают парамагнитными свойствами, не проникают через интактные клеточные мембраны и накапливаются в межклеточном пространстве. При повреждении клеток ионы гадолиния проникают внутрь, что позволяет визуализировать участки воспалительного отека, фиброза и некроза тканей. Широко применяется термин Lake Louise Criteria, объединяющий диагностические МРТ-признаки миокардита. Одним из ключевых преимуществ МРТ является способность дифференцировать воспалительные поражения миокарда от ишемических. Так, при миокардите характерно субэпикардиальное или трансмуральное накопление контрастного вещества, в то время как при инфаркте миокарда наблюдается субэндокардиальное накопление. Для миокардиальной дистрофии типично интрамиокардиальное распределение контраста. Накопление гадолиния в области сосочковых мышц может свидетельствовать о саркоидозе. Следует учитывать, что отсроченное контрастирование не всегда указывает на наличие активного воспаления, поскольку также встречается при фиброзе. Максимальная информативность МРТ с усилением достигается в острой фазе миокардита, когда наиболее выражены признаки воспаления.
Связь между снижением систолической функции левого желудочка (ЛЖ) и его дилатацией на фоне инфекционного процесса делает миокардит более вероятным диагнозом. Одышка при минимальной физической нагрузке является ранним и важным признаком левожелудочковой дисфункции. Она может усиливаться в положении лёжа из-за увеличения венозного притока к правым отделам сердца [5].
Этот патофизиологический механизм полностью подтверждается нашим клиническим наблюдением: у пациента А., 38 лет, расширение левых камер сердца и нарушение глобальной систолической функции ЛЖ сочетались с выраженной респираторной инфекцией. Как отмечено выше, лимфопения и гипопротеинемия предшествовали развитию клинически манифестного миокардита. Характерным признаком воспалительного поражения миокарда является увеличение частоты сердечных сокращений (ЧСС) в покое ≥80 уд./мин. Тахикардия у таких пациентов обусловлена активацией симпатоадреналовой системы в ответ на снижение сократительной функции ЛЖ. Электрокардиографические (ЭКГ) изменения при миокардите, как правило, неспецифичны. В остром и подостром периодах нередко наблюдаются нарушения проводимости — брадикардия, атриовентрикулярные блокады различной степени, блокады ножек пучка Гиса, а также нарушения возбудимости — желудочковые экстрасистолы, нередко с потенциально злокачественным течением [19].
При хроническом миокардите чаще выявляется синусовая тахикардия, реже — брадикардия (при очаговой форме заболевания). Согласно литературным данным, аритмии встречаются примерно у 30% пациентов, перенёсших миокардит, включая случаи лёгкой и средней тяжести [10].
Появление желудочковых аритмий и/или А–В-блокад может указывать на наличие гигантоклеточного, лимфоцитарного или саркоидного миокардита [2].
Важно учитывать, что изменения в конечной части комплекса QRS свидетельствуют о массивном поражении миокарда и нарастающей сердечной недостаточности. У нашего пациента на ЭКГ регистрировалась умеренная синусовая тахикардия и незначительный подъём сегмента ST по передней стенке ЛЖ (Рисунок 1). Эти изменения, а также повышение уровня тропонина I при остром миокардите могут симулировать картину инфаркта миокарда. Как упоминалось ранее, МРТ сердца с контрастированием является высокоинформативным методом верификации диагноза. Однако в данном клиническом случае проведение МРТ оказалось невозможным из-за выраженного снижения диуреза и тяжёлой церебральной гипоксии, развившихся в период интенсивной терапии. Согласно опубликованным данным, иммунная реакция в миокарде приводит к структурным и функциональным изменениям кардиомиоцитов, что, в свою очередь, вызывает либо локальное, либо системное снижение сократительной способности сердечной мышцы, дилатацию ЛЖ и/или нарушение проводящей системы сердца [20].
У пациента А., 38 лет, при эхокардиографическом исследовании отмечалось увеличение конечного диастолического размера ЛЖ и снижение его сократительной функции. Острый миокардит часто сопровождается неспецифической клинической симптоматикой: одышкой, учащённым сердцебиением, болями в грудной клетке. По мере прогрессирования воспалительного процесса возможно накопление жидкости в серозных полостях. В ряде исследований описано развитие двустороннего плеврального выпота при острых формах миокардита [9].
Подобная находка была зарегистрирована и у нашего пациента: по данным ультразвукового исследования визуализировался двусторонний экссудативный плеврит. С точки зрения клинико-морфологической классификации, большинство авторов выделяет следующие формы миокардита: псевдокоронарная форма (характеризуется болями в грудной клетке, имитирующими острый коронарный синдром); форма с явлениями застойной сердечной недостаточности (сопровождается снижением сократительной функции ЛЖ вплоть до развития кардиогенного шока); аритмическая форма (на первый план выходят симптомы нарушения проводимости и/или возбудимости: экстрасистолия ,блокады, тахи- или брадикардия); смешанная форма — сочетает признаки сердечной недостаточности, сохраняющейся от 2 недель до 3 месяцев (острая форма) или более 3 месяцев (хроническая форма) при отсутствии другой очевидной причины [3, 4, 20].
Клиницистам важно помнить, что при миокардитах, особенно с хроническим течением, часто выявляются признаки систолической дисфункции и ЛЖ при эхокардиографическом исследовании. Однако при длительно персистирующем миокардите эти изменения могут отсутствовать, несмотря на выраженное нарушение глобальной сократительной функции. Согласно литературным данным, показатели отсроченного накопления гадолиния при проведении МРТ сердца могут служить маркером неблагоприятного прогноза у пациентов с миокардитом даже с сохранённой фракцией выброса ЛЖ [21].
Повышение уровня кардиоспецифических маркеров — креатинфосфокиназы (КФК) и/или тропонина I — отражает степень повреждения миокарда и наиболее характерно для диффузных форм миокардита. Следует подчеркнуть, что миокардит — это полиэтиологическое заболевание, обусловленное широким спектром факторов: инфекционных, иммунных, аллергических, токсических, химических, физических, а также нарушениями обмена веществ. Наибольшая частота миокардитов наблюдается у лиц молодого и среднего возраста, при этом в подавляющем большинстве случаев заболевание имеет инфекционно-аллергическую природу. Что касается терапии, то при лёгких формах миокардита зачастую наблюдается спонтанное выздоровление без применения специфического лечения. При выраженных клинических проявлениях терапия подбирается с учётом предполагаемой этиологии и может включать глюкокортикостероиды, иммунодепрессанты, диуретики, антикоагулянты, ингибиторы ренин-ангиотензин-альдостероновой системы, препараты из группы ингибиторов натрий-глюкозного котранспортёра 2 типа и другие средства. При тяжёлом или крайне тяжёлом течении миокардит может привести к развитию постмиокардитического кардиосклероза и дилатационной кардиомиопатии, что в отдельных случаях требует трансплантации сердца.
Представленный клинический случай подчёркивает острое начало миокардита и его тесную связь с тяжёлой респираторной инфекцией, что должно быть учтено при диагностическом поиске и выборе тактики лечения пациентов с подобной клинической картиной.
Заключение
Миокардит остаётся одной из наименее изученных нозологических форм среди заболеваний системы кровообращения. В настоящей статье представлены результаты клинического наблюдения острого миокардита у 38-летнего пациента с двусторонней пневмонией. Диагноз острого миокардита был установлен на основании совокупности данных: анамнеза (отсутствие сердечно-сосудистых заболеваний в прошлом, развитие симптомов сердечной недостаточности на фоне респираторной инфекции); клинической картины (одышка в покое, усиливающаяся при физической нагрузке, повышение температуры тела до 39,8°C, учащённое сердцебиение, набухание шейных вен, пастозность голеней и стоп, частота дыхания — 26 в минуту, сатурация кислорода на атмосферном воздухе в покое — 87-88%, расширение границ относительной сердечной тупости влево на 1 см кнаружи от левой среднеключичной линии, ослабление I тона на верхушке сердца); данных эхокардиографии (снижение сократительной функции левого желудочка, расширение полостей сердца); лабораторных показателей (лейкоцитоз — 23,01×10⁹/л, лимфопения — 2,4%, ускоренная СОЭ — 80 мм/ч, гипопротеинемия — общий белок 32 г/л, гипоальбуминемия — 26 г/л, повышение уровня С-реактивного белка — 153,81 мг/л, фибриногена — 6230 мг/л (норма: 2000–4000), прокальцитонина — 21,06 нг/мл (норма: <0,05), Д-димера — 4,64 мг FEU/л (норма: 0–0,55), ферритина — 680,2 нг/мл (норма: 30-400), мозгового натрийуретического пептида — 530 пг/мл (норма: 0–300), ревматоидного фактора — 22,9 МЕ/мл (норма: 0-14), липазы — 96,2 U/I (норма: 13-60), а также активности печёночных трансаминаз и ГГТ). Дополнительно выявлялись протеинурия и гипертриглицеридемия. При серологическом исследовании было зафиксировано повышение титров антител класса IgG к цитомегаловирусу, вирусу простого герпеса (1 и 2 типов) и вирусу Эпштейна–Барр. Представленный клинический случай иллюстрирует развитие типичного острого миокардита, возникшего на фоне респираторной инфекции. Полиморфизм и неспецифичность симптомов, сопровождающих острый миокардит на фоне инфекционного заболевания, затрудняют своевременную диагностику и выбор адекватной терапевтической тактики. Важно подчеркнуть, что при наличии респираторной инфекции, особенно сопровождающейся дыхательной недостаточностью, целесообразно проведение эхокардиографического исследования и определение уровня натрийуретического пептида в сыворотке крови. Эти методы позволяют не только исключить тромбоэмболические осложнения, но и объективно оценить сократительную функцию желудочков сердца.
Вклад авторов. Все авторы подтверждают соответствие своего авторства согласно международным критериям ICMJE. Авторский вклад (по системе Credit): Муркамилов И.Т. – проведение исследования, верификация данных, создание черновика рукописи, визуализация; Айтбаев К.А. – концептуализация; Муркамилова Ж.А. – создание рукописи, методология; Райимжанов З.Р., Солижонов Ж.И., Гасанов К.А., Закиров О.Т., Хакимов Ш.Ш., Ыманкулов Д.С., Хабибуллаев К.К., Абдибалиев И.А. - проведение исследования, ресурсы и методология.
Прозрачность исследования. Исследование не имело спонсорской поддержки. Авторы несут полную ответственность за предоставление окончательной версии рукописи в печать.
Декларация о финансовых и других взаимоотношениях. Все авторы принимали участие в разработке концепции статьи и в написании рукописи. Окончательная версия рукописи была одобрена всеми авторами. Авторы не получали гонорар за статью.


