Мобилизация селезеночного изгиба при резекциях прямой кишки
Автор: Черниковский И.Л., Алиев И.И., Смирнов А.А., Саванович Н.В., Гаврилюков А.В.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Опыт работы онкологических учреждений
Статья в выпуске: 5 т.16, 2017 года.
Бесплатный доступ
Введение. Мобилизация селезеночного изгиба (МСИ) толстой кишки представляется достаточно сложным и длительным этапом лапароскопической операции, который сопряжен с возможными интра- и послеоперационными осложнениями. Дополнительные трудности возникают и по причине отсутствия общепринятой методики МСИ. Несмотря на достаточное количество публикаций по данной теме, вопрос о целесообразности рутинной МСИ при низких резекциях прямой кишки остается открытым. Цель - представить стратегию МСИ, принятую в нашей клинике, а также результаты хирургического лечения пациентов, перенесших низкие резекции прямой кишки, которым выполнялась или не выполнялась МСИ. Методы. Было проведено 2 ретроспективных анализа оперативных вмешательств. В первом случае были проанализированы результаты всех лапароскопических операций с МСИ (n=120). Во втором случае был проведен сравнительный анализ результатов операций с МСИ, из них 32 низкие передние резекции прямой кишки (НПРПК) и 20 брюшно-анальных резекций (БАР), в сравнении с НПРПК без МСИ (n=94). Результаты. При проведении первого анализа пациенты были разделены на 4 группы, перенесшие следующие лапароскопические операции: левостороннюю гемиколэктомию, низкую переднюю резекцию прямой кишки, колпроктэктомию, брюшно-анальную резекцию прямой кишки. При анализе интра- и послеоперационных осложнений значимых различий между группами не выявлено. При сравнении между группами НПРПК с МСИ и брюшно-анальных резекций с МСИ против НПРПК без МСИ выявлено, что различия в продолжительности операции, кровопотере, длительности госпитализации, количестве удаленных лимфоузлов были статистически незначимы. Несостоятельность анастомоза выявлена в 2 (6,3 %) случаях при НПРПК с МСИ, в 8 (8,5 %) - без МСИ и в 1 (5 %) случае при брюшно-анальной резекции (p=0,17). Выводы. При использовании данной методики лапароскопической МСИ можно добиться оптимальных результатов проведения этого сложного этапа операции. Рутинная мобилизация селезеночного изгиба при низких передних резекциях прямой кишки не является обязательной, так как не приводит к снижению частоты несостоятельности анастомозов и осложнений. Показано рутинное выполнение мобилизации селезеночного изгиба при лапароскопической БАР.
Колоректальный рак, лапароскопические операции, мобилизация селезеночного изгиба
Короткий адрес: https://sciup.org/140254143
IDR: 140254143 | УДК: 616.351-006-089:612.411 | DOI: 10.21294/1814-4861-2017-16-5-55-62
Mobilization of splenic flexure during rectal resection
Background. Splenic flexure mobilization (SFM) is a difficult step within both conventional and laparoscopic procedures, often associated with intra- and postoperative morbidity. Additional difficulties occur because of the lack of generally accepted methods for performing SFM. Despite many reports, the routine SFM during low rectal resections remains controversial. Aim. This paper presents the strategy for SFM used in our clinic, as well as the surgical treatment outcomes in patients who underwent low rectal resections with or without SFM. Methods. Two retrospective analyzes of the surgical procedures were made. In the first case, the results of all LS operations with SFM (n=120) were analyzed. In the second case, a retrospective analysis of the LS rectal resections was carried out (low anterior resection (LAR) with the SFM (n=32), pull-through rectal resection with the SFM (n=20) and LAR without SFM (n=94)). Results. In the first analysis, patients were divided into 4 groups: LS-left colectomy, LS-low anterior rectal resection, LS-colproctectomy, and LSpull-through rectal resection. There was no significant difference between the groups in terms of intra- and postoperative complications. In the second analysis, the differences in the operation time, blood loss and hospital stay between low rectal resections were not statistically significant.Anastomotic leakage was detected in 2 patients in the LAR with SFM group, in 8 patients (8.5 %, 8/94) in LAR without SFM group, and in 1 patient in pull-through rectal resection group (5 %, 1/20), p=0.17. Conclusions. Using the laparoscopic approach to SFM, optimal surgical outcomes can be achieved. Routine SFM during low anterior rectal resection is not necessary, because it does not lead to decreased incidence of anastomotic leakage and complications. Routine SFM during pull-through rectal resection is necessary.
Текст научной статьи Мобилизация селезеночного изгиба при резекциях прямой кишки
Введение. Мобилизация селезеночного изгиба (МСИ) толстой кишки представляется достаточно сложным и длительным этапом лапароскопической операции, который сопряжен с возможными интра- и послеоперационными осложнениями. Дополнительные трудности возникают и по причине отсутствия общепринятой методики МСИ. Несмотря на достаточное количество публикаций по данной теме, вопрос о целесообразности рутинной МСИ при низких резекциях прямой кишки остается открытым. Цель – представить стратегию МСИ, принятую в нашей клинике, а также результаты хирургического лечения пациентов, перенесших низкие резекции прямой кишки, которым выполнялась или не выполнялась МСИ. Методы. Было проведено 2 ретроспективных анализа оперативных вмешательств. В первом случае были проанализированы результаты всех лапароскопических операций с МСИ (n=120). Во втором случае был проведен сравнительный анализ результатов операций с МСИ, из них 32 низкие передние резекции прямой кишки (НПРПК) и 20 брюшно-анальных резекций (БАР), в сравнении с НПРПК без МСИ (n=94). Результаты. При проведении первого анализа пациенты были разделены на 4 группы, перенесшие следующие лапароскопические операции: левостороннюю гемиколэктомию, низкую переднюю резекцию прямой кишки, колпроктэктомию, брюшно-анальную резекцию прямой кишки. При анализе интра- и послеоперационных осложнений значимых различий между группами не выявлено. При сравнении между группами НПРПК с МСИ и брюшно-анальных резекций с МСИ против НПРПК без МСИ выявлено, что различия в продолжительности операции, кровопотере, длительности госпитализации, количестве удаленных лимфоузлов были статистически незначимы. Несостоятельность анастомоза выявлена в 2 (6,3 %) случаях при НПРПК с МСИ, в 8 (8,5 %) – без МСИ и в 1 (5 %) случае при брюшно-анальной резекции (p=0,17). Выводы. При использовании данной методики лапароскопической МСИ можно добиться оптимальных результатов проведения этого сложного этапа операции. Рутинная мобилизация селезеночного изгиба при низких передних резекциях прямой кишки не является обязательной, так как не приводит к снижению частоты несостоятельности анастомозов и осложнений. Показано рутинное выполнение мобилизации селезеночного изгиба при лапароскопической БАР.
Следует ли рутинно выполнять мобилизацию селезеночного изгиба ободочной кишки при передних и низких передних резекциях прямой кишки? Этот вопрос остается до конца нерешенным. Некоторые авторы считают, что МСИ является необходимым условием для формирования хорошо кровоснабжаемого колоректального анастомоза без натяжения [1]. Тем не менее опубликованы исследования, указывающие на то, что МСИ не влияет на непосредственные и отдаленные ре- зультаты операций при раке прямой кишки [2, 3]. Возможно, причиной разногласий является то, что мобилизация селезеночного изгиба представляется достаточно сложным и длительным этапом операции, сопряженным с возможными интра- и послеоперационными осложнениями (в первую очередь это ранение селезенки, повреждение хвоста поджелудочной железы, послеоперационный панкреатит). Кроме того, выполнение МСИ само по себе может привести к нарушению кровоснаб-
жения низводимого колотрансплантата. Известно, что данный этап хирургического вмешательства, как правило, требует расширения оперативного доступа (при лапаротомии) или постановки дополнительных рабочих портов и смены положения пациента на операционном столе. Сложности с МСИ возникают еще и по причине отсутствия общепринятой методики ее выполнения.
Помимо этого, селезеночный изгиб толстой кишки отличается большой вариабельностью сосудистой анатомии. В области СИ и нисходящей ободочной кишки находится зона слияния бассейнов верхней и нижней брыжеечных артерий. По сути, имеется 2 уровня анастомозирования указанных артериальных систем. Первый уровень – краевая артерия Драммонда, расположенная вдоль брыжеечного края нисходящей ободочной кишки. По данным R.M.S.V. Vadapalli et al. [7], последняя может отсутствовать у 4–20 % пациентов, и тогда принципиальное значение в сохранении кровоснабжения нисходящей ободочной кишки имеет дуга Риолана – анастомоз второго уровня, соединяющий левую ветвь средней ободочной артерии и левую ободочную артерию. Дуга Риолана встречается в подавляющем большинстве (60–90 %) случаев [8]. Однако по некоторым данным [9], в 43 % сосудистый анастомоз не выражен или слабо выражен, что обусловливает наличие так называемой точки Гриффита – участка критического кровоснабжения в этой зоне. Кроме того, нередки случаи, когда имеется нетипичное расположение левой ободочной артерии, участвующей в формировании дуги Риолана, что может приводить к ее повреждению при выполнении МСИ. В 20 % левая ободочная артерия отсутствует, в 33 % средняя толстокишечная артерия является основным питающим стволом [8]. В указанных случаях при высоком лигировании нижней брыжеечной артерии может нарушиться кровоснабжение СИ. Учитывая сложность и вариабельность анатомии СИ, следует пошагово отрабатывать методику МСИ для минимизации интраоперационных осложнений и снижения риска нарушения кровоснабжения низводимого колотрансплантата.
С внедрением в хирургическую практику лапароскопических (ЛС) и роботических технологий появились исследования, целью которых явилось изучение преимуществ и недостатков мини-инвазивных методик МСИ по сравнению с лапаротомным доступом. В работе J. Okuda et al. [10] проведена сравнительная оценка лапароскопических и традиционных резекций ободочной кишки с МСИ. Авторами прослеживаются классические плюсы и минусы лапароскопии: при ЛС вмешательствах меньше кровопотеря (p=0,011) и продолжительность госпитализации (p=0,001), но выше продолжительность операции (p=0,016) – 230 против 165 мин. По данным M.R. Marsden et al. [11], применение МСИ было одинаково безопасно при лапароскопических и открытых резекциях прямой кишки, но при открытых вмешательствах она выполнялась чаще – в 68 % против 32 % (p=0,001). Это косвенно свидетельствует о том, что хирурги считают лапароскопическую МСИ технически сложной процедурой и, несмотря на преимущества ЛС доступа, стараются избежать ее выполнения. На наш взгляд, указанный хирургический этап требует четкой методологии и стандартизации по аналогии с лапароскопической тотальной мезо-ректумэктомией (TME), что позволит уверенно и быстро выполнять МСИ в необходимых случаях.
В литературе описаны 4 способа лапароскопической МСИ: медиальный, латеральный, передний и в положении пациента на правом боку. Сегодня существует лишь одно исследование, сравнивающее эти способы [12]. Принципиально они отличаются тем, с какой стороны осуществляется доступ в сальниковую сумку. При медиальном способе (рис. 1) мобилизация начинается с лигирования нижних брыжеечных артерии и вены, доступ в сальниковую сумку осуществляется с каудальной стороны. При данном способе отмечается хорошая визуализация анатомических структур, способ удобен при высоком расположении селезеночного изгиба и у пациентов с избыточной массой тела [12]. При латеральном способе (рис. 2) в первую очередь осуществляется рассечение брюшины левого бокового канала, доступ в сальниковую сумку осуществляется с латеральной стороны. При переднем способе (рис. 3) доступ в сальниковую сумку осуществляется сверху, через желудочно-ободочную связку. Передний способ неудобен при висцеральном ожирении, спаечном процессе, облитерации сальниковой сум-
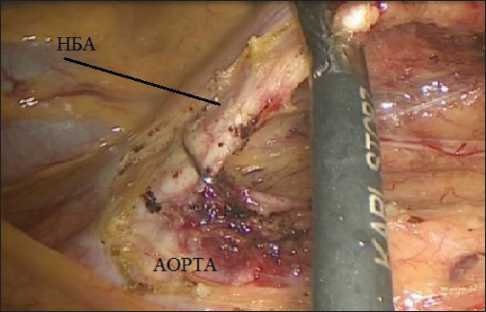
Рис. 1. Медиальный способ мобилизации селезеночного изгиба толстой кишки
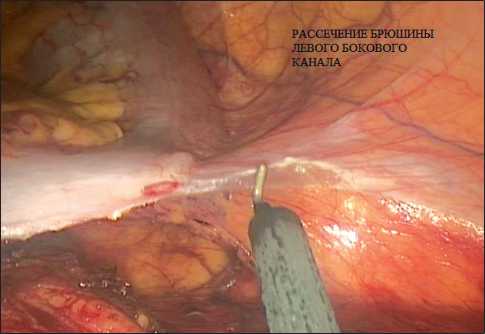
Рис. 2. Латеральный способ мобилизации селезеночного изгиба толстой кишки
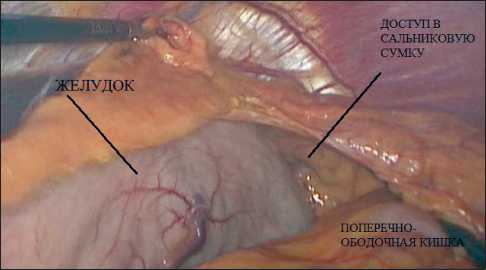
Рис. 3. Передний способ мобилизации селезеночного изгиба толстой кишки ки. По данным V. Benseler et al. [12], латеральный способ связан с большим числом интраоперационных осложнений, в первую очередь это повреждение селезенки – 17,7 % против 14,6 % – при медиальном и 10,6 % – при переднем (p=0,037). Способ МСИ в положении пациента на правом боку описан S. Gonsalves et al. [13] в небольшом исследовании, включающем 12 больных. Авторы сообщают об отсутствии интраоперационных осложнений, но данная методика требует специальной укладки пациента и операционного стола, позволяющего повернуть пациента практически вертикально.
В нашей клинике рутинно используется трехэтапная методика МСИ, предложенная проф. A. Parvaiz, однако не описанная в литературе [11]. Преимуществами данного способа являются:
-
- точная визуализация и полный контроль поджелудочной железы на всех этапах операции;
-
– контроль селезенки и области ее ворот;
-
– возможность выполнить удаление желудочно-сальниковой аркады при расширенной лимфодиссекции;
-
– малая продолжительность, в среднем – 15,5 (8–23) мин.
Считается, что МСИ является одним из самых трудных элементов лапароскопической колоректальной хирургии, сопоставимым по сложности с лапароскопической ТМЕ. Кривая обучения лапароскопической МСИ, с точки зрения ряда авторов, должна включать в себя не менее 50 самостоятельно выполненных хирургических процедур. Более того, есть мнение, что при низкой резекции прямой кишки следует начинать операцию с МСИ до перехода к ТМЕ, так как этот этап сложнее и требует большей концентрации хирурга [2, 11]. На наш взгляд, это спорное утверждение, поскольку не считаем необходимым рутинно выполнять МСИ при низких резекциях прямой кишки. Действительно, показания для МСИ не имеют однозначного решения. Некоторые авторы считают, что МСИ является необходимым условием для формирования хорошо кровоснабжаемого анастомоза без натяжения [1]. С другой стороны, существуют работы, указывающие на отсутствие различий в частоте интраоперационных осложнений, времени операции, кровопотере и несостоятельности колоректального анастомоза [3, 11] при выполнении МСИ и без. Ряд авторов указывают на то, что отказ от МСИ приводит к уменьшению длины удаляемого препарата толстой кишки и исследованию неадекватного количества лимфоузлов, что может привести к занижению стадии заболевания и отказу от проведения системной химиотерапии [14]. Однако в исследовании M. Katory et al. [2] при оценке отдаленных 6-летних результатов после передней резекции прямой кишки показано, что отказ от выполнения МСИ не влияет на онкологические результаты – не получено различий в количестве удаленных лимфоузлов (p=0,212) и в показателях
Таблица 1
Частота несостоятельности анастомоза при резекциях прямой кишки с МСИ и без применения этой методики, по данным литературы
Цель – представить стратегию применения МСИ, принятую в нашей клинике и провести оценку ее эффективности у больных, перенесших низкие резекции прямой кишки.
Материал и методы
Нами было проведено 2 ретроспективных анализа оперативных вмешательств. В первом случае были проанализированы результаты всех ЛС операций с МСИ (n=120), выполненных в отделении колопроктологии ГБУЗ «СПб КНПЦ СВМП(о)» в 2015–2016 гг. по поводу колоректального рака. В результате было сформировано 4 группы больных (табл. 2). Чаще всего МСИ проводили при ЛС левосторонней гемиколэктомии. Средний индекс массы тела (ИМТ) не отличался, однако в группах прослеживаются некоторые различия в гендерном соотношении.
Во втором случае был проведен ретроспективный анализ оперативных вмешательств с МСИ – НПРПК (n=32) и брюшно-анальных резекций
(n=20), а также НПРПК без МСИ (n=94), выполненных в 2015–2016 гг. Мужчин во всех группах оказалось достоверно больше: 22/10, 56/38 и 14/6 соответственно (p<0,05), но средний ИМТ не имел значимых различий (табл. 3).
В проведенном исследовании способ мобилизации селезеночного изгиба был условно разделен на 3 этапа и не имел различий при левосторонней гемиколэктомии и низкой резекции прямой кишки:
-
- медио-латеральная мобилизация: в латеральном направлении и краниально (максимально вверх) до нижнего края поджелудочной железы в эмбриональном слое вдоль фасции Герота с соблюдением техники CME (полная мезоколэктомия) (рис. 4);
-
– латеральная мобилизация – рассечение брюшины левого бокового канала до уровня селезеночно-ободочной связки (рис. 5);
– установка дополнительного 5-мм троакара в правом подреберье и пересечение желудочноободочной связки в бессосудистой зоне, сразу каудальнее желудочно-сальниковых сосудов; пересечение брыжейки поперечно-ободочной кишки под визуальным контролем нижнего края поджелудочной железы; пересечение селезеночноободочной связки (рис. 6).
При выполнении низкой передней резекции прямой кишки во всех случаях выполняли первые
Таблица 2
|
Объем выполненных операций |
||||
|
Показатель |
Левосторонняя гемиколэктомия |
Низкая передняя резекция прямой кишки |
Колпроктэктомия |
Брюшно-анальная резекция прямой кишки |
|
Число больных (n=120) |
66 (55,0 %) |
32 (26,7 %) |
2 (1,7 %) |
20 (16,7 %) |
|
Соотношение мужчин/женщин |
26:40 |
22:10 |
2:0 |
14:6 |
|
ИМТ, кг/м2 |
29 |
27 |
26 |
27 |
|
(23–36) |
(20–46) |
(25–28) |
(20–46) |
Таблица 3
Характеристика клинического материала (лапароскопические низкие резекции прямой кишки)
|
Показатель |
Низкая передняя резекция прямой кишки с МСИ (n=32) |
Объем выполненных операций Низкая передняя резекция прямой кишки без МСИ (n=94) |
Брюшно-анальная резекция прямой кишки (n=20) |
|
Соотношение мужчин/женщин |
22:10 |
56:38 |
14:6 |
|
27 |
31 |
27 |
|
|
ИМТ, кг/м2 |
(20–46) |
(23–39) |
(20–46) |
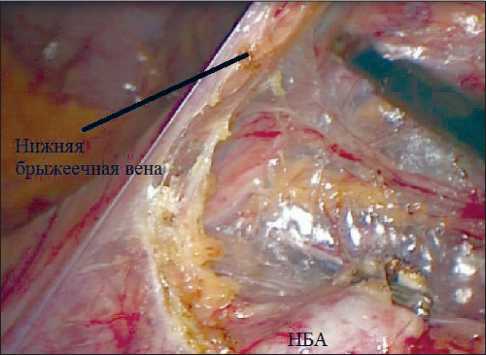
Рис. 4. Медио-латеральная мобилизация при трехэтапной МСИ
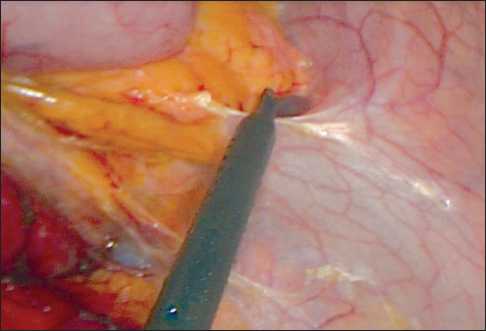
Рис. 5. Рассечение брюшины левого бокового канала до селезеночно-ободочной связки при трехэтапной мобилизации селезеночного изгиба толстой кишки
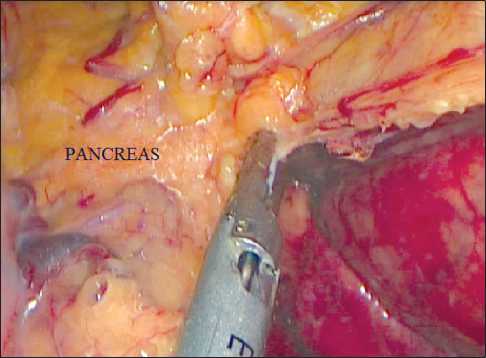
Рис. 6. Пересечение селезеночно-ободочной связки при трехэтапной мобилизации селезеночного изгиба толстой кишки
два этапа мобилизации СИ, описанные выше. Интраоперационно убеждались в достаточной длине низводимой ободочной кишки. Если ее длина оказывалась недостаточной, приступали к 3-му этапу МСИ, который в ряде случаев выполняли после извлечения препарата через мини-лапаротомный доступ и фиксации головки циркулярного степлера.
Следует отметить, что при брюшно-анальной резекции мы во всех случаях выполняли мобилизацию селезеночного изгиба, так как наличие избытка низведенной кишки в малом тазу позволяет достичь более приемлемых функциональных результатов, особенно в отношении функции держания. Кроме того, в большинстве случаев препарат извлекался трансанально, и, если длины колотрансплантата не хватало, представлялось крайне нежелательным возвращать его в брюшную полость через анальный канал для продолжения мобилизации в связи с риском инфицирования. В тех ситуациях, когда большой сальник имел протяженные сращения с селезеночным изгибом и нисходящей ободочной кишкой, препятствуя увеличению длины низведенной кишки, минилапаротомия выполнялась в левом подреберье для экстракорпорального разделения спаек сальника с ободочной кишкой.
Результаты
При сравнении 4 групп лапароскопических операций с МСИ повреждение селезенки отмечено в одном случае при левосторонней гемиколэктомии (1,5 %, 1/66) и в одном – при низкой передней резекции прямой кишки (3 %, 1/32). В обоих наблюдениях кровотечение остановлено лапароскопически, в связи с чем удалось избежать конверсии доступа и спленэктомии. Несостоятельность анастомоза при НПРПК клинически выявлена в 2 (6 %) из 32 случаев (табл. 4). При низких передних резекциях прямой кишки МСИ выполнена у 32 больных, что составило 25 % от общего числа НПРПК (n=126).
При сравнительном анализе результатов низких резекций не выявлено статистической разницы в средней продолжительности операций – 188, 167 и 203 мин (p>0,05), объеме кровопотере – 175, 105 и 162 мл (p>0,05), длительности госпитализации – 10, 10,5 и 12 койко-дней (р>0,05) соответственно. При сравнении двух групп больных, перенесших МСИ, с группой пациентов, которые МСИ не подвергались, не выявлено значимых различий в отношении количества удаленных лимфоузлов (табл. 5). Интраоперационное повреждение селезенки отмечено в 1 (3 %) случае при НПРПК с МСИ. Несостоятельность анастомоза развилась у 2 (6,3 %) больных в группе с МСИ, у 8 (8,5 %) – без МСИ, у 1 (5 %) больного при брюшно-анальной резекции (p=0,17) (табл. 6).
Таким образом, МСИ не влияла не частоту как несостоятельности анастомоза, так и интра-и послеоперационных осложнений. Более того,
Таблица 4
Частота интра- и послеоперационных осложнений при лапароскопических операциях с МСИ
|
Вид осложнений |
Объем выполненных операций Низкая передняя Брюшно-анальная Левосторонняя резекция прямой Колпроктэктомия резекция прямой гемиколэктомия кишки кишки |
|
Повреждение селезенки Повреждение хвоста поджелудочной железы |
1 (1,5 %) 1 (3 %) 0 0 0000 |
Таблица 5
Непосредственные результаты лапароскопических низких резекций прямой кишки отмечена тенденция к более часто возникающей несостоятельности колоректального анастомоза при выполнении МСИ. Выполнение МСИ по описанному способу статистически не влияло на продолжительность хирургического вмешательства.
Заключение
Мобилизацию селезеночного изгиба толстой кишки оптимально выполнять лапароскопическим
Список литературы Мобилизация селезеночного изгиба при резекциях прямой кишки
- Finan P.J. Why I (nearly) always mobilise the splenic flexure in rectal cancer surgery. Ann R Coll Surg Engl. 2008; 90 (8): 641-642
- Katory M., Tang C.L., Koh W.L., Fook-Chong S.M.C., Loi T.T., Ooi B.S., Eu K. W. A 6-year review of surgical morbidity and oncologic outcome after high anterior resection for colorectal malignancy without splenic flexure mobilisation. Colorectal Dis. 2008; 10: 165-9
- Brennan D.J., Moynagh M., Brannigan A.E., Gleeson F., Rowland M., O’Connell P.R. Routine mobilization of the splenic flexure is not necessary during anterior resection for rectal cancer. Dis Colon Rectum 2007; 30: 302-7
- Jamali F.R., Soweid A.M., Dimassi H., Bailey C., Leroy J., Marescaux J.Evaluating the Degree of Difficulty of Laparoscopic Colorectal Surgery. Arch Surg. 2008; 143 (8): 762-767. DOI: 10.1001/archsurg.143.8.762
- Tubbs R.S., Loukas M., Shoja M.M. Bergman's Comprehensive Encyclopedia of Human Anatomic Variation. John Wiley & Sons. 2016. 1309


