Модель определения коэффициента диффузии в растворах электролитов
Автор: Жигжитова С.Б., Балданова Д.М., Бадмаев С.С.
Журнал: Вестник Бурятского государственного университета. Химия. Физика @vestnik-bsu-chemistry-physics
Статья в выпуске: 2, 2024 года.
Бесплатный доступ
Предложена модель для определения коэффициента диффузии в растворах электролитов. Данная модель основана на связи между плазменным состоянием системы зарядов и гидродинамическим приближением ионов в растворах. В данном состоянии вещества многочастичные взаимодействия однозначно формализуются плазменными колебаниями. Для расчета необходимых параметров развиваемой модели использованы имеющиеся справочные данные электрической проводимости, общепринятые в химической термодинамике. Полученные значения коэффициента диффузии по предложенной расчетной формуле согласуются с литературными данными, что подтверждает перспективность данного метода оценки диффузии в системе.
Растворы электролитов, коэффициент диффузии, электрическая проводимость, вязкость, плазменно-гидродинамическое приближение
Короткий адрес: https://sciup.org/148328731
IDR: 148328731 | УДК: 541.13:54-145 | DOI: 10.18101/2306-2363-2024-2-3-7
Model for determining the diffusion coefficient in electrolyte solutions
In the article, we propose a model for determining the diffusion coefficient in electrolyte solutions. This model is based on the correlation between the plasma state of the charge system and the hydrodynamic approximation of ions in solutions. In this state of matter, many-particle interactions are uniquely formalized by plasma oscillations. To calculate the necessary parameters of the developed model, we have used available reference data on electrical conductivity, generally accepted in chemical thermodynamics. The values of the diffusion coefficient obtained using the proposed calculation formula are consistent with the literature data, which confirms the perspectiveness of this method for assessing diffusion in the system.
Текст научной статьи Модель определения коэффициента диффузии в растворах электролитов
Жигжитова С. Б., Балданова Д. М., Бадмаев С. С. Модель определения коэффициента диффузии в растворах электролитов // Вестник Бурятского государственного университета. Химия. Физика. 2024. Вып. 2. С. 3–7.
Диффузия ионов зависит от подвижности ионов, их способности двигаться в среде, а также от коэффициента вязкости среды, который влияет на скорость диффузии. Все эти параметры важны при изучении процессов диффузии ионов.
Согласно Дебаю-Фалькенгагену ионы могут совершать гармонические колебания в неравновесных условиях. Движение ионов в процессах диффузии обусловлено градиентом концентрации вещества. Потенциальная энергия взаимодействия ионов определяется следующим выражением:
U = 2 E ea^a • где ea — заряд иона; ^a — потенциал. Известно, что ea^a = Ua . Тогда U = | EUa •
при сложении энергии U a появляется множитель 1/2, поскольку она учтена дважды. В соответствии с законами механики движение ионов при диффузии возможно только под действием силы Fa :
dU a
F n =--
a .
dr
Таким образом, учитывая данные условия, 1 a 2
F a можно представить в виде: dU a
dr
.
Эффективная сила F эф связана с F a следующим соотношением (4):
F =
Fэф
_y dUa = 2f
dr a
.
Запишем силу Стокса для ионов, принимая их за сферические объекты:
( R^Fa = 6n^R 1 + - V •
V rD )
здесь П — вязкость; R — радиус сольватированных ионов; r D — дебаевский радиус и V — скорость ионов [2].
Следовательно, эффективную силу можно представить:
F* = 2 ■ 6 nn R 1 + - |v .
V rD )
Подвижность b — это отношение скорости движения ионов V к эффективной силе эф
b = V-
F эф
R^ ’ 2 • 6 nn R 1 + —
V rD )
С другой стороны, по закону Эйнштейна подвижность можно представить через диффузию
b=-D- kT
Б
.
Коэффициент диффузии можно получить, объединив уравнения (7) и (8:
D = 1 •
kT
Б
( r\
6 nn R 1 + -
V r D J
здесь n — коэффициент вязкости, равный [1]
П =
N A e 2 exp( - —) 411 •Ю - 12
Б
6 n AR (1 + —) rD
Тогда, подставив вязкость (10) в формулу (9), получим окончательное выражение, позволяющее рассчитать коэффициент диффузии:
kJA
Б
^ Ш
Ne 2 exp•I.II • 10 1 a
V кБТ J
Результаты расчета коэффициента диффузии для водных растворов по формуле (11) приведены ниже.
Для хлорида цезия CsCl при 25 °С
Таблица 1
|
C, моль/л |
0,1 |
0,5 |
1 |
2 |
3 |
5 |
|
Ʌ, Ом-1 см2моль-1 |
128 |
118 |
113 |
107 |
98,7 |
85 |
|
D теор·10-5 , см2·сек- 1 |
1,62 |
1,75 |
1,87 |
1,90 |
1,95 |
2,01 |
|
D лит [3] |
- |
1,86 |
1,91 |
2,09 |
- |
- |
Для хлорида натрия NaCl при 25 °С
Таблица 2
|
С, моль/л |
0.001 |
0.005 |
0.01 |
0.1 |
0.5 |
|
Л , Ом-1 см2моль-1 |
123 |
111 |
118 |
106 |
93 |
|
D pac4 •Ю" 5, см2сек-1 |
1,653 |
1,556 |
1,160 |
1,517 |
1,450 |
|
Dлиm •Ю " 5 , см2сек-1 |
1,584 |
1,506 |
1,544 |
1,482 |
1,469 |
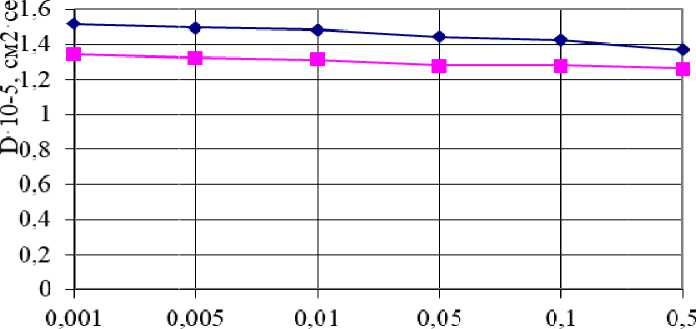
>- расч -в- лит С, моль/л
Рис. 1. За в ис им о ст ь ко э ф фициент а д иффуз ии D хлорида лития LiCl от концентрации при 25 °С
Заключение
Т а к и м об р а зом , ре з ультаты исследования показывают, что ис по льзование у равн ен и я ( 11) для оц енки диффузии в системе было эффективным. Лит е р а т урные значения и зн аче н и я, полученные путем расчета, совпадают в пр ед ел а х по г решн о ст и . Это г овори т о т ом, чт о для анализа процессов диффузии в рассматриваемой системе п ред ложенный метод оценки диффузии может быт ь п рим ен ен с д ос т аточн ой т очн ос т ь ю .
Список литературы Модель определения коэффициента диффузии в растворах электролитов
- Балданова Д. М., Танганов Б. Б. Плазменно-гидродинамическая концепция состояния ионов в растворах электролитов в оценке некоторых свойств: монография. Москва: Издательский дом Академии естествознания, 2012. 100 с. Текст: непосредственный. EDN: QKDAKP
- Плазменно-гидродинамическая теория растворов электролитов и электропроводность / М. М. Балданов, Д. М. Балданова, С. Б. Жигжитова, Б. Б. Танганов // Доклады АН ВШ РФ. 2006. № 1(6). С. 25-33. Текст: непосредственный. EDN: KVQJPN
- Справочник химика. Т. 3 / под редакцией Б. П. Никольского. Москва: Химия, 1969. 1005 с. Текст: непосредственный.


