Модель прогнозирования клинических исходов острой лучевой болезни человека
Автор: Пустовойт В.И., Умников А.С., Богомолов А.В.
Рубрика: Научные статьи
Статья в выпуске: 1 т.35, 2026 года.
Бесплатный доступ
Острая лучевая болезнь остаётся одной из наиболее клинически сложных форм радиационного поражения человека, требующей точных и воспроизводимых инструментов прогнозирования клинического исхода. При невозможности проведения рандомизированных клинических исследований в радиационной медицине особую значимость имеют модели прогнозирования клинического исхода острой лучевой болезни человека, основанные на ретроспективных данных. Цель исследования – обеспечение приемлемой точности прогноза клинических исходов острой лучевой болезни человека, стандартизация диагностического процесса и обоснование персонализированной лечебной тактики в условиях ограниченного времени и ресурсов за счёт разработки и валидации модели прогнозирования, учитывающей индивидуальные дозовые нагрузки, клиниколабораторные показатели состояния поражённого и динамики заболевания. Модель построена на международной выборке, сформированной по результатам ретроспективного анализа 1441 клинического случая острой лучевой болезни за последние 70 лет с применением линейного дискриминантного анализа. Прогноз клинического исхода острой лучевой болезни – благоприятный или неблагоприятный – делается на основании шести клиникорадиобиологических показателей: цитогенетическая доза, степень тяжести болезни, инкорпорация радионуклидов, день после облучения, длительность облучения и масса тела пациента. Построенная модель обеспечила приемлемую точность: при общей точности 94,8% точность прогнозирования для благоприятных исходов составила 97,4%, для неблагоприятных исходов – 80,3%. Высокое качество модели подтверждено результатами анализа классификационной матрицы и ROCанализа. Разработанная модель представляет собой первый пример применения линейного дискриминантного анализа для слепой классификации клинических исходов острой лучевой болезни человека на основе клиникорадиобиологических показателей, что обеспечивает её воспроизводимость, объяснимость и потенциал для автоматизации в системах медицинской сортировки, диагностики и экстренного реагирования при радиационных инцидентах.
Острая лучевая болезнь, радиационное поражение человека, клинический исход острой лучевой болезни, прогнозирование исхода острой лучевой болезни, клинико-радиобиологический показатель, дискриминантный анализ
Короткий адрес: https://sciup.org/170211678
IDR: 170211678 | УДК: 616-001.28-037 | DOI: 10.21870/0131-3878-2026-35-1-117-126
A predictive model for clinical outcomes in human acute radiation syndrome
Acute radiation syndrome remains one of the most clinically complex forms of human radiation injury, necessitating accurate and reproducible tools for forecasting clinical outcomes. Given the ethical and practical limitations associated with conducting randomized clinical trials in radiation medicine, predictive models based on retrospective data acquire particular significance. The aim of this study was to ensure an acceptable level of accuracy in forecasting clinical outcomes of human ARS, to standardize diagnostic procedures, and to justify personalized therapeutic strategies under conditions of limited time and resources through the development and validation of a prognostic model that integrates individual radiation dose burdens, clinical and laboratory indicators, and disease dynamics. The model was constructed using an international dataset derived from a retrospective analysis of 1441 clinical cases of acute radiation syndrome accumulated over the past 70 years, utilizing linear discriminant analysis. The forecasted clinical outcome – favorable or unfavorable – is based on six clinicoradiobiological parameters: cytogenetic dose, severity of the syndrome, radionuclide incorporation, time elapsed since exposure, duration of exposure, and patient body weight. The model demonstrated acceptable accuracy: with an overall accuracy of 94,8%, the predictive accuracy for favorable outcomes was 97,4%, and for unfavorable outcomes – 80,3%. The high performance of the model was corroborated by the results of the classification matrix and ROC analysis. This model represents the first documented application of linear discriminant analysis for blind classification of ARS clinical outcomes in humans based on clinicoradiobiological parameters, thus offering reproducibility, interpretability, and potential for automation in systems of medical triage, diagnosis, and emergency response during radiation incidents.
Текст научной статьи Модель прогнозирования клинических исходов острой лучевой болезни человека
Острая лучевая болезнь (ОЛБ) остаётся одной из наиболее клинически сложных форм радиационного поражения человека, исход которой определяется множеством факторов, включая характер и мощность воздействия, пути поступления радионуклидов, индивидуальную радиочувствительность и своевременность лечебно-диагностических мероприятий [1]. Несмотря на значительный прогресс в области радиационной биологии и медицины, задача прогнозирования клинического исхода ОЛБ продолжает оставаться актуальной и во многом нерешённой [2].
Основным источником клинических данных, использующихся для изучения течения и последствий ОЛБ, по-прежнему остаётся авария на Чернобыльской атомной электростанции [3, 4]. К настоящему времени накоплен большой массив информации о дозах облучения, динамике гематологических и клинических показателей, а также об эффективности терапевтических подходов у ликвидаторов последствий аварии и населения территорий, подвергшихся воздействию радиации [5]. Однако с момента чернобыльской катастрофы прошло почти четыре десятилетия,
Пустовойт В.И. – зав. отд., д.м.н.; Умников А.С. – зав. лаб., к.м.н.; Богомолов А.В.* – вед. науч. сотр., д.т.н., проф. ФГБУ ГНЦ ФМБЦ им. А.И. Бурназяна ФМБА России.
что объективно ограничивает возможности верификации диагностических и прогностических методов и моделей [6-8].
Отсутствие этически допустимой возможности проведения рандомизированных клинических исследований с участием человека при радиационных поражениях приводит к необходимости опоры на ретроспективные когортные исследования и математические методы, позволяющие интегрировать разнородные данные и формализовать процессы стратификации и прогнозирования. В условиях дефицита актуальных эмпирических наблюдений создание математических моделей становится не только востребованным направлением, но и единственно возможным способом поддержки принятия объективных клинико-прогностических решений, доказательность которых соответствует современному уровню развития медицинской информатики [9].
Применяемые на практике клинические системы анализа тяжести и прогнозирования исходов ОЛБ основаны преимущественно на интеграции данных о дозе облучения, клинических симптомах и динамике гематологических показателей. Однако в большинстве случаев эти подходы обладают значительной долей субъективности, опираются на экспертные заключения и не имеют формализованных алгоритмов принятия решений. В условиях ограниченной репрезентативности современных данных и высокой вариабельности клинического течения ОЛБ это создаёт существенные риски ошибочной стратификации и затрудняет персонификацию лечебно-диагностических стратегий [10].
В ряде практических руководств, разработанных после радиационных аварий, включая чернобыльскую, используются шкалы прогноза, основанные на эвристических правилах и клинико-экспертной оценке. Такие системы, как правило, не обеспечивают достаточную воспроизводимость результатов и не могут быть непосредственно перенесены в иные контексты радиационного воздействия. Кроме того, при многофакторной этиологии поражения и наличии сочетанных травм клиническая интерпретация результатов прогнозирования исходов ОЛБ становится ещё более неоднозначной, что требует перехода к более строгим и воспроизводимым аналитическим инструментам [11, 12].
Целью исследования является обеспечение приемлемой точности прогноза клинических исходов ОЛБ, стандартизации диагностического процесса и обоснование персонализированной лечебной тактики в условиях ограниченного времени и ресурсов за счёт разработки и валидации модели прогнозирования исходов ОЛБ человека, учитывающей индивидуальные дозовые нагрузки, клинико-лабораторные показатели состояния поражённого и динамику заболевания.
Материалы и методы
В основу исследования положены международные результаты ретроспективного анализа 1441 клинического случая ОЛБ различной степени тяжести, зафиксированных в период с 1950 по 2025 гг., в том числе: 1223 случая с благоприятным клиническим исходом (БИ) ОЛБ (выздоровление пациента) и 218 случаев с неблагоприятным клиническим исходом (НИ) ОЛБ (смерть пациента) [2, 11].
В исследование включены наблюдения, задокументированные в ходе ликвидации последствий радиационных аварий, а также случаи, полученные в результате инцидентов на производственных и исследовательских объектах, связанных с источниками ионизирующего излучения [11]. Все случаи, включённые в анализ, соответствовали критериям достоверно установленной дозы облучения, полной клинической документации и наличия подтверждённого клинического исхода.
Данные были деперсонифицированы и агрегированы в единую базу с последующим качественным контролем и устранением дублирующих показателей. Проведение анализа соответствовало принципам Хельсинкской декларации и не предполагало вмешательства в лечебный процесс.
Для построения прогностической модели использованы количественные и категориальные клинико-радиобиологические показатели, отражающие физико-дозиметрические характеристики воздействия и индивидуальные показатели реакции организма [2]. Все показатели прошли этап стандартизации и предварительной проверки на полноту, непротиворечивость и диагностическую значимость. Для каждого пациента, включённого в выборку, был известен клинический исход ОЛБ, БИ или НИ, определившие группы пациентов.
Для построения модели прогнозирования клинических исходов ОЛБ человека на основании клинической доступности и подтверждённой значимости в предыдущих исследованиях по прогнозированию исходов ОЛБ отобраны следующие клинико-радиобиологические показатели:
-
- цитогенетическая доза облучения (Гр), определённая на основе анализа частоты хромосомных аберраций в лимфоцитах периферической крови и отражающая индивидуальный уровень биологически эффективного радиационного воздействия;
-
- клиническая степень тяжести ОЛБ, установленная на основании комплекса диагностических критериев, включая динамику лейкопоэза, выраженность геморрагического и гастроинтестинального синдромов, а также характер течения заболевания;
-
- наличие инкорпорации радионуклидов, подтверждённое результатами радиометрического и спектрометрического обследования;
-
- время, прошедшее после облучения (сутки), как показатель фазы развития клинической картины и потенциального окна терапевтической интервенции;
-
- длительность облучения (часы), отражающая темп накопления дозы и потенциал к радиобиологической репарации;
-
- масса тела пациента (кг), являющаяся одним из биомаркеров индивидуальной устойчивости и метаболической реакции на радиационное воздействие.
Отобранные показатели обеспечивают воспроизводимость модели и возможность её применения в условиях специализированных центров радиационной медицины и в рамках систем экстренного реагирования.
Законы распределений массива каждого отобранного показателя в группах «НИ» и «БИ» соответствуют нормальному распределению, что подтверждено с помощью критерия Шапиро-Уилка. Отсутствие в массиве значений каждого показателя аномальных значений подтверждено с помощью критерия Граббса для одновременной проверки на выброс наименьшего и наибольшего значения показателя в массиве [13].
Поскольку все независимые переменные (клинико-радиобиологические показатели) непрерывные, а их массивы имеют нормальное распределение, имеется одна качественная зависимая переменная (исход ОЛБ), а решающее правило должно быть интуитивно понятно медицинскому персоналу, чтобы обеспечивать доверие к получаемым результатам, для построения прогностической модели клинического исхода ОЛБ человека использован метод линейного дискриминантного анализа.
Проведение линейного дискриминантного анализа осуществлено с использованием программного пакета Statistica 13 (TIBCO Software Inc.), обеспечивающего полный спектр процедур анализа. Для валидации модели применялась кросс-проверка с выборочным исключением, а качество классификации оценивалось на основе анализа классификационной матрицы и ROC-анализа.
Результаты и обсуждение
В результате линейного дискриминантного анализа построены две прогностические функции, отражающие принадлежность пациента к одной из двух категорий клинического исхода – БИ и НИ:
БИ = -42,1558 - 0,4528х Y 1 + 13,4621 х Y 2 + 0,2655х Y з + 0,1695х Y 4 + 1,5316х Y 5 + 0,6764х Y 6 ;
НИ = -65,4085 + 0,7934х Y 1 + 17,0002х Y 2 + 5,7139х Y з + 0,1237х Y 4 + 1,883х Y 5 + 0,7152х Y 6 , где Y 1 – цитогенетическая доза, Гр; Y 2 – степень тяжести ОЛБ (1, 2, 3 или 4); Y 3 – инкорпорация радионуклидов (да – 1; нет – 0); Y 4 – день после облучения; Y 5 – длительность облучения, часы; Y 6 – масса тела, кг.
Для каждого пациента рассчитываются значения двух дискриминантных функций, а прогнозируемый клинический исход ОЛБ определяется максимальной рассчитанной величиной: если значение функции НИ превышает значение функции БИ, прогнозируется развитие НИ ОЛБ и наоборот.
Структура уравнений дискриминантных функций отражает относительный вклад каждого клинико-радиобиологического показателя в прогноз исхода ОЛБ. Так, наиболее выраженное влияние на формирование модели оказали переменные Y г (степень тяжести) и Y 3 (инкорпорация), коэффициенты которых в функции НИ превышают соответствующие значения в функции БИ более чем в два раза. Это подтверждает доминирующую роль тяжести клинических проявлений и внутреннего радиоактивного загрязнения в формирование НИ ОЛБ.
Особенно высокий вклад в формирование прогноза обеспечивает цитогенетическая доза, которая в модели ассоциируется с увеличением вероятности НИ ОЛБ. Положительный коэффициент в функции НИ и отрицательный в функции БИ указывает на прямую зависимость между увеличением уровня облучения и риском НИ.
Значимое прогностическое значение имеет также клиническая степень тяжести ОЛБ, которая отражает выраженность патофизиологических нарушений. Присутствие высоких коэффициентов в двух дискриминантных функциях, особенно в НИ, подчёркивает её центральное значение в стратификации пациентов.
Инкорпорация радионуклидов оказывала выраженное влияние на прогноз клинического исхода ОЛБ. Величина её коэффициента в функции НИ является одной из самых высоких, что указывает на значительный вклад этого показателя в формирование НИ ОЛБ.
Дополнительное значение имеют такие показатели как длительность облучения и время, прошедшее с момента воздействия до поступления пациента в стационар. Оба показателя характеризуются положительными значениями коэффициентов дискриминантных функций, что свидетельствует о повышении риска при увеличении длительности экспозиции и отсрочке начала медицинской помощи.
Масса тела пациента также показала статистически достоверную связь с клиническим прогнозом ОЛБ. Несмотря на сравнительно меньший коэффициент, переменная была сохранена в модели на основании клинической целесообразности, позволяющей учитывать индивидуальные особенности адаптивного потенциала организма.
Совокупный анализ всех переменных позволяет утверждать, что они обладают статистической значимостью и клинической интерпретируемостью. Это создаёт основу для объективного, стандартизированного и персонализированного подхода к прогнозированию клинических исходов ОЛБ, а также обеспечивает практическую применимость модели как в клинических условиях, так и при медицинской сортировке поражённых.
Формализация в виде дискриминантных функций позволяет использовать модель в автоматизированных клинико-диагностических системах, обеспечивая объективную, воспроизводимую и стандартизированную оценку прогноза клинического исхода ОЛБ. Расчёт может быть реализован как в табличных форматах (Excel), так и в виде скриптов (Python) или веб-приложений для клинического применения.
Исследование диагностической эффективности модели проведено на основе анализа классификационной матрицы (четырёхпольной таблицы сопряжённости, таблицы 2x2), которая отражает соответствие между прогнозируемым и фактическим клиническим исходом ОЛБ (табл. 1).
Классификационная матрица
Таблица 1
|
Прогнозируемый исход ОЛБ |
Фактический исход ОЛБ |
Всего |
|
|
выздоровление |
смерть |
||
|
БИ |
1191 |
32 |
1223 |
|
НИ |
43 |
175 |
218 |
|
Всего |
1234 |
207 |
1441 |
Согласно табл. 1, разработанная модель продемонстрировала высокую общую точность прогнозирования клинических исходов ОЛБ, составившую 94,8%. Распространённость случаев с НИ в выборке составила 84,9%.
Точность прогноза в группе с БИ составила 97,4%, что подтверждает высокую чувствительность модели в отношении стабильных форм течения ОЛБ. Это обстоятельство имеет практическое значение, поскольку позволяет надёжно исключать тяжёлые последствия при наличии типичной динамики клинических и лабораторных показателей.
В группе НИ точность классификации составила 80,3%, что также является удовлетворительным показателем при прогнозировании летальных исходов и тяжёлых осложнений ОЛБ. Меньшая точность прогноза в этой категории, по-видимому, связана с меньшим объёмом доступной выборки, а также с клинической гетерогенностью терминальных форм ОЛБ и высокой индивидуальной вариабельностью реакции организма на радиационное поражение, включая различия в скорости декомпенсации и сопутствующих заболеваниях.
При этом доля ошибок первого рода (ложная тревога, гипердиагностика – ошибочная оценка НИ) составила 3,0%, а доля ошибок второго рода (пропуск цели – ошибочная оценка БИ) составила 2,2%.
Анализ табл. 1 показывает, что с позиций доказательной медицины разработанная модель характеризуется следующими показателями [13, 14]:
-
– чувствительность (истинно положительные результаты) – 82,7%;
-
– специфичность (истинно отрицательные результаты) – 80,3%;
-
– сбалансированная точность (среднее арифметическое чувствительности и специфичности) – 81,5%;
-
– диагностическое отношение шансов составляет 19,5 раза, что существенно больше единицы, поэтому свидетельствует о высоком качестве прогноза;
-
– оценки положительной и отрицательной прогностической ценности составляют соответственно 96,5% и 84,5%: обе величины достаточно близки к 100%, что свидетельствует о высокой про-гностичности модели, это же подтверждается оценками коэффициента ложных срабатываний (3,5%),
коэффициента ложного пропуска (15,5%) и оценками отношения правдоподобия, которые составили 4,2 раза для положительного результата и 21,5 раза – для отрицательного результата;
-
– среднее гармоническое точности и полноты (F 1 -мера) составило 0,97, оценка коэффициента корреляции Мэттьюса равна 0,72, что также подтверждает высокие прогностические качества модели;
-
– величина индекса Фаулкса-Мэллоуза составляет 0,89, что достаточно, с точки зрения практики, близко к идеальному случаю;
-
– оценка коэффициента Жаккара, равная 0,94, и оценка маркированности, равная 0,81, свидетельствуют о высоком сходстве классов БИ и НИ;
-
– оценка информированности (индекс Юдена), характеризующая вероятность принятия обоснованного решения, составляет 0,63.
Высокое качество построенной модели подтверждается и результатами ROC-анализа (рис. 1).
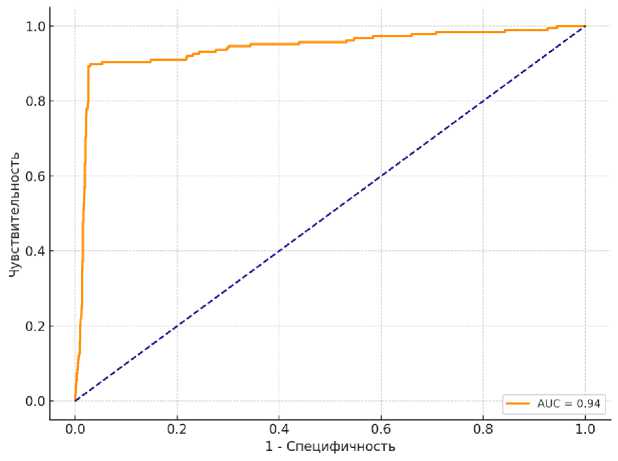
Рис. 1. ROC-кривая модели прогнозирования клинического исхода ОЛБ.
Величина площади области, ограниченной ROC-кривой и осью абсцисс, составила 0,94, что свидетельствует о высокой эффективности прогнозирования клинического исхода ОЛБ разработанной моделью [13]. Значительная чувствительность в отношении БИ и приемлемая точность в отношении НИ делают модель пригодной для практического использования в условиях ограниченного времени, дефицита ресурсов и необходимости быстрого принятия решений, в том числе в составе цифровых платформ поддержки принятия клинических решений, включая цифровые приложения, применяемые для медицинской сортировки поражённых в условиях чрезвычайных ситуаций [9, 15].
Сравнение полученных результатов с данными, представленными в отечественной и зарубежной литературе, свидетельствует о преимуществах разработанной модели по основным критериям точности.
В известных моделях прогноз исхода ОЛБ, как правило, определялся на основе показателей суммарной дозы, степени лейкопении и наличия синдромов раннего радиационного поражения [16]. Подобные шкалы (например, радиационно-гематологическая классификация ВОЗ и шкала METREPOL) имеют широкое клиническое распространение, однако не учитывают индивидуальные особенности пациента и не отражают взаимосвязь между переменными [17].
Разработанная модель обладает рядом существенных преимуществ. В отличие от моделей, ориентированных исключительно на одномоментную клиническую оценку, предложенная модель интегрирует как показатели статики (доза, масса тела), так и показатели динамики (время после облучения, клиническая степень тяжести), что расширяет её применимость в различных клинических сценариях [18].
Проведённое пилотное исследование возможностей применения прогнозирования клинических исходов ОЛБ моделей, основанных на алгоритмах машинного обучения (например, деревья решений, продукционные системы, фреймы, нейронные сети), показало, что такие модели демонстрируют сопоставимую точность, однако уступают в клинической интерпретируемости и требуют больших объёмов обучающих данных [15]. Разработанная модель обеспечивает интуитивно понятную логику принятия решений за счёт математически выверенной структуры уравнений и объяснимости каждого коэффициента, что делает её более удобной для встраивания в применяемые на практике протоколы диагностики и медицинской сортировки.
Разработанная модель имеет потенциал применения в клинической практике и системах экстренного реагирования при ограничениях времени и ресурсов. Техническая реализация в формате Excel, Python и веб-интерфейсов делает модель универсальной и доступной для любых категорий медицинского персонала, в том числе в тактических планшетах врачей.
Тем не менее, разработанная модель имеет ограничения. Использованная при её построении ретроспективная выборка включает преимущественно данные по клиническим исходам ОЛБ при тотальном и комбинированном облучении, что ограничивает её применимость к другим клиническим сценариям ОЛБ. Кроме того, в модель не включены показатели, связанные с иммунным и метаболическим ответом, а также показатели, характеризующие долгосрочные исходы ОЛБ.
Отмеченная тенденция к гипердиагностике требует осторожной интерпретации результатов прогнозирования. В условиях единичных случаев модель снижает риск недооценки тяжести ОЛБ, однако при массовых радиационных поражениях её использование может привести к нерациональному использованию ресурсов. Поэтому разработанную модель следует применять в сочетании с клинической экспертизой и эпидемиологическими исследованиями.
Совершенствование разработанной модели возможно за счёт включения биомаркеров радиационных поражений и валидации на актуализированных репрезентативных когортах. Внедрение модели в клинические системы поддержки принятия решений позволит повысить оперативность, объективность и стандартизацию медицинской помощи в условиях экстремальных и чрезвычайных ситуаций радиационного генеза.
Заключение
Разработана и исследована модель прогнозирования клинического исхода ОЛБ человека, которая продемонстрировала приемлемую точность прогнозирования и высокое качество, подтверждённое результатами анализа классификационной матрицы и ROC-анализа.
С учётом воспроизводимости, объяснимости и доступности для автоматизации целесообразно внедрение разработанной модели в практику медицинской сортировки, клинической диагностики и экстренного реагирования при радиационных инцидентах.
Совершенствование модели предполагает расширение предикторной базы с учётом современных биомаркеров, показателей иммунного статуса и метаболического ответа с валидацией на независимых репрезентативных выборках пациентов с ОЛБ.


