Моделирование акустических сигналов при оптоакустическом преобразовании для осесимметричных несферических форм эритроцитов
Автор: Кравчук Д.А.
Журнал: Научное приборостроение @nauchnoe-priborostroenie
Рубрика: Математические методы и моделирование в приборостроении
Статья в выпуске: 2 т.29, 2019 года.
Бесплатный доступ
В работе проведено моделирование промежуточных форм при трансформации эритроцитов на примере трехмерных фигур для последующего исследования изменения оптоакустических сигналов. Смоделированы пространственные фигуры эритроцитов с помощью полинома Чебышева. Разработана модель изменения формы эритроцитов для моделирования акустического сигнала с целью определения формы эритроцитов, используя оптоакустический эффект. Известно, что эритроциты переносят кислород и углекислый газ. Кислород переносится из легких в ткани, где он обменивается на CO2. Здоровый эритроцит имеет двояковогнутую форму, клетка является гибкой и принимает форму колокола, когда она проходит через очень маленькие кровеносные сосуды. Эритроцит покрыт мембраной, состоящей из липидов и белков, без ядра и содержит гемоглобин - красный, богатый железом белок, который связывает кислород. Перед выделением из костного мозга в периферическую кровь эритроциты теряют свои ядра, что дает преимущества уменьшенного веса и превращения в двояковогнутый диск с повышенной деформируемостью по сравнению с более жестким сфероидальным.
Оптоакустический эффект, акустический сигнал, эритроциты, лазер
Короткий адрес: https://sciup.org/142218223
IDR: 142218223 | УДК: 535.015 | DOI: 10.18358/np-29-2-i8389
Modeling of acoustic signals during optoacoustic conversion for axisymmetric non-spherical forms of erythrocytes
In this paper, the modeling of intermediate forms in the transformation of red blood cells using the example of three-dimensional figures for the subsequent study of changes in optoacoustic signals was carried out. The spatial shapes of erythrocytes are modeled using the Chebyshev polynomial. A model for changing the shape of erythrocytes has been developed for modeling an acoustic signal in order to determine the shape of erythrocytes using an optoacoustic effect. Erythrocytes are known to carry oxygen and carbon dioxide (CO2). Oxygen is transferred from the lungs to the tissue, where it is exchanged for CO2. A healthy red cell is biconcave, the cell is flexible and takes the form of a bell when it passes through very small blood vessels. The erythrocyte is covered with a membrane consisting of lipids and proteins, without nucleus and contains hemoglobin - a red, iron-rich protein that binds oxygen. Before isolation from the bone marrow into the peripheral blood, the ery throcytes lose their nuclei, which gives the advantages of reduced weight and transformation into a biconcave disc with increased deformability compared to the more rigid spheroidal.
Текст научной статьи Моделирование акустических сигналов при оптоакустическом преобразовании для осесимметричных несферических форм эритроцитов
При воздействии короткого лазерного импульса на тканевую жидкую среду происходит поглощение света, и в результате термоупругого расширения излучается импульс акустического давления, который можно зарегистрировать ультразвуковым преобразователем. Форма и длительность акустического сигнала может говорить о форме и количестве объектов в жидкости, участвующих в поглощении лазерного импульса в биожидкости. В работах [1–11] проводились расчеты сформированного акустического сигнала в результате оптоакустического преобразования для математических моделей неагрегированных и агрегированных эритроцитов, в том числе с учетом кислородона-сыщения. В этих исследованиях для упрощения использовалась сферическая модель формы эритроцита. В настоящей работе приведена математическая модель патологических форм эритроцитов для исследования изменения форм эритроцитов с помощью оптоакустического метода.
Структурная организация мембраны эритроцитов человека позволяет ей претерпевать большие обратимые деформации, сохраняя при этом свою структурную целостность в течение 4-месячного пребывания в кровообращении. Мембрана обладает высокой эластичностью, быстро реагирует на приложенные гидравлические напряжения. В то время как нормальные эритроциты могут деформироваться с линейным расширением примерно до 250 %, увеличение площади поверхности на 3–4 % приводит к лизису клеток. Следовательно, важной особенностью индуцированных деформаций эритроцитов как in vitro , так и in vivo является то, что они не вызывают значительного изменения площади поверхности мембраны [12].
Снижение отношения площади поверхности клеток к объему и, как следствие, увеличение сферичности клеток является отличительной чертой эритроцитов при наследственных сфероцитозе (HS), эллиптоцитозе (HE) и гипергидратирован-ном стоматоцитозе (OHS). В случае HS и HE повышенная сферичность является результатом потери площади поверхности ячейки, в то время как в случае OHS она является результатом увеличенного объема ячейки.
HS является распространенной наследственной гемолитической анемией, поражающей все этнические группы, но особенно распространена у людей североевропейского происхождения (1 на 3000 человек). HS обычно ассоциируется с доминантным наследованием (75 %), хотя случаи, когда наследование не является доминантным (25 %), — не редкость. Типичная HS характеризуется наличием гемолиза с анемией, желтухой, желчными камнями и наличием сфероцитов на мазках периферической крови. Тем не менее клинические проявления HS варьируются от легкой до очень тяжелой анемии. Общей чертой всех форм HS является потеря площади поверхности мембраны и результирующее изменение формы клеток от дискоцитов к стоматоцитам, к сфероцитам. Поскольку эритроциты с уменьшенной площадью поверхности мембраны не могут эффективно пройти через селезенку, они изолируются и удаляются из кровотока селезенкой. Важно отметить, что тяжесть анемии связана со степенью уменьшения площади поверхности мембраны [12].
Рис. 1. Геометрия формирования акустического сигнала при оптоакустическом преобразовании
МАТЕМАТИЧЕСКАЯ МОДЕЛЬ
Оптоакустический эффект описывается уравнением [13, с. 282], [14], которое можно записать через потенциал скорости ϕ как:
(
V 2
I
—
1 д_) с2 б t2J
ф =
β ρC p
Ht ,
Рассмотрим геометрию нерегулярного поглотителя лазерного излучения в жидкости с азимутальной симметрией. Запишем в сферических полярных координатах ( r ' , 0 ', ф ') с помощью замены r' = F ( S '); F ( S' ) — функция, связывающая r' и 0 (рис. 1).
Используем сферические гармоники для параметризации морфологии клеток [16, 17]. Этот набор функций может соответствовать как симметричным, так и несимметричным объектам. В этом случае контур ячейки можно разложить по полиномам Лежандра
r ' ( 0 ' ) = R e
где c — скорость звука, ρ — плотность жидкости, β — коэффициент расширения изобарического объема, C p — удельная теплоемкость, t — время и H t — функция нагрева, определяемая как тепловая энергия, внесенная оптическим лучом; p = — р б ф / 9 t .
Если оптическое излучение с интенсивностью I 0 распространяется вдоль оси X и изменяется со временем синусоидально, то функция нагрева может быть выражена как Ht( x , t ) = μI 0 e – ωt . Здесь μ — коэффициент оптического поглощения освещенной среды. Для такой функции нагрева поле звукового давления в установившемся режиме сводится к выражению [15]:
V
к
—
-1 - 1 v 2 д 2 J
ф=<
\а>в0 о (внутри поглотителя),
0 (снаружи поглотителя).
1 + ^ a n P n ( cos S ')
n
где R e — радиус сферической оболочки, охватывающей эритроцит; α n — параметр, описывающий форму; P n — многочлен Лежандра степени n . Любая произвольная функция между 0 < 0' < п может быть выражена через базисные векторы. Используем это условие для получения нормальной формы дискоцита. Двумерное поперечное сечение фигуры и трехмерная фигура приведены на рис. 2.
Расстояние r'(0') точки на поверхности для сфероидальной частицы запишем в виде:
r-(0-) =
ab
[ b2 sin2 0' + a2 cos2 0 ' ]
где a и b — полуоси.
На рис. 3, 4 приведены сфероиды с различными пропорциями, причем у всех частиц объем неизменный. Уравнения для несферического объекта имеют вид:
а
–1
–2
–3
–4
–1
–2
–3
–4
–4
б
–4
–5–5
–4 –3 –2
–1 0 1
x ,
2 мкм
Рис. 2. Моделируемая форма здорового эритроцита. а — изометрия, б — поперечное сечение
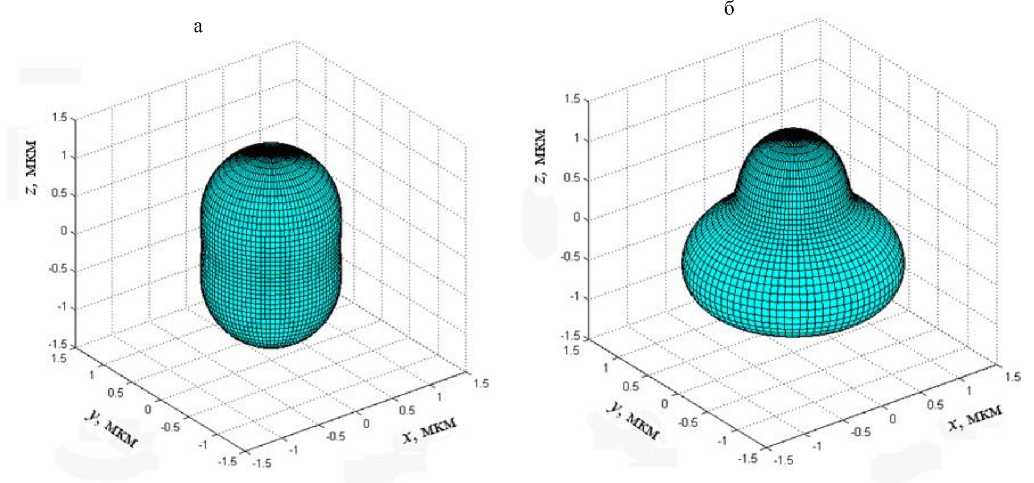
Рис. 3. Частицы, построенные с помощью многочлена Чебышева с ε = 0.25. а — n = 2, б — n = 3
i kr π F ( θ ) 2 π
p ( r , k ) =-— А Sin OdO f r o 2d r ,J e- k W (5)
4 πr 0 0 0
Расчет интеграла проводится численным методом с использованием полинома Чебышева для различных сферических и осесимметричных несферических частиц, поглощающих лазерное излучение и формирующих акустическое поле.
МОДЕЛИРОВАНИЕ
Для построения фигуры с помощью многочлена Чебышева расстояние от точки на поверхности можно записать в виде [18]:
r'O) = R c [ 1 + £ T „ (cos O ') ] , (6)
где T B (cos O ') = cos n O' — многочлен Чебышева
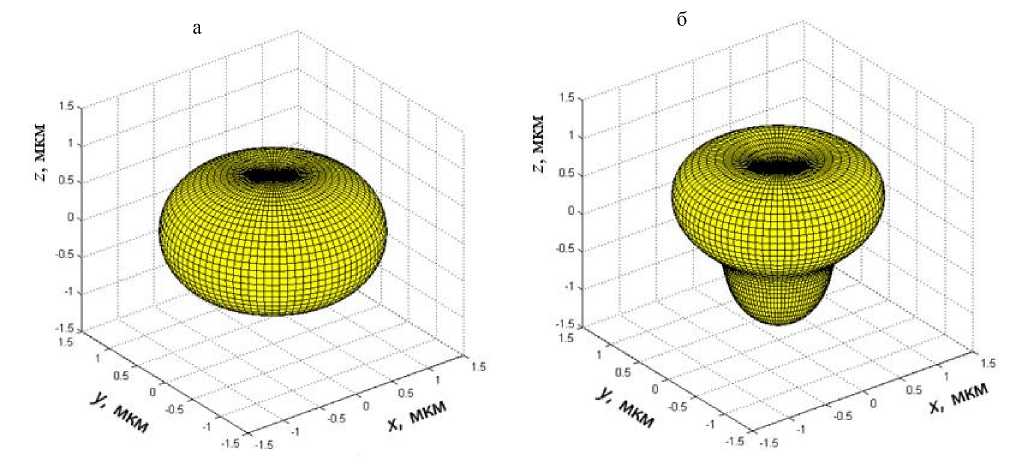
Рис. 4. Частицы, построенные с помощью многочлена Чебышева с ε = –0.25. а — n =2, б — n =3
степени n , где n определяет параметр волнистости, R c — радиус невозмущенной сферы, а ε — параметр деформации.
Частица формируется непрерывным деформированием сферы с использованием многочлена Чебышева степени n .
Частицы с фиксированным объемом приведены на рис. 3 для ε = 0.25 и рис. 4 для ε = –0.25. При четном значении n частицы симметричны относительно плоскости, перпендикулярной оси симметрии. Значения пиков, прогибов (кривизны поверхности) возрастают по мере увеличения величины ε.
Зрелая клетка имеет ширину около 7.8 мкм и толщину 1.7 мкм. Двояковогнутая форма (рис. 2) обеспечивает максимальную гибкость, а форма колокола используется для прохождения самых маленьких капилляров, которые имеют диаметр всего 5 мкм. Способность эритроцитов восстанавливаться после повторяющихся напряжений турбулентной циркуляции зависит от конструкции мембраны.
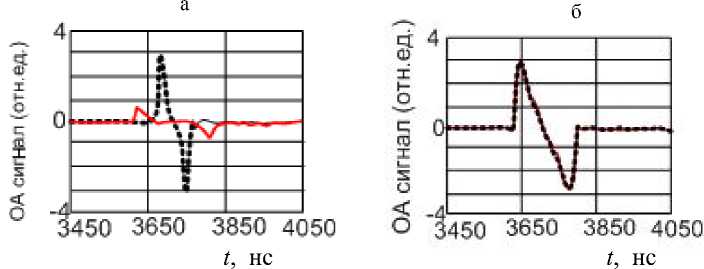
Рис. 5. Моделируемый акустический сигнал, формируемый дискоци-том и патологически измененным эритроцитом при оптоакустическом преобразовании (ОА).
Приведены сигналы в направлениях θ = 0 (пунктир) и θ = π/2 (сплошная линия) на ось симметрии: (a) дискоцит; (б) сфера
На рис. 5 приведен рассчитанный акустический сигнал, формируемый в результате оптоакустического преобразования в жидкости от дискоцитов и сфероидальных моделей эритроцитов с одинаковым объемом. В моделировании использовались параметры лазерной установки LIMO 100-532/1064U [1, 8–10]. Моделирование проводилось в среде Matlab 2017.
ЗАКЛЮЧЕНИЕ
Для определения формы эритроцитов с помощью оптоакустического эффекта была разработана двухмерная модель изменения формы эритроцитов для моделирования акустического сигнала.
Рассчитанные акустические сигналы отличаются для разных частиц в зависимости от их ориентации. Акустический импульс рассчитан, когда приемник расположен при θ = 0, как показано на рис. 5, а. Амплитуда сигнала уменьшается в четыре раза, а длительность акустического сигнала в три раза увеличивается при зондировании в направлении θ = π/2. Для однородной сферы сигналы идентичны со всех сторон (рис. 5, б). Моделирование параметрической поверхности является активной областью исследований в анализе медицинских изображений [16–20]. Поэтому сложные формы могут быть смоделированы с использованием сферических гармонических функций. Можно также предположить, что акустические сигналы от клеток и органелл могут быть получены через сферические гармонические функции для количественной оценки их морфологий.
Список литературы Моделирование акустических сигналов при оптоакустическом преобразовании для осесимметричных несферических форм эритроцитов
- Starchenko I.B., Kravchuk D.A., Kirichenko I.A. An optoacoustic laser cytometer prototype//Biomed Eng. 2018. Vol. 51, is. 5. P. 308-312 DOI: 10.1007/s10527-018-9737-8
- Кравчук Д.А., Старченко И.Б. Теоретическая модель для диагностики эффекта кислородонасыщения эритроцитов с помощью оптоакустических сигналов//Прикл. физ. 2018. № 4. С. 89-94.
- Кравчук Д.А. Математическая модель обнаружения внутриэритроцитарных инфекций с помощью оптоакустического метода//Biomed. Photonics. 2018. Т. 7, № 3. C. 36-42 DOI: 10.24931/2413-9432-2018-7-3-36-42
- Кравчук Д.А., Старченко И.Б. Модель формирования оптоакустического сигнала от эритроцитов для лазерного цитомера//Лазер. мед. 2018. T. 22, № 1. С. 57-61.
- Кравчук Д.А., Старченко И.Б. Математическое моделирование оптикоакустического сигнала от эритроцитов//Вест. нов. мед. техн. 2018. № 1. С. 96-101 DOI: 10.24411/1609-2163-2018-15947
- Кравчук Д.А., Старченко И.Б. Математическое моделирование оптоакустического сигнала от агрегированных эритроцитов для оценки уровня агрегации//Научн. приборостр. 2018. Т. 28, № 1. С. 30-36. URL: http://iairas.ru/mag/2018/full1/Art4.pdf
- Кравчук Д.А., Старченко И.Б. Моделирование процесса насыщения кислородом биологических тканей с помощью оптоакустического метода//Научн. приборостр. 2018. Т. 28, № 2. С. 20-24. URL: http://iairas.ru/mag/2018/full2/Art3.pdf
- Кравчук Д.А., Старченко И.Б. Модель формирования оптоакустического сигнала от агрегированных эритроцитов//Изв. Юго-Запад. гос. ун-та. Серия "Управление, вычислительная техника, информатика. Медицинское приборостроение". 2018. Т. 8, № 2 (27). С. 82-90.
- Орда-Жигулина Д.В., Орда-Жигулина М.В., Старченко И.Б., Кравчук Д.А. Экспериментальная установка для исследования оптоакустической проточной цитометрии//Моделирование, оптимизация и информационные технологии. 2018. Т. 6, № 3 (22). С. 21-29.
- Старченко И.Б., Кравчук Д.А., Кириченко И.А. Прототип оптоакустического лазерного цитомера//Мед. техн. 2017. № 5. C. 4-7.
- Кравчук Д.А., Старченко И.Б. Математическая модель формирования оптоакустического сигнала для оценки уровня агрегации эритроцитов//Вест. новых медицинских технологий. 2019. № 1. С. 119-123.
- Mohandas N., Gallagher P.G. Red cell membrane: past, present, and future//Blood. 2008. Vol. 112. P. 3939-3948
- DOI: 10.1182/blood-2008-07-161166
- Morse P.M., Ingard K.U. Theoretical Acoustics. Princeton, 1968. 949 p.
- Westervelt P.J., Larson R.S. Laser-excited broadside array//J. Acoust. Soc. Am. 1973. Vol. 54, is. 1. P. 121-122
- DOI: 10.1121/1.1913551
- Diebold G.J. Photoacoustic monopole radiation: Waves from objects with symmetry in one, two and three dimensions//Photoacoustic imaging and spectroscopy. Ed. by L.V. Wong. London. 2009. P. 3-17
- DOI: 10.1201/9781420059922.pt1
- Khairy K., Howard J. Spherical harmonics-based parametric deconvolution of 3D surface images using bending energy minimization//Med. Image Anal. 2008. Vol. 12. P. 217-227.
- Khairy K., Foo J., Howard J. Shapes of red blood cells: comparison of 3D confocal images with the bilayer-couple model//Cell Mol Bioeng. 2008. Vol. 1, is. 2-3. P. 173-181
- DOI: 10.1007/s12195-008-0019-5
- Mugnai A., Wiscombe W.J. Scattering from nonspherical Chebyshev particles. I: cross sections, single-scattering albedo, asymmetry factor, and backscattered fraction//Appl. Opt. 1986. Vol. 25, is. 7. P. 1235-1244
- DOI: 10.1364/AO.25.001235
- Zhang H.F., Maslov K., Sivaramakrishnan M., Stoica G., Wang L.V. Imaging of hemoglobin oxygen saturation variations in single vessels in vivo using photoacoustic microscopy//Appl. Phys. Lett. 2007. Vol. 90, is. 5. P. 1-3
- DOI: 10.1063/1.2435697
- Savery D., Cloutier G. Effect'of red blood cell clustering and aisotropy on ultrasound blood backscatter: A Monte Carlo study//IEEE Trans. Sonics Ultrason. 2005. Vol. 52, no. 1. P. 94-103. URL: https://www.lbum-crchum.com/publications-fichiers/w62ieeeuffc005Savery.pdf


