Моделирование кинетики химических реакций методом второго порядка для неявных систем
Автор: Кнауб Л.В., Новиков А.Е., Новиков Е.А.
Журнал: Вестник Красноярского государственного аграрного университета @vestnik-kgau
Рубрика: Математика
Статья в выпуске: 10, 2014 года.
Бесплатный доступ
Построен двухстадийный L-устойчивый метод второго порядка для решения неявных систем. Метод отличается от классических схем приближенным нахождением производной решения. Приведены результаты численного моделирования кинетики химической реакции.
Дифференциально-алгебраическая задача, метод типа розенброка, химическая кинетика
Короткий адрес: https://sciup.org/14084952
IDR: 14084952 | УДК: 519.622
Modeling of the chemical reaction kinetics by the second order method for implicit systems
The two-stage L-stable method of the second order for solving the implicit systems is developed. The method differs from the classical schemes by the approximate finding of the solution derivative. The numerical modeling results of the chemical reaction kinetics are presented.
Текст научной статьи Моделирование кинетики химических реакций методом второго порядка для неявных систем
F ( x , x ', t ) = 0 , x ( 1 0) = x 0 , 1 0 < t < t k ,
где x и F – вещественные N -мерные вектор-функции; t – независимая переменная. Современные численные методы обычно предполагают задание явной зависимости производной [1–2], то есть
x' = f (t, x), x (10) = x0
t 0 < t < t k ■
Приведение задачи (1) к виду (2) требует дополнительных затрат на шаг интегрирования, которые связаны с обращением матрицы Fy. Разрешенная задача (2) жесткая, что приводит к необходимости применения L-устойчивых методов, которые нуждаются в обращении матрицы Якоби. Наиболее известные алгоритмы решения задачи (1) основаны на многошаговых численных формулах [3]. Однако многие практические задачи описываются жесткими непрерывно-дискретными системами, которые в современной литературе называют гибридными задачами [4]. Для них характерным является непрерывное описание режимов, смена которых происходит дискретно. В такой ситуации многошаговые методы могут быть малоэффективны. При решении жестких задач широкое распространение получили методы типа Розенброка [5]. Здесь построен двухстадийный L-устойчивый метод второго порядка точности решения неявных задач. Метод отли- чается от классических схем типа Розенброка приближенным нахождением производной решения. Приведены результаты численного моделирования кинетики химической реакции.
Численная схема. Используя обозначение x'=y, задачу (1) можно переписать в виде системы дифференциально-алгебраических уравнений x ' = y, F (x, y, t) = 0, t о < t < tk.
с начальными условиями x ( t о )= x о и y ( t о )= у о . Дополнительное условие y ( t о )= у о можно вычислить, например, решая задачу F ( x о , у , t о )=0 методом установления [6]. Ниже будем предполагать существование и единственность решения задачи (3) и невырожденность матрицы D n = F ny + ahF nX , где a - числовой коэффициент, h - шаг интегрирования, а F ny и F nX - частные производные функции F ( x , у , t ), вычисленные в точке t n . Тогда m -стадийный метод типа Розенброка для численного решения задачи (3) имеет вид [6]
m
m
x n + 1 = x n + Е Pk x • У п + 1 = У п + Е Р к •
i = 1
i = 1
Dk = hF,y.' У,, + Евук,У — ah2F j=1 7
i - 1
i - 1
hF x , + Е в у к x , У п + Е в к , t n + h - Z в 9
j = 1 7
i - 1
i ah
kx
h • у,+Е в ky i j=1
где a , p i , P ij - числовые коэффициенты. При применении численных формул (4) для решения задачи (2) получим классические методы типа Розенброка [5]. Так как у о вычисляется приближенно, будем предполагать выполненным соотношение || F ( x о , у о , t о )|| < Ch p , где || - 1| - некоторая норма в R N , C - константа, не зависящая от величины шага интегрирования, p - порядок точности метода.
Для решения (3) рассмотрим формулу типа Розенброка вида xn+1 = xn + P1 k1 + Р2 k2x • Уп+1 = Уп + P1 k1У + P 2 k2У •
Dk = h [F„ - Уп — alF - F (xn,у,, t,)], k = a-l (kx - Ну, ) / h, (5) D,kx = hF„ ■(Уп + в2,kУ)-ah2F. -hFn(x, + в21 k,yn + в2,F,tn + в21 h), k7 = a
k x - h ( У , + в 21 k" ) ] / h .
Разложим стадии k ix и k iy в ряды Тейлора по степеням h и подставим в первую формулу (5). Сравнивая полученное представление приближенного решения с рядом Тейлора для точного решения, получим условия второго порядка точности схемы (5)
Р 1 + Р 2 = 1 , в 21 Р 2 = 0.5 - fl ■
Разлагая F n +i = F ( x n +i , у п +i , t n +i ) в ряд Тейлора с учетом (6), получим
F n + i = a - 2 ( a 2 - 2 a + 0.5 ) F + O ( h 2 ) .
Условие F n +i =O( h 2) приводит к уравнению a 2-2 a +0.5=0. Данное соотношение обеспечивает L - устойчивость схемы (5) при решении разрешенной задачи. Уравнение a 2-2 a +0,5=0 имеет два вещественных корня. Из численных экспериментов следует, что корень a=1-0,5 ^ 2 предпочтительнее, потому что он приводит к более эффективным расчетам. Требование L -устойчивости промежуточной численной формулы приводит к соотношению ^ 21 = a . В результате получим коэффициенты L -устойчивого метода (5) второго порядка
P i = в 2i = а = 1 - 0.542 , p 2 = 1 - а = 0.5-42 .
Контроль точности. Неравенство для контроля точности построим по аналогии [6-8], то есть на каждом шаге следует проверять неравенство
II k2 - К II< е, где к i x и к 2 x заданы при описании численной схемы (5), s - требуемая точность расчетов, где || -1| - некоторая норма в RN. В расчетах использовалась норма max
1 < i < N
। g i । ; . 1 x n 1 + r
где r - положительное число. Если | y n |< r , то по i -й компоненте решения контролируется абсолютная ошибка rε ; в противном случае контролируется относительная ошибка ε . В отличие от методов типа Розенброка решения разрешенных систем производная в численной формуле (5) вычисляется приближенно, и поэтому при выборе шага дополнительно проверяется неравенство || D n -1 F n || <е .
Тестовый пример. Задача взята из [9], схема реакции имеет вид
2FLB+1CO, --FLBT+H2O . ZLA+FLB < < / K > FLBT+ZHU -
2 2 2 4 k 2
FLB+ZHU < - FLB .ZHU .
где к есть константа скоростей стадий. Последнее уравнение реакции описывает равновесие. Значение K s вычисляется по формуле
Приток углекислого газа на единицу объема обозначается через Fin, где klA - коэффициент массопе-реноса, H - константа Генри и p(CO2) - парциальное давление углекислого газа. В расчетах значение дав- ления p(CO2) предполагается независимым от углекислого газа [CO2], причем k1=18,7, k2=0,58, k3=0,09, k4=0,42, K=34,4, klA=3,3, Ks=115,83, H=737 и p(CO2) =0,9.
Процесс начинается путем смешивания 0,444 моль/литр реагента FLB с 0,007 моль/литр элемента ZHU. В начальный момент времени концентрация углекислого газа полагается равным 0,00123 моль/литр. По переменной у 6 начальное условие задается формулой у 0,6 = K s • y 0,1 * у 0,4 . По остальным компонентам начальные условия равны нулю. Теперь, вводя обозначения концентраций реагентов по формулам y 1 =[FLB], у 2 =[CO 2 ], у 3 =[FLBT], у 4 =[ZHU], у 5 = [ ZLA ] и у 6 =[FLB.ZHU], получим систему уравнений вида
Му' = f ( у ) , у ( 0 ) = у 0 , у '( 0 ) = у ‘ , у £ R 6 , 0 < t < 180 . (6)
Ранг матрицы M равен пяти и она имеет вид
< 1 0 0 0 0 0 Л
М =
0 0 0 0 1 0
ч 0 0 0 0 0 0 ;
Функция f ( y ) записывается следующим образом:
f 1 = - 2 r + r 2 - r3 - r , f 2 = - 0.5 r - r4 - 0.5 r + F in , f 3 = r - r + r , f 4 =- r 2 + r 3 - 2 r 4 , f 5 = r 2 - r 3 + r 5 , f 6 = Ks * у 1 * у 4 - у 6 •
Значения переменных r i , 1 < i < 5 , и Fin задаются формулами:
rl = ki • у4 • У^2 , r2 = k2 • у3 • у4 , r3 = 7 k2 • у1 • у5 , K r4 = k3 * у1 * у42 , r5 = k4 * у62 * у22 , Fin = klA *[ p (CO2)/H - у 2 ].
Начальные условия имеют вид у0 =(0.444, 0.00123, 0., 0.007, 0., Ks ■ уw • ум)T, у0 = f (у0).
Результаты расчетов. Расчеты проводились на PC Intel(R) Core(TM) i7-3770S CPU@3.10GHz с двойной точностью. Задаваемая точность £ расчетов полагалась равной 10-2. Моделирование выполняется на интервале времени [0,180]. Решение в конце интервала интегрирования имеет вид у1 = 0.115, у 2 = 0.120 *10-2, у 3 = 0.161, у4 = 0.366 *10-3, у 5 = 0.171 * 10-1, у6 = 0.487 *10-2.
Зависимость концентрации CO 2 от времени приведена на рисунке.
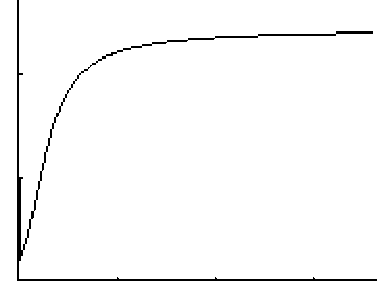
Зависимость концентрации CO 2 от времени
Заключение. Из результатов сравнения построенного алгоритма интегрирования с методом типа Ро-зенброка для разрешенных задач следует, что эффективности алгоритмов отличаются незначительно. Отсюда можно сделать вывод, что построенный алгоритм можно применять для решения как разрешенных, так и неразрешенных относительно производной задач.


