Моделирование пульсирующих потоков крови для задач оптической когерентной томографии в офтальмологии
Автор: Фролов Сергей Владимирович, Потлов Антон Юрьевич, Проскурин Сергей Геннадьевич, Фролова Татьяна Анатольевна
Рубрика: Междисциплинарный подход в задачах регенеративной медицины
Статья в выпуске: S, 2020 года.
Бесплатный доступ
Оптическая когерентная томография - метод неинвазивной медицинской диагностики, основанный на зондировании исследуемого биообъекта излучением ближнего инфракрасного диапазона с последующим детектированием и анализом обратно отраженного и рассеянного назад потока фотонов. Большинство систем оптической когерентной томографии используется в офтальмологии для диагностики состояния сетчатки, зрительного нерва и переднего отрезка глаза. Целью проводимых исследований является повышение достоверности физического моделирования сетчатки глаза на основе использования фантомов, в которых достигается имитация деформаций и вибраций стенок кровеносных сосудов. Описываются методы формирования фантома сетчатки глаза, содержащего специальные полости (имитаторы кровеносных сосудов) пригодные для прокачивания кровеимитирующей жидкости. Сетчатка глаза моделируется как многослойная структура. Матриксом для каждого слоя является двухкомпонентный прозрачный жидкий силикон. В качестве поглощающего агента применяется спектральный краситель Indian ink. Частицы диоксида титана служат рассеивателями. Слои формируются последовательно от нижнего (сосудистая оболочка) до верхнего (внутренняя пограничная мембрана). Массовые доли специальных добавок, как и толщина каждого слоя, подбираются индивидуально. Все кровеносные сосуды представлены в виде протяженных связанных полостей. Формирование основания и сложной сети моделируемых кровеносных сосудов выполняется посредством технологии трехмерной печати. Представлено техническое устройство для формирования пульсирующих потоков крови в фантомах сетчатки глаза, содержащих в своем составе имитаторы кровеносных сосудов и насос с регулируемым потоком для прокачки кровеимитирующей жидкости, электромоторов и вибромотора для регулируемых деформаций и вибраций стенок гибкой трубки. При изменении в установке характеристик работы насоса и вибромотора в формируемом ламинарном потоке в микротрубке создаются турбулентности, что приближает достоверность имитации кровотока в сосудах. С использованием разработанного устройства проведены исследования методом оптической когерентной томографии пульсирующего потока в микротрубках, имитирующих кровеносные сосуды. Разработанные фантомы и устройство могут быть использованы для тестирования офтальмологических ультразвуковых и систем оптической когерентной томографии, при проведении научных биомедицинских исследований, в задачах разработки и отладки новых модификаций метода оптической когерентной томографии.
Сетчатка человека, тканеподобный фантом, гемодинамика, ламинарный поток, пульсирующие потоки, прозрачный силикон, абсорбирующие и рассеивающие агенты, микрофлюидика, доплеровская оптическая когерентная томография
Короткий адрес: https://sciup.org/148309594
IDR: 148309594 | УДК: 617.7-07 | DOI: 10.25586/RNU.V9187.20.05.P.047
Modeling of pulsating flows blood for optical coherent tomography in ophthalmology
Keywords: human retina, tissue-like phantom, hemodynamics, laminar flow, pulsating flows, transparent silicone, absorbing and scattering agents, microfluidics, doppler optical coherence tomography
Текст статьи Моделирование пульсирующих потоков крови для задач оптической когерентной томографии в офтальмологии
Оптическая когерентная томография (ОКТ) – метод неинвазивной медицинской диагностики, основанный на зондировании исследуемого биообъекта излучением ближнего инфракрасного диапазона с последующим детектированием и анализом обратно отраженного и рассеянного назад потока фотонов [1]. Ожидаемый объем рынка ОКТ-систем на 2020 г. составляет порядка 2 млрд долларов США. Подавляющее большинство ОКТсистем закупается и используется в офтальмологии [2]. ОКТ-системы используются в этой сфере медицины для диагностики состояния сетчатки, зрительного нерва и переднего отрезка глаза. Причем некоторые современные ОКТ-системы позволяют получать диагностическую информацию не только о строении исследуемых объектов, но и об их функциональном состоянии. Функциональная диагностика на основе ОКТ в первую очередь включает в себе цветовое картирование кровотока и ангиографию [3]. Вопросы, связанные с безопасными и доступными методами тестирования офтальмологических ОКТ-систем в режиме получения структурных изображений, во многом решены. Известно достаточно большое количество подходов к формированию фантомов сетчатки глаза и зрительного нерва, позволяющих имитировать их слоистую структуру и оптические свойства [4]. Аналогичным образом обстоят дела c фантомами переднего отрезка глаза. Вопросы, связанные с формированием и использованием офтальмологических фантомов для тестирования режимов функциональной визуализации, во многом остаются открытыми. Фантомы для функциональной диагностики в ОКТ должны не просто повторять геометрические и оптические свойства моделируемого объекта, но и имитировать движение кровеимитирующих жидкостей в отдельных участках этого объекта.
Фролов С.В. и др. Моделирование пульсирующих потоков крови для задач оптической...
Целью проводимых исследований является повышение достоверности физического моделирования сетчатки глаза на основе использования фантомов, в которых достигается имитация движение кровеимитирующих жидкостей, деформаций и вибраций стенок кровеносных сосудов.
Материалы и методы
Задачу по физическому моделированию пульсирующих потоков крови в центральной артерии и центральной вене сетчатки глаза предлагается условно разбить на две части. Первая часть – это формирование фантома сетчатки глаза [5], содержащего в себе специальные полости (имитаторы кровеносных сосудов), пригодные для прокачивания кровеимитирующей жидкости. Вторая часть – создание специального технического средства для формирования пульсирующих потоков крови в фантомах, содержащих в своем составе имитаторы кровеносных сосудов.
Предлагаемые подходы к решению первой части поставленной задачи во многом сходны с классическими [6]. Сетчатка глаза моделируется как многослойная структура. Матриксом для каждого слоя является двухкомпонентный прозрачный жидкий силикон. Для придания каждому из слоев характерных оптических свойств используются специальные добавки [7–9]. В качестве поглощающего агента применяется спектральный краситель Indian ink. Частицы диоксида титана служат рассеивателями. Слои формируются последовательно от нижнего (сосудистая оболочка) до верхнего (внутренняя пограничная мембрана). Массовые доли специальных добавок, как и толщина каждого слоя, подбираются индивидуально. Для устойчивости формируемого фантома нижний слой располагается на прочном основании толщиной в несколько сантиметров. Для защиты тонких структур в составе фантома он накрывается специальной крышкой, имитирующей хрусталик и роговицу. Расстояние от верхней поверхности крышки до верхнего слоя фантома подбирается таким образом, чтобы соответствовать реальному расстоянию от роговицы до сетчатки глаза. Форма крышки также делается физиологичной. Основание и защитная крышка сочленяются с помощью специальных защелок. Из основания берут начало имитируемые кровеносные сосуды, пронизывающие сосудистую оболочку сетчатки глаза. Все кровеносные сосуды представлены в виде протяженных полостей. Все эти полости являются связанными. Имитатор центральной артерии сетчатки глаза делится на несколько ответвлений, которые ветвятся еще раз. Имитатор центральной вены сетчатки глаза построен аналогичным образом. Причем все мелкие ответвления сосудов попарно соединены. Входы в имитаторы центральной артерии и центральной вены сетчатки глаза снабжены стандартными катетерами. Формирование основания и выступающей из него сложной сети моделируемых кровеносных сосудов осуществлено посредством технологии трехмерной печати прозрачной фотополимерной смолой на основе полилактида. Защитная крышка изготавливается аналогичным образом. Все слои сетчатки глаза наносились на эту основу вручную с использованием миниатюрной кисточки и специального увеличительного стекла со светодиодной подсветкой.
Для формирования пульсирующих потоков в имитаторах кровеносных сосудов разработано специальное устройство, включающее в себя: В1 – впускной клапан, В2 – насос с регулируемым потоком, В3 – гибкую трубку, В4 – электромотор для деформаций гибкой трубки по ходу часовой стрелки, В5 – вибромотор, В6 – электромотор для дефор- маций гибкой трубки против хода часовой стрелки, В7 – ультразвуковой расходомер, В8 – выпускной клапан, В9 – блок управления работой устройства, В10 – источник питания (обобщенная схема процесса моделирования кровотока в сосудах фантома сетчатки глаза рис. 1).
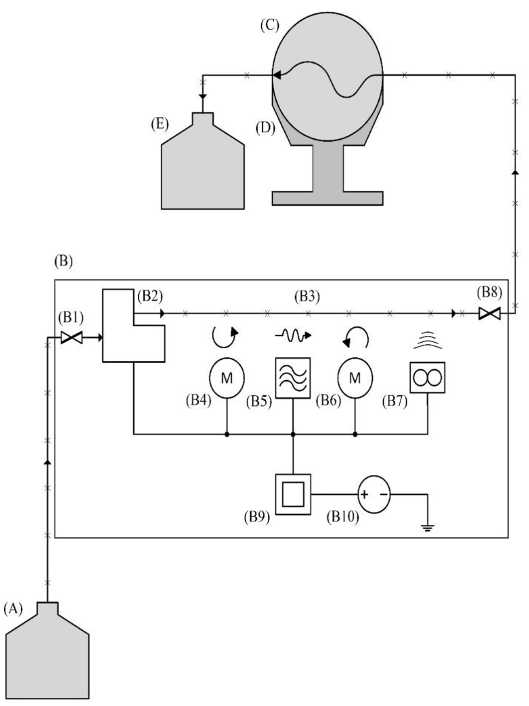
Рис. 1. Схематичное описание проводимых экспериментов по формированию потоков со сложной структурой. Перечень элементов на схеме: А – емкость с кровеимитирующей жидкостью; B – формирователь пульсирующих потоков; C – фантом сетчатки глаза; D – подставка для фиксации тканеимитирующего фантома с кровеносным сосудом; E – емкость для отработанной кровеимитирующей жидкости
Фантом фиксируется в специальной подставке. Полая модель кровеносного сосуда одним своим концом с помощью гибкой трубки соединяется с выходным клапаном устройства для создания пульсаций кровезаменяющей жидкости [10, 11]. Второй конец полой модели кровеносного сосуда с помощью другой гибкой трубки соединяется с емкостью для отработанной кровеимитирующей жидкости. Входной клапан для формирования пульсирующих потоков в фантомах кровеносных сосудов с помощью еще одной гибкой трубки соединяется с емкостью, в которой имеется достаточный запас кровеимитирующей жидкости [12]. Производится включение блока управления устройства для создания пульсаций потоков. Запускается насос с регулируемым потоком, который обеспечивает прокачку кровеимитирующей жидкости через гибкую трубку из емкости с кровеимитирующей жидкостью в виде ламинарного потока. Комбинация из электромотора для
Фролов С.В. и др. Моделирование пульсирующих потоков крови для задач оптической...
регулируемых деформаций гибкой трубки по ходу часовой стрелки, вибромотора для формирования регулируемых вибраций стенок гибкой трубки и электромотора для регулируемых деформаций гибкой трубки против хода часовой стрелки обеспечивает трансформацию ламинарного потока кровеимитирующей жидкости в гибкой трубке в турбулентный поток. Ультразвуковой расходомер бесконтактно контролирует поток перед выпускным клапаном. Если характеристики потока нуждаются в корректировке, блок управления посылает электрические сигналы насосу с регулируемым расходом, электромоторам для деформаций гибкой трубки и вибромотору для динамического изменения параметров их работы. Турбулентный поток через выходной клапан и гибкую трубку доставляется в полые модели кровеносных сосудов в составе фантома сетчатки глаза, проходит сквозь них и через еще одну гибкую трубку вытекает в емкость для отработанной кровеимитирующей жидкости [15].
Результаты и обсуждение
Фантом сетчатки глаза и устройство для формирования пульсирующих потоков в нем были изготовлены и протестированы в лабораторных условиях. В качестве матрикса для изготовления фантомов использовался двухкомпонентный прозрачный платиновый силикон линейки Sorta Clear 12, Sorta Clear 18 и Sorta Clear 40, где число после торговой марки обозначает твердость по Шору. В качестве специальных добавок чаще всего использовались нанопорошок диоксида титана (рассеивающий агент) и краситель Indian Ink (поглощающий агент) [4, 13]. Основа для фантома и его крышка изготавливались из прозрачной фотополимерной смолы на основе полилактида фирмы eSUN [14]. Кровеимитирующая жидкость представляла собой 1%-й раствор интралипида в воде [10]. Протяженная полость в слое силикона создавалась посредством добавления в жидкий силикон тонкой проволоки. После затвердевания фантома проволока извлекалась.
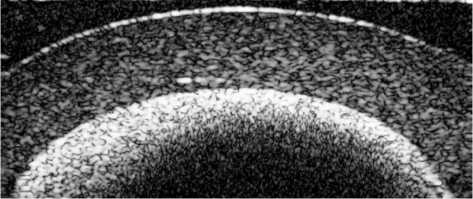
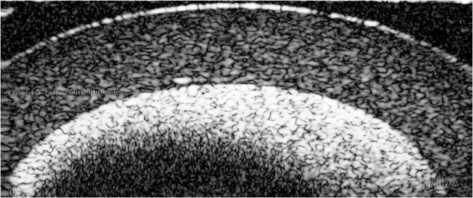
Различные стадии исследования методом ОКТ потоков в микротрубках представлены на рисунке 2.
Для формирования потоков была использования упрощенная версия системы (рис. 1). В ситуации, когда фантом, устройство для формирования пульсирующих потоков в нем и емкости для работы с кровеимтирующей жидкостью успешно интегрированы, но еще не запущены ОКТ, система фиксирует отсутствие потока в микротрубке (рис. 2, а). Есть ламинарный поток в трубке после запуска насоса (рис. 2, б). Варьируя характеристики работы насоса, а также двух электродвигателей и вибромотора, удается добиться турбулентностей в формируемом потоке (рис. 2, в – д). Причем сложная геометрия профиля турбулентного потока также может приводить к возникновению 2p-неопределенностей [10] в отдельных участках внутреннего просвета исследуемой микротрубки.
Таким образом, теоретическая и практическая возможности формирования сложных фантомов сетчатки глаза, учитывающих кровоток, обоснованы. Рассмотрим возможности практического применения полученных результатов. Типичные офтальмологические ОКТ-системы имеют специфичную систему сканирования для удобного и эффективного обследования пациентов. В связи с этим фантом сетчатки для такой системы должен быть компактным, иметь удобный корпус и сохранять работоспособность под различными углами к поверхности. Предложенный фантом сетчатки четко удовлетворяет этим требованиям.
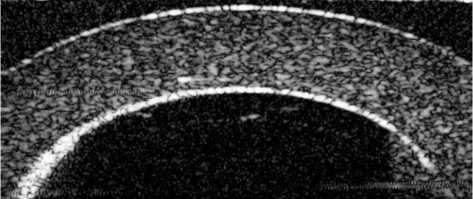
а
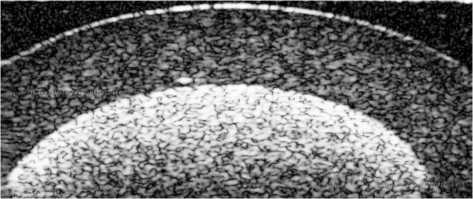
б
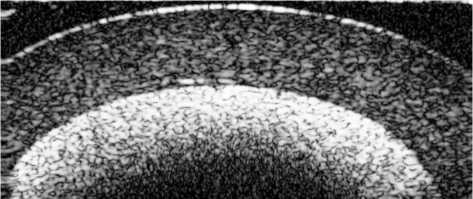
в
г
д
Рис. 2. Стадии формирования пульсирующего потока в кровеносном сосуде: а – исходное состояние с отсутствующим потоком; б – ламинарный поток; в–д – завихрения в центральной, правой и левой частях сосуда соответственно
Фролов С.В. и др. Моделирование пульсирующих потоков крови для задач оптической...
Прочная основа и физиологичная крышка защищают внутреннее содержимое фантома от повреждений. Слои фантома имеют один и тот же матрикс, что обеспечивает их прочное сцепление. К тому же сложная структура из имитаторов кровеносных сосудов объединяет и дополнительно укрепляет слои фантома. Система из трубок, снабжающих кровеимитирующую жидкость, герметична, а мощность насоса является регулируемой, что позволяет фантому работать под любыми углами к поверхности. Поскольку крышка фантома имитирует роговицу, сканирование имитатора сетчатки глаза может производиться бесконтактно с типичного для офтальмологических ОКТ-систем расстояния и с типичным уровнем аберраций.
Следует также отметить высокую физиологичность формируемых в потоке пульсаций и вибраций стенок сосудов за счет создания с помощью насоса, электромоторов и вибромотора регулируемого расхода, деформаций и вибраций трубок, по которым течет кро-везаменяюшая жидкость. Например, гибкая трубка может быть пережатой (посредством деформации на 300 градусов) основную продолжительность времени, но каждые 0,9 секунды на 0,1 секунды разжиматься, имитируя раскрытие митрального клапана сердца. Разжимание может сопровождаться заданным уровнем вибраций стенок гибкой трубки и частичным ее пережатием в другом месте (деформация на 100 градусов как имитация неполной проходимости сосуда).
Выводы
Описаны оригинальные фантомы сетчатки глаза и способ формирования пульсирующих потоков в них. Высокая эффективность предложенных решений достигается за счет учета физиологических особенностей глаза человека и технических особенностей офтальмологических ОКТ-систем.
Ключевые особенности разработанных фантомов сетчатки: разветвленная сеть кровеносных сосудов, изготовленная по технологии 3D-печати; защитная крышка, имитирующая роговицу и хрусталик; прочное основание фантома, являющееся частью сети имитаторов кровеносных сосудов.
Ключевые особенности устройства для формирования пульсирующих потоков в полостях фантомов: использование двух электромоторов для управляемой деформации трубки с потоком кровеимитирующей жидкости; использование вибромотора для обеспечения колебаний стенок имитаторов кровеносных сосудов; контроль работы электромоторов, вибромотора и насоса на основе данных с ультразвукового расходомера.
Показаны примеры формирования полостей в силиконовой основе фантома и потоков со сложной структурой в микротрубках фантома.
Разработанные фантом и устройство могут быть использованы для тестирования офтальмологических ультразвуковых и ОКТ-систем при проведении научных биофизических исследований, в задачах разработки и отладки новых модификации метода ОКТ. Особый интерес представляют задачи разработки новых методов оценки абсолютной и относительной скоростей потоков биологических жидкостей (не только крови, но и лимфы), не проявляющих 2p-неопределенности и эффективно работающих даже при углах, близких к 90 градусам, к исследуемому сосуду.
Публикуется с разрешения «Журнала радиоэлектроники»
Список литературы Моделирование пульсирующих потоков крови для задач оптической когерентной томографии в офтальмологии
- Zimnyakov D.A., Tuchin V.V. Optical tomography of tissues. Quantum Electron, 2002, vol. 32, no. 10, pp. 849-867.
- Mwanza J.C., Budenz D.L. New developments in optical coherence tomography imaging for glaucoma. Current Opinion in Ophthalmology, 2018, vol. 29, no. 2, pp. 121-129. DOI: 10.1097/ICU.0000000000000452
- Lumbroso B., Huang D., Chen C.J. Clinical OCT Angiography Atlas. Jaypee Brothers Medical Publishers, 2015, 174 p.
- Chae Y.G., Park E.K., Jeon M.Y. Jeon B.-H., Ahn Y.-C. Stiffness Comparison of Tissue Phantoms using Optical Coherence Elastography without a Load Cell. Current Optics and Photonics, 2017, vol. 1, no. 1, pp. 17-22. DOI: 10.3807/COPP.2017.T1.017
- Lv X., Chen H., Liu G., Shen S., Wu Q., Hu C., Li J., Dong E., Xu R.X. Design of a portable phantom device to simulate tissue oxygenation and blood perfusion. Applied Optics, 2018, vol. 57, no. 14, pp. 3938-3946. DOI: 10.1364/AO.57.003938


