Модельные хлорофилл- и хинон-содержащие системы, восстанавливающие кислород и теллурит
Автор: Ременников В.Г., Гирва М.В., Белевич И.О.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 6, 2005 года.
Бесплатный доступ
Установлено, что модельные системы, содержащие хлорофилл а в водном растворе детергента и аскорбата, при освещении способны восстанавливать оксианионы теллурита, что сопровождается почернением среды. Восстановление теллурита, вероятно, происходит по механизму фотооксидазной реакщ1и. Теллурит восстанавливается и в хинон-содержащих модельных системах.
Короткий адрес: https://sciup.org/147204359
IDR: 147204359 | УДК: 579.047.64.042
Model chlorophyll-contain systems, reducing of oxygen and tellurite
It was found that model systems, content a chlorophyll a at aqueous solution of detergent and ascorbate on the light was reduce oxyanions of the tellurite and medium appear black in colour. Quinine-content systems reduce oxyanions of the tellurite too.
Текст научной статьи Модельные хлорофилл- и хинон-содержащие системы, восстанавливающие кислород и теллурит
В. Г. Ременников, М. В. Гирёва, И. О. Белевич
Пермский государственный университет, 614990, Пермь, ул. Букирева, 15
Установлено, что модельные системы, содержащие хлорофилл а в водном растворе детергента и аскорбата, при освещении способны восстанавливать оксианионы теллурита, что сопровождается почернением среды. Восстановление теллурита, вероятно, происходит по механизму фотооксидазной реакции. Теллурит восстанавливается и в хинон-содержащих модельных системах.
Изолированные пигменты - хлорофилл, бактериохлорофилл - и их безмагниевые производные, инкубируемые в водном растворе детергентов, способны к фотоокислению кислородом (Шапошникова, Красновский, Дроздова, 1971; Шапошникова, Красновский, 1973), которое сопровождается поглощением его из среды инкубации. Проведение исследований на модельных пигментных системах правомерно, так как первичные процессы, проходящие с пигментом в результате взаимодействия его со светом, и первичные фотохимические изменения в клетке вряд ли существенно отличаются in vivo и in vitro (Евстигнеев, 1975).
Цель настоящей работы - оценка возможности восстановления теллурита с использованием хлорофилла а и хинона в модельных экспериментах.
Объекты и методы исследования
В работе использовали химически чистый хлорофилл а фирмы Fluka AG, Buchs и серные пурпурные бактерии Ectothiorhodospira halophila 51/1в 9624, полученые из коллекции кафедры микробиологии Московского госуниверситета.
Степень фотоиндуцированного поглощения кислорода хлорофиллом а и клетками Е. halophila изучали полярографическим методом с использованием электрода Кларка в герметичной ячейке объемом 1.5 мл в условиях непрерывного перемешивания. Содержание хлорофилла а в водном растворе детергента Тритона Х-100 (0.3%) составляло 0.4 мкМ. Время преинкубации хлорофилла в растворе детергента - 5 мин. Клетки Е. halophila, выращенные в анаэробных условиях до стационарной фазы, вносили в измерительную ячейку в объеме 500 мкл (конечная плотность ОГ175о=2.7), содержащую 50 мМ трис-HCl- буфер (pH 7.6), 10 мМ трис -аскорбат, 20 % NaCl.
Хинон-содержащая система представляла собой водный раствор хинона (витамин К3) в концентрации 10"4 М. Определение степени поглощения кислорода, обусловленное окислением ионов железа и 1,4-нафтохинона, проводили в среде, содержащей 50 мМ трис-НС1-буфер (pH 7.6), 10 мМ ас-корбат-трис, с присутствием 50 мкМ FeSO4, 1 мкМ и 10 мкМ 1,4-нафтохинон.
Результаты и обсуждение
В водном растворе Тритона Х-100 на свету в присутствии хлорофилла а и аскорбата наблюдается поглощение кислорода. Как видно из рис.1, поглощение кислорода прекращается при выключении
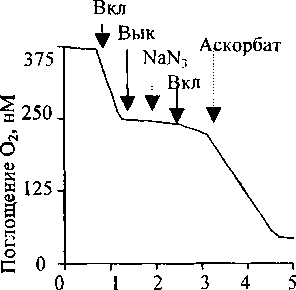
Время, мин
Рис. 1. Фотоиндуцированное поглощение кислорода хлорофиллом а в водном растворе Тритона Х-100 и аскорбиновой кислоты.
Среда инкубации: 50 мМ трис-НС1-буфер (pH 7.6), 10 мМ трис-аскорбат. Добавки: 1 0 мМ NaN3, 100 мМ трис-аскорбат , Вкл и Вык -включение и выключение света
света и добавлении азида, но возобновляется после включения света. При этом ингибирующее действие азида снимается внесением высоких концентраций аскорбиновой кислоты.
Скорость фотоиндуцированного поглощения кислорода зависит от количественного содержания пигмента и линейно возрастает при увеличении его концентрации от 0.005 до 2.0 мкг/мл, что свидетельствует о возможности использования полярографического метода для определения хлорофилла а в растворе в низких концентрациях. При достижении максимальной скорости поглощения кислорода на фоне увеличения концентрации хлорофилла более чем 2.0 мкг/мл линейность данного процесса нарушается (рис. 2).
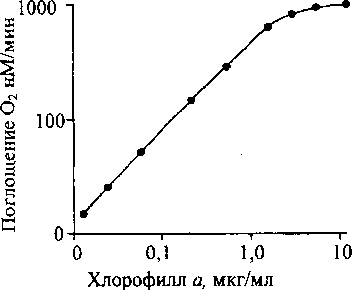
Рис. 2. Зависимость скорости фотоиндуцированного поглощения кислорода от концентрации хлорофилла а
Сравнивая влияние азида натрия на поглощение кислорода клетками Е. halophila и хлорофиллом а отмечаем, что поведение данных объектов сходно. Как видно из рис. 3, уровень ингибирования фотооксидазной реакции, как хлорофиллом а, так
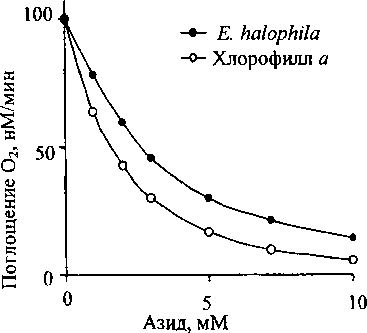
Рис. 3. Зависимость скорости фотоиндуцированного поглощения кислорода клетками Е. halophila и хлорофиллом а, встроенным в мицеллы детергента Тритона
Х-100, от концентрации азида и интактными клетками Е. halophila, зависит от концентрации в среде азида и существенно повышается с увеличением последнего. Схожесть кинетики процессов указывает на идентичность их природы.
Скорость фотооксидазной реакции модельных пигментсодержащих систем и бактериальных клеток не зависит от значения pH среды инкубации (рис. 4), что согласуется с данными опытов, проведенных на изолированных из клеток комплексах реакционных центров, пигмент-белковых комплексах светособирающей антенны (Ременников, Самуилов, 1980) и хлорофилле a (Abdourashitova et al., 1984).
О2, мкМ
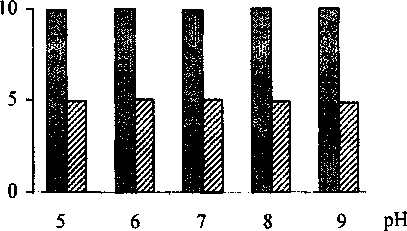
и хлорофилл а и клетки Е. halophila
Рис. 4. Влияние pH среды инкубации на фотооксидазную активность клеток Е. halophila и бактериохлорофилла а. Данные выражены в мкМ О2, поглощенного за 1 мин.
Таким образом, можно полагать, что фотооксидазная активность пурпурных бактерий Е. halophila обусловлена непосредственным взаимодействием бактериохлорофилла антенны с кислородом. Возможно, что этот процесс выполняет приспособительную функцию, биологический смысл которой заключается в удалении кислорода из среды инкубации и обеспечении анаэробных условий, необходимых для развития бактериальной популяции.
По нашим данным, фотооксидазная реакция способна восстанавливать не только кислород, но и оксианионы теллурита (рис. 5).
Рис. 5. Фотовосстановление теллурита калия хлорофиллом а (1, 2, 3) и хиноном (4, 5)
В первой пробирке - результат восстановления теллурита хлорофиллом а, встроенным в мицеллы детергента Тритона Х-100; в качестве донора электронов использована аскорбиновая кислота в концентрации 10 мМ. В данном случае происходит восстановление теллурита до теллура (Мооге, Kaplan, 1992), что выражается в почернении содержимого пробирки.
Во второй пробирке в теллурит добавлен азид натрия (NaN3) 10 мМ. Азид ингибирует процесс восстановления теллурита подобно подавлению фотооксидазной реакции (Барский и др., 1986; Ре-менников, 1996). В результате добавления 100 мМ аскорбиновой кислоты происходит снятие ингибирующего действия азида и наблюдается восстановление теллурита до элементарного теллура, о чем свидетельствует черное окрашивание (пробирка 3). Азид, ингибирующий фотоокисление хлорофилла а, является конкурентом аскорбата и кислорода (Барский и др., 1986) (и, вероятно, теллурита). Следовательно, азид конкурентно подавляет процесс взаимодействия аскорбата и окисленной молекулы хлорофилла. Наряду с этим азид является окислителем, так как конкурирует с кислородом -акцептором электронов, поступающих от возбужденного хлорофилла.
Аналогичный результат получен нами в опыте с использованием хинонов (пробирки 4, 5). Хиноны -компоненты энергопреобразующих биомембран, способные к обратимым одно- и двухэлектронным реакциям окисления-восстановления (Олескин, Самуилов, 1988, Нокс и др., 2004). Так, водный раствор хинона в присутствии ЮмМ аскорбиновой кислоты восстанавливает теллурит калия до теллура. Данный процесс подавляется о-фенантролином -ингибитором фотоиндуцированного поглощения кислорода (пробирка 5).
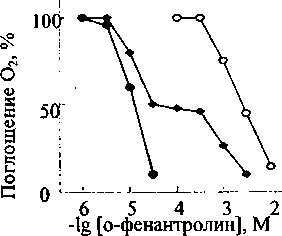
ч Установлено, что присутствие о-фенантролина подавляет процесс темнового поглощения О2, который обусловлен окислением ионов железа и 1,4-нафтохинона, восстановленных аскорбатом (рис. 6).
"4* FeSO4 и 1,4-нафтохинон
1,4-нафтохинон
Рис. 6. Влияние о-фенантролина на поглощение кислорода.
100% соответствует 0,1 мкМ О2, поглощенного за 1 мин.
По нашим данным, степень ингибирования возрастает с увеличением концентрации о-фенантролина. Однако концентрации, подавляющие поглощение кислорода, существенно зависят от условий среды инкубации. В среде, содержащей ионы железа, действие ингибитора проявляется при его концентрации более 5.0 мкМ. Ингибирующая концентрация о-фенантролина в среде с 1,4-нафтохиноном, восстановленным аскорбатом, составляет 0.5 мМ. В условиях смешивания компонентов двух сред наблюдается двухфазность подавления поглощения О2 о-фенатролином. Первая фаза обусловлена ингибированием процесса окисления ионов железа, а вторая - окислением 1,4-нафтохинона. Хорошо выраженное плато отражает различие в чувствительности этих двух компонентов к данному ингибитору.
На этом основании можно сделать вывод о том, что о-фенантролин оказывает ингибирующее действие на систему фотоиндуцированного переноса электронов и систему дыхания. Ингибирование обусловлено взаимодействием о-фенантролина с молекулами мембранного фонда хинонов (в реакционном центре атом железа не меняет своей валентности, а в системе дыхания негемовое железо не функционирует), следствием чего является изменение их окислительно-восстановительных свойств. Ингибирование процесса окисления хинонов мембранного фонда также должно привести к накоплению восстановленной формы QB и QA.
Таким образом, эксперименты, проведенные с использованием хлорофилла а и хинона в модельных условиях, подтверждают вывод о том, что восстановление теллурита калия протекает при участии фотооксидазной реакции. Данный механизм обусловлен переносом электронов с аскорбата и непосредственным взаимодействием бактериохлорофилла а антенны с ТеО32" по следующей схеме: аскорбат -> бактериохлорофилл а -> ТеО32" —»Те°. Данный процесс можно считать экологически важным, поскольку при этом идет восстановление и детоксикация теллурита до менее токсичного теллура.
Список литературы Модельные хлорофилл- и хинон-содержащие системы, восстанавливающие кислород и теллурит
- Барский Е.Л. и др. Ингибирующее действие азида на фотовосстановление кислорода хлорофиллом а в мицеллах Тритона Х-100//Биофизика. 1986. Т. 31, №5. С. 789-792.
- Евстигнеев В. В. О некоторых вопросах эволюции фотосинтетического пигментного аппарата//Происхождение жизни и эволюционная биохимия. М.: Наука, 1975. С. 80-89.
- Красновский А.А., Войновская К.И. Обратимое фотохимическое восстановление и окисление бактериохлорофилла и бактериофеофитина//Докл. АН СССР. 1951. Т. 81, 5. С. 879-882.
- Нокс П.П. и др. Временная стабилизация электрона в хинонной акцепторной части реакционных центров из бактерий Rhodobacter sphaeroides дикого типа и мутанта SA(L223) в зависимости от продолжительности световой активации//Биохимия. 2004. Т. 69, №. 8. С.1096-1103.
- Олескин А.В., Самушов В.Д. Хиноиы и их взаимодействие с ферментными комплексами энерго-преобразующих биомембран//Биохимия. 1988. Т. 53, №10. С. 1619-1627.
- Ременников В. Г., Самуилов В. Д. Взаимодействие компонентов фотосинтетической цепи переноса Rhodospirillum rubrum с кислородом//Докл. АН СССР. 1980. Т. 252. С. 491-494.
- Ременников В. Г. Фотооксидазная активность, ее роль в бактериальном фотосинтезе: Дис... д-ра биол. наук. Пермь, 1996. 325 с.
- Шапошникова М.Г., Дроздова Н.Н., Красновский Л.А. Изучение фотоокисления хлорофилла в водном растворе детергента Тритона Х-100//Биохимия. 1971. Т. 36, № 7. С. 704-711.
- Шапошникова М.Г., Красновский А.А. Сравнительное изучение фотоокисления аналогов хлорофилла в водных растворах детергентов//Там же. 1973. Т. 38, № I.e. 193-201.
- Abdourashitova F.D., Barsky E.L, Gusev M. V. et al. Photooxidase activity and chlorophyll fluorescence of Anabaena variabilis, isolated membranes and pigment-protein complexes treated with detergents and phospholipids II Photobiochem. Photobiophys. 1984. №8. p. 133-142.
- Moore M.D., Kaplan S. Identification of intrinsic highlevel resistance to rare-earth oxides and oxyanions in members of the class Proteobacteria: characterization of tellurite, selenite, and rhodium sesquioxide reduction in Rhodobacter sphaeroides II J. Bacteriol. 1992. Vol. 174. P. 1505-1514.


