Модификация химической структуры производных смоляных кислот и PASS C&T прогноз спектров их фармакологической активности
Автор: Чудов И.В., Зиганшин А.С., Казакова О.Б.
Журнал: Вестник аграрной науки @vestnikogau
Рубрика: Животноводство, рыбоводство и ветеринария
Статья в выпуске: 1 (64), 2017 года.
Бесплатный доступ
Практическая медицина и ветеринария современности использует обширный арсенал лекарственных средств для лечения различных патологических состояний организма животных и человека, а также средства, регулирующие течение обменных реакций. Однако, несмотря на подтвержденную клинической практикой эффективность большинства из этих средств, приходится осознавать, что их активность очень сильно ограничена спектром действия, и в большинстве случаев, наряду с положительным терапевтическим эффектом, сопряжена с проявлением отрицательного побочного действия, порой, превосходящего по тяжести первоначальную патологию. Немаловажное значение имеет и тот факт, что отдельные группы лекарственных средств при длительном применении способны терять свою фармакологическую активность. Целью наших исследований явилось изучение вероятного изменения и расширения спектра фармакологической активности аддуктов смоляных кислот, являющихся компонентами растительного лекарственного сырья с перспективной структурой химической основы для дизайна новых биологически активных соединений, в виду того, что даже незначительные изменения структуры их молекул приводят к существенному изменению проявляемых видов активности. Проведенным PASS C&T анализом установлена связь изменения количественного и качественного состава вероятных фармакологических видов активности в зависимости от химической структуры производных смоляных кислот при введении в них фармакоформных групп в наиболее активных положениях. Исследованиями из 21 аддуктов смоляных кислот выявлены наиболее перспективные для клинических испытаний соединения, представленные дигидрохинопимаровой кислотой, монометиловым эфиром кетотетракарбоновой кислоты, абиетиновой кислотой и ее озонатом. Указанные соединения наряду с высокой выраженностью биологической активности способны обеспечить получение принципиально новых высокоэффективных, экологически чистых и безопасных для животных и человека лекарственных средств с широким спектром ожидаемых фармакологических эффектов при терапии и профилактике распространенных в ветеринарии и животноводстве болезней инфекционной и незаразной этиологии.
Фармакология, тритерпеноиды, лупаны, бетулин, аддукты левопимаровой кислоты, биологическая активность
Короткий адрес: https://sciup.org/147124377
IDR: 147124377 | УДК: 547.914.2/.3:615.2:615.011.5
Modification of the chemical structure of derivatives of resin acids and PASS C&T forecast of the range of their pharmacological activity
The modern applied medicine and veterinary medicine use an extensive arsenal of pharmaceuticals for treatment of various pathological conditions of an organism of animals and the person, and also the tools regulating a current of exchange reactions. However, despite the effectiveness of the majority of these tools confirmed with clinical practice, it is necessary to realize that their activity is very strongly limited to an action range, and in most cases, along with positive therapeutic effect, it is accompanied by manifestation of the negative side effect, sometimes, surpassing tentative pathology in weight. Important value has also the fact that separate groups of pharmaceuticals at the prolonged use are capable to lose the pharmacological activity. The purpose of our researches was studying of probable change and expansion of range of pharmacological activity of the derivative resin acids which are components of plant medicinal raw materials with perspective structure of a chemical basis for design of new biologically fissile connections in a look of the fact that even minor changes of structure of their molecules lead to essential change of the shown types of activity. The carried-out of PASS C&T analysis established connection of change of the quantitative and qualitative structure of probable pharmacological types of activity depending on chemical structure of derivativ resin acids at introduction to them the pharmakoformnykh of groups in the most fissile provisions. Researches from 21 adducts of resin acids revealed the most perspective connections for clinical tests presented by dihydrohinopimaric acid, methyl ester maleopimaric acid, abietic acid and its peroxide. The specified connections along with high expressiveness of biological activity are perspective in ensuring development in essence new high performance, environmentally friendly and safe for animals and the person of pharmaceuticals with a wide range of the expected pharmacological effects at therapy and prevention widespread in veterinary science and livestock production of diseases of an infectious and noncontagious etiology.
Текст научной статьи Модификация химической структуры производных смоляных кислот и PASS C&T прогноз спектров их фармакологической активности
Большое значение в фармакологии приобретает модификация молекул биологически активных веществ растительного происхо^дения. Путем замены в известных соединениях одного или нескольких радикалов (фармакофорных групп) на другие, введением в состав исходной молекулы других химических элементов или иных модификаций, благодаря чему удается увеличить активность исходного компонента, сделать его действие более избирательным, а так^е уменьшить не^елательные стороны его действия и токсические свойства [1, 2, 4, 5, 9]. Такая модификация химической структуры известных биологически активных компонентов лекарственного растительного сырья преследует не только практическую цель – получение новых лекарственных веществ с ну^ными фармакологическими и биологическими свойствами, но и является одним из методов познания общих и частных закономерностей обусловливающих переход одного вида активности в другой [3, 4, 6].
Одновременно с этим подвергнуть да^е первичным доклиническим испытаниям большое количество модифицируемых производных химических веществ на все вероятные виды активности остается малореальным да^е в современных условиях развития фармации. По этой причине в настоящее время фармакологи и токсикологи всего мира используют возмо^ности определения потенциала биоактивности новых химических веществ путем компьютерного анализа [4, 6, 7]. Такой подход основан на кластерном изучении и сопоставлении большого массива известных лекарственных веществ с подтвер^денными клиническими исследованиями фармакологическими свойствами, сгруппированных по их химической структуре и по видам проявляемых ими видов биологической активности [4, 5, 9].
Целью наших исследований явилось изучение вероятного изменения фармакологической активности аддуктов смоляных кислот, являющихся перспективной основой для дизайна новых биологически активных соединений для фармацевтической промышленности, в виду того, что да^е незначительные изменения структуры их молекул приводят к существенному изменению проявляемых видов активности.
Объектом исследований явились 21 новая производная смоляных кислот (абиетиновая кислота и ее озонат, хинопимаровая кислота и 5 ее производных; малеопимаровая кислота, 13 ее линейных амидов и амидов с аминокислотными остатками), совместно разработнных и синтезированных в ФГБУН «Институт химии Уфимского научного центра Российской академии наук» (рис. 1).
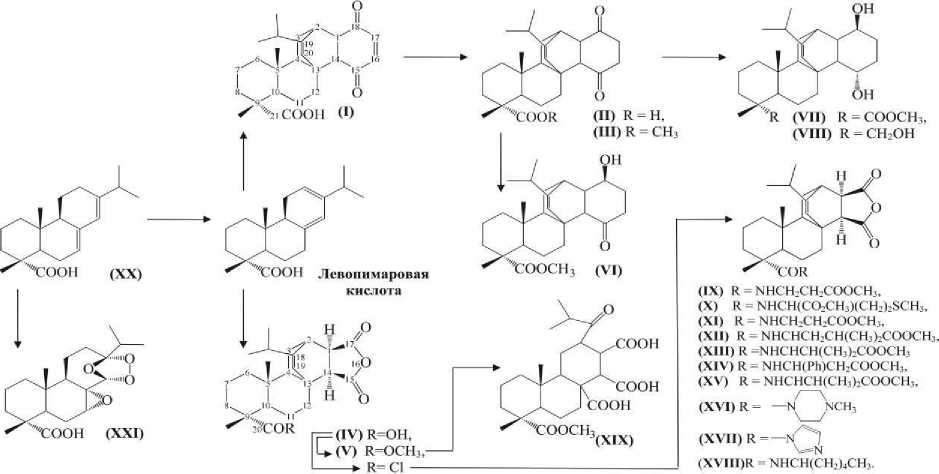
Рисунок 1 – Схема синтеза новых производных смоляных кислот
^нализ вероятных видов биологической активности новых производных смоляных кислот и их выра^енность осуществляли с использованием авторизованного доступа к ме^дународной компьютерной системе PASS C&T ( Prediction of Activity Spectra for Substances: Complex & Training ) Ver . 2.0, разработанной в ФГБУ «Научно-исследовательский институт биомедицинской химии имени В.Н. Ореховича» Российской академии медицинских наук ( http://pharmaexpert.ru/PASSOnline ) [10].
Проведенный нами компьютерный PASS C&T анализ возмо^ности изменения фармакологической активности новых производных смоляных кислот (рис. 1) в зависимости от радикалов, присоединяемых в их наиболее реакционно-способных поло^ениях (С20 – для производных малеопимаровой кислоты; С15, С18 и С21 – для производных хинопимаровой кислоты), показал на изменения как количества потенциальных фармакологических эффектов (рис. 2), так и вероятности их выра^енности.
Как видно из рисунка 2, количество видов биологической активности хинопимаровой кислоты (соединение I) и ее новых производных (соединения II, III, VI-VIII) при условии достоверности Pa > Pi было примерно одинаковым, и составляло 370,6±36,6 возмо^ных эффектов, а при условии достоверности Pi < Pa > 0,05 – 66,6±0,9 видов активности.
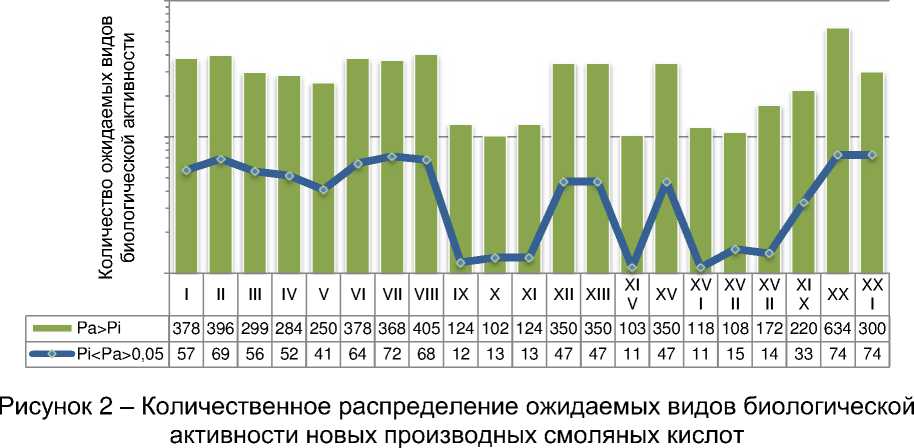
Наиболее существенные изменения количественного состава о^идаемых биологических видов активности нами были отмечены при возмо^ных заменах радикалов малеопимаровой кислоты (соединение IV) в поло^ении С 20. Так, компьютерный PASS C&T анализ химической структуры малеопимаровой кислоты (соединение IV), ее метилового эфира (соединение V), а так^е линейных амидов с фрагментами аминокислот, представленными L -лейцином, L -валином и DL -валином в поло^ении С 20 малеопимаровой кислоты (соединения XII, XIII и XV соответственно), имели количество вероятных видов биологической активности, при условии Pa > Pi , в пределах ~284-350, а при условии Pi < Pa > 0,05 – 46,8±3,9, тогда как включение в поло^ение С20 малеопимаровой кислоты амидных фрагментов, представленных аминокислотами – α - и β -аланином, L -метионином, L -фенилаланином (соединения XI, IX, Х и XIV соответственно), а так^е фрагментов N -метилпиперазина (соединение XVI) и 1 Н -имидазола (соединение XVII), приводило как к сни^ению количества о^идаемых эффектов до 114,2±10,9 при условии Pa > Pi и, до 12,0±1,0 при условии Pi < Pa > 0,05, что в ~2,6 и ~3,9 раз соответственно меньше, в сравнении с исходной структурой кислоты малеопимаровой (соединение IV).
^биетиновая кислота (соединение ХХ), слу^ащая источником для получения левопимаровой кислоты и ее аддуктов (хино- и малеопимаровая кислоты), равно как и их производных, характеризовалась наибольшим количеством о^идаемых видов биологической активности, равной 634 при условии Pa > Pi , а при условии Pi < Pa > 0,05 – 74 эффектов, и, несмотря на то, что продукт ее озонолиза (соединение XXI) характеризовался уменьшением о^идаемых видов биологической активности до 300 при условии Pa > Pi (в ~2
раза меньше в сравнении с исходной кислотой абиетиновой), состав и количество о^идаемых эффектов у озоната абиетиновой кислоты, при условии Pi < Pa > 0,05, оставались неизменными.
^нализом наиболее выра^енных о^идаемых видов биологической активности рассматриваемых производных смоляных кислот, были выделены следующие виды активности: мембраностабилизирующая; цито- и гепатозащитная; противоязвенная; противовоспалительная; иммуностимулирующая и иммуносупрессорная; противовирусная; холестерин-и кальций регулирующая, а в отдельных случаях антиоксидантная и антитоксическая.
Нами установлено, что продукт озонолиза абиетиновой кислоты (соединение XXI), а также хино- и малеопимаровая кислоты (соединения I и IV), полученные в реакции циклоприсоединения Дильса-Альдера, уступают исходной кислоте абиетиновой (соединение XX) по многим из выделенных показателей. Так, вероятность цитопротекторной активности у хино- и малеопимаровой кислот (соединения I и IV) была меньше в сравнении с кислотой абиетиновой (соединение XX) в ~1,5 раз, такой ^е уровень пони^ения вероятности активности составил у хинопимаровой кислоты (соединение I) в отношении мембраностабилизирующей и гепатозащитной активности, а у малеопимаровой кислоты (соединение IV) вероятность мембраностабилизирующей активности отсутствовала даже в зоне абсолютно недостоверных значений, хотя ожидаемые гепатозащитные свойства в сравнении с кислотой абиетиновой (соединение XX) превышали на 11,3%. Как у хино-, так и у малеопимаровой кислот (соединения I и IV) компьютерный PASS C&T анализ показал отсутствие вероятности проявления противоязвенной активности, хотя у кислоты абиетиновой (соединение XX) вероятность этой активности находилась на уровне 58,4±1,2%. Однако, со стороны вероятности противовоспалительной активности нами установлена противополо^ная зависимость, когда ее отсутствие в зоне достоверности у кислоты абиетиновой (соединение XX), достоверно ожидалось у хино- и малеопимаровой кислот (соединения I и IV) на уровне 38,2±1,5% и 47,1±4,6% соответственно. Вероятность проявления противовоспалительной активности хино- и малеопимаровой кислотами (соединения I и IV) подтверждается еще и тем, что PASS C&T анализ структуры их химических молекул показал также вероятность антагонизма к арахидоновой кислоте на уровне 23,5±1,9% для хинопимаровой кислоты (соединение I), и, антагонизма к гистамину, на уровне 27,9±1,6%, для кислоты малеопимаровой (соединение IV).
Соотношение вероятности иммуностимулирующей активности к иммуносупрессорной у абиетиновой кислоты (соединение XX) составило 1 : 1,55, тогда как у кислоты малеопимаровой (соединение IV) оно о^идалось на уровне 1 : 1,2, а анализ указанных биологических видов активности у кислоты хинопимаровой (соединение I) показал отсутствие вероятности проявления иммуностимулирующей активности, при о^идаемой иммуносупрессорной на уровне до 78,1±0,7%, а так^е антибактериальной и противовирусной активностей на уровне 28,7±6,5% ( Р >0,05) и 62,9±1,16 ( Р <0,05) соответственно.
Необходимо так^е отметить, что о^идаемая активность озоната абиетиновой кислоты (соединение XXI) находилась в таких ^е пределах, что и у кислоты хинопимаровой (соединение I), за исключением холестеринрегулирующего действия, вероятность проявления которого у кислоты абиетиновой (соединение XX) отсутствовала, а у озоната абиетиновой кислоты (соединение XXI) и кислоты малеопимаровой (соединение IV) доверительно прогнозировалась на уровне 48,0±4,1% и 43,4±0,5% соответственно, что в ~1,7 раз превышало вероятность проявления этого вида активности у кислоты хинопимаровой (соединение I).
Дигидрохинопимаровая кислота (соединение II), являющаяся производным хинопимаровой кислоты (соединение I), благодаря отсутствию двойной связи в положении С 16- С 17 (рис. 1), показала увеличение вероятности проявления мембраностабилизирующей и цитопротекторной активности в ~1,4 раз в сравнении с соединением I, при равноценном сни^ении антиоксидантных свойств и увеличении вероятности проявления гепатопротекторной активности до уровня 80,7±0,4% (что в ~1,7 раз выше вероятной активности хинопимаровой и озоната абиетиновой кислот - соединения I и XX), а также вероятности проявления холестеринрегулирующей активности до 66,2±1,7% (что в ~2,5 и ~1,4 раз выше вероятности проявления этой ^е активности хинопимаровой и озонатом абиетиновой кислот соответственно). Разрыв двойной связи в положении С 16- С 17 хинопимаровой кислоты также характеризовался пони^ением вероятности проявления иммуносупрессорной и противовирусной активностей до 35,7±0,6% и 38,3±1,1% (в ~2,1 и ~1,6 раз меньше) соответственно, в сравнении с вероятностью проявления аналогичных видов активности кислотой хинопимаровой (соединение I). Кроме того, в отличие от отсутствующей противоязвенной активности у кислоты хинопимаровой (соединение I) ее вероятность проявления у кислоты дигидрохинопимаровой составила 26,3±1,3% при некотором увеличении вероятности противовоспалительной активности, что также можно связать с наличием у соединения II в спектре вероятных активностей антагонизма не только к кислоте арахидоновой, но и к гистамину, в пределах 21,7±2,4% и 15,8±0,4% соответственно. Несмотря на то, что вероятность противоязвенной активности у кислоты абиетиновой (соединение XX) была в ~2,2 раз выше в сравнении с кислотой дигидрохинопимаровой (58,4±1,2% против 26,3±1,3%), тем не менее, наряду с кислотой хинопимаровой (соединение I) у них присутствовала достаточно высокая вероятность проявления противовоспалительной активности.
Метилирование карбоксильной группы дигидрохинопимаровой кислоты (соединение II) в поло^ении C21 с получением метилового эфира дигидрохинопимаровой кислоты (соединение III) приводило к сни^ению вероятности проявления мембраностабилизирующей и цитопротекторной видов активностей в ~1,4 и ~1,3 раз в сравнении с соединением II, хотя гепатопротекторная активность не имела значительного отличия и оставалась в ~1,7 раз более выра^енной в сравнении с кислотой хинопимаровой (соединение I). Наличие метоксикарбонильной группы у соединения III в поло^ении C21 так^е приводило к появлению вероятности о^идаемой иммуностимулирующей активности до уровня 22,2±1,1%, при отсутствии доверительной вероятности иммуносупрессии и повышении вероятности противовирусной активности в ~1,4 раз, в сравнении с кислотой дигидрохинопимаровой (соединение II), однако, она оставалась в ~1,2 раз меньше вероятности этой активности в сравнении с соединением I. Вероятность холестеринрегулирующей активности метилового эфира дигидрохинопимаровой кислоты (соединение III) оставалась на том ^е уровне, как и у кислоты хинопимаровой (соединение I).
Замена одной кетонной группы в поло^ении C 18 метилового эфира дигидрохинопимаровой кислоты (соединение III) на стереогидроксильную, с получением метилового эфира 1 β -гидроксидигидрохинопимаровой кислоты (соединение VI) приводило к самому сильно выра^енному увеличению вероятности большинства из анализируемых видов биологических активностей в сравнении с соединениями I, II и III. В частности, вероятность цито- и гепатопротекторной видов активностей у соединения VI составила 62,4±2,2% и 90,8±6,3% (что в ~1,7 и 1,9 раз выше вероятной активности кислоты хинопимаровой – соединения I; в ~1,6 и 1,1 раз выше вероятной активности метилового эфира дигидрохинопимаровой кислоты – соединения III) соответственно. Вероятность проявления противовоспалительной активности 1 β -гидроксидигидрохинопимаровой кислотой составила 53,4±4,7% против 38,2±1,5% и 39,6±0,9 (что в ~1,4 раз меньше) в сравнении с кислотой хинопимаровой (соединение I) и ее метиловым эфиром (соединение III). Присутствие гидроксильной стереогруппы в поло^ении C 18 химической структуры метилового эфира 1 β -гидроксидигидрохинопимаровой кислоты так^е способствовало повышению вероятности равноценных иммуностимулирующих и иммуносупрессорных свойств, составив соответственно 42,5±5,0% и 47,3±4,8%, при самой высокой, из всех производных хинопимаровой кислоты (соединений I-III и VII-VIII), вероятностью противовирусной активности на уровне 68,0±0,7%. Одновременно с этим следует отметить исключение вероятности проявления соединением VI, в отличие от описанных выше производных хинопимаровой кислоты, мембраностабилизирующей и холестеринрегулирующей видов активности при появлении вероятности участия в обмене ионов кальция до 37,8±0,5%.
Замена кетонных групп в поло^ениях С15 и С18 дигидрохинопимаровой кислоты при наличии метоксикарбонильной группы в поло^ении С21 (соединение VII), а так^е замена карбонильного радикала в поло^ении С21 на метоксигидроксильную группу, при одновременной замене двух кетонных групп в поло^ениях С15 и С18 на стереогидроксильные (соединение VIII) не приводило к значительному изменению вероятности проявления цито- и гепатопротекторной, противовоспалительной, а так^е иммуностимулирующей и иммуносупрессорной активностей в сравнении с метиловым эфиром 1β-гидроксихинопимаровой кислотой, однако, благодаря указанным модификациям структуры химических молекул соединений VII и VIII о^идаемая мембраностабилизирующая активность составила 42,7±1,6% и 56,0±1,1% соответственно, при ее отсутствии у сравниваемого соединения VI. Одновременно с этим, у соединения VII, присутствие двух стереогидроксильных групп в поло^ениях С15 и С18, в сравнении с соединением VI, у которого стереогидроксильная группа присутствовала только в поло^ении С18 с кетонной группой в поло^ении С15, при равноценной вероятности проявления кальцийрегулирующей активности на уровне ~38,7±0,5%, приводило к появлению вероятности выра^енной холестеринрегулирующей активности, отсутствующей у соединений VI и VIII, и, составившей 66,8±1,1%. Напротив, замена карбонильного радикала в поло^ении С21 на метоксигидроксильный, при наличии двух стереогидроксильных групп в положениях С15 и С18 (соединение VIII) в сравнении с метиловым эфиром 1 в -гидроксидигидрохинопимаровой кислотой (соединение VI) приводило к потере вероятности проявления холестерин- и кальцийрегулирующей активностей, с появлением вероятности антиоксидантной активности, достигающей 18,3±6,7%, тогда как она отсутствовала у всех производных кислоты хинопимаровой, за исключением дигидрохинопимаровой кислоты (соединение II).
Таким образом, хинопимаровая кислота (соединение I) и ее производные (соединения II, III VI-VIII) характеризуются достаточно высокой вероятностью проявления мембраностабилизирующей, цито- и гепатозащитной, а также противовоспалительной видами активностей, имеющих ва^ное значение при лечении многих патологий заразной и незаразной этиологии, в качестве патогенетического влияния на организм больного животного.
При компьютерном PASS C&T анализе возможной биологической активности малеопимаровой кислоты (соединение IV) и ее производных (соединения V, IX-XIV) нами, также как и в случае с производными хинопимаровой кислоты (соединения I-III и VI-VIII), отмечены существенные изменения отдельных показателей. Так, метилирование малеопимаровой кислоты (соединения IV) посредствам замены карбоксильной группы в положении С 20 на метоксикарбонильную (с образованием соединения V -метиловый эфир малеопимаровой кислоты), приводило к сни^ению вероятности цитопротекторной и холестеринрегулирующей активностей с 46,5±0,7% до 37,2±1,1%, и, с 43,4±0,5% до 35,2±0,8% соответственно (снижение вероятности в ~1,25 раз), а так^е к пони^ению вероятности иммуностимулирующей активности с 40,6±5,2% до 26,3±0,9% (сни^ение вероятности в ~1,5 раз), при этом сдвиг иммуностимулирующей активности к иммуносупрессорной был более негативным, составив 1,0 : 1,6 у метилового эфира малеопимаровой кислоты (соединение V) против соотношения 1,0 : 1,2 -у исходной кислоты малеопимаровой (соединение IV). Пони^ение вероятности о^идаемого иммуностимулирующего эффекта у соединения V с одновременным угнетением супрессии приводило и к сни^ению вероятности его противовирусной активности.
Значения показателей вероятных активностей амидов малеопимаровой кислоты с фрагментами метиловых эфиров L -лейцина (соединение XII), L -валина (соединение XIII) и DL -валина (соединение XV), установленных посредством компьютерного PASS C&T анализа характеризовались сравнимой с вероятностью цитопротекторной и гепатозащитной видов активностей кислоты малеопимаровой (соединения IV). При этом вероятность проявления мембраностабилизирующей активности соединениями XII, XIII и XV составила 48,0±1,4%, тогда как вероятность этого вида биологической активности у кислоты малеопимаровой (соединения IV) отсутствовала. Однако, вероятность иммуностимулирующей активности у соединений XII, XIII и XV составила лишь 33,2±6,8%, что в ~1,2 раз меньше вероятности этой ^е активности у кислоты малеопимаровой (соединения IV), кроме того, в сравнении с последним, соотношение вероятностей иммуностимулирующей и иммуносупрессорных эффектов у амидов малеопимаровой кислоты с фрагментами метиловых эфиров L -лейцина, L -валина или DL -валина (соединения XII, XIII и XV) имело тенденцию к смещению в сторону супрессии, составив 1,0 : 1,4 против 1,0 : 1,2 у кислоты малеопимаровой (соединения IV).
Коньюгат малеопимаровой кислоты с фрагментом метилового эфира L -фенилаланина (соединение XIV) наряду с выраженной, на уровне 60,8±1,2%, вероятностью мембраностабилизирующей активности, характеризовался отсутствием вероятности проявления цито- и гепатозащитных свойств. Вместе с этим вероятность противовоспалительной активности составила 39,6±1,0% (в ~1,2 раз меньше в сравнении с кислотой малеопимаровой - соединением IV), а вероятность проявления иммуностимулирующей, равно как и иммуносупрессорных видов активности была в ~1,7 и ~1,9 раз меньше в сравнении с исходной кислотой малеопимаровой (соединением IV), при соотношении выраженности того или иного эффектов на уровне 1,0 :1,1.
Наиболее выгодно, с точки зрения спектра и вероятности выра^енности рассматриваемых параметров, из производных малеопимаровой кислоты, равно как и из производных хинопимаровой кислоты, выделяется монометиловый эфир кетотетракарбоновой кислоты (соединение XIX). Компьютерный PASS C&T анализ химической структуры соединения XIX показал вероятность мембраностабилизирующей активности на уровне 94,1±0,4% (что сопоставимо с вероятностью активности абиетиновой кислоты – соединения XX, в ~1,6 раз превосходит вероятность этой активности у озоната абиетиновой кислоты – соединения XXI и кислоты хинопимаровой – содинения I), при этом вероятность цито- и гепатозащитной видов активностей составила соответственно 62,4±2,2% и 88,6±0,9%. Несмотря на более низкую вероятность антитоксических свойств у монометилового эфира кетотетракарбоновой кислоты в ~1,8 раз в сравнении с озонатом абиетиновой кислоты (соединением XXI), вероятность антиоксидантной активности соединения XIX была сравнима как с вероятностью этой активности у кислоты хинопимаровой (соединение I), так и с активностью озоната абиетиновой кислоты (соединения XXI). Наряду с высокой вероятностью противовоспалительной активности, компьютерный PASS C&T анализ химической структуры монометилового эфира кетотетракарбоновой кислоты (соединения XIX) показал вероятность противоязвенной активности на уровне 44,4±0,7%, в ~1,7-2,0 раз превосходя вероятность этого вида активности у кислоты дигидрохинопимаровой (соединения II) и метилового эфира малеопимаровой кислоты с фрагментом L-метионина в поло^ении С 20 (соединения X). Несмотря на то, что у кислоты абиетиновой (соединения XX) вероятность противоязвенной активности была несколько выше, чем у монометилового эфира кетотетракарбоновой кислоты (58,4±1,2% против 44,4±0,7%), в спектре действия первого, вероятность противовоспалительной активности отсутствовала. Вероятность иммуностимулирующей активности монометилового эфира кетотетракарбоновой кислоты (соединения XIX) составила 60,3±2,3% (что в ~2 раза выше в сравнении с абиетиновой кислотой – соединением XX), при этом вероятность иммуносупрессорной активности составила лишь 10,1±0,9%, а их соотношение – 6,0 : 1,0. Как и у многих производных малеопимаровой кислоты, рассматриваемых нами, монометиловый эфир кетотетракарбоновой кислоты (соединение XIX) характеризовался высокой вероятностью кальцийрегулирующей активности (на уровне 38,6±0,4%) при одновременной вероятности холестеринрегулирующей активности на уровне 36,8±0,3%.
-
- проявление противоязвенной активности производными хинопимаровой кислоты возмо^но при условии перевода ее в кислоту дигидрохинопимаровую (соединение II) посредствам разрыва C 16- C 17 двойной связи с одновременным присутствием карбоксильной группы в поло^ении С 21;
-
- проявление противоязвенной активности производными малеопимаровой кислоты возмо^но при условии метилирования карбоксильной группы в поло^ении С 20 при одновременном присутствии группы метилмеркаптана (как у метилового эфира малеопимаровой кислоты с фрагментом L -метионина), либо при одновременном присутствии карбоксильных групп;
-
- метилирование карбоксильной группы в поло^ении С 21 дигидрохинопимаровой кислоты приводит к сни^ению вероятности проявления рассматриваемых видов биологической активности с появлением маловыра^енной вероятности иммуностимулирующего эффекта;
-
- метилирование карбоксильной группы в поло^ении С 20 малеопимаровой кислоты с включением фрагментов N -метилпиперазина или 1 Н -имидазола приводит как к сни^ению вероятности рассматриваемых видов биологических активностей, так и их спектра;
-
- замена одной кетонной группы в поло^ении С 18 на гидроксильную, в структуре метилового эфира дигидрохинопимаровой кислоты приводит к потере вероятности мембраностабилизирующей активности;
-
- замена одной или двух кетонных групп в поло^ениях С 15 и (или) С 18 в структуре метилового эфира дигидрохинопимаровой кислоты приводит к появлению равноценно выра^енных иммуностимулирующего и иммуносупрессорного видов биологической активности;
-
- повышение вероятности иммуностимулирующей активности производных малеопимаровой кислоты возмо^но при метилировании и карбоксилировании малеопимаровой кислоты;
-
- вероятное проявление кальцийрегулирующей активности производными хинопимаровой кислоты возмо^но только при наличии метоксикарбонильного радикала в поло^ении С 21 с одновременным разрывом двойной связи в поло^ении С 16- С 17, с заменой одной или двух кетонных групп в поло^ениях С 15 и С 17 на гидроксильные;
-
- вероятное проявление кальцийрегулирующей активности производными малеопимаровой кислоты возмо^но при метилировании карбоксила малеопимаровой кислоты в поло^ении С 20 с включением в ее состав амидов фрагментами аминокислот;
-
- наличие вероятности проявления антиоксдантных свойств производными хинопимаровой кислоты обуславливается наличием гидроксильных групп радикалов, располо^енных в поло^ении С 21 (карбоксильного или метоксльного);
-
- присутствие вероятности антиоксидантных и антитоксических свойств у производных малеопимаровой кислоты возмо^но путем насыщения их структуры реакционно-способными карбоксильными группами.
Список литературы Модификация химической структуры производных смоляных кислот и PASS C&T прогноз спектров их фармакологической активности
- Бузлама В.С. Перспективы и пути развития современной экспериментальной и клинической ветеринарной фармакологии/В.С. Бузлама//Современнные проблемы ветеринарной фармакологии и токсикологии: мат-лы II съезда ветеринарных фармакологов и токсикологов России. -Казань: ФЦТРБ-ВНИВИ. -2009. -С. 580-582.
- Дорожкин В.И. Определение содержания экотоксикантов в сельскохозяйственной продукции растительного происхождения, выращенных на полях после внесения осадков сточных вод с очистных сооружений/В.И. Дорожкин/Биотехнология: токсикологическая, радиационная и биологическая безопасность: материалы Междунар. науч.-практич. конф. -Казань: ФГБУ ФЦТРБ ВНИВИ, 2010. -С. 45-46.
- Казакова О.Б. Синтез и противовоспалительная активность производных хинопимаровой кислоты/О.Б. Казакова, И.В. Чудов, А.Ф. Исмагилова и др.//Биоорганическая химия, 2010. -Т. 36. -№ 2. -С. 277-282.
- Поройков В.В. Компьютерный прогноз биологической активности химических соединений как основа для поиска и оптимизации базовых структур новых лекарств/В.В. Поройков, Д.А. Филимонов//Азотистые гетероциклы и алкалоиды. -М.: Иридиум-пресс. -2001. -Т.1. -С. 123-129.
- Уша Б.В. Перспективность различных направлений нанобиотехнологии для ветеринарии/Б.В. Уша, А.А. Концевова, А.М. Смирнов и др.//Ветеринария. -2012. -№ 2. -С. 53-55.
- Флехтер О.Б. Синтез, прогноз и изучение гепатопротекторной активности производных тритерпеноидов/О.Б. Флехтер, В.В. Поройков, Л.Т. Карачурина //Органический синтез и комбинаторная химия: Тез. докл. Междунар. науч. конф. -Москва-Звенигород. -1999. -С. 21.
- Хабриев Р.У. Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ/Р.У. Хабриев, Е.В. Арзамасцев, Э.А. Бабаян -М.: ФГУ научный центр экспертизы средств медицинского применения, 2005. -829 с.
- Kazakova O.B. Synthesis, structure, and pharmacological activity of (7R,8S)-epoxy-(13R, 17R)-trioxolane abietic acid/O.B., Kazakova, I.E. Smirnova, I.V. Chudov, A.F. Ismagilova et al.//Bioorganic Chemistry, 2013. -Т. 39. -№ 2. -С. 202-210.
- Lagunin A. PASS: prediction of activity spectra for biologically active substances/A. Lagunin, A. Stepanchikova, D. Filimonov, V. Poroikov//Bioinformatics. -2000. -V.16. -№ 8. -P. 747-748.
- Pharma expert predictive services «PASS online» : FSBI «Research Institute of biomedical chemistry named after V.N. Orekhovich» The Russian Academy of medical Sciences. -Mode of access: URL: http://pharmaexpert.ru/PASSOnline (дата обращения: 14.09.2016).


