Модификация метода импрегнации серебром для исследования энтеральной нервной системы
Автор: Марков И.И., Низаметдинова Д.Р., Маркова В.И.
Журнал: Морфологические ведомости @morpholetter
Рубрика: Методы исследования
Статья в выпуске: 3 т.33, 2025 года.
Бесплатный доступ
Отсутствие адекватных методов гистологического исследования энтеральной нервной системы является значительным препятствием для получения достоверных результатов о ее структурной организации на микроскопическом уровне. Использование классических методов импрегнации азотнокислым серебром, к сожалению, не дает удовлетворительных результатов. Цель исследования – доказать эффективность универсального метода импрегнации в идентификации межнейрональных цитоплазматических синцитиальных связей в структурах энтеральной нервной системы человека. Изучены суправитальные препараты стенки кишечника беспородных половозрелых кошек (n=7) и биопсийные фрагменты тонкой и толстой кишки (n=30) длиной 20 см (тонкая кишка) и длиной 10 см (толстая кишка). Фрагменты кишечника после тщательной предварительной подготовки подвергались препарированию в водной среде под стереомикроскопом. Стенка фрагментов разделялась на слизистую и мышечную оболочки, и подслизистую основу. Каждая из оболочек, мышечная, слизистая и подслизистая основа фиксировались в 10% не содержащем метанол формалине в отдельном флаконе. Небольшие фрагменты кишечной стенки обрабатывают 0,2% растворами гидроксидов бария, кальция и магния, размещением их на смоченной этими растворами стекловате. Затем на поверхность фрагментов наносят капли растворов указанных растворов. Нитрата серебра осаждают в сильнощелочной среде (pH=11–13) с использованием 4% гидрохинона в качестве восстановителя. Образование и осаждение гидроокиси серебра происходит как за счет активности самого катиона, так и за счет еще более реакционноспособного аниона. В результате образуются плохо растворимые соединения, которые осаждаются на аргирофильных структурах. Восстановленное из гидроокиси металлическое серебро в виде кристаллов откладывается в точном соответствии с локализацией и концентрацией протравных соединений. Адаптированный метод универсальной импрегнации – результат нанотехнологического принципа искусственного перенаправленного метода коррекции естественных восстановительных свойств клеточных конструкций. Разработанный способ позволяет достичь значительно лучших результатов при изучении гистологических препаратов энтеральной нервной системы по сравнению с имеющимися.
Энтеральная нервная система, кишечник, домашняя кошка, метод импрегнации, нитрат серебра
Короткий адрес: https://sciup.org/143185376
IDR: 143185376 | DOI: 10.20340/mv-mn.2025.33(3).974
The silver impregnation methods modification for the enteric nervous system study
The lack of adequate methods for histological examination of the enteric nervous system is a significant obstacle to obtaining reliable results on its structural organization at the microscopic level. The use of classical methods of impregnation with silver nitrate, unfortunately, does not provide satisfactory results. The aim of the study was to prove the effectiveness of the universal impregnation method in identifying interneuron cytoplasmic syncytial connections in the human enteric nervous system. We studied supravital preparations of the intestinal wall of mongrel mature age cats (n=7) and biopsy fragments of the small and large intestine (n=30) 20 cm long (small intestine) and 10 cm long (large intestine). After careful preliminary preparation, intestinal fragments were dissected in an aqueous medium under a stereomicroscope. The wall of the fragments was divided into the mucous and muscular membranes, and the submucosa. Each of the intestinal membranes, muscularis propria, mucosa, and submucosa were fixed in 10% methanolfree formalin in a separate vial. Small fragments of the intestinal wall were treated with 0.2% solutions of barium, calcium, and magnesium hydroxides by placing them on glass wool moistened with these solutions. Drops of these solutions were then applied to the surface of the fragments. Silver nitrate was precipitated in a highly alkaline medium (pH=11–13) using 4% hydroquinone as a reducing agent. The formation and precipitation of silver hydroxide occurs due to both the activity of the cation itself and the even more reactive anion. This results in the formation of poorly soluble compounds that precipitate on argyrophilic structures. Metallic silver, reduced from the hydroxide, is deposited in the form of crystals in precise accordance with the location and concentration of the mordant compounds. The adapted universal impregnation method is the result of a nanotechnological principle of an artificially redirected method for correcting the natural restorative properties of cellular constructs. The developed method allows for significantly improved results in the study of histological specimens of the enteric nervous system compared to existing methods.
Текст научной статьи Модификация метода импрегнации серебром для исследования энтеральной нервной системы
Markov II, Nizametdinova DR, Markova VI. The silver impregnation methods modification for the enteric nervous system study. Morfologicheskie Vedomosti – Morphological newsletter. 2025;33(3):974. (3).974
Article received 06 May 2025 Article accepted 05 Oktober 2025
Введение. Значительным препятствием для получения достоверных результатов о структурной организации энтеральной нервной системы на светооптическом уровне является отсутствие адекватных методов исследования. Первые исследования энтеральной нервной системы были выполнены с использованием муравьиной [1] и уксусной [2] кислот. Однако, методы идентификации нейроцитов с их отростками – это метод Гольджи и его различные модификации. В частности, метод Фокса с хромовокислым цинком [3]. Метод Гольджи – это знаменитая методика – «черная реакция» - открытый Гольджи в 1873 году, главный метод изучения тотальных препаратов головного мозга [4]. Почти все работы знаменитого лауреата Нобелевского премии Сантьяго Рамона-и-Кахаля выполнены с использованием ранних вариантов этого метода. В настоящее время метод Гольджи используется в патологической гистологии крайне редко, поскольку в его основе лежит импрегнация не срезов, а целых блоков [4]. Другой классический нейрогистологический метод – метод суправитального окрашивания периферических нервных окончаний метиленовым синим Эрлиха. Краситель вводится или инъекционно в рыхлую соединительную ткань, или в серозные полости, или в кровеносное русло, после предварительной его перфузии физиологическим раствором. Концентрация раствора для внутрисосудистого введения – 0,2% при температуре 37°С. Наиболее контрастные препараты получены Догелем [5] при фиксации препаратов пикриново-кислым аммиаком или молибденово-кислым аммиаком. К сожалению, даже примененное Догелем новое технические решение – неиспользование фиксатора, насыщенного раствора пикринового кислого аммония, не предохраняет препараты от обесцвечивания. И тем не менее, именно Догель впервые представил неопровержимые доказательства существования межнейрональных цитоплазматических синцитиальных связей – он «реально стал родоначальником прямого анатомического факта ретикуляризма» (цит. по [6], c 14). И в то же время, представления о структуре синапсов значительно расширились в связи с внедрением в нейрогистологию импрег-национного метода Бильшовского-Грос, классическая пропись которого известна каждому нейрогистологу, и, по мнению Колосова (1978), он оригинален и незаменим [7]. Чтобы получить желаемые результаты, используя метод Бильшовского-Грос, приходится применять различные вариации классической прописи. Это связано с тем, что метод «капризный и требуется ловкость рук», как пишет Fayrter (1951) [8]. Более того, «техника при изучении нервной системы имеет первостепенное значение» (цит. по [9]), а для «убедительности приводимых в морфологических исследованиях материалов очень важны иллюстрации» (цит. по [10], с. 239). Однако, для большинства нейрогистоло-гических работ, эти два условия оказались невыполнимыми. В итоге, они иллюстрированы или схемами и рисунками, выполненными с помощью рисовальных аппаратов, или некачественными микрофотографиями.
Для идентификации межнейронных цитоплазматических связей нельзя использовать ни рутинные гистологические методы окраски по Шпильмайеру, Нисслю, толуидиновым синим, крезиловым фиолетовым, ни новые цитохимические красители, вторичные антитела и другие маркеры нейроцитов. Причина одна – все они не выявляют нейрофиб-риллярный аппарат и отростки нейроци-тов – морфологический субстрат проведения нервных импульсов.
Цель исследования – доказать эффективность универсального метода импрегнации в идентификации межнейрональных цитоплазматических синцитиальных связей в энтеральной нервной системе человека.
Материалы и методы исследования. Изучены суправитальные препараты стенки кишечника беспородных половозрелых кошек (n=7) и биопсийные фрагменты тонкой и толстой кишки (n=30) длиной 20 см (тонкая кишка) и длиной 10 см (толстая кишка). Материал получен и использован в соответствии с полным соблюдением российских и международных этических нормативных документов, ре- гламентирующих исследования на животных.
Фрагменты кишечника после тщательной предварительной подготовки (освобождения от слизистых наслоений, промывания водопроводной водой) подвергались гидро-препарированию под стереомикроскопом. Стенка фрагментов разделялась на слизистую и мышечную оболочки, и подслизистую основу. Каждая из оболочек, мышечная, слизистая и подслизистая основа фиксировались в 10% не содержащем метанол формалине в отдельных флаконах.
Для одновременного выявления нервных и сосудистых элементов энтеральной нервной системы человека был модифицирован универсальный метод импрегнации аргирофильных структур [11]. Фиксация расслоенных оболочек стенки кишки, слизистой и мышечной оболочек и подслизистой основы, проводится без смены раствора в течение 1,5 месяцев. Увеличение сродства серебра к сосудистой стенке кровеносных и лимфатических микрососудов, к нейроцитам и их отросткам, и к сателлитной глии осуществляется предварительным осаждением на них гидрооксида магния, кальция и бария. В первоначальной прописи метода это достигается перфузией через брюшную аорту и воротную вену их слабых растворов. Небольшие фрагменты кишечной стенки обрабатывают 0,2% растворами гидроксидов бария, кальция и магния, размещением их на смоченной этими растворами стекловате. Затем на поверхность фрагментов наносят капли растворов. Ар-гирофилия (способность к осаждению серебра) проявляется при осаждении гидроксида серебра из нитрата серебра в сильнощелочной среде (pH=11–13) с использованием 4% гидрохинона в качестве восстановителя. При этом следует особо отметить, что структуры, обработанные гидроксидами Mg2+, Ca2+, Ba2+, сохраняют высокую восстановительную способность. Это связано с тем, что они, в процессе фиксации в формалине, подвергаются меньшему воздействию муравьиной кислоты, чем окружающие их ткани. Фрагменты оболочек стенки кишечника сушатся на фильтре и помещаются в 1–10% рас- творы нитрата серебра. Концентрация первого раствора нитрата серебра и его экспозиция на препарате определяется опытным путем в каждом конкретном случае. На ранних сроках импрегнации более высокое средство к серебру проявляется у стенки кровеносных и лимфатических микрососудов, а на поздних сроках – у структурных элементов нервной ткани. После стандартных манипуляций, проведения через батарею спиртов и просветления в ксилоле препараты толщиной до 40–80 мкм и площадью до 15 см² (3,0х5,0 см) заключались в канадский бальзам.
При необходимости возможна коррекция дефектов фиксации объектов путем внесения изменений в процессе импрегнации. Первоочередная 5–7-ми минутная обработка в 0,6% растворе сульфата серебра необходима для компенсации малой растворимости сульфатов кальция и бария. Только после этого допустим переход к обработке в концентрированном растворе нитрата серебра. Идея метода состоит в том, что осаждение гидроокиси серебра из раствора его сернокислой соли происходит значительно специфичнее и полнее на нервных структурах.
Результаты и обсуждение. Разработанная модификация универсального метода импрегнации при точном выполнении всех рекомендаций позволяет получить просветленные в канадском бальзаме препараты большой площади до 6,0х8,0 см. В них идентифицируются все аргирофильные структуры: нейроциты, глиоциты, межнейрональные синцитиальные связи, лимфатические и кровеносные микрососуды (рис. 1, 2). Была выявлена еще одна особенность импрегнирован-ных препаратов – отсутствие свободных нервных окончаний (рис. 3, 4). Это показатель полного выявления нервных структур, обнаруженный еще Догелем: «исследования показали, что по мере использования метиленового синего и завершения окраски нервных ветвей, количество выявляемых нервных окончаний неуклонно снижается» (цит. по [12]).
Это связано с тем, что в результате обменной реакции между гидроокисями Ca2+ и Ba2+ и сернокислым серебром образуются три новых слаборастворимых сое-
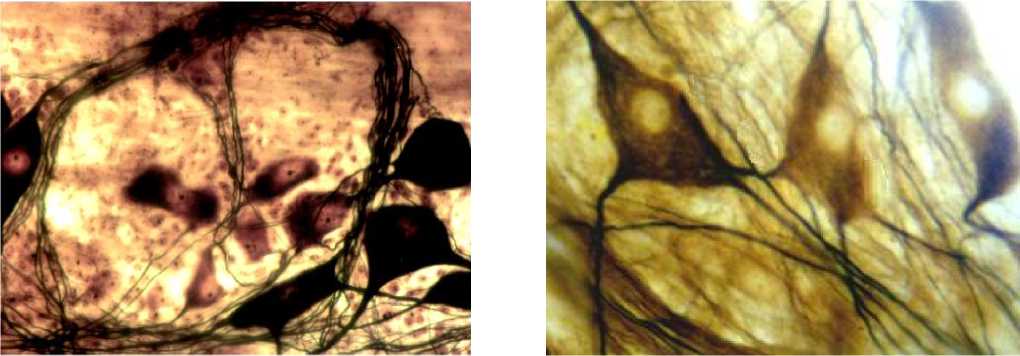
Рис. 1. Микрофото гистологического препарата толстой кишки кошки, импрегни-рованного серебром в авторской модификации. Ув.: х600
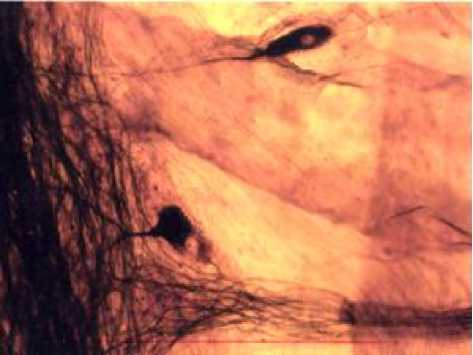
Рис. 3. Микрофото гистологического препарата тонкой кишки кошки, импрегни-рованного серебром в авторской модификации. Ув.: х200
единения – гидроокись серебра и сернокислые соли кальция и магния. Mg, Ca и Ba находятся в самом начале ряда активности металлов и легко вытесняют серебро из его различных соединений. Катионы Ca2+ и Ba2+ активно захватывают сернокислый анион серебра, образуя нерастворимые сульфаты. Освобожденные катионы серебра тотчас же взаимодействуют с гидроксильными группами. Образование и осаждение гидроокиси серебра происходит как за счет активности самого катиона, так и за счет еще более реакционноспособного аниона. В результате образуются плохо растворимые соединения, которые не уходят в раствор, а остаются на арги-
Рис. 2. Микрофото гистологического препарата толстой кишки кошки, импрегни-рованного серебром в авторской модификации. Ув.: х600
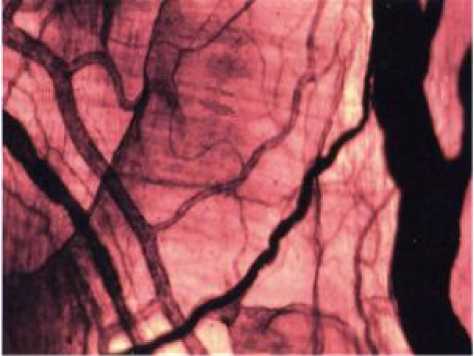
Рис. 4. Микрофото гистологического препарата тонкой кишки, импрегнированно-го серебром в авторской модификации. Ув.: х200
рофильных структурах. Именно поэтому восстановленное из гидроокиси металлическое серебро в виде кристаллов– зародышей откладывается в точном соответствии с локализацией и концентрацией протравных соединений. Адаптированный метод универсальной импрегнации – результат нанотехнологического принципа искусственного перенаправленного метода коррекции естественных восстановительных свойств клеточных конструкций. Он достигается путем нанесения на стенки микрососудов и нервных структур резко реакционноспособного покрытия из молекулярного слоя гидроокисей Mg2+, Ca2+ и Ba2+.
Классические нейрогистологиче-ские методы Гольджи, Бильшовского-Грос и Рамон-и-Кахаля требуют тщательного освобождения исследуемого материала от фиксатора путем длительного его отмывания в воде. Это связано с тем, что указанные методы требуют длительной фиксации (не менее 4 месяцев) в 10% формалине и длительной импрегнации в 0,75% AgNO 3 (до 48 часов) [4]. В противном случае необходимо применять химически малоактивные фиксаторы, такие как этанол. И в том, и в другом случаях при импрегнации используются восстановительные свойства не фиксаторов, а только самой нервной ткани. Но ткань – это чрезвычайно слабый восстановитель, поэтому реакция восстановления на нервных структурах протекает довольно медленно и для ее активации необходимы длительные экспозиции в растворе нитрата серебра при повышенной температуре. Качественное отличие метода импрегнации по Бильшовскому-Грос от других «серебря-


