Модификация поверхности ортодонтических имплантатов нанокомпозитными покрытиями на основе хитозана и металлов
Автор: Суетенков Д.Е., Горин Д.А., Портнов С.А., Карагайчев А.Л., Терентюк Г.С., Захаревич A.M., Хлебцов Б.Н., Фирсова И.В.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Стоматология
Статья в выпуске: 3 т.9, 2013 года.
Бесплатный доступ
Цель: изучение свойств металлполимерных наноструктурированных покрытий ортодонтических имплантатов. Материал и методы. Для создания нанокомпозитных покрытий использовались хитозан низкой и средней молекулярной массы, З-аминопропил-3-метоксисилан и суспензии наносфер золота, диаметром 5 нм и 10 нм, стабилизированных цитратом натрия. Для создания подслоя перед нанесением полиионных покрытий использовался 2 мг/мл водный раствор полиэтиленимина. Была изучена динамика нанесения полионных покрытий методом пьезокварцевого микровзвешивания. Нанесение покрытий производилось с помощью установки «ПОЛИИОН-1М». Морфология создаваемых покрытий изучалась методом атомно-силовой микроскопии, элементный состав покрытий — методом вторичной ионной масс-спектрометрии. Результаты. Наилучший перенос среди структур хитозан/металлы показали структуры с хитозаном малой молекулярной массы и на-ночастицами металлов диаметром 8-10 нм. Анализ значений среднеквадратической шероховатости поверхности позволяет утверждать, что наночастицы золота образуют наиболее плотное покрытие на подслое З-аминопропил-3-метоксисилана. Заключение. Биосовместимые нанокомпозитные покрытия в области челюст-но-лицевой хирургии могут считаться патогенетически обоснованным и эффективным методом снижения риска постоперационных воспалительных осложнений путем достижения местного средне-длительного антибактериального эффекта.
Имплантаты, нанокомпозитные покрытия, наносферы металлов, хитозан
Короткий адрес: https://sciup.org/14917770
IDR: 14917770
Текст научной статьи Модификация поверхности ортодонтических имплантатов нанокомпозитными покрытиями на основе хитозана и металлов
Адрес: 410064, г. Саратов, ул. Антонова, д. 17А, кв. 44
Тел.: 89272219984
значительных количествах, могут приводить и к ряду негативных эффектов [5]. Таким образом, целесообразно применение как хитозансодержащих средств, так и наночастиц благородных металлов для обеспечения противовоспалительного и антибактериального эффектов в полости рта. В современной научной литературе [6] также показаны перспективы применения биосовместимых пленок Ленгмюра — Блоджетт в медицинских целях.
Одним из способов создания нанокомпозитных материалов является метод полиионной сборки, имеющий 3 модификации: адсорбция из растворов полиэлектролитов [7], полив и центрифугирование [8], спрей-метод [9]. Этот метод позволяет создавать наноразмерные полимерные покрытия, состоящие из слоев (органических) полиэлектролитов противоположного знака. Использование коллоидов неорганических наночастиц, стабилизированных органическими соединениями, позволяет создавать нанокомпозитные покрытия методом полиионной сборки.
С другой стороны, благородные металлы имеют длительную историю применения в медицинских целях. Ранее была показана возможность использования серебряных покрытий для терапии кариеса и в некоторых приложениях зубного протезирования. В частности, в работе Л. Д Гожай [4] показана возможность использования серебряных покрытий для исключения токсического и аллергического действия мономеров акрила зубных протезов на слизистую оболочку полости рта. Такое покрытие поверхности получают методом восстановления серебра из его соединений. Наблюдения показали, что при таком подходе происходит снижение дискомфорта от применения ортопедических конструкций и эпителиза-ция поражений слизистых оболочек.
Механизм действия соединений золота основан на их способности угнетать макрофаги, тормозя тем самым развитие патологических иммунных реакций. Это обосновывает изучение противовоспалительного эффекта золота, потенциально наиболее биоинертного металла. Кроме того, некоторые препараты золота обнаружили антибактериальное действие, в частности против Helicobacter pylori, а также антигрибковую активность [10]. Эксперименты P. Mukherjee клиники Рочестера (Миннесота, США) показали [11], что наночастицы золота блокировали функцию VEGF, имели антиопухолевое действие, не оказывая токсического действия на клетки.
В последнее время появляются возможности не только получить дополнительные лечебные свойства при применении золота и серебра, но и снизить количество нежелательных эффектов за счет использования новых технологий. Нанесение антибактериальных нанокомпозитных покрытий на дентальные имплантаты или другие конструкции, например временные устройства ортодонтической опоры, применяющиеся при хирургических пособиях, позволит контролировать течение раневого процесса и уменьшит риск воспалительных постоперационных осложнений.
Цель: оптимизация поверхности имплантатов путем применения полиионных структур, содержащих хитозан и наночастицы металлов.
Материал и методы. В качестве полиэлектролитов для создания нанокомпозитных покрытий использовались хитозан низкой и средней молекулярной массы и 3-аминопропил-3-метоксисилан (АПМОС). Суспензии наносфер золота, имевших диаметр 5 нм и 10 нм, стабилизированных цитратом натрия, были синтезированы по методике Френса [12]. Для всех экспериментов использовалась вода, очищенная с помощью установки «Водолей» и имевшая удельное сопротивление более 5 МОм·см.
Для создания подслоя перед нанесением полии-онных покрытий использовался 2 мг/мл водный раствор полиэтиленимина (PEI, 50% водный раствор, Mw=600–1000 кДа, Aldrich).
На часть образцов вместо покрытия PEI создавалось покрытие с помощью АПМОС. Такая обработка поверхности была использована с целью оценить, насколько хуже сорбируются биосовместимые компоненты, чем бионесовместимые.
Использовались ортодонтические имплантаты (ОИ) производства Конмет (РФ) (рис. 1). Поверхность ОИ перед нанесением структур обрабатывалась травлением гелем, содержащим 37% ортофосфор-ной кислоты в течение 1 минуты. Нанесение нано-композитных покрытий производилось с помощью установки «ПОЛИИОН-1М» [13].
Динамика процесса осаждения полиэлектролитов и наночастиц предварительно изучалась микрогра-виметрическим методом, для чего покрытия наносили на поверхность пластин кварцевых резонаторов промышленного производства (собственная частота колебаний 8.0 МГц). Частота колебаний резонатора измерялась после нанесения каждого слоя. По изменению частоты с нанесением слоев делались выводы о динамике осаждения растворов.

Рис. 1. Ортодонтический имплантат производства «Конмет» (РФ)
Морфология создаваемых покрытий изучалась методом атомно-силовой микроскопии с использованием зондовой нанолаборатории «Интегра Спектра» (NT-MDT, Россия). Атомно-силовые исследования покрытий проводились при комнатной температуре (20-25ºС) в полуконтактном режиме с использованием кантилеверов NSG 01 (NT-MDT, резонансная частота 15–190 кГц, жесткость 2.5–10 Н/м). В связи с высокой рельефностью поверхности имплантатов максимальный размер сканируемой области был ограничен до 10×10 мкм, частота сканирования составляла 1 Гц. СЭМ-исследование модифицированной поверхности ОИ проводили в лаборатории INCA (Oxford Instruments).
Элементный состав покрытий изучался методом вторичной ионной масс-спектрометрии, для чего использовалась установка на базе масс-спектрометра МИ-1305 (CCCР) [15]. Бомбардировка образцов велась положительными ионами кислорода с энергией 4 КэВ, регистрировались положительные вторичные ионы.
Результаты. Сначала методом пьезокварцевого микровзвешивания была изучена динамика нанесения полионных покрытий на основе пар «хитозан — коллоидное золото» и серебро, стабилизированное поливинилпирролидоном медицинским с хитозаном различной молекулярной массы и наночастицами различных средних диаметров (3–5 и 8–10 нм). Покрытия имели структуру PEI/Au/ {Хитозан/Au} 5. Наилучший перенос среди структур хитозан/металлы показали структуры с хитозаном малой молекулярной массы и наночастицами металлов диаметром 8–10 нм (табл. 1).
Таблица 1
Данные QCM-измерений поверхности ОИ
|
№ |
Структура |
[ΔF], Гц |
|
1 |
Хитозан н.м.м./Au-5 |
77 |
|
2 |
Хитозан н.м.м./Au-10 |
552 |
|
3 |
Хитозан с.м.м./Au-5 |
65 |
|
4 |
Хитозан с.м.м./Au-10 |
462 |
|
5 |
АПМОС/Au-5 |
576 |
Для изучения морфологии нанокомпозитных покрытий на поверхности ОИ были приготовлены 4 группы образцов с 2 типами предварительной обработки
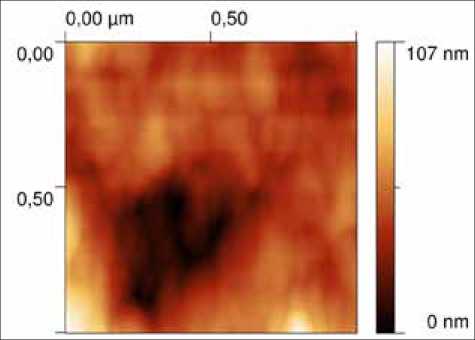
Рис. 2. АСМ-изображение нанесенного покрытия

Рис. 3. Морфология поверхности ОИ


D1 = 25.^5nm k

1 * .*C1
. r = 71.51 nm
D2 = 22 M nm

w 15,00 w wo н им! L— ша злззи" о* esc •«” Uto «15» o«.«vay. 1«Л«Л«
! , । । I MRVA TEW
PMtolWK» W П4ПМЙМ»
Рис. 4. СЭМ покрытия ОИ и размеры золотых частиц при увеличении в 62,15 кх

Рис. 5. Поверхность ОИ с определением химического состава при увеличении в 2,5 кх
поверхности и 2 вариантами структуры покрытий. Кроме того, еще 2 образца выполняли роль контрольных для проведения ВИМС-измерений, на них никакие покрытия не создавались, поверхность одного из двух образцов была подвергнута травлению. Затем для каждого образца были получены изображения размером 1×1 мкм, по которым вычислялась среднеквадратическая шероховатость поверхности (рис. 2, 3).
Поверхность ОИ с лучшими характеристиками переноса структур изучали с помощью СЭМ (рис. 4, 5),
Химический состав модифицированной поверхности ОИ
Таблица 2
|
Спектр |
C |
O |
P |
S |
Ti |
Au |
Итог |
|
1 |
5,08 |
3,5 |
0,29 |
0,49 |
90,64 |
100 |
|
|
2 |
5,97 |
5,01 |
0,18 |
88,84 |
100 |
||
|
3 |
8,38 |
3,55 |
0,27 |
0,56 |
87,23 |
99,99 |
|
|
4 |
4,99 |
6,89 |
0,61 |
0,57 |
83,58 |
3,35 |
99,99 |
|
6 |
2,45 |
7,72 |
0,29 |
89,53 |
99,99 |
||
|
7 |
6,03 |
9,01 |
82,57 |
2,39 |
100 |
||
|
8 |
3,21 |
13,77 |
83,01 |
99,99 |
|||
|
Макс. |
8,38 |
13,77 |
0,61 |
0,57 |
90,64 |
3,35 |
100 |
|
Мин. |
1,72 |
3,5 |
0,27 |
0,18 |
82,53 |
2,35 |
|
|
Сред. зн. |
5,56125 |
7,9025 |
0,414 |
0,474 |
87,005 |
3,03 |
99,995 |
что показало наличие частиц металлов на всей поверхности с их скоплениями в области зон с большей шероховатостью.
Обсуждение. Анализ значений шероховатости позволяет утверждать, что наночастицы золота образуют наиболее плотное покрытие на подслое 3-аминопропил-3-метоксисилана. Структура покрытий с подслоем адгезива мало отличалась от структуры покрытий, полученных при использовании в качестве подслоя хитозана низкой молекулярной массы. Присутствие золота в полученных образцах было подтверждено методом вторично-ионной масс-спектрометрии.
Метод Ленгмюра — Блоджетт позволяет создавать биосовместимые нанокомпозитные покрытия, годные к применению в медицине, в частности в стоматологии. Одной из задач в направлении применения покрытий Ленгмюра — Блоджетт в медицине является, на наш взгляд, упрощение и убыстрение процесса создания таких покрытий, когда это связано с непосредственным взаимодействием с пациентом. В таких случаях оправданным становится использование спрей-метода. При распылении полиэлектролита адсорбция каждого слоя ограничена плотностью полимера. Однако можно снизить влияние этого фактора на качество получаемых полиэлектро-литных слоев за счет увеличения концентрации полимера и времени адсорбции полимеров.
Заключение. Таким образом, получение полии-онных структур, содержащих хитозан и наночастицы золота и серебра, динамика осаждения их слоев для различных молекулярных масс хитозана определяют возможность среднедлительного влияния на окружающие имплантат ткани с противовоспалительным и антибактериальным эффектом. Необходимо продолжить изучение свойств стоматологических имплантатов с модифицированной поверхностью в экспериментальных и клинических условиях.
Список литературы Модификация поверхности ортодонтических имплантатов нанокомпозитными покрытиями на основе хитозана и металлов
- Angelatos A.S. Katagiri К., Caruso F. Bioinspired colloidal systems via layer-by-layer assembly//Soft Matter. 2006. Vol. 2. P. 18-23
- Yi H. Wu L.-Q., Bentley W. E. Biofabrication with Chitosan//Biomacromolecules. 2005. Vol. 6, № 6. P. 2881-2894
- Тумшевиц O.H., Белоусова Ю.Б., Тумшевиц В. О. Исследование влияния хитозансодержащих композиций на ткани пародонта крыс с моделью сахарного диабета//Стоматология детского возраста и профилактика. 2007. № 4. С. 39-41
- Гожая Л.Д. Аллергические заболевания в ортопедической стоматологии. М.: Медицина, 1988. 156 с.
- Копейкин В. В. Лекарственные серебросодержащие препараты и их медико-биологические свойства//Серебро в медицине, биологии и технике. Препринт № 2. Новосибирск, 1993. С. 36-40
- Tang Z., Wang Y, Podsiadlo P., Kotov N.A. Biomedical Applications of Layer-by-Layer Assembly: From Biomimetics to Tissue Engineering//Article first published online: 16 NOV -2006. DOI: 10.1002/adma. 200600113. Adv. Mater. 2006. Vol. 18. P. 3203-3224
- Ruths J., Essler F, Decher C, Riegler H. Polyelectrolytes I: Polyanion/Polycatio Multilayers at the Air/Monolayer/Water Interface as Elements for Quantitative Polymer Adsorption Studies and Preparation of Hetero-superlattices on Solid Surfaces//Langmuir. 2000. Vol. 16. P. 8871-8878
- Lee Seung-Sub, Lee Ki-Bong, Hong Jong-Dai. Evidence for spin coating electrostatic self-assembly of polyelectrolytes//Langmuir. 2003. Vol. 19. P. 7592-7596
- Joseph В., Schlenoff S. T, Dubas T. F. Sprayed polyelectrolyte multilayers//Langmuir. 2000. Vol. 16. P. 9968-9969
- Inhibition of HIV Fusion with Multivalent Gold Nanoparticles/M.-C. Bowman, Т.Е. Ballard, C.J. Eckerson, D.L. Feldheim [et al.]//J.Am. Chem. Soc. 2008. № 130 (22). P. 6896-6897
- Antiangiogenic Properties of Gold Nanoparticles/P. Mukherjee, R. Bhattacharya, P. Wang [et al.]//Clin. Cancer. Res. 1.2005. №11. P. 3530
- Золотые наночастицы: синтез свойства, биомедицинское применение/Л. А. Дыкман, В. А. Богатырев, С. Ю. Щего-лев, Н.Г. Хлебцов. М.: Наука, 2008. 320 с.
- Автоматизированная установка для получения нано-размерных покрытий методом полиионной сборки/С. А. Пор-тнов, A.M. Ященок, А.С. Губский [и др.]//Приборы и техника эксперимента. 2006. № 5. С. 1-6.


