Модификация радиочувствительности овец
Бесплатный доступ
Установлено, что при остром воздействии g-излучения в сублетальной (2 Гр) и летальной (6 Гр) дозах через девять месяцев после пролонгированного облучения овец в дозах 0,5 и 0,1 Гр соответственно отсутствует выраженная активация процесса свободнорадикального перекисного окисления липидов (ПОЛ). В плазме крови животных наблюдали снижение интенсивности спонтанной хемилюминесценции (СХЛ), тенденцию к повышению концентрации малонового диальдегида (МДА) и слабое изменение содержания диеновых и триеновых конъюгатов (ДК и ТК), а также уровня концентрации a-токоферола и ретинола. Однократное острое воздействие g-излучения в дозах 2 и 6 Гр увеличивало интенсивность процесса свободнорадикального ПОЛ в плазме крови овец. При развитии лучевой патологии регистрировали повышение интенсивности СХЛ и концентрации МДА, ДК, ТК и a-токоферола при одновременном снижении уровня содержания ретинола. Сравнительный анализ полученных данных по интенсивности процесса свободнорадикального ПОЛ в плазме крови и выживаемости овец показал, что пролонгированное облучение в дозах 0,1 и 0,5 Гр модифицирует реакцию организма на последующее острое воздействие g-излучения в сублетальной и летальной дозах.
Овцы, свободнорадикальное пол, пролонгированное облучение, g-излучение, радиоиндуцированное поражение, малые дозы облучения, радиочувствительность
Короткий адрес: https://sciup.org/170170156
IDR: 170170156
Sheep radiosensitivity modification
Acute exposure of sheep to g-radiation at sublethal (2 Gy) and lethal (6 Gy) doses following nine-month prolonged irradiation of the animals with doses of 0,5 and 0,1 Gy, respectively, was found to result in no pronounced activation of free radical lipid peroxidation. Analysis of animals blood plasma showed decrease in the spontaneous chemiluminescence intensity, tendency towards an increase in the level of malonic dialdehyde and weak change in concentration of diene and triene conjugates (DC and TC), as well as a-tocopherol and retinol. On the contrary, a single acute exposure of the sheep to g-radiation at 2 and 6 Gy caused increase in the rate of free radical lipid peroxidation in plasma. When animals developed a radiation-induced abnormalities, increased levels of spontaneous chemiluminescence intensity, concentration of malonic dialdehyde, DC, TC and α-tocopherol were registered with simultaneous reduction in the retinol level. A comparative analysis of obtained data on the rate of free radical lipid peroxidation in the blood plasma and survival of sheep showed that prolonged exposure at doses of 0,1 and 0,5 Gy modifies response of animals to subsequent acute g-radiation exposure at sublethal and lethal doses.
Текст научной статьи Модификация радиочувствительности овец
В механизмах биологического действия ионизирующих излучений важная роль принадлежит свободнорадикальному перекисному окислению липидов (ПОЛ). Значительный интерес к процессу свободнорадикального ПОЛ обусловлен тем, что он протекает во всех типах клеточных мембран и участвует в регуляции метаболизма клеток. При этом свободные радикалы, наряду с вторичными мессенджерами (ионы Са2+, циклические аденозинмонофосфат и гуанозинмонофосфат (цАМФ и цГМФ), фосфоинозитолы) выполняют функцию регуляторных молекул в биохимических реакциях.
Ранее нами было показано [9], что пролонгированное облучение овец в дозах 0,1 и 0,5 Гр ингибирует интенсивность процесса свободнорадикального ПОЛ в течение всего периода исследования (90 сут) и характеризуется снижением в плазме крови содержания малонового диальдегида, диеновых и триеновых конъюгатов и α-токоферола при одновременном повышении уровня ретинола. В свою очередь, модификация интенсивности процесса свободнорадикального ПОЛ приводит к изменению активности аденилатциклазы и проницаемости плазматической мембраны для ионов Са2+ в клетках периферической крови.
Модификация интенсивности процесса свободнорадикального ПОЛ при воздействии γ-излучения в дозах 0,1 и 0,5 Гр может быть одним из факторов повышения радиорезистентности организма животных к последующему облучению в больших дозах. Поэтому целью исследования стала оценка интенсивности процесса свободнорадикального ПОЛ в плазме крови овец, подвергнутых острому воздействию γ-излучения в сублетальной (2 Гр) и летальной (6 Гр) дозах однократно и повторно после пролонгированного облучения в дозах 0,1 и 0,5 Гр.
Мирзоев Э.Б.* – вед. науч. сотр., д.б.н.; Кобялко В.О. – ст. науч. сотр., к.б.н. ГНУ ВНИИСХРАЭ.
Материалы и методы
Эксперименты были проведены на 23 овцах породы «Прекос» (живая масса 30-37 кг; возраст 1-1,5 года). Животных содержали в условиях вивария ГНУ ВНИИСХРАЭ Россельхозакаде-мии. Рационы овец были сбалансированы по основным питательным веществам согласно нормам ГНУ ВИЖ Россельхозакадемии [10].
Первая серия экспериментов выполнена на 11 овцах. Две группы подопытных животных (по 4 головы в каждой) через девять месяцев после пролонгированного воздействия Y-излучения в дозах 0,5 и 0,1 Гр, были повторно облучены в сублетальной (2 Гр) и летальной (6 Гр) дозах соответственно. Контрольную группу составили интактные животные (3 головы).
Вторая серия опытов проведена на 12 овцах. Две группы подопытных животных (по 4 головы в каждой) были облучены однократно в сублетальной (2 Гр) и летальной (6 Гр) дозах. Контролем служили интактные животные (4 головы).
Облучение овец проводили на установке ГУЖ-24 с источником излучения 137Cs (энергия Y-квантов 0,67 МэВ). Мощность дозы Y-излучения составляла 1,5 Гр/час. Интенсивность и равномерность облучения контролировали с помощью клинического дозиметра типа 27012 и сферической ионизационной камеры АК-253. Неравномерность облучения не превышала 15%.
Кровь отбирали из яремной вены овец в пробирки с цитратом натрия (конечная концентрация 0,38%) на 1-е, 2-е, 3-и, 5-е, 7-е, 10-е, 15-е, 20-е, 25-е и 30-е сутки. Плазму крови получали общепринятым способом. В плазме крови животных исследовали динамику показателей свободнорадикального ПОЛ: интенсивность спонтанной хемилюминесценции (СХЛ), содержание малонового диальдегида (МДА), диеновых и триеновых конъюгатов (ДК и ТК), а также концентрации а-токоферола и ретинола. Кроме того, учитывали общее состояние животных, реакцию на внешние раздражители, аппетит, функциональное состояние желудочно-кишечного тракта.
Регистрацию СХЛ осуществляли на собранной из стандартных блоков установке, работающей в квантовометрическом режиме и предназначенной для регистрации сверхслабых световых потоков [5]. Содержание продуктов свободнорадикального ПОЛ МДА, ДК и ТК определяли методом спектрометрии [4, 6]. Оптическую плотность образцов измеряли при длине волны Х=532; Х=233; Х=275 нм соответственно. Концентрации а-токоферола и ретинола - микроколо-ночной высокоэффективной жидкостной хроматографии [15].
Результаты обрабатывали методом вариационной статистики с использованием t-критерия Стьюдента. Различия значений считали достоверными при р<0,05 [7].
Результаты
Лучевое поражение животных сопровождается усилением неферментативных окислительных процессов, возникновением свободных радикалов, гидропероксидов как в липидах, так и водных фазах организма. При активации процесса свободнорадикального ПОЛ возрастает интенсивность хемилюминесценции крови и клеток тканей, которая характеризует окисление белковых, углеводных и липидных компонентов. Кроме того, цепной механизм инициирования этого процесса выявляет многообразие продуктов (МДА, ДК и ТК), количественное определение которых служит оценкой его интенсивности.
Через девять месяцев у овец, подвергнутых пролонгированному воздействию γ-излучения в дозах 0,1 и 0,5 Гр, регистрировали активацию процесса свободнорадикального ПОЛ. Так, интенсивность СХЛ в плазме крови облучённых животных составляла 23,4±6,2 и 25,1±4,8 имп./10 с соответственно, а у интактных – 17,2±0,5 имп./10 с.
Облучение овец в дозе 2 Гр на фоне пролонгированного воздействия γ-излучения в дозе 0,5 Гр ингибировало интенсивность СХЛ в плазме крови (рис. 1). Максимальное уменьшение уровня показателя наблюдали на 5-15-е сутки исследования (34-50% от исходных данных). В то же время однократное острое воздействие в дозе 2 Гр увеличивало интенсивность СХЛ. Величина показателя возрастала на 2-е, 3-и, 20-е и 25-е сутки исследования и составила 162%, 149%, 142% и 161% соответственно (р<0,05).
% от контроля
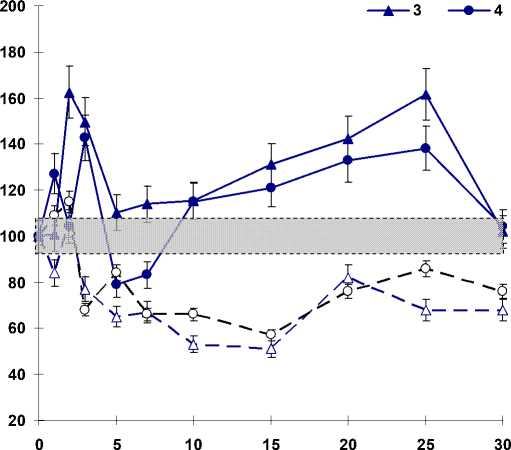
Сроки исследований, сутки
Рис. 1. Интенсивность СХЛ в плазме крови овец, подвергнутых острому воздействию γ-излучения в сублетальной и летальной дозах однократно и повторно после пролонгированного облучения в дозах 0,5 и 0,1 Гр.
1 – 0,5+2 Гр; 2 – 0,1+6 Гр; 3 – 2 Гр; 4 – 6 Гр; I1 – контроль.
В плазме крови овец, подвергнутых γ-воздействию в летальной дозе (6 Гр) на фоне пролонгированного облучения в дозе 0,1 Гр, наблюдали нелинейный характер изменений интенсивности СХЛ. Так, к исходу вторых суток значение показателя возрастало на 14%, в период с 3 по 15-е сутки регистрировали снижение её уровня в 1,2 и 1,7 раза. В последующие сроки (20-30-е сутки) отмечали некоторое повышение интенсивности СХЛ, хотя значения её были ниже исходных данных. В то же время однократное острое воздействие в летальной дозе (6 Гр) усиливало интенсивность СХЛ в плазме крови на 1-е и 3 сутки после облучения. Максимальное повышение регистрировали на 3 сутки, что составило 142% от исходных данных (p<0,05). В дальнейшем на 5-е и 7-е сутки наблюдали уменьшение уровня показателя с последующим увеличением на 15-25-е сутки (121-138% от исходных данных, p<0,05).
Следовательно, однократное облучение овец в сублетальной (2 Гр) и летальной (6 Гр) дозах приводит к повышению интенсивности СХЛ в плазме крови. Уровень интенсивности её был сравнительно одинаков, однако при облучении овец в дозе 6 Гр отмечали сдвиг максимума значений к начальным срокам исследования. Кроме того, регистрировали снижение величины показателя относительно исходных данных. Напротив, при повторном облучении овец в дозах 2 и 6 Гр после пролонгированного воздействия в дозах 0,5 и 0,1 Гр наблюдали ингибирование интенсивности СХЛ.
Оценка количества промежуточных и конечных продуктов процесса свободнорадикального ПОЛ выявила следующие особенности. Содержание МДА в плазме крови повторно облучённых овец в дозе 2 Гр имело тенденцию к увеличению (рис. 2). В то же время однократное острое воздействие в дозе 2 Гр повышало уровень МДА в плазме крови овец. Максимальные значения отмечали на 7-е и 15-е сутки.
% от
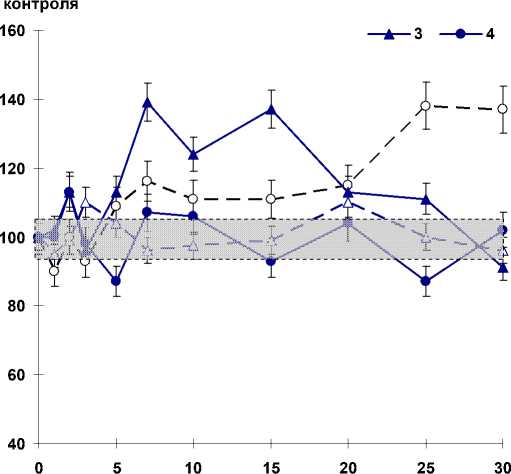
Сроки исследований, сутки
Рис. 2. Концентрация МДА в плазме крови овец, подвергнутых острому воздействию γ-излучения в сублетальной и летальной дозах однократно и повторно после пролонгированного облучения в дозах 0,5 и 0,1 Гр.
1 – 0,5+2 Гр; 2 – 0,1+6 Гр; 3 – 2 Гр; 4 – 6 Гр; – контроль.
Облучение овец в летальной дозе на фоне пролонгированного воздействия в дозе 0,1 Гр снижало концентрацию МДА в плазме крови в начальные сроки исследования с последующим повышением на 5-30-е сутки. Напротив, однократное острое воздействие в летальной дозе увеличивало значение показателя к исходу вторых сутки. На 3-и, 5-е сутки и последующие сроки исследования регистрировали фазовый характер изменений. Следует отметить, что минимальные значения этого показателя были ниже исходных данных на 13,7%.
Содержание ДК в плазме крови повторно облучённых животных имело тенденцию к снижению (рис. 3). При однократном остром облучении овец в дозе 2 Гр отмечали нелинейный характер изменений. Так, на 1-е сутки исследования регистрировали тенденцию к увеличению значений показателя, а на 2-е и 3 сутки – снижение. Облучение овец в летальной дозе на фоне пролонгированного воздействия в дозе 0,1 Гр выявило достоверное снижение значений показателя на 30-е сутки. В то же время однократное воздействие в летальной дозе (6 Гр) повышало уровень ДК в период с 1 по 15-е сутки развития лучевой патологии.
% от контроля 1 2
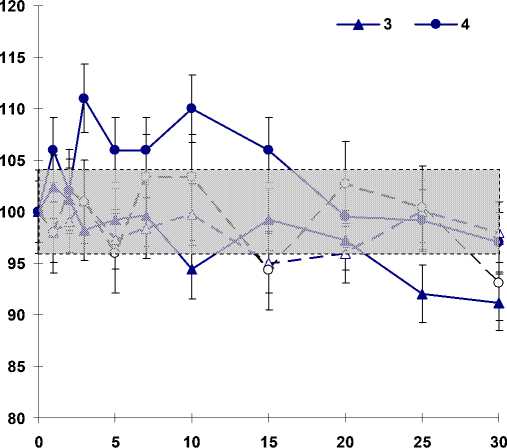
Сроки исследований, сутки
Рис. 3. Содержание ДК в плазме крови овец, подвергнутых острому воздействию γ-излучения в сублетальной и летальной дозах однократно и повторно после пролонгированного облучения в дозах 0,5 и 0,1 Гр.
1 – 0,5+2 Гр; 2 – 0,1+6 Гр; 3 – 2 Гр; 4 – 6 Гр; I-___J – контроль.
Определение концентрации ТК в плазме крови овец, подвергнутых повторному острому воздействию γ-излучения в дозе 2 Гр, выявило тенденцию к повышению значений показателя (рис. 4). В то же время концентрация ТК в плазме крови однократно облучённых овец возрастала. На 1-е сутки после воздействия в дозе 2 Гр содержание ТК составило 157% (p<0,05). В дальнейшем на 2-е и 3-и сутки регистрировали некоторое уменьшение уровня показателя, хотя его значения были выше исходных на 20% и 27% соответственно. Максимальное увеличение составило 191% на 20-е сутки исследования (p<0,05).
Облучение овец в летальной дозе на фоне пролонгированного воздействия в дозе 0,1 Гр обнаружило тенденцию к снижению уровня ТК. Следует отметить, что динамика значений показателя при повторном облучении носила нелинейный характер. В то же время однократное острое воздействие в летальной дозе (6 Гр) повышало содержание ТК в плазме крови овец. Так, на 1-е сутки после воздействия значение этого показателя составило 256% от исходных данных (p<0,05). В течение всего периода исследования изменения концентрации ТК в плазме крови носили нелинейный характер при максимуме значений на 10-е сутки (488%, p<0,05).
% от контроля
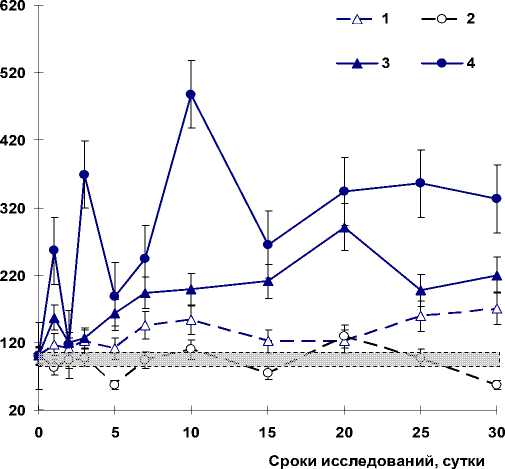
Рис. 4. Содержание ТК в плазме крови овец, подвергнутых острому воздействию γ-излучения в сублетальной и летальной дозах однократно и повторно после пролонгированного облучения в дозах 0,5 и 0,1 Гр.
1 – 0,5+2 Гр; 2 – 0,1+6 Гр; 3 – 2 Гр; 4 – 6 Гр; I____1– контроль.
Процесс свободнорадикального ПОЛ регулируется биоантиоксидантами, к числу которых относят α-токоферол и ретинол. Определение концентрации жирорастворимых витаминов в плазме крови овец, подвергнутых острому воздействию γ-излучения в сублетальной и летальной дозах однократно и повторно после пролонгированного облучения в дозах 0,1 и 0,5 Гр, обнаружило следующие особенности. Так, у овец, облучённых в дозе 2 Гр, на фоне пролонгированного воздействия в дозе 0,5 Гр в течение всего периода исследования не наблюдали существенных изменений концентрации α-токоферола (рис. 5). В то же время однократное облучение овец в дозе 2 Гр повышало уровень α-токоферола в плазме крови. Достоверные различия значений отмечали на 1-е (257%), 5-10-е (245-210%) и 30-е (186%) сутки.
Облучение овец в летальной дозе на фоне пролонгированного воздействия в дозе 0,1 Гр приводило к уменьшению концентрации α-токоферола в плазме крови. Напротив, однократное острое облучение увеличивало уровень α-токоферола в плазме крови. Максимальные значения показателя регистрировали на 2-е (274%, р<0,05), 5-10-е (253-194%, р<0,05) и 30-е (170%, р<0,05) сутки исследования.
% от контроля
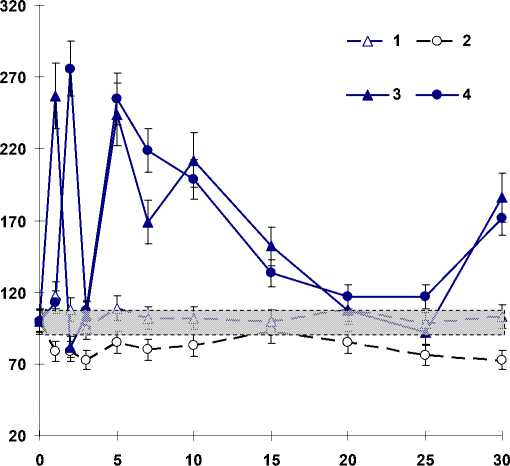
Сроки исследований, сутки
Рис. 5. Содержание α-токоферола в плазме крови овец, подвергнутых острому воздействию γ-излучения в сублетальной и летальной дозах однократно и повторно после пролонгированного облучения в дозах 0,5 и 0,1 Гр.
1 – 0,5+2 Гр; 2 – 0,1+6 Гр; 3 – 2 Гр; 4 – 6 Гр; – контроль.
Содержание ретинола в плазме крови овец, подвергнутых острому воздействию γ-излучения в дозе 2 Гр на фоне пролонгированного облучения в дозе 0,5 Гр, было ниже исходных данных в течение первых 10 суток (рис. 6). В последующие сроки уровень этого показателя возрастал до исходных значений. Однократное острое воздействие γ-излучения в сублетальной дозе (2 Гр) также снижало концентрацию ретинола. Так, на 1-е сутки уменьшение составило 68% (р<0,05), а на 5-7-е сутки – 64-40% (р<0,05). В дальнейшем значения показателя возрастали, хотя и были ниже исходных данных.
Облучение овец в летальной дозе (6 Гр) на фоне пролонгированного воздействия в дозе 0,1 Гр приводило к снижению концентрации ретинола в течение всего срока исследования. В то же время однократное острое воздействие γ-излучения в дозе 6 Гр обнаружило нелинейный характер изменений значений показателя. Содержание ретинола на 2-е сутки было ниже исходных данных на 83,7% (р<0,05), а на 5-7-е сутки – на 59,6-85,1% (р<0,05).
Оценка клинических показателей выявила наиболее короткий латентный период и выраженные симптомы лучевой болезни у овец, однократно облучённых в летальной дозе (6 Гр). Через 3 часа после воздействия наступала вялость, а на 7-е сутки отмечали диарею. К концу исследования фиксировали депрессию и эпиляцию. На 25-е сутки пали две овцы, а на 30-е сутки – остальные. В то же время у животных, облучённых повторно в сублетальной и летальной дозах, после пролонгированного воздействия в малых дозах, отмечали сглаженный характер проявления клинических симптомов. Причём, при повторном облучении в летальной дозе гибели овец не наблюдали.
% от контроля
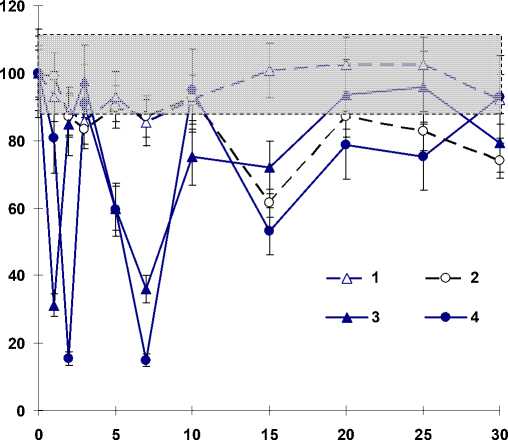
Сроки исследований, сутки
Рис. 6. Содержание ретинола в плазме крови овец, подвергнутых острому воздействию γ-излучения в сублетальной и летальной дозах однократно и повторно после пролонгированного облучения в дозах 0,5 и 0,1 Гр.
1 – 0,5+2 Гр; 2 – 0,1+6 Гр; 3 – 2 Гр; 4 – 6 Гр; C-’-J – контроль.
Таким образом, при повторном остром воздействии γ-излучения в сублетальной (2 Гр) и летальной (6 Гр) дозах через девять месяцев после пролонгированного облучения овец в дозах 0,5 и 0,1 Гр отсутствовала выраженная активация процесса свободнорадикального ПОЛ. В то же время однократное облучение овец в дозах 2 и 6 Гр инициировало процесс свободнорадикального ПОЛ в плазме крови. Следствием активации процесса свободнорадикального ПОЛ явилось изменение концентрации α-токоферола и ретинола. В целом изменения интенсивности процесса свободнорадикального ПОЛ после однократного воздействия γ-излучения в сублетальной и летальной дозах регистрировали до проявления клинических симптомов лучевой болезни, что позволяет рассматривать их в качестве патогенетического фактора.
Обсуждение результатов
Сравнительный анализ показателей процесса свободнорадикального ПОЛ при однократном и повторном облучении овец в сублетальной и летальной дозах выявил различия. Так, при однократном воздействии отмечали увеличение, а при повторном – уменьшение интенсивности СХЛ. Изменения концентрации продуктов свободнорадикального ПОЛ (МДА, ДК и ТК) в плазме крови повторно облучённых животных носили менее выраженный характер.
Модификация ответной реакции организма при однократном и повторном облучении животных в сублетальной и летальной дозах, вероятно, зависит от исходного уровня показателя. Согласно закону исходного уровня (правило Вильдера): если исходный уровень показателя соответствует нижней границе нормы, то ответная реакция состоит в его повышении до средних величин; если он находится близко к верхней границе нормы – реакция заключается в его снижении; если входит в диапазон средних величин – реакция отсутствует [8].
После пролонгированного облучения овец в дозах 0,1 и 0,5 Гр отмечали ингибирование процесса свободнорадикального ПОЛ, которое, возможно, обусловлено модификацией системы антиоксидантной защиты [1, 13], поэтому можно предположить, что предварительное облучение животных изменяет исходный уровень показателя и «границы нормы реакции».
В целом полученные данные демонстрируют, что пролонгированное воздействие ионизирующим излучением в дозах 0,1 и 0,5 Гр модифицирует ответную реакцию организма овец при повторном облучении в сублетальной и летальной дозах и повышает радиорезистентность организма.
Аналогичные результаты получены на лабораторных животных. Установлено, что предварительное облучение мышей в дозе 0,1 Гр за 5 час до воздействия в повреждающей дозе 2 Гр снижает интенсивность процесса свободнорадикального ПОЛ при одновременном уменьшении количества однонитевых разрывов в ДНК тимоцитов и числа клеток в тимусе [14]. Предполагается, что защитный эффект предварительного воздействия связан не только с активацией ферментов репарации ДНК, но и антиоксидантных систем организма, которые ингибируют процесс свободнорадикального ПОЛ, стабилизируют структуры клеточных мембран и уменьшают вероятность окислительной деструкции молекулы ДНК.
Повышение радиорезистентности организма млекопитающих зависит от большего числа факторов, к числу которых можно отнести величину дозы хронического (пролонгированного) и острого облучения, мощности дозы и время после первого воздействия [16, 17, 19]. Полученные результаты указывают на возможность проявления радиорезистентности и через девять месяцев после предварительного пролонгированного облучения в дозах 0,1 и 0,5 Гр. Необходимо отметить, что повышение радиорезистентности овец при повторном облучении в сублетальной и летальной дозах не является классическим примером проявления индукции адаптивного ответа (АО). Однако механизмы их реализации могут быть схожи.
В настоящее время предложены гипотезы, объясняющие развитие АО в клетках млекопитающих [2, 11, 12]. В качестве пускового события рассматриваются свободнорадикальное перекисное окисление плазматической мембраны клеток и активация рецепторов фактора роста [2].
Передача информации от вторичных посредников, в частности от ионов Са2+ и цАМФ, различным белкам внутри клеток происходит путём их фосфорилирования и осуществляется протеинкиназой С. Предполагается, что при действии ионизирующих излучений в малых дозах активность протеинкиназы С за счёт увеличения пассивной проницаемости мембраны для ионов Са2+ и, соответственно, роста его внутриклеточной концентрации поддерживается аномально продолжительное время, что повышает скорость фосфорилирования клеточных белков.
Возможно, протеинкиназа С выполняет ключевую роль и в индукции АО, так как ингибиторы фермента подавляют его развитие [3]. В свою очередь, протеинкиназа С активирует эндонуклеазу [20], которая повышает резистентность клеток к последующему воздействию ионизирующих излучений в больших дозах [18]. Кроме того, протеинкиназа С участвует в экспрессии генов металлотионеинов, так как ингибиторы фермента блокируют индукцию синтеза мРНК металло-тионеинов, а активаторы, напротив, увеличивают. Дополнительным доказательством является то, что антагонисты ионов Са2+ также подавляют развитие АО, индуцированного рентгеновским излучением или H 2 O 2 . Следовательно, полученные нами данные дополняют и подтверждают роль процесса свободнорадикального ПОЛ в повышении радиорезистентности млекопитающих.
Выводы
Показано, что пролонгированное воздействие ионизирующим излучением в дозах 0,1 и 0,5 Гр модифицирует ответную реакцию организма овец при повторном облучении в сублетальной и летальной дозах и повышает радиорезистентность организма. Полученные данные дополняют и подтверждают роль процесса свободнорадикального ПОЛ в модификации радиочувствительности овец и указывают на возможность проявления радиорезистентности через девять месяцев после предварительного пролонгированного облучения в малых дозах.
Список литературы Модификация радиочувствительности овец
- Барабой В.А., Олейник С.А., Блюм И.А., Хмелевский Ю.В. Прооксидантно-антиоксидантный гомеостаз у морских свинок после фракционированного рентгеновского облучения в малых дозах и коррекция его нарушений антиоксидантным комплексом//Радиационная биология. Радиоэкология. 1993. Т. 34, вып. 2. С. 240-246.
- Боднарчук И.А. Гипотеза о механизме индукции адаптивного ответа при облучении клеток млекопитающих в малых дозах//Радиационная биология. Радиоэкология. 2002. Т. 42, № 1. С. 36-43.
- Гильяно Н.Я., Бондарев Г.Н., Бикинеева Е.Г., Красотская Г.И., Носкин Л.А. Влияние ингибиторов протеинкиназы С и NО-синтазы на радиационно-индуцированный цитогенетический адаптивный ответ в клетках китайского хомячка в культуре//Радиационная биология. Радиоэкология. 2001. Т. 41, № 6. С. 659-663.
- Гончаренко М.С., Латинова А.М. Метод оценки перекисного окисления липидов//Лабораторное дело. 1985. № 1. С. 60-61.
- Журавлев А.И., Асанов М.И. Чувствительность и рабочие характеристики современных хемилюминометров//Биофизика. 1991. Т. 36, вып. 3. С. 489-497.
- Журавлев А.И., Мяльдзин А.Р., Баранов А.В. Методы регистрации свободнорадикального окисления липидов в сыворотке, плазме и мембранах клеток крови: Метод. указ. М.: МВА, 1989. С. 12.
- Лакин Г.Ф. Биометрия: учебное пособие для биол. спец. вузов: 4-изд., перераб. и доп. М.: Высшая школа, 1990. 352 с.
- Лейтес С.М. Правила исходного состояния и его значение в физиологии и патологии//Проблемы регуляции обмена веществ в норме и патологии. М.: Медицина, 1977. С. 5-23.
- Мирзоев Э.Б., Кобялко В.О. Интенсивность свободнорадикального перекисного окисления липидов, активность аденилатциклазы и проницаемость плазматической мембраны для ионов Са2+ в клетках периферической крови овец, облучённых в малых дозах//Радиационная биология. Радиоэкология. 2009. Т. 49, № 3. С. 261-267.
- Нормы и рационы кормления сельскохозяйственных животных. Справочное пособие: 3-е издание, переработанное и дополненное/под ред. А.П. Калашникова, В.И. Фисинина, В.В. Щеглова, Н.И. Клейменова. М.: Россельхозакадемия, 2003. 456 с.
- Пелевина И.И., Алещенко А.В., Антощина М.М., Кудряшова О.В., Семенова Л.П., Серебряный А.М. Реакция популяции клеток на облучение в малых дозах//Радиационная биология. Радиоэкология. 2003. Т. 43, № 2. С. 161-166.
- Пелевина И.И., Алещенко А.В., Антощина М.М., Рябченко Н.И., Семенова Л.П., Серебряный А.М. Индивидуальная вариабельность в проявлении адаптивного ответа клеток человека на воздействие ионизирующей радиации и подходы к её определению//Радиационная биология. Радиоэкология. 2007. Т. 47, № 6. С. 658-666.
- Рева А.Д., Живалюк О.Б., Лукьяненко А.И., Егорова Е.Г., Дворецкий А.И. Содержание глутатиона и активность глутатион-S-трансферазы в органах и крови крыс после хронического облучения в малых дозах//Радиационная биология. Радиоэкология. 1994. Т. 34, вып. 6. С. 769-773.
- Рябченко Н.И., Иванник Б.П., Хорохорина В.А., Дзиковская Л.А., Синькова Р.В., Рябченко В.И., Грошева И.П., Дегтярева Е.В. Влияние предварительного адаптирующего облучения на содержание продуктов перекисного окисления липидов в сыворотке крови и повреждение ДНК в тимусе облучённых мышей//Радиационная биология. Радиоэкология. 2000. Т. 40, № 6. С. 659-661.
- Скурихин В.Н., Двинская Л.М. Определение альфа-токоферола и ретинола в плазме крови с/х животных методом микроколоночной высокоэффективной жидкостной хроматографии//Сельскохозяйственная биология. 1989. № 4. С. 127-129.
- Черникова С.Б., Готлиб В.Я., Пелевина И.И. Влияние малых доз ионизирующей радиации на чувствительность к последующему облучению//Радиационная биология. Радиоэкология. 1993. Т. 33, вып. 1(4). С. 537-541.
- Feinendegen L.E. The role of adaptive responses following exposure to ionizing radiation//Hum. Exp. Toxicol. 1999. V. 18, N 7. P. 561-585.
- Ramana C.V., Boldogh I., Izumi T., Mitra S. Activation of apurinic/apyrimidinic endonuclease in human cells by reactive oxygen species and its correlation with their adaptive response to genotoxicity of free radicals//Proc. Natl. Acad. Sci. USA. 1998. V. 95. P. 5061-5066.
- Wolff S. The adaptive response in radiobiology: evolving insights and implications//Environ. Health. Perspect. 1998. V. 106, suppl. 1. P. 277-283.
- Yacoub A., Kelley M.R., Deutsch P.W. The DNA repair activity of human redox/repair protein APE/Ref-1 is inactivated by phosphorylation//Cancer Research. 1997. V. 57. P. 5457-5459.


