Модуляция опухолетоксического действия свободных радикалов оксидом азота
Автор: Загребельная Г.В., Кондакова И.В.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Экспериментальные исследования
Статья в выпуске: 3-4 (3-4), 2002 года.
Бесплатный доступ
Короткий адрес: https://sciup.org/14053919
IDR: 14053919
Текст статьи Модуляция опухолетоксического действия свободных радикалов оксидом азота
Свободнорадикальные реакции занимают важное место в механизме противоопухолевой активности антрациклиновых антибиотиков [1] и лучевой терапии [14, 15]. В результате свободнорадикальных реакций образуются активированные кислородные метаболиты, которые в высоких концентрациях могут вызывать повреждения нуклеиновых кислот, белков, углеводов, инициацию перекисного окисления липидов, инактивацию ферментов [3]. Итак, образование свободных радикалов ведет к нарушению различных клеточных функций, следствием чего являются ингибирование пролиферации и индукция апоптоза [4, 6, 9].
Развитие резистентности опухолевых клеток к свободнорадикальному повреждению связано с увеличением антирадикальных процессов в них [13], активации адаптивных реакций клеток на повреждение и отбор наиболее автономных, злокачественных клонов [2], что представляет одну из актуальных проблем в современной онкотерапии. В последние годы большое внимание уделяется оксиду азота (NO) как возможному модулятору опухолетоксических воздействий [3]. Однако литературные данные о механизме сочетанного воздействия свободных радикалов и оксида азота противоречивы. NO способен как потенцировать свободнорадикальные реакции, так и ингибировать их [3], проявляя, таким образом, антиоксидантные свойства [10, 11]. Такая неоднозначность, полученная при оценке взаимодействия NO со свободными радикалами, не позволяет правильно интерпретировать его эффект на клеточном уровне и затрудняет рекомендации его в плане перспективного использования для терапии опухолей.
Целью работы было исследование способности NO-генерирующих соединений модулировать опухолетоксическое действие свободнорадикальных агентов.
Методика исследования
Эксперименты проводились на половозрелых мышах линии DBA/2 массой 15–20 г разводки питомника Научно-исследовательской лаборатории экспериментального биомоделирования ТНЦ СО РАМН. В работе использовали штаммы асцитной мастоцитомы Р-815, перевиваемой внутрибрюшинно. Асцитную жидкость с опухолевыми клетками брали на седьмые сутки после трансплантации опухоли и трижды отмывали средой RPMI-1640. Жизнеспособность клеток определяли с использованием трипанового синего. Свободнорадикальное воздействие вызывали гидропероксидом третичного бутила (ГПТБ) («Merck») и 2,2’азо-бис(2-амидинопропаном) (АБАП), который при термическом разложении (t = 37oC) образует пероксирадикалы [11]. Источниками NO были нитропруссид натрия (SNP) и нитрит натрия (NaNO2) («Sigma»), который в ходе циклических реакций превращается в оксид азота [3]. Для эндогенной генерации NO в опухолевых клетках применяли L-аргинин (отечественного производства марки х.ч.). Активность NO-синтазы ингибировали с помощью метилового эфира нитроаргинина («Sigma»).
Пролиферативную активность опухолевых клеток определяли по включению меченного радионуклидами предшественника синтеза нуклеиновых кислот [3H]-тимидина («Изотоп») в ДНК. Опухолевые клетки доводили средой RPMI-1640 до конечной концентрации 1млн/мл. Клетки культивировали в присутствии различных концентраций NO-генерирующих соединений и свободнорадикальных агентов в 96-луночных круглодонных планшетах в объёме 200 мкл среды культивирования. Во все лунки добавляли [3H]-тимидин по 0,1 мкCi на лунку. Планшеты инкубировали 18 ч в атмосфере 5% СО2 при 37оС. После инкубации клетки переносили с помощью 12-канального сборщика клеток “Flow” на стекловолоконные фильтры, промывая ячейки планшеты физиологическим раствором, этиловым спиртом (96%) и трихлоруксусной кислотой (30%). В высушенных фильтрах измеряли радиоактивность на жидкостном сцинтилляционном счётчике Mark-III (Tracor Analytic) в сцинтилля- торе Lumax (Lumac Systems inc.). Изменение скорости синтеза ДНК выражали в процентах по отношению к контролю.
Полученные данные обрабатывали статистически с использованием непараметрического критерия Вилкоксона – Манна–Уитни.
Результаты
Соединения, используемые нами для индукции свободнорадикального окисления, существенно отличаются друг от друга по структуре, однако они оба могут служить источниками пероксирадикалов. Показано, что распад трет бутилгидропероксида (ГПТБ) происходит при его взаимодействии с внутриклеточными ионами переменной валентности, главным образом железа и меди, с образованием пероксидных радикалов [1]. Термолизис АБАП также приводит к их накоплению [11].
Высокие концентрации АБАП и ГПТБ более чем 10 и 0,5 мМ соответственно угнетали скорость синтеза ДНК опухолевых клеток. Уменьшение концентрации ГПТБ и АБАП до 0,1 и 5 мM соответственно приводило к снижению их антипролиферативного эффекта с последующей стимуляцией пролиферации опухолевых клеток, достигающей максимальных значений при концентрации ГПТБ 1нМ и АБАП 0,5 мM (рис. 1).
Цитотоксический эффект доноров оксида азота был выражен слабее по сравнению с противоопухолевым действием пероксирадикалов (рис. 2). SNP снижал пролиферативную активность опухолевых клеток в концентрациях 10-3 –10-5 М, более низкие концентрации не влияли на скорость синтеза ДНК. NaNO2 оказывал цитотоксическое действие в концентрациях 10-3 М. Стиму- ляция пролиферации опухолевых клеток наблюдалась при концентрации NaNO2 10-6–10-8 М. Слабое стимулирующее действие на пролиферацию оказывал эндогенный источник оксида азота L-аргинин (субстрат NO-синтазной реакции). Причем ингибирование NO-синтазной реакции метиловым эфиром нитроаргинина практически не изменяло скорости синтеза ДНК по сравнению с контрольной популяцией опухолевых клеток. Вероятно, это обусловлено наличием в клетках мастоцитомы Р-815 индуцибельной NO-синтазы, которая не проявляет своей активности до стимуляции.
Комбинация нетоксических доз продуцентов NO и низкотоксичных доз пероксидных радикалов приводила к увеличению включения [3H]-тимидина в ДНК по сравнению с контрольной популяцией опухолевых клеток, инкубированных только с источниками пероксидных радикалов, либо не влияла на неё (табл. 1).
Из всех изученных нами NO-генерирующих соединений L-аргинин проявлял наибольшую активность в плане подавления противоопухолевого действия пероксидных радикалов. В связи с этим можно предположить, что данный эффект обусловлен способностью пероксирадикалов опосредованно, через изменение внутриклеточного ионного гомеостаза, стимулировать активность индуцибельной NO-синтазы, что приводит к наработке оксида азота.
Использование цитотоксических доз ГПТБ и АБАП и доноров оксида азота в низкотоксичных концентрациях вызывало к снижение опухолеток-сичности пероксирадикалов (табл.2). Ранее установлено, что оксид азота может защищать опухолевые клетки от ГПТБ-индуцированной
Таблица 1
Сочетанное действие NO-генерирующих соединений и субтоксических доз пероксидных радикалов на включение [3H]-тимидина в клетки мастоцитомы Р-815
|
Соединение |
Контроль |
SNP (1нМ) |
NaNO 2 (1 нМ) |
L-аргинин (5 мМ) |
|
Контроль |
100 |
124,2± 20 |
143,8± 18 |
112,6± 18,7 |
|
АБАП (10 мМ) |
54,9± 5,9 |
68,3± 8,2 |
135,6± ± 16,9* |
168± 14,8** |
|
АБАП (1 мМ) |
107± 12,8 |
125,6± 16,6* |
142,6± 21,8* |
180± 21,1** |
|
ГПТБ (100 нМ) |
67,8± 17,5 |
100,3± 12* |
111,5± 10,2* |
199,6± 54,2* |
|
ГПТБ (1мкМ) |
3,7± 1,6 |
97,2± 3,8** |
107± 18,3** |
249± 33** |
Примечание. * – p<0,05; **- p<0,01 – показатели достоверности различий по сравнению с действием свободнорадикальных агентов в соответствующих концентрациях. Результаты выражены в процентах по отношению к контролю.
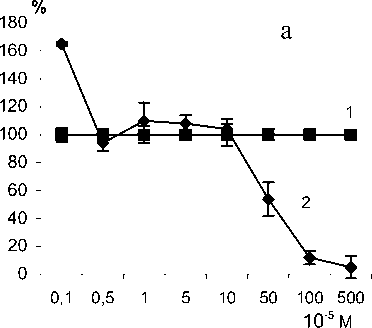
Рис. 1. Влияние источников пероксидных радикалов на включение [3Н]-тимидина в ДНК клеток мастоцитомы Р815 (2) (M±m) по сравнению с контролем: а – гидропероксид третичного бутила (1); б – 2,2’азо-бис(2-амидинопропан) (3).
Результаты выражены в процентах по отношению к контролю
mM
180 %
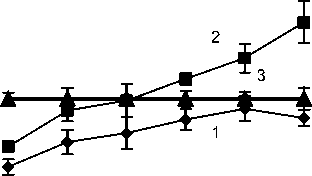
0 -3 -4 -5 -6 -7-8
10 10 10 10 1010
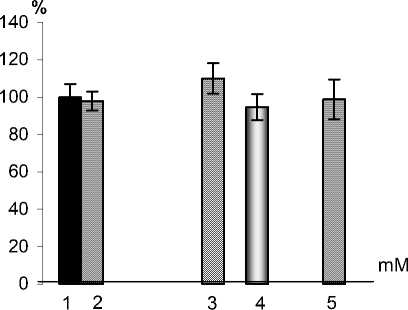
Рис. 2. Влияние NO-генерирующих соединений (а) (1 – нитропруссид натрия, 2 – нитрит натрия) (M±m) на включение [3Н]-тимидина в ДНК клеток мастоцитомы Р815 по сравнению с контролем (3) и различных концентраций L-аргинина (б) (2 – 1 мМ; 3 – 5 мМ; 5 - 10 мМ) и метилового эфира нитроаргинина (4 – 5 мМ) (M±m) на включение [3Н]-тимидина в ДНК опухолевых клеток по сравнению с контролем (1). Результаты выражены в процентах по отношению к контр
Таблица 2
Влияние NO-генерирующих соединений на токсический эффект пероксидных радикалов в клетках мастоцитомы Р-815
|
Соединение |
Контроль |
АБАП (20мМ) |
ГПТБ (10 мкМ) |
|
Контроль |
100 |
16± 3,1 |
14,9± 2,7 |
|
SNP, 10-3 М |
54,4± 11,5 |
14± 3,5 |
13± 3,3 |
|
SNP, 10-4 М |
71± 12,2 |
117± 7,8** |
29± 4,6* |
|
SNP, 10-5 М |
100,5± 10,6 |
102± 9** |
36,4± 5,7* |
|
NaNO 2 , 10-3 М |
52± 7,8 |
64,3± 11* |
8,2± 2,1** |
|
NaNO 2, 10-4 М |
94± 8,9 |
93± 8* |
13± 3,7 |
|
NaNO 2, 10-5 М |
180± 17,8 |
121± 14,7** |
29± 4,7* |
|
L-аргинин, 5 мМ |
113± 16,7 |
150± 17** |
37,6± 7,3* |
Примечание. * – p<0,05; ** – p<0,01 – показатели достоверности различий по сравнению с действием свободно-радикальных агентов в соответствующих концентрациях. Результаты выражены в процентах по отношению к контролю.
цитотоксичности двумя путями: уменьшать содержание каталитических железосодержащих центров и химически модифицировать свободные радикалы [18].
Слабое потенцирование антипролифератив-ного эффекта ГПТБ проявлял NaNO 2 в концентрации 10-3 М. Таким образом, инкубация опухолевых клеток с NO-генерирующими соединениями в нетоксичных концентрациях не приводила к значительному изменению пролиферативной активности, но при использовании их в сочетании с пероксирадикалами наблюдалась стимуляция синтеза ДНК.
Таким образом, оксид азота вызывает стимуляцию пролиферативной активности клеток мышиной мастоцитомы Р-815. На основании полученных результатов можно предположить, что оксид азота – один из факторов, способствующих появлению резистентных клонов опухолевых клеток.


