Модуляция жизнеспособности клеток, иммобилизованных в пористо-проницаемом инкубаторе из никелида титана, под действием инфракрасного и ультрафиолетового излучений
Автор: Гюнтер Сергей Викторович, Кокорев О.В., Ходоренко В.Н., Дамбаев Г.Ц.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Экспериментальные статьи
Статья в выпуске: 4-2 т.19, 2015 года.
Бесплатный доступ
Клеточный ответ на электромагнитное излучение зависит от многих факторов, в том числе клеточного микроокружения. Клетки по-разному реагируют пн исследуемые типы излучения малой интенсивности. Воздействие инфракрасного и ультрафиолетового излучений малой интенсивности приводит к достоверному изменению количества жизнеспособных клеток. Жизнеспособность клеток опухоли Эрлиха, селезенки и костного мозга мышей С57ВЛ/6 в пористо-проницаемом инкубаторе из никелида титана изменяется при облучении инфракрасным и ультрифиолетовым спектрами электромагнитного излучения. Инфракрасное излучение вызывает увеличение жизнеспособности клеток опухоли Эрлиха, костного мозга и селезенки в 4,6, 2,5 и 1,3 раза, ультрафиолетовое излучение - в 3,9, 1,5 и 1,2 раза соответственно по сравнению с контрольной, в которой инкубировали клетки только при естественном освещении.
Скаффолд, экстрацеллюлярный матрикс, инкубатор-носитель клеток, пористый никелид титана, инфракрасное и ультрафиолетовое излучения
Короткий адрес: https://sciup.org/142140718
IDR: 142140718
Viability modulation of cells immobilized in porous tini-based alloy scaffold under infrared and ultraviolet radiation
Cellular response to electromagnetic radiation depends on many factors including the microenvironment of cell. Different cells (spleen, bone marrow, and Ehrlich''s adenocarcinoma), respond to the studied types of low-intensity radiation. Exposure to infrared (IR) and ultraviolet (UV) radiation of low intensity leads to significant change in the number of viable cells. Effects of low-intensity infrared (IR) and ultraviolet (UV) radiation on the number of viable cells were evaluated against the control group in which cells were exposed to natural daylight. The results showed that IR irradiation led to a 4.6-, 2.5-, and 1.3-fold increase in viable Ehrlich tumor, bone marrow, and spleen cells, respectively, while UV exposure led to a 3.9-, 1.5-, and 1.2-fold increase, respectively. The data show that the extracellular environment of bone marrow, tumor and spleen cell populations affects their viability and proliferative potency in porous TiNi-based scaffolds. IR- and UV irradiation of cell cultures immobilized in the scaffold affects the cell viability in populations of bone marrow, tumor, and spleen cells. In case of IR irradiation, cell viability was significantly improved, at the same time UV irradiation suppressed cell proliferation activity. The effect of IR irradiation can be used to resuscitate the cell area. The effect of UV irradiation can be used to destroy residual tumor lesions or other pathological cell populations.
Текст научной статьи Модуляция жизнеспособности клеток, иммобилизованных в пористо-проницаемом инкубаторе из никелида титана, под действием инфракрасного и ультрафиолетового излучений
Введение в практику экспериментальной биологии и медицины методов длительного культивирования клеток, в том числе клеток-предшественников специализированных тканей, создало предпосылки для разработки новых технологий заместительной клеточной и тканевой терапии и конструирования биоискусственных органов [1, 2].
Ответственный этап использования культивированных клеток – трансплантация в зону повреждения. Успех предшествующей работы и эффект лечения зависят от того, какая часть клеток попадет в зону дефекта, адгезируют ли культивированные клетки к тканям, сохранят ли они активное функциональное состояние. С точки зрения создания технологии пересадки выращенных in vitro клеток немаловажно обеспечение оптимальных условий реципиентного ложа. Проблемой остается длительное сохранение функциональной активности имплантированных клеток in vivo. Простое введение суспензии клеток-предшественников оказалось малоэффективным, поэтому возникла необходимость поиска адекватного носителя для трансплантации клеток в организм реципиента [3–7].
Используемый клеточной и тканевой инженерией междисциплинарный подход направлен в первую очередь на создание композиционных материалов для восстановления утраченных функций отдельных тканей или органов в целом. Основные принципы этого подхода заключаются в разработке и применении при имплантации в поврежденный орган или ткань носителей из различных биоматериалов, которые используются в сочетании с донорскими клетками и/или биоактивными веществами [8–9].
Материалы, применяемые в тканевой инженерии, должны обладать широким спектром специфических свойств. До тех пор пока новая ткань организма-хозяина в месте имплантации полностью не восстановится,
материал, применяемый для изготовления конструкции, должен поддерживать рост клеток и их организацию в ткань, а имплантат – беспрепятственно отводить продукты обмена клеток [8].
Матриксы (скаффолды) должны обладать многофункциональностью: эластичностью и механической прочностью; биосовместимостью на белковом и клеточном уровне; способностью создавать условия для прикрепления клеток и стимулировать пролиферацию и дифференциацию клеток; возможностью стерилизации без изменения медико-технических свойств. Для реализации потенциала культивированные клетки, организованные в сложные трехмерные структуры, должны определенное время находиться в зафиксированном к носителю состоянии [8–10].
В последние годы активно используют пористо-проницаемые инкубаторы из никелида титана в конструировании биосовместимых матриксов применительно к задачам тканевой инженерии и трансплантологии. Многообещающей является перспектива использования биоматриксов для регенерации поврежденных опухолями и другими этиологиями тканей желез и печени, изготовления биоимплантатов кровеносных сосудов и воздухоносных путей, закрытия дефектов мягких и костных тканей [11– 14].
Методы выделения необходимого количества жизнеспособных клеток не всегда обеспечивают нужный результат, при этом качество взятой у больного ткани различно и зависит от многих причин: степени заболевания пациента, возраста, количества пунктата и т. д. Одна из актуальных проблем клеточной трансплантологии – достижение необходимого количества жизнеспособных клеток для трансплантации. Исследователи эту проблему решают различными путями: совершенствованием методов выделения клеток, увеличением количества взятого биоматериала, применением различных биостимуляторов роста и пролиферации с использованием как химических, так и физических факторов [15–17].
Сложным и важным физическим фактором, воздействующим на клеточные процессы, является электромагнитное излучение. Биологическое поле клеток постоянно изменяется под действием различных видов электромагнитного излучения, существующих как между клетками и тканями, так и с пространством биосферы. Незначительные вариации параметров облучения могут вызывать изменение реакции клеток, вплоть до их гибели, поэтому какая-либо некорректность постановки опыта и задания начальных условий иссле- дования может привести к недостоверным результатам [18, 19].
Электромагнитные волны модифицируют состояние билипидной клеточной мембраны, усиливая или уменьшая проникновение воды в цитоплазму клетки, при этом изменяя поляризацию мембраны и тем самым сигнальную систему клетки. Эти эффекты заметны при увеличении интенсивности излучения – улучшение циркуляции крови в капиллярах и т. д. [20, 21].
При воздействии на ткани инфракрасного (ИК) излучения происходит его поглощение молекулами воды, кислородом, ферментами, мембранами клеток и другими структурами. Выделяющееся при излучении тепло увеличивает колебательную энергию молекул, изменяя процессы в термодинамической системе. Под действием ИК-излучения усиливается биологическая активность клеток, ускоряется кровоток, повышается деятельность желез, снимается мышечный спазм, снижается болевой синдром и т. д. [22, 23].
Под влиянием ультрафиолетового (УФ) излучения изменяются свойства биополимеров – белков и нуклеиновых кислот. Молекулы биополимеров содержат кольцевые группы молекул, которые интенсивно резонируют, то есть поглощают излучение с короткой длиной волны (около 280 нм). Эта поглощенная энергия может передаваться по цепи атомов в пределах молекулы без существенной потери, пока не достигнет слабых связей между атомами и не разрушит их. В течение такого процесса, называемого фотолизом, образуются части молекул, радикалы и ионы, воздействующие на клеточные структуры. Примером служит денатурация белков под действием ультрафиолетового излучения. УФ-излучение, взаимодействуя с веществом, в том числе органическим, часто вызывает его ионизацию, так называемый фотоэлектрический эффект, нарушающий биохимические реакции в клетках. [24]. Таким образом, реакция клеток на электромагнитное воздействие индивидуальна и зависит от множества факторов, включая клеточное микроокружение.
Цель работы – исследование воздействия электромагнитных волн УФ (370 нм) и ИК (860 нм) диапазонов малой интенсивности на клетки различных биологических тканей (селезенки, костного мозга и аденокарциномы Эрлиха), иммобилизованные в пористо-проницаемом инкубаторе из никелида титана (патент на изобретение № 2438699 «Способ изготовления вакцины для лечения аденокарциномы Эрлиха в эксперименте» от 10.01.2012) [25]. В работе поставлены задачи: определить степень воздействия излучения малой интенсивности на клеточную суспензию и

Рис. 1. Пористо-проницаемые инкубаторы из никелида титана, применяемые в клеточной терапии: а – инкубаторы; б – единичный инкубатор
б

Размер:
2,5 х 2,5 х 4 мм
провести сравнительный анализ жизнеспособности клеток, иммобилизованных в пористо-проницаемом никелиде титана, при ИК- и УФ-облучениях.
Материал и методы
В работе использовали пористо-проницаемые инкубаторы из никелида титана, разработанные в НИИ медицинских материалов и имплантатов с памятью формы (Томск, Россия).
Пористые инкубаторы получены методом саморас-пространяющегося высокотемпературного синтеза с проницаемой пористостью около 70%. Инкубаторы вырезаны электроэрозионным способом из медицинского сплава ТН-10 (рис. 1).
Топографию поверхности образцов и структуру порового пространства изучали с использованием растрового электронного микроскопа Quanta 200 3D.
Животные – мыши С57BL\6, массой 20–24 г, возраст 18–12 недель, самцы.
Опухоль – карцинома Эрлиха (асцитный вариант), доза перевивки 5 х 106 клеток.
Выделяли клетки из асцетической жидкости мышей C57BL/6 методом центрифугирования. Затем ресуспен-дировали в полной культуральной среде, состоящей из среды RPMI-1640 (ООО «Панэко», Москва) c 10% эмбриональной телячьей сывороткой, 250 мг/л глутамина и 40 мкг/мл гентамицина (ООО «Панэко», Москва). В аналогичной среде использовали клетки костного мозга и селезенки мышей C57BL/6, полученные по соответствующим методикам.
Раскапывали клетки в 96-луночный планшет по 2 х 105 клеток на лунку, сверху размещали конструк- цию со встроенными светодиодами необходимой длины волны. Облучение проводили на расстоянии 1 см от поверхности жидкости. Культивировали клетки необходимое время в светонепроницаемом СО2-ин-кубаторе при 37 °C и 100% влажности. По окончании культивирования подсчитывали их жизнеспособность с помощью трипанового синего. Для каждого светодиода отводили 3 лунки с образцами клеточной суспензии. Предварительно в опытные лунки добавляли стерильные образцы из пористо-проницаемого никелида титана размером 2,5 х 2,5 х 2 мм, составляющие приблизительно 1/10 культурального объема.
Группы сравнения: первая (контроль) – процент жизнеспособных клеток в культуральной среде; вторая – процент жизнеспособных клеток в присутствии пористого никелида титана; третья – процент жизнеспособных клеток после облучения ИК-спектром малой интенсивности в присутствии пористого никелида титана (контрольная культура облучалась аналогичное время дневным искусственным светом); четвертая – процент жизнеспособных клеток после облучения УФ-спектром малой интенсивности в присутствии пористого никелида титана (контрольную культуру облучали аналогичное время дневным искусственным светом).
Воздействие облучения на клетки и образцы инкубаторов осуществлялось светодиодами типа L-53SF6C (ИК-излучение) и LLT-UVLED11 (УФ-излучение) (Китай) в течение 4 ч при мощности излучения 4–6 мВт/см2 и последующим адаптационным периодом 20 ч. После 30 мин обработки 0,25% раствором трипсина-ЭДТА планшеты центрифугировались. Ресуспендировали клеточные суспензии и подсчитывали количество жизнеспособных клеток с помощью 0,4% трипанового сине-

Рис. 2. Клетки на поверхности образца из никелида титана (SEM) на 7-е сутки после засева: а – селезеночные; б – опухолевые

го. Далее вычисляли процент трипаннегативных клеток от общего количества и анализировали данные статистически.
Статистическую обработку проводили общепринятыми методами с помощью программного пакета Statistica 6.0. Поскольку в исследовании присутствовали выборки, закон распределения числовых показателей в которых отличался от нормального, по данным проверки при помощи критерия Колмогорова – Смирнова, до- стоверность различий изучаемых признаков проверяли при помощи непараметрического U-критерия Манна – Уитни (попарные сравнения независимых совокупностей показателей).
Результаты
Исследования взаимодействия различных клеток с поверхностью пористо-проницаемого никелида титана показали, что поверхность материала является ад-
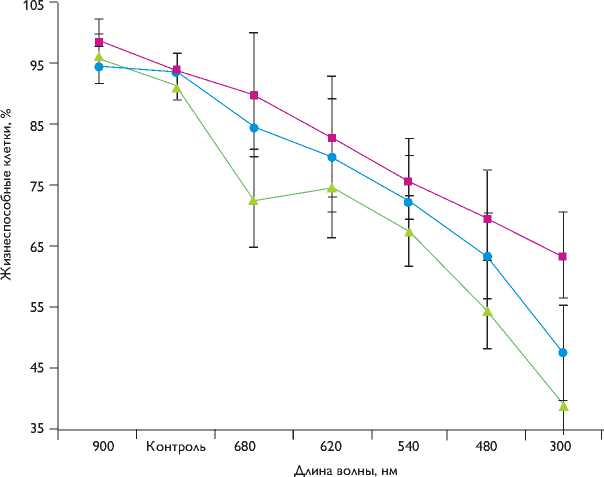
• Селезенка
■ Опухоль Эрлиха
-A- Костный мозг
Рис. 3. Жизнеспособность клеток-мишеней при воздействии излучения различных длин волн малой интенсивности в течение 4 ч
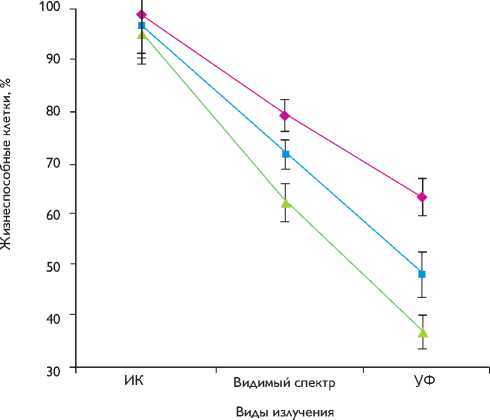
Рис. 4. Сравнение искусственного дневного облучения клеточных популяций с ИК- и УФ-спектрами
-
• Опухоль Эрлиха
-
■ Селезенка
Костный мозг гезирующей и биосовместимой с этим типом клеток подложкой. На внутренней поверхности образцов из никелида титана наблюдали прикрепленные размножающиеся клетки (рис. 2). Опухолевые клетки активно росли и размножались в пористом пространстве инкубатора из никелида титана и заполняли все поры инкубатора в течение 28–30 суток в условиях in vitro.
В исследованиях по влиянию ИК- и УФ-облучений на клетки опухоли Эрлиха, селезенки и костного мозга мышей линии С57BL/6 отмечено, что значимые показатели прослеживаются при воздействии излучения на клетки более 4 ч (рис. 3).
При воздействии ИК-излучения малой интенсивности на все исследуемые популяции клеток наблюдается достоверное повышение количества жизнеспособных клеток по сравнению с искусственным дневным облучением. При УФ-излучении – достоверное снижение жизнеспособности клеточных популяций (рис. 4).
В организме человека клеточное микроокружение и глубина залегания клеток от поверхности играют основную роль в защите от различного вида излучений. Мы попытались охарактеризовать действие ИК- и УФ-излучений на клеточные суспензии, иммобилизованные в пористо-проницаемом никелиде титана.
Отмечено достоверное изменение жизнеспособности клеточных культур в культуральной среде пористого никелида титана с последующим действием излучения. В эксперименте получено однонаправленное действие обоих излучений диапазона волн: инфракрас- ное излучение вызывает увеличение жизнеспособности клеток опухоли Эрлиха, костного мозга и селезенки в 4,6, 2,5 и 1,3 раза, ультрафиолетовое – в 3,9, 1,5 и 1,2 раза соответственно по сравнению с контрольной, в которой инкубировали клетки только при естественном освещении (рис. 5).
Такая реакция клеток на ИК- и УФ-излучения связана с преобразованием энергии спектров излучений в тепловую энергию пористых инкубаторов из никелида титана. При этом происходит сглаживание тепловой энергии в водной среде инкубатора, проявляющееся в возникновении «мягкого» градиента воздействия температуры на клеточную пролиферацию. Инфракрасное и ультрафиолетовое излучения нагревают стенки пор инкубатора и матричную основу, а жидкая окружающая среда за счет проницаемой структуры инкубатора не позволяет разогреваться до критических (для клеток) температур (43–45 °С), что оказывает благоприятное воздействие на процессы клеточной пролиферации (быстроделящихся) стволовых и опухолевых типов клеток. Более того, пористый инкубатор создает экран от прямого воздействия ультрафиолетовых лучей, предохраняя клетки от деградирующего влияния.
Заключение
Полученные данные показывают, что ИК- и УФ-излучения малой интенсивности изменяют жизнеспособность клеток и численность клеточных популяций костного мозга, опухолевых клеток и клеток селезенки:
■ Опухоль Эрлиха

Костный мозг
■ Селезенка
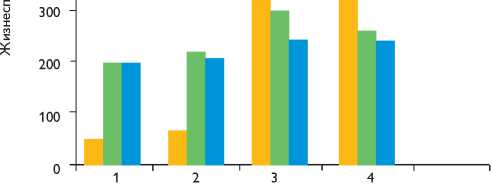
Группа
Рис. 5. Зависимость жизнеспособных клеток опухоли Эрлиха, костного мозга и селезенки от типа воздействия в различных условиях: 1 – питательной среде; 2 – пористых инкубаторах из никелида титана без облучения; 3 – пористых инкубаторах из нике-лида титана после инфракрасного облучения; 4 – пористых инкубаторах из никелида титана после ультрафиолетового облучения
активно повышают (ИК-спектр) или подавляют пролиферативную активность (УФ-спектр).
Эффект воздействия ИК-спектра можно применять в реанимации популяции клеток после выделения из тканевых структур для увеличения количества малочисленной популяции до необходимой величины. Также действие УФ-спектра, возможно, найдет применение в уничтожении остаточных опухолевых очагов или других патологических клеточных популяций.
Присутствие пористо-проницаемых инкубаторов из никелида титана изменяет параметры взаимодействия клеток костного мозга, опухолевых клеток и клеток селезенки с внешней средой, увеличивая их жизнеспособность и пролиферативные потенции. Даже клеточные популяции при УФ-облучении в условиях пористого инкубатора изменяют модуль жизнеспособности на положительный. Аналогичный эффект можно наблюдать и в живых организмах при ультрафиолетовом излучении.
Результаты данного исследования используют при разработке инкубаторов-носителей клеточных культур с размещением в матричной пористой структуре инкубатора миниатюрного генератора электромагнитного излучения с заданными параметрами воздействия.
Работа выполнена при поддержке программы «Научный фонд им. Д.И. Менделеева Национального исследо- вательского Томского государственного университета» (№ проекта 8.1.42.2015).
Список литературы Модуляция жизнеспособности клеток, иммобилизованных в пористо-проницаемом инкубаторе из никелида титана, под действием инфракрасного и ультрафиолетового излучений
- Badylak S.F., Taylor D., Uygun K. Whole-organ tissue engineering: decellularization and recellularization of three-dimensional matrix scaffolds//Annu. Rev. Biomed. Eng. 2011. Vol. 13. P. 27-53.
- Atala A. Engineering tissues, organs and cells//J. Tissue Eng. Regen. Med. 2007. Vol. 1. P. 83-96.
- L'Heureux N., McAllister T.N., de la Fuente L.M. Tissue-engineered blood vessel for adult arterial revascularization//New Engl. J. Med. 2007. Vol. 357. P. 1451-3.
- Baptista P.M., Siddiqui M.M., Lozier G., Rodriguez S.R., Atala A., Soker S. The use of whole organ decellularization for the generation of a vascularized liver organoid//Hepatology. 2010. Vol. 53. P. 604-17.
- Badylak S.F. Regenerative medicine and developmental biology: the role of the extracellular matrix//Anat. Rec. 2005. Vol. 287 B. P. 36-41.
- Ott H.C., Matthiesen T.S., Goh S.-K., Black L.D., Kren S.M., Netoff T.I., Taylor D.A. Perfusion-decellularized matrix: using nature's platform to engineer a bioartificial heart//Nature Med. 2008. Vol. 14. P. 213-21.
- Taylor D.A. From stem cells and cadaveric matrix to engineered organs//Curr. Opin. Biotechnol. 2009. Vol. 20. P. 598-605.
- Бенч Л., Джонс Д. Биоматериалы, искусственные органы и инжиниринг тканей. М.: Техносфера, 2007. 304 с.
- Orlando G., Wood K.J., Stratta R.J., Yoo J.J., Atala A., Soker S. Regenerative medicine and organ Transplantation: past, present, and future//Transplantation. 2011. Vol. 91. P. 1310-7.
- Orlando G., Baptista P., Birchall M., De Coppi P., Farney A., Guimaraes-Souza N.K., Opara E., Rogers J., Seliktar D., Shapira-Schweitzer K., Stratta R.J., Atala A., Wood K.J., Soker S. Regenerative medicine as applied to solid organ transplantation: current status and future challenges//Transpl. Int. 2011. Vol. 24. P. 223-32.
- Кокорев О.В., Дамбаев Г.Ц., Ходоренко В.Н., Гюнтер В.Э. Применение пористо-проницаемых инкубаторов из никелида титана в качестве носителей клеточных культур//Клеточная трансплантология и тканевая инженерия. 2010. Т. 5. № 4. С. 31-37.
- Медицинские материалы и имплантаты с памятью формы: В 14 томах//Под ред. В.Э. Гюнтера. Медицинские материалы с памятью формы. Т. 1. Томск: Изд-во МИЦ, 2011. 534 с.
- Медицинские материалы и имплантаты с памятью формы: В 14 томах//Под ред. В.Э. Гюнтера. Имплантаты с памятью формы в хирургии. Т. 11. Томск: Изд-во МИЦ, 2012. 398 с.
- Kokorev O.V., Hodorenko V.N., Chekalkin T.L., Dambaev G.Ts., Gunther V.E. Porous TINI-based alloy scaffold for cell tissue engineering//Journal of Advanced Scientific Research. 2014. Vol. 5. № 3. P. 01-06.
- Almine J.F., Bax D.V., Mithieux S.M., Nivison-Smith L., Rnjak J., Waterhouse A., Wise S.G., Weiss A.S. Elastin-based materials//Chem. Soc. Rev. 2010. Vol. 39. P. 3371-9.
- Kanematsu A., Yamamoto S., Ozeki M., Noguchi T., Kanatani I., Ogawa O., Tabata Y. Collagenous matrices as release carriers of exogenous growth factors//Biomaterials. 2004. Vol. 25. P. 4513-20.
- Price A.P., England K.A., Matson A.M., Blazar B.R., Panoskaltsis-Mortari A. Development of a decellularized lung bioreactor system for bioengineering the lung: the matrix reloaded//Tissue Eng. A. 2010. Vol. 16. P. 2581-91.
- Альбертс Б., Брейт Д. Молекулярная биология клетки. Т. 1. М.: Мир, 1994. 350 с.
- Тучин В.В. Оптическая биомедицинская диагностика. Т. 2. М., 2007. 367 c.
- Ремизов А.Н. Медицинская и биологическая физика. М.: Высш. школа, 1996. 608 с.
- Исаков В.Л. Основные вопросы разработки методических рекомендаций по лазерной медицине//Применение лазеров в биологии и медицине. К., 1995. С. 7-20.
- Антонов В.Ф., Черныш А.М., Пасечник В.И. Биофизика. М.: Физика, 2000. 154 с.
- Вайль Н.С. Инфракрасные лучи в клинической диагностике и медико-биологических исследованиях. М.: Медицина, 1996. 278 с.
- Мейер А., Зейтц Э. Ультрафиолетовое излучение. М.: Науч. лит-ра, 1989. 574 с.
- Патент RU № 2438699. Способ изготовления вакцины для лечения адэнокарциномы Эрлиха в эксперименте//С.В. Гюнтер, О.В. Кокорев. 7 с.


