Молекулярно-биологические изменения в миокарде самцов мышей BALB/c на разных сроках аутоиммунного миокардита
Автор: Мельникова Е.А., Сентябрева А.В., Цветков И.С., Косырева А.М.
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 4 т.33, 2025 года.
Бесплатный доступ
Цель: оценить морфологические и молекулярно-биологические изменения миокарда у самцов мышей BALB/c на 14-е, 28-е, 42-е и 60-е сутки экспериментального аутоиммунного миокардита. Материалы и методы. Экспериментальный аутоиммунный миокардит индуцировали у половозрелых самцов мышей BALB/c (n=60) путём трёхкратной подкожной иммунизации гомогенатом миокарда свиньи с полным адъювантом Фрейнда. Животных выводили из эксперимента на 14-е, 28-е, 42-е и 60-е сутки. Проводили морфологическое исследование с окраской гематоксилином и эозином, по Маллори, иммуногистохимическое исследование (CD3, CD68) и количественную ПЦР в реальном времени для оценки экспрессии генов Hif1a, Nfkb, Il1b, Il6, Il10 и Tgfb. Результаты. На 14-е сутки выявлены признаки острого воспаления: лимфогистиоцитарная инфильтрация CD3+ Т-лимфоцитами и повышение экспрессии Hif1a, Nfkb, Il1b и Tgfb. К 28-м суткам отмечалось снижение экспрессии провоспалительных генов и формирование очагов фиброза. На 42-е сутки возрастали уровни экспрессии Il6, Il10, Hif1a и Tgfb; морфологически определялись признаки повреждения кардиомиоцитов. К 60-м суткам сохранялась высокая экспрессия Il6 и Il10 при наличии миоцитолиза. Заключение: Выявленная динамика молекулярно-биологических изменений свидетельствует о формировании хронического воспалительного процесса с преобладанием противовоспалительных цитокинов IL-6 и IL-10 на поздних сроках аутоиммунного миокардита у самцов мышей BALB/c, что может способствовать прогрессированию заболевания и развитию дилатационной кардиомиопатии.
Миокардит, воспаление, аутоиммунные заболевания, иммунный ответ, экспериментальная модель
Короткий адрес: https://sciup.org/143185411
IDR: 143185411 | УДК: 616.127-002-092.9:577.2 | DOI: 10.20340/mv-mn.2025.33(4).981
Molecular and biological changes in the myocardium of male BALB/c mice at different stages of autoimmune myocarditis
Objective: to evaluate morphological and molecular biological changes in the myocardium of male BALB/c mice on days 14, 28, 42, and 60 of experimental autoimmune myocarditis. Materials and Methods. Experimental autoimmune myocarditis was induced in adult male BALB/c mice (n=60) by three subcutaneous immunizations with porcine myocardial homogenate in complete Freund's adjuvant. Animals were sacrificed on days 14, 28, 42, and 60. Morphological examination was performed using hematoxylin and eosin staining, Mallory's trichrome staining, immunohistochemical analysis (CD3, CD68), and real-time quantitative PCR to assess the expression of Hif1a, Nfkb, Il1b, Il6, Il10, and Tgfb genes. Results. On day 14, signs of acute inflammation were detected: lymphohistiocytic infiltration with CD3+ T lymphocytes and increased expression of Hif1a, Nfkb, Il1b, and Tgfb. By day 28, a decrease in pro-inflammatory gene expression and formation of fibrosis foci were observed. On day 42, expression levels of Il6, Il10, Hif1a, and Tgfb increased; morphologically, signs of cardiomyocyte damage were identified. By day 60, high expression of Il6 and Il10 persisted in the presence of myocytolysis. Conclusion. The identified dynamics of molecular biological changes indicate the formation of a chronic inflammatory process with a predominance of anti-inflammatory cytokines IL-6 and IL-10 at late stages of autoimmune myocarditis in male BALB/c mice, which may contribute to disease progression and development of dilated cardiomyopathy.
Текст научной статьи Молекулярно-биологические изменения в миокарде самцов мышей BALB/c на разных сроках аутоиммунного миокардита
(4).981
Mel’nikova EA, Sentyabreva AV, Tsvetkov IS, Kosyreva AM. Molecular and biological changes in the myocardium of male BALB/c mice at different stages of autoimmune myocarditis. Morfologicheskie Vedomosti – Morphological newsletter. 2025; 33(4):981. (4).981
Миокардит – воспалительное заболевание миокарда – имеет полиморфные клинические проявления: от бессимптомного течения, легкой одышки и кратковременной боли в грудной клетке до тяжелых форм с развитием сердечной недостаточности и внезапной сердечной смерти. Одним из наиболее жизнеугрожающих осложнений миокардита является развитие дилатационной кардиомиопатии (ДКМП) [1]. До 30% всех случаев миокардита, подтвержденного морфологическим исследованием биоптатов, прогрессирует с развитием ДКМП и хронической сердечнососудистой недостаточности [1]. ДКМП является одной из наиболее частых причин трансплантации сердца. Согласно данным 36-го отчета о трансплантации сердца у взрослых международного регистра трансплантации торакальных органов ISHLT (International Society for Heart and Lung Transplantation), 51% трансплантаций сердца перенесли пациенты с ДКМП [2].
Для изучения дилатационной кардиомиопатии воспалительной этиологии часто используют модели экспериментального аутоиммунного и вирусного миокардита [3], однако исследований, посвященных молекулярным механизмам развития и прогрессирования миокардита и дилатационной кардиомиопатии, по-прежнему недостаточно. В литературе выделяют три фазы миокардита: острую, подострую и хроническую. Однако представления о длительности острой фазы различаются. Так, по данным одних авторов, острая фаза продолжается до 7 суток и соответствует активации врожденного иммунного ответа, характеризуясь инфильтрацией макрофагами и нейтрофилами, выработкой провоспалительных цитокинов и первичным повреждением кардиомиоцитов, а активация адаптивного иммунитета происходит в подострую фазу [4]. Другие авторы к острой фазе относят период до 14 суток [5], по-видимому, включая в нее не только реакции врожденного, но и начальные проявления адаптивного иммунного ответа, связанные с презентацией антигена и активацией Т-лимфоцитов. Подострая фаза (до 28 суток) характеризуется активацией адаптивного иммунного ответа и дальнейшим повреждением кардиомиоцитов; в эту же фазу возможно разрешение заболевания. Хроническая фаза (после 28 суток) миокардита характеризуется процессами фиброза, ремоделированием экстрацеллюлярного матрикса и формированием ДКМП [4]. Однако исследования, посвященные изучению молекулярно-биологических изменений в миокарде на более поздних сроках развития экспериментального аутоиммунного миокардита, немногочисленны. Согласно полученным нами данным, экспериментальный аутоиммунный миокардит у самцов мышей линии BALB/c протекает более тяжело, чем у самок [6].
ЦЕЛЬ ИССЛЕДОВАНИЯ: оценить морфологические и молекулярно-биологические изменения миокарда у самцов мышей BALB/c на 14-е, 28-е, 42-е и 60-е сутки экспериментального аутоиммунного миокардита.
МАТЕРИАЛ И МЕТОДЫ
Исследование выполнено на половозрелых самцах мышей BALB/c (n=60) массой тела 18–25 г (Филиал «Столбовая» ФГБУН НЦБМТ ФМБА России). При работе с экспериментальными животными руководствовались принципами Европейской конвенции о защите позвоночных животных, используемых для экспериментов (ETS 123, Страсбург, 1986), и директивы Европейского парламента и Совета Европейского Союза (2010/63/EU, Страсбург, 2010). На проведение исследования получено разрешение био-этической комиссии НИИ морфологии человека им. акад. А.П. Авцына ФГБНУ «РНЦХ им. акад. Б.В. Петровского», протокол № 8 от 20 октября 2022 г. До начала исследования лабораторных животных 7 суток содержали в условиях вивария для адаптации малыми группами (n=5) в клетках размерами 425×276×153 мм в условиях естественного светового режима при температуре 19–21°С и относительной влажности воздуха 40–60%. Животные получали полнорационный корм и воду ad libitum.
Для моделирования аутоиммунного миокардита самцам (n=40) опытных групп подкожно вводили фрагмент тяжелой цепи α-миозина (Ac-RSLKLMATLFSTYASADR, MedChemExpress, США) в дозе 150 мкг с 120 мкл полного адъюванта Фрейнда (Sigma-Aldrich, США) на 0 день [6]. Вторую инъекцию с такими же концентрациями α-миозина в комплексе с неполным адъювантом Фрейнда такого же объема проводили на 7-й день. Мышам (n=20) контрольной группы подкожно вводили такой же объем NaCl 0,9%.
Мышей выводили из эксперимента в разные сроки: на 14-й день, соответствующий фазе острого миокардита (n=15); на 28 сутки, соответствующие фазе перехода в подострую фазу аутоиммунного миокардита (n=15); на 42 сутки, соответствующие фазе перехода подострого миокардита в хроническую фазу (n=15) и на 60й день после второй иммунизации, соответствующий фазе хронического миокардита (n=15). Данные о количестве животных внутри каждой группы представлены в таблице 1.
Животных выводили из эксперимента под золетиловым наркозом (Virbac S.A., Франция) в дозе 50 мг/кг. Для гистологического исследования фрагменты левого желудочка и предсердия фиксировали в 10%-м забуференном формалине (БиоВитрум, Россия). Для qRT-PCR исследования фрагменты правого желудочка помещали в фиксатор IntactRNA («Евроген», Россия).
Таблица 1. Распределение животных по группам
|
Срок |
Группа |
n |
|
14 сутки |
Контрольная группа |
5 |
|
α-миозин |
10 |
|
|
28 сутки |
Контрольная группа |
5 |
|
α-миозин |
10 |
|
|
42 сутки |
Контрольная группа |
5 |
|
α-миозин |
10 |
|
|
60 сутки |
Контрольная группа |
5 |
|
α-миозин |
10 |
Для получения гистологических срезов сердца использовали стандартную методику. Проводили обезвоживание, проводку в спиртах возрастающих концентраций, ксилоле и парафине. Заливку блоков осуществляли в автоматизированном гистологическом процессоре Tissue-Tek VIP 5 Jr и аппарате Tissue-Tek TEС-5 (Sakura, Япония). Для оценки морфологической структуры миокарда, выявления клеточной инфильтрации и степени повреждения кардиомиоцитов использовалась окраска гематоксилином и эозином как стандартный и широко применяемый метод гистологического анализа. На гистологических препаратах миокарда, окрашенных гематоксилин-эозином, подсчитывали число лимфо-гистиоцитарных клеток на стандартное поле зрения (10 000 мкм2) для оценки клеточной инфильтрации в миокарде при ув. ×1000. Для оценки фиброза в миокарде использовали окраску по Маллори. Для оценки повреждений миокарда использовали окраску по Ли (ГОПФ). Для выявления лимфоцитов срезы миокарда исследовались иммуногистохимическим методом с использованием антител к лимфоцитам CD3+ (1:500; 103R-96, Cell Marque, США). Окрашивание проводилось в иммунострейнере Leica BondMAX (Германия).
Методом qRT-PCR во фрагментах миокарда определяли уровни экспрессии мРНК Hif1a – фактора, индуцируемого гипоксией, транскрипционного фактора Nfkb, провоспалительных цитокинов Il1β и Il6 и противовоспалительных цитокинов Il10 и Tgfβ. Для выделения мРНК использовали реактив ExtractRNA («Евроген», Россия), обратную транскрипцию проводили с использованием набора MMLV RT Kit («Евроген», Россия). Амплификацию с использованием смеси для ПЦР qPCRmix-HS SYBR («Евроген», Россия), содержащей флюоресцентный интеркали-рующий краситель SYBR Green I, проводили на амплификаторе Real-Time DTprime (ДНК-Технология, Россия). В качестве референса использовали ген домашнего хозяйства Gapdh.
Для анализа экспрессии генов использовали метод определения порогового цикла и вычисления относительной экспрессии гена по методу ΔCt. Праймеры (табл. 2) подбирали с помощью программного обеспечения Primer-BLAST.
Таблица 2. Последовательность использованных праймеров (видоспецифичны для Mus musculus)
|
Ген |
Праймер |
Последовательность (5′–3′) |
|
Gapdh |
forward |
AGGCCGGTGCTGAGTATGTC |
|
reverse |
TGCCTGCTTCACCACCTTCT |
|
|
Hif1a |
forward |
AGGATGAGTTCTGAACGTCGAAA |
|
reverse |
CTGTCTAGACCACCGGCATC |
|
|
Nfkb |
forward |
GGTGGAGGCATGTTCGGTA |
|
reverse |
TGACCCCTGCGTTGGATT |
|
|
Il1b |
forward |
ACAACGTGAGCTTCTTCGGA |
|
reverse |
CACATGCGCCGACTCAAAAA |
|
|
Il6 |
forward |
CCACTTCACAAGTCGGAGGC |
|
reverse |
GGAGAGCATTGGAAATTGGGGT |
|
|
Il10 |
forward |
TAAGTGGCAAAGGGGGCGAG |
|
reverse |
AGGCTGAGCCCCAATGATGT |
|
|
Tgfb |
forward |
GTACTCTGGCAGTGACCCCG |
|
reverse |
AACTGCTCCACCTTGGGCTT |
Статистический анализ проводили в программе GraphPad Prism 10.0 (GraphPad Software, США) с использованием непараметрических критериев сравнения. Нормальность распределения данных определяли с помощью критерия Колмогорова-Смирнова. При множественных сравнениях использовали критерий Краскела-Уоллиса и post-hoc тест Двасс-Стил-Кричлоу-Флигнера. Данные приведены в виде медианы и верхнего/нижнего квартилей (Ме (LQ 25%; UQ 75%)). Различия считали значимыми при p<0.05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
По данным qRT-PCR анализа по уровню экспрессии Hif1a, Nfkb, Il1b, Il6, Il10 и Tgfb в миокарде контрольных групп на 14, 28, 42 и 60 сутки статистически значимо не различались (табл. 3). Поэтому было принято решение объединить их в одну общую контрольную группу, не разделяя по срокам исследования.
Таблица 3. Экспрессия мРНК Hif1α, Nfkb, Il1b, Il6, Il10 и Tgfb в миокарде контрольных групп (К) на 14-е (К14), 28-е (К28), 42-е (К42) и 60-е (К60) сутки у самцов мышей BALB/c. Данные приведены в виде Ме (LQ 25%- UQ 75%)
|
Параметр |
Самцы |
Статисти ческие различия (p) |
||||
|
К14 (n=5) |
К28 (n=5) |
К42 (n=5) |
К60 (n=5) |
|||
|
Фактор, индуцируемый гипоксией |
Hif1α |
1179,0 (885,9–1524,5) |
840,1 (547,2–687,5) |
840,1 (744,1–897,4) |
897,4 (231,1–2924,0) |
- |
|
Транскрипционный фактор |
Nfκb |
123,8 (17,0–322,1) |
104,6 (55,5–648,4) |
122,7 (21,2–272,0) |
151,9 (52,4–1750,0) |
- |
|
Провоспалительные цитокины |
Il1β |
132,5 (27,5–395,4) |
72,5 (46,8–588,0) |
70,8 (27,9–453,3) |
115,6 (36,2–1263,0) |
- |
|
Il6 |
27,5 (15,8–114,9) |
85,0 (0,2–179,1) |
73,3 (28,5–401,0) |
67,5 (37,5–143,9) |
- |
|
|
Противовоспалительные цитокины |
Il10 |
88,0 (13,9–180,3) |
100,9 (25,2–155,9) |
55,0 (4,0–195,2) |
82,6 (0,0–486,4) |
- |
|
Tgfβ |
64,7 (24,9–138,7) |
66,9 (16,8–26,3) |
22,4 (10,4–735,9) |
66,5 (4,9–510,3) |
- |
|
На гистологических препаратах миокарда самцов контрольной группы мышей поперечная исчерченность кардиомиоцитов сохранена, наблюдаются диффузно рассеянные кардиомиоциты (рис. 1А).
На 14-е сутки развития миокардита на гистологических препаратах миокарда отмечалась очаговая субэпикардиальная лимфоидно-гистиоцитарная инфильтрация, выраженный периваскулярный отёк и мышечные контрактуры (рис. 1Б). Изменения наблюдались как в предсердии, так и в желудочке, при этом в предсердиях они были более выраженными. При ИГХ исследовании в препаратах отмечалась субэпикардиальная инфильтрация CD3+ Т-лимфоцитами (рис. 1В).
На 28-е сутки эксперимента в желудочках преобладала диффузная лимфоидно-гистиоцитарная инфильтрация, очаговые скопления лимфоцитов были единичными (рис. 1Г). В предсердиях наблюдался периваскулярный отек, вакуолизация кардиомиоцитов и гиперэозинофилия цитоплазмы. У 2 из 10 самцов наблюдались очаги фиброза в предсердии (рис. 1Д).
На 42-е сутки аутоиммунного миокардита у 3 из 10 самцов была обнаружена очаговая субэпикардиальная лимфоцитарная и гистиоцитарная инфильтрация, у 4 из 10 самцов выявлялась диффузная лимфоидно-гистиоцитарная инфильтрация. В кардиомиоцитах как желудочков, так и предсердий наблюдалась вакуолизация цитоплазмы, единичные контрактурные повреждения с более выраженными изменениями в предсердии (рис. 1Е). Фибротические изменения наблюдались в предсердиях у 4 из 10 самцов.
На 60-е сутки развития миокардита у самцов в единичных кардиомиоцитах определялись признаки некроза: кариорексис, миоцитолизис (рис 1 Ж). В кардиомиоцитах наблюдалась гиперэозинофилия цитоплазмы и единичные контрактурные повреждения (рис. 1З). В предсердиях отмечалась вакуолизация кардиомиоцитов, признаки некроза кардиомиоцитов были более выраженными.
Таким образом, на 14-е, 28-е и 42-е сутки после второй иммунизации, в миокарде как предсердий, так и желудочков определяется увеличение числа инфильтрирующих миокард клеток, на 42-е и 60-е сутки наблюдается повреждение кардиомиоцитов, что свидетельствует о развитии аутоиммунного миокардита. На 28-е и 42-е сутки отмечается появление очагов фиброза, что может свидетельствовать о переходе миокардита в ДКМП.
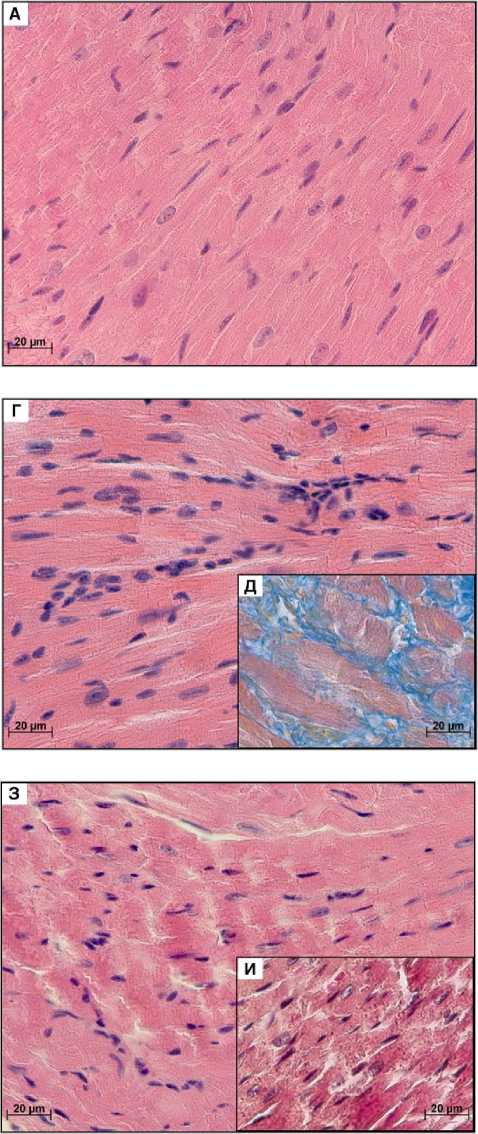
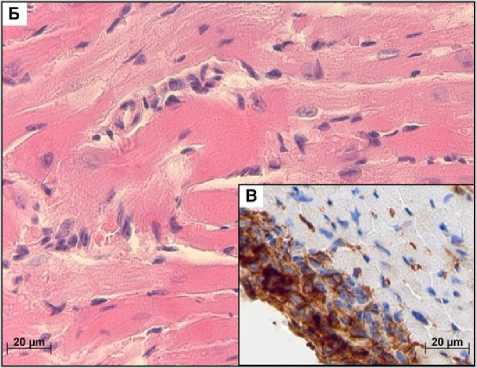
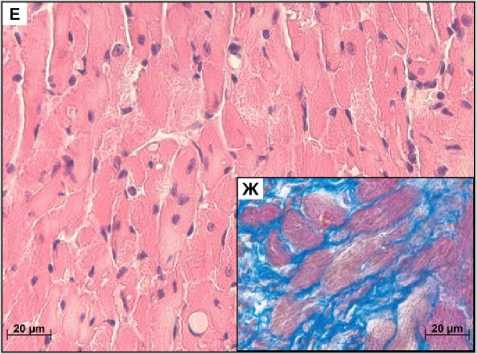
Рис. 1. Морфологическая характеристика миокарда самцов мышей BALB/c контрольной и экспериментальной групп. А. Контрольная группа: кардиомиоциты с поперечной исчерчен-ностью. Б. 14-е сутки: лимфоцитарная и гистиоцитарная инфильтрация, контрактурные повреждения. В. 14-е сутки: субэпикардиальная лимфоцитарная инфильтрация, ИГХ окрашивание с антителами к CD3. Г. 28-е сутки: диффузная лимфоцитарная и ги-стиоцитарная инфильтрация. Д. 28-е сутки: очаговый фиброз, окраска по Маллори. Е. 42-е сутки: диффузная лимфоцитарная и гистиоцитарная инфильтрация, вакуолизация цитоплазмы кардиомиоцитов. Ж. 42-е сутки: очаговый фиброз, окраска по Маллори. З. 60-е сутки: диффузная лимфо-гистиоцитарная инфильтрация, кардиомиоцитолиз, интерстициальный отек, исчезновение поперечной исчерченности. И. 60-е сутки: кардиомиоцитолиз, некроз кардиомиоцитов, окраска по Ли (ГОПФ), ув. ×640
При морфометрическом исследовании числа лимфо-гистиоцитарных клеток в срезах миокарда по сравнению с контрольной группой и 60-ми сутками развития аутоиммунного миокардита наблюдалось увеличение их количества на 14, 28 и 42 сутками (рис. 2). Увеличение числа лимфо- гистиоцитарных клеток в миокарде на 14-е, 28-е и 42-е сутки по сравнению с контрольной группой свидетельствует о развитии воспалительной реакции. На 60-е сутки развития аутоиммунного миокардита число лимфоцитов и гистиоцитов не отличалось от такового в контрольной группе.
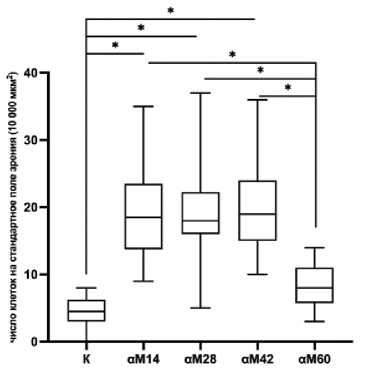
Рис. 2. Количество лимфо-гистиоцитарных клеток в миокарде самцов мышей BALB/c контрольной группы (К), на 14-е (αМ14), 28-е (αМ28), 42-е (αМ42) и 60-е (αМ60) сутки развития аутоиммунного миокардита в стандартном поле зрения (10 000 мкм2)
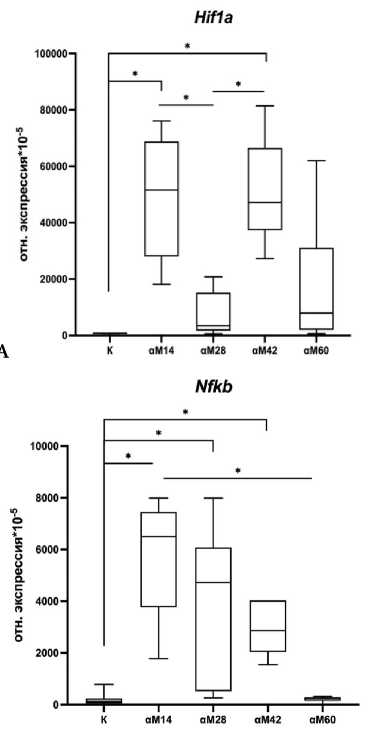
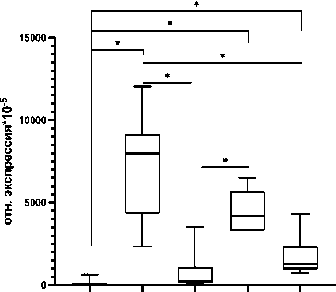
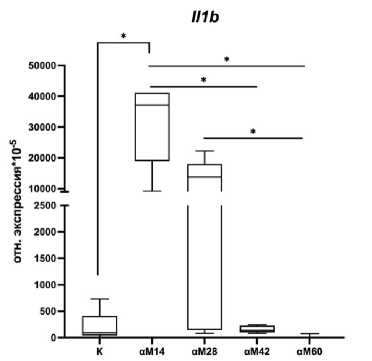
По данным qRT-PCR анализа по сравнению с контрольной группой на 14-е сутки развития миокардита наблюдалось повышение уровня экспрессии мРНК фактора, индуцируемого гипоксией, Hif1a, транскрипционного фактора Nfkb, провоспалительного цитокина Il1b и противовоспалительного цитокина Tgfb в желудочках (рис. 3). Данные изменения в уровне экспрессии генов могут быть следствием увеличением числа лимфоцитов и гистиоцитов в миокарде. что является характерным для развития острой фазы воспалительной реакции.
По сравнению с 14-ми сутками аутоиммунного миокардита, на 28-е сутки уровень экспрессии мРНК Hif1a, Tgfb, Nfkb и Il1b в миокарде снижался, тогда как экспрессия Il6 и Il10 не изменялась и не отличалась от контрольной группы.
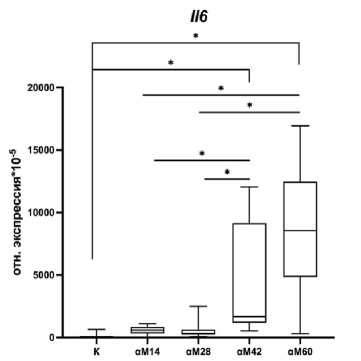
По сравнению с 28-ми сутками, на 42-е сутки аутоиммунного миокардита уровни экспрессии мРНК Hif1a, Tgfb, провоспалительного цитокина Il6 и противовоспалительного цитокина Il10 повышались.
По сравнению с 42-ми сутками аутоиммунного миокардита, на 60-е сутки уровень экспрессии Il6 и Il10 не изменялся и был устойчиво высоким, чем в контрольной и других опытных группах (рис. 3 Д, Е).
При аутоиммунном миокардите воспалительная реакция формируется за счет активации сигнальных каскадов, включающих как про-, так и противовоспалительные медиаторы. Одним из ключевых регуляторов воспаления является HIF-1α, экспрессия которого усиливается в условиях низкого содержания кислорода и за счет перекрестного взаимодействия с NF-κB-зависимым сигнальным путем. В условиях аутоиммунного миокардита воспаление сопровождается развитием локальной гипоксии, что способствует активации HIF-1α [7]. Провоспалительные цитокины (IL-1β, TNF-α), DAMP (Damage associated molecular pathogen), окислительный стресс и гипоксия стимулируют NF-κB через активацию IκB-киназы (IKK), что, в свою очередь, приводит к усилению активности HIF-1α [8]. Сигнальный путь NF-κB способствует синтезу провоспали-тельных цитокинов и играет важную роль в развитии воспаления в миокарде.
TGF-β играет ключевую роль как противовоспалительный цитокин, участвуя в поляризации макрофагов по М2 фенотипу, регенерации тканей и развитии фиброза. Однако при аутоиммунном миокардите он может проявлять и про-воспалительную активность [9]. В литературе описана взаимосвязь между HIF-1α и TGF-β1. Так, показано, что в культуре макрофагов человека, гипоксия приводит к увеличению экспрессии как HIF-1a, так и TGF-b1, тогда как сайленсинг гена HIF-1a вызывает снижение экспрессии как HIF-1a, так и TGF-b1, однако данный механизм их синергического взаимодействия до конца не изучен [10]. Другой механизм взаимосвязи TGF-β и HIF-1α связан с мишенью рапа-мицина у млекопитающих – комплексом 1 (mTORC1), который активируется через молекулярный путь TGF-β/Smad3/mTORC1/HIF-1α. Так, на культуре мезангиальных клеток человека было выявлено, что добавление рапамицина в условиях нормоксии снижает экспрессию HIF-1a и коллагена I типа, однако не влияет на экспрессию TGF-b [11], но данный механизм не был исследован при миокардите, переходящем в ДКМП.
В
Tgfb
Б К <11414 aM28 ОМ42 аМ60
Г
Д
Е
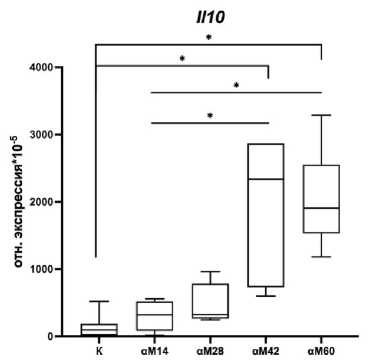
Рис. 3. Экспрессия мРНК А) фактора, индуцируемого гипоксией, Hif1a , Б) противоспалительного цитокина Tgfb , В) транскрипционного фактора Nfkb , Г) провоспалительного цитокина Il1b , Д) провоспалительного цитокина Il6 и Е) противовоспалительного цитокина Il10 в миокарде самцов контрольных и опытных групп, на 14-е, 28-е, 42-е и 60-е сутки аутоиммунного миокардита. К –контрольная группа (n=20); αМ14 – группа мышей, подвергшиеся введению α-миозина и выведенные на 14-е сутки после второй иммунизации (n=10); αМ28 – группа мышей, подвергшиеся введению α-миозина и выведенные на 28-е сутки после второй иммунизации (n=10); αМ42 – группа мышей, подвергшиеся введению α-миозина и выведенные на 42-е сутки после второй иммунизации (n=10); αМ60 – группа мышей, подвергшиеся введению α-миозина и выведенные на 60-е сутки после второй иммунизации (n=10). Для множественных сравнений использовался критерий Краскела-Уоллиса. Данные приведены в виде Ме (LQ 25%; UQ 75%)
Таким образом, согласно морфологическому и qRT-PCR исследованиям, на 14-е сутки экспериментального аутоиммунного миокардита развивается острая фаза воспаления. Инфильтрирующие миокард клетки, такие как макрофаги и лимфоциты, наблюдаемые на гистологических препаратах на 14-е сутки, экспрессируют Hif1a, Il1b, Nfkb и Tgfb. Кроме того, известно, что кардиомиоциты способны синтезировать Hif1a, Nfkb в условиях гипоксии и при воспалении, а также Tgfb при ремоделировании внеклеточного матрикса сердца. Кроме того, сами кардиомиоциты могут секретировать IL-1β через образование инфламмасомы (ASC, NLRP3 и др [12, 13].
При исследовании группы мышей на 28-е сутки аутоиммунного миокардита было установлено снижение экспрессии Hif1a и Tgfb. Так, наши данные согласуются с результатами Hua et al. [5], которые показали аналогичное снижение экспрессии Hif1a на 21-е сутки при аутоиммунном миокардите у мышей BALB/c. В другом исследовании у крыс Lewis при экспериментальном аутоиммунном миокардите экспрессия Tgfb снижалась к 28 суткам [14]. Данные изменения на 28-е сутки аутоиммунного миокардита могут быть связаны с переходом заболевания в фазу подострого воспаления. Наблюдаемые очаги фиброза на 28-е сутки могут быть связаны с активацией фибробластов под действием Tgfb в острую фазу миокардита.
Анализ группы животных на 42-е сутки эксперимента выявил повышение экспрессии мРНК Hif1a, Tgfb, Il6 и Il10. Повышение экспрессии Il6 может быть связано с переходом в хроническую фазу воспаления, в то время как увеличение экспрессии Il10 может быть следствием развития компенсаторной реакции. В литературе описано, что М2, противовоспалительные, макрофаги участвуют в продукции TGF-β, что ведет к стабилизации HIF-1α [11,15]. Повышение экспрессии Il10 вместе с Il6 предположительно связано с их участием в сигнальном пути JAK1/STAT3/SOCS3. Так, при добавлении ингибитора JAK1, тофацитиниба, в культуру макрофагов мыши RAW264.7 снижалась экспрессия
Il10, что показывает, что IL-6 может влиять на экспрессию IL-10 [16]. Camporeale, A., et al. [17], показали, что при аутоиммунном миокардите подавление STAT3 сигнального пути ингибитором SFI-066 устраняло как повышение концентрации комплимента C3, так и образование антимиозиновых антител. Повышение продукции Il6 также может влиять на экспрессию Hif1α. IL-6 может связываться с ферментом глутамиламинопептидазой (gp160), что вызывает активацию пути STAT3/HIF-1α [18]. Нами показано, что на 42-е сутки развития миокардита в кардиомиоцитах выявляется вакуолизация цитоплазмы, что свидетельствует о повреждении клеток. В ответ на повреждение кардиомиоциты, как было описано ранее, могут экспрессировать Hif1a и Tgfb, что и было нами выявлено с помощью qRT-PCR. Повышение уровня экспрессии Il6 может быть следствием инфильтрации миокарда лимфоцитами, гипоксии, или повреждения кардиомиоцитов [19].
На 60-е сутки миокардита, у мышей опытной группы сохранялось повышенное уровни экспрессии Il6. Сохранение высокой экспрессии Il6 может быть связано с развитием хронического воспаления, а также быть следствием миоцитолиза. По данным литературы длительное повышение IL-6 угнетает базовую сократимость кардиомиоцитов, что приводит к снижению фракции выброса сердца [20]. По-видимому, на 60-е сутки аутоиммунного миокардита возможно появление признаков ДКМП, однако, это требует дальнейшего изучения.
ЗАКЛЮЧЕНИЕ
Таким образом, по нашим данным, на ранних сроках развития аутоиммунного миокардита отмечается выраженная очаговая лимфоидная и гистиоцитарная инфильтрация миокарда с повышением экспрессии Il1b, Nfkb и Hif1a, которые участвуют в остром воспалительном ответе. На 28-е сутки заболевания в миокарде выявлена выраженная диффузная лимфо-гистиоцитарная инфильтрация, однако экспрессия провоспали-тельних и транскрипционных факторов была снижена, что может объяснять переход от острой фазы воспаления к подострой. Также в данную фазу были выявлены очаги фиброза, что указывает на активацию процессов ремоделирования экстрацеллюлярного матрикса и замещение погибающих или поврежденных кардиомиоцитов соединительной тканью. На 42-е сутки аутоиммунного миокардита наблюдали очаги некроза, что сопровождалось повышением экспрессии Hif1a и Tgfb, Il6 и Il10. Данная реакция может быть следствием повреждения кардиомиоцитов, в свою очередь, которое приводит к увеличению продукции активных форм кислорода, способных стимулировать образование HIF-1α. На 60-е сутки был выявлен миоцитолиз кардиомиоцитов с повышением экспрессии Il6 и Il10, что характерно для хронической фазы воспаления. Полученные данные расширяют знания о молекулярно-биологических изменениях в миокарде в разные сроки аутоиммунного миокардита у самцов. Однако необходимы дальнейшие исследования молекулярнобиологических изменений в миокарде на поздних сроках аутоиммунного миокардита для понимания механизмов перехода миокардита в ДКМП. Полученные данные в дальнейшем могут быть использованы для создания подходов к персонализированной терапии миокардита и диагностики ДКМП с учетом фазы заболевания.


