Молекулярно-генетическая оценка риска детерминированности повышенной активности ангиотензинпревращающего ферментапри геморрагической лихорадке с почечным синдромом
Автор: Байгильдина Асия Ахметовна, Исламгулов Денис Владимирович, Камилов Феликс Хусаинович, Хабелова Тамара Александровна, Минниахметов Илдар Рамилевич
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Биохимия
Статья в выпуске: 1 т.6, 2010 года.
Бесплатный доступ
Цель работы - изучение активности ангиотензинпревращающего фермента (АПФ) в сыворотке крови и поли¬морфизма гена рецептора ангиотензина II (AT II) 1 типа при геморрагической лихорадке с почечным синдромом (ГЛПС) как возможного предиктора заболевания. Обследованы 409 больных в возрасте от 15 до 65 лет. Актив¬ность АПФ определялась кинетически с использованием набора фирмы ВьМггапп (Швейцария). Геномная ДНК из периферической крови выделялась методом фенол-хлороформной экстракции, генотипирование локусов изучаемой ДНК проводилась методом ПЦР синтеза ДНК. Статистически незначимое снижение активности АПФ наблюдается только в лихорадочный период среднетяжелой и тяжелой формы без осложнений; во все осталь¬ные периоды и при всех формах наблюдается статистически значимая гиперактивность АПФ. При тяжелой форме без осложнений наблюдаются резкие колебания активности АПФ в динамике болезни. При осложненной форме имеет место статистически значимая стабильно высокая активность фермента на всем протяжении бо¬лезни. Анализ полиморфизма гена рецептора АТ II 1 типа свидетельствуют о том, что аллели *А1166 и *С1166, а также, генотипы *А1166 А1166 и *С1166 С1166 не ассоциированы со степенью тяжести течения ГЛПС. По¬вышение активности АПФ при ГЛПС не носит адаптивный характер из-за дефектов в рецепции АТ II и является адекватным метаболическим ответом организма в ответ на внедрение эндотелиотропного вируса
Ангиотензинпревращающий фермент, геморрагическая лихорадка с почечным синдромом, ген рецептора ангиотензина ii 1 типа
Короткий адрес: https://sciup.org/14916998
IDR: 14916998
Molecular-genetic assessment of angiotensin-converting enzyme hyperactivity determinancy risk at hemorrhagic fever with renal syndrome
The research aimed to explore the changes of angiotensin-converting enzyme (ACE) blood activity and polymorphism of the angiotensin II type 1 receptor gene as disease predictor at hemorrhagic fever with renal syndrome (HFRS). In exami¬nation 409 patients at the age of 15-65 years were involved. ACE blood activity with the help of Bbhlmann (Switzerland) ACE kinetic test was determined. Blood genomic DNA by phenol- chloroformic extraction was isolated, genetic locuses by polymerase chain reaction of DNA synthesis were researched. It was shown that the ACE blood activity at HFRS is risen and these changes the significanter the severer form of disease. Nonsignificant rising of enzyme activity only in feveric period of both ungravic and gravic forms was observed. In gravic form significant changes of ACE activity are observed, in complicated form - stable high enzyme activity during all disease took place. Analysis of angiotensin II type 1 receptor gene polymorphism shown that alleles *A1166 and *C1166, genotypes *A1166 A1166 and *C1166 C1166 are not associated with HFRS severity. Made conclusion that high ACE activity is not adaptive reaction due to defect in angiotensin II binding and it is an adequate metabolic response of an organism to endotheliotropic virus action
Текст научной статьи Молекулярно-генетическая оценка риска детерминированности повышенной активности ангиотензинпревращающего ферментапри геморрагической лихорадке с почечным синдромом
Методы. В исследование включили 409 больных с серологически подтвержденным методом непрямых флюоресцирующих антител диагнозом ГЛПС (346 мужчин и 63 женщин) в возрасте от 15 до 65 лет (средний возраст 33,6±3,5 лет), находившихся на стационарном лечении в МУ «Инфекционная клиническая больница № 4» г. Уфы и в отделении гемодиализа Республиканской клинической больницы им. Г.Г. Куватова в 2003-2008 годах. Критериями исключения из групп исследования были наличие в анамнезе гипертонической болезни, болезней сердца и сосудов, сахарного диабета, ревматизма, злокачественных заболеваний, заболеваний печени и почек. При определении степени тяжести ГЛПС использовали классификацию Б.З. Сиротина [9]. Среднетяжелая форма выявлена у 252 больных (61,6%), тяжелая без осложнений – у 109 больных (26,7%), тяжелая с осложненным течением – у 48 больного (11,7%). Группу контроля составили 52 практически здоровых лица, сопоставимых по полу и возрасту.
Для определения активности АПФ взятие крови объемом 5 мл производили путем венепункции локтевой вены утром натощак. Собранную в специальные пробирки без антикоагулянтов кровь выдерживали 2 часа при температуре 18°С, после чего центрифугировали при температуре 4°С и 1000g и собирали сыворотку. Образцы сыворотки крови для анализа хранили при температуре -20°С не более 6 месяцев. Активность АПФ в сыворотке крови определяли кинетическим ме тодом с использованием набора фирмы «Вьhlmann»
450097 г. Республика Башкортостан, г. Уфа, бульвар Х. Давлетшиной, д.18., кв. 101.
Тел. 89173484738;
(Швейцария). Абсорбцию света регистрировали с помощью ИФА-ридера «Вench mark» компании «Вio-Rad». Для генетического исследования пробы венозной крови брали в пробирки типа вакутейнера с ЭДТА. ДНК выделяли из периферической крови методом фенольно-хлороформной экстракции [ 10 ] . Анализ полиморфизма A1166С гена AGTR1 проводили методом полимеразной цепной реакции синтеза ДНК с последующим ферментативным гидролизом с использованием эндонуклеазы рестрикции BstDEI « Сибэнзим». Результаты амплификации оценивали с помощью электрофореза в 2% агарозном геле с последующим окрашиванием бромидом этидия и визуализацией в проходящем ультрафиолетовом свете. В результате амплификации участка гена AGTR1 , содержащего нуклеотидную замену А1166С, получали ампликон длиной 225 п.о. Ампликон, содержащий аллель * С1166 , несет сайт узнавания фермента рестрикции BstDEI , и, расщепляясь, образует продукты размером 110 и 115 п.о., в то время как фрагмент ДНК, содержащий аллель * А1166 , остается нерасщепленным. Наличие фрагмента длиной 225 п.о. после обработки BstDEI соответствует генотипу * А1166 /* А1166 , двух фрагментов (110 и 115 п.о.) – генотипу * С1166 /* С1166 и трех (110, 115 и 225 п.о.) – гетерозиготному генотипу * А1166 /* С1166 .
Обработку результатов исследования проводили с использованием стандартного статистического пакета программ Statistica 7.0 for Windows и SPSS 13. Результаты исследования активности АПФ оценивали методами непараметрической статистики: определяли медиану (Ме), интерквартильный интервал [25% и 75%], достоверность межгрупповых различий средних величин оценивали при помощи критерия Манна-Уитни. Результаты исследования представляли как Ме [Ԛ1; Ԛ3]. При сравнении частот генотипов, аллелей в группах больных ГЛПС с различной степенью тяжести заболевания использовали критерий2 (хи-квадрат) Пирсона. Для всех видов анализа различия принимали за значимые при р<0,05.
Результаты. Определение активности АПФ в сыворотке крови больных ГЛПС показало, что она в равной степени зависит и от периода заболевания, и от степени его тяжести (табл. 1). Лихорадочный период заболевания при среднетяжелой форме характеризуется статистически незначимой тенденцией к снижению активности АПФ, в остальные периоды данной формы наблюдается статистически значимый рост активности фермента с пиком в период полиурии – в 3,1 раза выше значений для контроля (рис. 1). Аналогичная тенденция к изменению изучаемого показателя имеет место и при тяжелой форме болезни без осложнений. Однако, несмотря на динамику, сходную со среднетяжелой формой, активность фермента в полиурический период и в период восстановленного диуреза неосложненной формы ГЛПС достигает более высоких значений (в 3,5 раз выше контрольных значений) вплоть до статистически значимых различий в последний период не только с группой контроля, но и между данными группами больных при восстановлении диуреза. Осложненная форма ГЛПС имеет отличную от остальных форм болезни динамику изменения активности АПФ: гиперактивность энзима без значительных колебаний от периода к периоду регистрируется в течение всей болезни также с максимумом в полиурический период – в 3,3 раза выше контрольных значений – и со статистически незначимой тенденцией к снижению в период восстановленного диуреза. При присоединении осложнений статистически значимыми становятся не только раз- личия с контролем, но различия со среднетяжелой и неосложненной формами болезни. Нормализации изучаемого показателя к периоду восстановленного диуреза при всех формах тяжести ГЛПС на фоне базисной терапии не происходит.
Тип полиморфизма, последовательность праймеров и номенклатура аллелей анализируемых полиморфных локусов гена ген рецептора (тип 1) ангиотензина II ( AGTR1 ) представлены в таблице 2. Результаты оценки распределения частот аллелей и генотипов полиморфного локуса А1166С гена AGTR1 у больных ГЛПС в зависимости от степени тяжести заболевания представлены в таблице 3. Во всех изученных выборках распределение частот генотипов соответствовало распределению Харди-Вайнберга. Сравнительный анализ распределения частот генотипов полиморфного локуса A1166C гена AGTR1 не выявил статистически значимые различия между группами больных с различной степенью тяжести
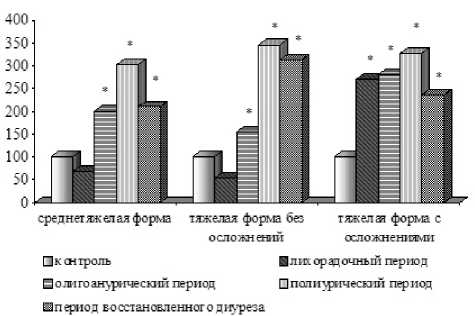
Рис. 1. Активность АПФ в сыворотке крови больных ГЛПС в зависимости от тяжести заболевания (% к контролю); * – статистическая значимость различий с контролем
Таблица 1
Активность АПФ в сыворотке крови больных ГЛПС различной степени тяжести на фоне базисной лекарственной терапии (мкмоль/л х мин)
|
Период заболевания |
Форма заболевания |
||
|
среднетяжелая |
тяжелая без осложнений |
тяжелая с осложнениями |
|
|
лихорадочный |
12,4 [8,8; 18,2] р>0,07 |
9,7 [1,1; 14,1] р>0,06; р1>0,9 |
49,0 [42,4; 50,3] р<0,002; р2<0,006; р3<0,006 |
|
олиго- |
36,2 [28,2;54,7] |
28,2 [21,2; 47,7] |
50,8 [45,9; 63,5] |
|
анурический |
р<0,006 |
р<0,019; р1>0,38 |
р<0,003; р2<0,03; р3<0,009 |
|
полиурический |
55,0 [35,3; 71,5] р<0,0006 |
60,9 [50,6; 77,6] р<0,0002; р1>0,2 |
59,2 [45,9; 70,6] р<0,0001; р2>0,4; р3>0,5 |
|
восстановленного диуреза контроль 18,05 [15,0; 21,5] |
38,0 [34,4; 45,9] р<0,0001 |
56,5 [44,1; 59,0] р<0,0004; р1<0,02 |
49,4 [42,4; 58,3] р<0,0001; р2<0,03; р3>0,14 |
Примечание: р – значимость различий с группой контроля; р1 – значимость различий между среднетяжелой формой и тяжелой формой без осложнений; р2 –значимость различий между среднетяжелой формой и тяжелой формой с осложнениями; р3 – значимость различий между тяжелой формой без осложнений и тяжелой формой с осложнениями.
Тип полиморфизма, последовательность праймеров и номенклатура аллелей анализируемых полиморфных локусов
Таблица 2
|
ген [OMIM], локализация |
полиморфизм (аллели) |
праймеры (фермент рестрикции) |
|
АGTR1 [106165] 3q21-q25 |
А1166С *А1166 - 225 п.о. *С1166 - (110 п.о.+115 п.о.) |
5' GСАССАTGTTTTGАGGTTGА 3' 5' TGTGGСTTTGСTTTGTСTTG 3' (ВstDEI ) |
Таблица 3
Распределение частот генотипов и аллелей полиморфного локуса A1166С генома AGTR1 у больных ГЛПС различной степени тяжести заболевания
|
форма заболевания |
генотипы |
аллели |
||||
|
*А/*А |
*А/*С |
*С/*С |
*А |
*С |
||
|
n |
84 |
65 |
6 |
233 |
77 |
|
|
среднетяжелая |
pi±Sp, СI% |
54,19±4,00 |
41,94±3,96 |
3,87±1,55 |
75,16±2,45 |
24,84±2,45 |
|
тяжелая без |
n |
54 |
30 |
6 |
138 |
42 |
|
осложнений |
pi±Sp, СI% |
60,00±5,16 |
33,33±4,97 |
6,67±2,63 |
76,67±3,15 |
23,33±3,15 |
|
тяжелая с |
n |
32 |
12 |
3 |
76 |
18 |
|
осложнениями |
pi±Sp, СI% |
68,09±6,80 |
25,53±6,36 |
6,38±3,57 |
80,85±4,06 |
19,15±4,06 |
Примечание: n – абсолютное число генотипов (аллелей); pi – частота; Sp – ошибка pi.;2 – хи квадрат; p – уровень значимости; df – число степеней свободы.
ГЛПС (p>0,05). Выявлено равнозначное распределение частот генотипа *C1166 / *C1166 в группах больных со средней и тяжелой формой UKGС (54% и 60% соответственно). Гетерозиготный генотип *A1166 / *C1166 встречался почти на 10% больше у больных с средней тяжестью (42%) по сравнению с тяжелой формой ГЛПС (33%). У больных более тяжелой формой ГЛПС отмечено почти в 2 раза увеличение частоты генотипа *C1166 / *C1166 (6,7%) по сравнению со средней степенью тяжести заболевания (3,9%) (рис. 2).
Обсуждение. Основная часть АПФ синтезируется в эндотелии сосудов и в норме. Около 90% фермента фиксирована на эндотелиальной мембране и только около 10% его активности приходится на плазму крови. Основным эффектором АПФ является АТ II, действие которого реализуется через специфические ангиотензиновые рецепторы. Наибольшее значение имеет рецептор АТ II 1 типа, через стимуляцию которого реализуется большинство как физиологических, так и патофизиологических эффектов данного пептида: вазоконстрикция, увеличение минутного объема сердца, стимуляция секреции альдостерона и подавление вазопрессина, повышение уровня ингибитора тканевого активатора плазминогена, стимуляция выработки цитокинов с инициацией воспалительного процесса в сосудистой стенке, стимуляция генерации активных форм кислорода и др. [11, 12]. При ГЛПС, вызываемом эндотелиотропным вирусом, имеет место как гиперактивация эндотелия, так и его повреждение [13, 14], что ведет, с одной стороны, к усиленной экспрессии ее клетками АПФ, а с другой – к протеолитическому отщеплению молекул фермента от поврежденных эндотелиоцитов и, как следствие, – к повышению пула плазменного АПФ. Нельзя исключить также усиленную экспрессию АПФ по принципу обратной связи вследствие отсутствия его прессорного эффекта в результате нарушения рецепции продукта катализируемой им реакции – АТ II. Нами выявлены значительные сдвиги в активности данного фермента зависимости от тяжести ГЛПС и наличия осложнений: среднетяжелая форма характеризуется наименее выраженной по сравнению с остальными формами болезни активностью фермента и отсутствием его «скачков» в динамике, при тяжелой форме заболевания без осложнений имеет место выраженный подъем активности к периоду развития полиурии, а при наличии осложнений гиперактивность АПФ наблюдается на всем протяжении заболевания со с статистически значимыми межгрупповыми различиями. Однако изучение полиморфизма гена рецептора АТ II 1 типа показало, что аллели *А1166 и *С1166, а также генотипы *А1166/*А1166, *А1166/*С1166 и *С1166/*С1166 не ассоциированы с со степенью тяжести течения ГЛПС, что позволяет сделать вывод о том, что высокая активность АПФ при ГЛПС, которая тем выраженнее, чем тяжелее течение болезни, не обусловлена нарушенной рецепцией АТ II из-за отсутствия васкулярного эффекта и может быть расценена как вполне адекватная реакция макроорганизма в ответ на метаболические изменения, первоначально обусловленные действием хантавируса – возбудителя ГЛПС.
Заключение .
-
1. У больных ГЛПС выявлено статистически значимое повышение в крови активности АПФ, зависящее от периода и степени тяжести заболевания.
-
2. Сравнительный анализ распределения частот генотипов полиморфного локуса A1166C гена ангиотензина II AGTR1 не выявил статистически значимые
-
3. Повышение активности АПФ при ГЛПС, особенно выраженное при тяжелой форме, не носит адаптивный характер из-за дефектов в рецепции АТ II при ГЛПС и является адекватным метаболическим ответом организма в ответ на внедрение эндотелио-тропного вируса.
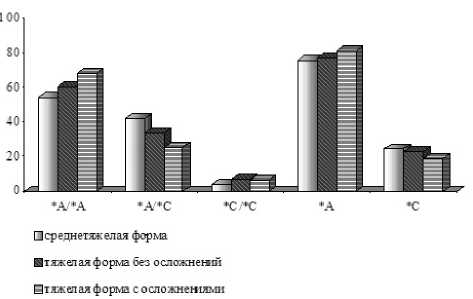
Рис. 2. Распределение частот генотипов и аллелей полиморфного локуса А1166С генома АGTR1 у больных ГЛПС в зависимости от тяжести заболевания (%)
различия между группами больных с различной степенью тяжести ГЛПС.
Список литературы Молекулярно-генетическая оценка риска детерминированности повышенной активности ангиотензинпревращающего ферментапри геморрагической лихорадке с почечным синдромом
- Behavioural and structural factors in health: an empirical analysis/K. Stronks, H. Van de Mheen, Loomon et al.//Sociology of health and illness. -1996. -№ 18. -P. 653-674.
- Assiciation between angiotensin II type 1 receptors gene and human essential hypertension/H. Fan, S. Li, W. Gu et al.//Chung Hua I Hsueh I ChuanHsuen Tsa Chi. -1998. -Vol. 1015. -№ 2. -P. 101-103.
- Association between renin-angiotensin system gene polymorphism and essential hypertension: a community-based study/X. Jiang, H. Sheng, J. Li et al.//J Hum Hypertens. -2009. -№ 3. -P. 176-181.
- Angiotensin II type 1 receptor gene polymorphism predicts development of hypertension and metabolic syndrome/P. Palatini, G. Ceolotto, F. Dorigatti et al.//Am J Hypertens. -2009. -№ 2. -P. 208-214.
- Synergistic effects on angiotensin-converting enzyme and angiotensin II receptor gene polymorphism on risk of myocardial infarction/A. Bonnardeaux, L. Tiret, O. Poirier et al.//Lancet. -1994. -Vol. 344. -№ 3. -P. 910-913.
- Synergistic effects of angiotensin converting enzyme and angiotensin II type 1 receptor gene polymorphisms on ischemic events/P.P. van Geel, Y.M. Pinto, A.H. Zwinderman et al.//XX Congress of the European society of Cardiology. -Abstract. -P. 386.
- Полиморфизм генов ренин-ангиотензиновой системы и дисфункция эндотелия у мужчин, перенесших инфаркт миокарда в молодом возрасте/О.А. Беркович, Е.А. Баженова, Н.В. Вахрамеева и др.//Артериальная гипертензия. -2008. -Т. 14. -№ 3. -C. 239-244.
- Mutations in genes in the renin-angiotensin system are associated with autosomal recessive renal tubular dysgenesis/O. Gribouval, M. Gonzales, Neuhaus et al.//Nature Genet. -2005. -№ 37. -P. 964-968.
- Сиротин, Б.З. Геморрагическая лихорадка с почечным синдромом. Монография/Б.З. Сиротин. -Хабаровск. -1994. -300 с.
- Маниатис, Т. Методы генетической инженерии. Молекулярное клонирование/Т. Маниатис, Э. Фрич, Дж. Сембрук. -М.: Мир, 1984. -352 с.
- Дроздова, Г.А. Клеточные механизмы артериальной гипертензии/Г.А. Дроздова//Патологическая физиология. -2000. -№ 2. -C. 26-31.
- Galle, J. Angiotensin II and oxidized LDL: an unholy alliance creating oxidative stress/J. Galle, K. Heermeier//Nephrol Dial Transplant. -1999. -№ 14. -P. 2585-2589.
- Камилов, Ф.Х. Состояние целостности эндотелия сосудов при ГЛПС/Ф.Х. Камилов, А.А. Байгильдина, В.Ш. Вагапова //Морфология. -2008. -№ 4. -C. 72.
- Камилов, Ф.Х. Экспрессия VCAM-1 как отражение активации эндотелия при ГЛПС/Ф.Х. Камилов, А.А. Байгильдина//Морфология. -2008. -№ 2. -C. 57.


