Молекулярно-генетические изменения тканей яичек пациентов с COVID-19
Автор: Демяшкин Григорий Александрович, Болдырев Дмитрий Владимирович, Щекин Владимир Иванович, Жиганова Марианна Сергеевна
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 2 т.30, 2022 года.
Бесплатный доступ
Несмотря на определенный прогресс в изучении влияния инфекции COVID-19 на человеческий организм, многие вопросы, связанные с возникающими патологическими процессами после перенесения заболевания, а также с развитием так называемого «постковидного» синдрома, остаются не разрешенными. Одним из таких вопросов является влияние SARS-CoV-2 на мужскую фертильность. Результаты проведенных ранее в данном направлении исследований противоречивы, в связи с чем на данный момент нет чётких доказательств непосредственного поражения мужских гонад коронавирусом. Таким образом, гипотеза о потенциальной таргетности яичек для SARS-CoV-2 нуждается в подтверждении. Цель исследования: оценка молекулярно-генетического профиля образцов препаратов тканей яичек у пациентов с COVID-19. Образцы тканей яичек пациентов с подтвержденным COVID-19 (n=96, возраст 25-91 год) были изучены методом полимеразной цепной реакции в режиме реального времени для определения экспрессии вирусной РНК SARS-CoV-2 и генов, кодирующих белковые комплексы АПФ-2 и фурина. Критериями исключения были: эпидемический паротит, бесплодие, сепсис, бактериальная инфекция, носительство ВИЧ, вирусов гепатита В и С, Эпштейна-Барра. Контрольную группу наблюдений (n=20) составили архивные парафиновые блоки аутопсийного материала нормальных яичек, полученные не позднее 6 часов после констатации биологической смерти, без макроскопических признаков наличия воспалительного и/или опухолевого процесса, все пациенты этой подгруппы были фертильны и ранее не подвергались воздействию токсинов или лекарственных препаратов. В результате исследования у пациентов, пораженных COVID-19, было зафиксировано наличие генетического материала коронавируса в яичках. Кроме того, в ткани яичек выявлена повышенная экспрессия АПФ-2 и фурина, что определяет благоприятные условия для поражения SARS-CoV-2. Таким образом, по результатам ПЦР-тестирования препаратов яичковых тканей на наличие РНК вируса SARS-CoV-2, оценки экспрессии АПФ-2 и фурина, можно с большой вероятностью утверждать о потенциальной таргетности мужских половых клеток, клеток Сертоли и Лейдига для него.
Яички, sars-cov-2, апф-2, фурин, фертильность
Короткий адрес: https://sciup.org/143178904
IDR: 143178904 | DOI: 10.20340/mv-mn.2022.30(2).573
Molecular genetic changes in the testis tissues of COVID-19 patients
Despite some progress in studying the impact of COVID-19 infection on the human body, many issues related to emerging pathological processes after the transfer of the disease, as well as the development of the so-called «post-COVID» syndrome, remain unresolved. One such issue is the impact of SARS-CoV-2 on male fertility. The results of previous studies in this direction are contradictory, and therefore at the moment there is no clear evidence of direct damage to male gonads by coronavirus. Thus, the hypothesis of potential testicular targeting for SARS-CoV-2 needs to be confirmed. The aim of the study was to assess the molecular genetic profile of samples of testicular tissue preparations from patients with COVID-19. Testicular tissue samples from patients with confirmed COVID-19 (n=96, age 25-91 years) were studied by real-time polymerase chain reaction to determine the expression of SARS-CoV-2 viral RNA and genes encoding protein complexes of ACE- 2 and Furin. The exclusion criteria were: mumps, infertility, sepsis, bacterial infection, carriage of HIV, hepatitis B and C, Epstein-Barr. The control of observations (n=20) consisted of archival paraffin blocks of autopsy material of normal testicles, obtained no later than 6 hours after the declaration of biological death, without macroscopic signs of the presence of an inflammatory and / or tumor process, all patients of this subgroup were fertile and had not previously been exposed to toxins or drugs. As a result of the study, in patients affected by COVID-19, the presence of the genetic material of the coronavirus in the testicles was recorded. In addition, an increased expression of ACE-2 and Furin was found in the testicular tissue, which determines favorable conditions for SARS-CoV-2 damage. Thus, based on the results of PCR testing of testicular tissue preparations for the presence of SARS-CoV-2 virus RNA, assessment of the expression of ACE-2 and Furin, it is possible to assert with a high probability the potential targeting him on male germ cells, Sertoli and Leydig cells.
Текст научной статьи Молекулярно-генетические изменения тканей яичек пациентов с COVID-19
Демяшкин Г.А., Болдырев Д.В., Щекин В.И., Жиганова М.С. Молекулярно-генетические изменения тканей яичек пациентов с COVID-19. Морфологические ведомости. 2021;30(2):573 (2).573
Demyashkin GA, Boldyrev DV, Shchekin VI, Zhiganova MS. Molecular genetic changes in the testis tissues of Covid-19 patients. Morfologicheskie Vedomosti – Morphological newsletter. 2022;30(2):573 (2).573
Введение. Появление, а затем и чрезвычайно быстрый темп распространения новой коронавирусной инфекции COVID-19, вызванной вирусом SARS-CoV-2, привели к более 120 миллионам случаев инфицирования и около 2 500 000 смертей по всему миру [1]. Проникновение вируса SARS-CoV-2 в клетки происходит посредством специфического взаимодействия вируса с ангиотензин-превращающим ферментом 2 (далее - АПФ-2) и сериновой протеазой – фурином [2]. Обладая троп-ностью к этим белкам, локализующимся на мембранах различных клеток, SARS-CoV-2 может приводить к поражению многих органов, таких как почки, сердце, кишки, легкие и другие, поэтому COVID-19 можно рассматривать как системное заболевание [1]. При этом вопрос о поражении органов мужской репродуктивной системы, и в первую очередь процессов сперматогенеза, остается открытым.
Согласно проведенному ПЦР-анализу (далее – полимеразной цепной реакции – ПЦР) SARS-CoV-2 был обнаружен в тканях яичка, при иммуногистохимическом исследовании выявили увеличение концентрации рецепторов AПФ-2 в сперматогониях, клетках Лейдига и Сертоли [2-8]. Однако проведенные секвенирования генома (далее - scRNA-seq) мужских половых клеток и их микроокружения с целью обнаружения SARS-CoV-2 демонстрировали спорные результаты, в большинстве случаев следов вируса как в яичках, так и сперме не было обнаружено [9-11]. Тем не менее, авторы других работ утверждают обратное [12]. Учитывая минимальное количество информации о возможном повреждающем действии SARS-CoV-2 на мужские гонады, а также очевидный интерес к проблеме мужской фертильности в условиях широкого распространения заболевания COVID-19, проведение научных работ в данном направлении является остро актуальным.
Цель исследования: оценка молекулярно-генетического профиля образцов препаратов тканей яичек у пациентов с COVID-19.
Материалы и методы исследования. Дизайн эксперимента состоял в следующем. На основании анамнестических, клинических и морфологических данных были сформированы группы, каждая из которых включала подгруппы согласно возрастной периодизации ВОЗ (табл. 1). I группа наблюдения (n=96) в возрасте от 25 до 91 года, (в среднем 59 лет) – аутопсий-ный материал яичек пациентов, умерших с установленным клиническим и патологоанатомическим диагнозом коронавирусная инфекция (COVID-19, ПЦР+). Критерии исключения: эпидемический паротит, бесплодие, сепсис, бактериальная инфекция, носительство ВИЧ, вирусов гепатита В и С, Эпштейна-Барра. Группа наблюдения II (n=20) – архивные парафиновые блоки (2015–2016 гг.) аутопсийного материала нормальных яичек, полученных не позднее 6 часов после констатации биологической смерти, без макроскопических признаков наличия воспалительного и/или опухолевого процесса, все пациенты этой подгруппы имели по крайней мере одного генетически собственного ребенка и ранее не подвергались воздействию токсических веществ.
Таблица 1
Распределение наблюдений по группам, согласно возрастной периодизации ВОЗ (2014)
|
возраст|age |
подгруппа|subgroup |
n |
возраст|age |
подгруппа|subgroup |
N |
|
25–44 (молодой|young) |
I – COVID-19 |
9 |
61–75 (пожилой|old) |
I – COVID-19 |
43 |
|
II – контроль | control |
5 |
II – контроль | control |
5 |
||
|
45–60 (средний|mature) |
I – COVID-19 |
17 |
76–90 (старческий|senile); >90 (долгожители| centenarians) |
I – COVID-19 |
27 |
|
II – контроль | control |
5 |
II – контроль | control |
5 |
Количественные данные, полученные в ходе ПЦР в режиме реального времени (далее ПЦР-РВ), были проанализированы с использованием рангового дисперсионного анализа ANOVA.
Результаты исследования и обсуждение. При морфологическом исследовании яичек во всех образцах обнаружили признаки вирусного орхита (рис. 1). В большинстве извитых семенных канальцах наблюдали частые отслоения мужских половых клеток от базальной мембраны, которая была утолщена и разрыхлена. Перитубулярное пространство – отечное, с умеренной воспалительной инфильтрацией (плазмоциты, тучные клетки, лимфоциты, единичные нейтрофилы и эозинофилы). Кроме того, отмечали обильные внутрисосудистые тромбозы и слущение эндотелио-цитов, снижение количества половых клеток; утолщение и отек интерстициальной ткани, миграцию плазмоцитов, микротромбы в просвете кровеносных сосудов мелкого калибра.
Во всех изученных образцах (n=96) в ткани яичка при ПЦР-РВ обнаружен SARS-CoV-2, в то время как в ткани придатка (n=96) она была отрицательная. При ПЦР-РВ анализе экспрессии АПФ-2 и фу-рина в тканях яичка и придатка яичка (n=96) показали приблизительно схожие паттерны экспрессии, нормализованные по GAPDH (глицеральдегид-3-фосфат дегидрогеназе, табл. 3). В ткани яичка у пациентов с COVID-19 отмечали увеличение экспрессии АПФ-2 по сравнению с контролем почти в 7 раз – 8,46±0,85 против 1,23±0,02 (p<0,01, соответственно). В SARS-CoV-2-позитивных образцах относительная экспрессия АПФ-2 в тканях яичка была выше в 1,8 раз, чем в тканях придатка яичка (4,74±0,61, p<0,01). При распределении экспрессии АПФ-2 отмечали тенден- цию к ее уменьшению с возрастом в обеих группах (табл. 4).
Экспрессия фурина в тканях яичка у COVID-19-пациентов была выше почти в 3 раза по сравнению с мужчинами контрольной группы – 6,18±0,42 против 2,18±0,68 (p<0,01, соответственно). В тканях яичка экспрессия фурина превалировала в 1,5 раза над значениями в тканях придатка яичка (4,22±0,54, p<0,01), а также не зависела от возраста (табл. 5).
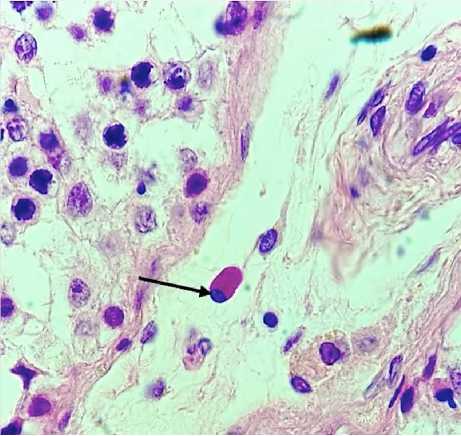
Рис. 1. Микроскопическая картина яичка (случай К., 58 лет). Обозначения: стрелка – миграция плазмоцита. Окр.: гематоксилином и эозином. Ув.: х 1000.
Настоящее исследование посвящено изучению SARS-CoV-2 вирусной нагрузки в яичках и придатках яичек у пациентов с подтвержденным диагнозом COVID-19 в разных возрастных группах с использованием ПЦР-РВ. При ПЦР-РВ
SARS-CoV-2 был обнаружен во всех изучаемых образцах (n=96) тканей яичка, что частично согласуется с результатами других исследований и свидетельствует о по-
Таблица 2
Используемые праймеры для SARS-CoV-2, АПФ-2 и фурина
|
гены | genes |
5´-праймер | 5´-primer |
3´-праймер | 3´-primer |
|
SARS-CoV-2 |
WuhanCoV-spk2-f 5'-TTTCCTCGTGAAGGTGTCTTTGT-3 ' |
|
|
WuhanCoV -spk2-r 5'-TGTGGTTCATAAAAATTCCTTTGTG-3 ' |
||
|
WuhanCoV-spk2-hex-p5'-HEX-TCAAATGGCACACACTGGTTTGT-BHQ1 |
||
|
АПФ-2 | ACE-2 |
ACCTCACTATTTGAAAGCACTTGGT |
GCTTGCTTGAGCAGGAAGTTTATTT |
|
фурин | Furin |
CCACATGACTACTCTGCTGATGG |
CGAAGTGAACTTGGTCAGCGT |
Таблица 3
|
гены | genes |
яичко | testis |
придаток яичка | epididymis |
p |
||
|
I – COVID-19 |
II – контроль | control |
I – COVID- 19 |
II – контроль | control |
||
|
АПФ-2|ACE-2 |
8,46±0,85 |
1,23±0,02 |
4,74±0,61 |
1,28±0,42 |
p<0,01 |
|
фурин | Furin |
6,18±0,42 |
2,18±0,68 |
4,22±0,54 |
2,56±0,82 |
p<0,01 |
Таблица 4
Распределение экспрессии АПФ-2 при ПЦР-РВ по возрастам в условных единицах
|
возраст | age |
подгруппа | subgroup |
АПФ-2 | ACE-2 |
возраст | age |
подгруппа | subgroup |
АПФ-2 | ACE-2 |
|
25–44 years (молодой | young) |
I – COVID-19 |
8,54±0,12 * |
61–75 years (пожилой | old) |
I – COVID-19 |
8,49±0,21 * |
|
II – контроль | control |
2,79±0,11 |
II – контроль | control |
0,85±0,14 |
||
|
45–60 years (средний | mature) |
I – COVID-19 |
8,51±0,14 * |
76–90 years (старческий | senile); > 90 (долгожители | centenarians) |
I – COVID-19 |
8,39±0,33 * |
|
II – контроль | control |
1,34±0,21 |
II – контроль | control |
0,52±0,22 |
Примечание: * - достоверность различий с показателями контроля p<0,01
Таблица 5
Распределение экспрессии фурина при ПЦР-РВ по возрастам в условных единицах
|
возраст | age |
подгруппа | subgroup |
фурин | Furin |
возраст | age |
подгруппа | subgroup |
фурин | Furin |
|
25–44 years (молодой | young) |
I – COVID-19 |
5,43±0,11 * |
61–75 years (пожилой | old) |
I – COVID-19 |
6,23±0,11 * |
|
II – контроль | control |
4,17±0,12 |
II – контроль | control |
4,21±0,12 |
||
|
45–60 years (средний | middle) |
I – COVID-19 |
5,52±0,12 * |
76–90 years (старческий| senile); > 90 (долгожители| Centenarians) |
I – COVID-19 |
5,69±0,13 * |
|
II – контроль | control |
4,18±0,11 |
II – контроль | control |
4,22±0,13 |
Примечание: * - достоверность различий с показателями контроля p<0,01
Результаты ПЦР-РВ на АПФ-2 и фурин в условных единицах
тенциальной уязвимости мужской половой железы к этому антигену. Однако, вероятность проникновения вируса через гематотестикулярный барьер можно рассматривать лишь гипотетически.
В литературе описаны случаи, подтверждающие способность некоторых вирусов приводить к развитию спермато-генной недостаточности в результате прямого воздействия на мужские половые клетки, сопровождающиеся местными воспалительными реакциями. Например, при паротите, вирусных инфекциях Эбола, Зика и SARS-CoV. Однако, SARS-CoV-2 не был найден в адлюминальном ком-партменте извитых семенных канальцев. Проводя аналогию между полученными данными по вирусам паротита, Эбола, Зика, результатами настоящего и ранее про- веденных исследований, можно высказать предположение о возможности SARS-CoV-2 проникать через гематотестикулярный барьер и поражать мужские половые клетки [12-13, 7].
Другой механизм, который также не исключается в случае COVID-19 - цито-киновое воздействие. При эпидемическом паротите увеличивается продукция цитокинов в основном TNF-α, IL-6 и нарушается функционирование гематотестикуляр-ного барьера, что снижает количество контактных белков клеток Сертоли, в первую очередь ZO-1 белка приводя к де-компартментализации семенных канальцев (клетки Сертоли являются таргетными для вируса) [14]. Вирус Зика, также снижает проницаемость гематотестикулярного барьера, что приводит к поражению кле- ток Сертоли и ухудшению барьерных свойств мужских гамет [15]. При инфицировании вирусом Эбола в гематотестику-лярном барьере и микроокружении наблюдается повышение активности иммунокомпетентных клеток [13]. При этом ПЦР-РВ на указанные инфекции в тканях яичек демонстрировали присутствие вирусной РНК [15-19].
SARS-CoV-2 не был выявлен в придатках яичек. Этот факт свидетельствует о способности вируса инфицировать только клетки, характерные для паренхимы мужских гонад, а именно – половые клетки, клетки Сертоли и Лейдига, и позволяет исключить поражение стромального компонента, представленного рыхлой волокнистой соединительной тканью в обоих органах. Учитывая, что придаток яичка является резервуаром для дозревания сперматозоидов, то полученный отрицательный результат на SARS-CoV-2 позволяет считать потенциально таргетными для SARS-CoV-2 мужские половые клетки, не достигшие фазы формирования.
Возбудитель COVID-19 преимущественно поражает органы дыхательной и мочевыделительной систем, желудочнокишечного тракта, сердце [20-22], тенденция к инфицированию которых может быть обоснована значительной экспрессией АПФ-2 и фурина в аппарате Гольджи, за счет которых вирус способен проникать в клетки. SARS-CoV-2 содержит внеклеточный, трансмембранный и внутриклеточный домены. Первый образован субъединицей, которая связывается с мембранным рецептором АПФ-2 через рецептор-связывающий домен, вторая субъединица способствует образованию комплекса «вирус-рецептор» [2]. Нами наблюдалось значительное увеличение экспрессии генов, кодирующих молекулярные компоненты АПФ-2 и фурина, что свидетельствует о потенциальной таргетности тканей яичек к проникновению в них и воздействию SARS-CoV-2. В то же время, выявленное снижение экспрессии АПФ-2 с возрастом можно связать с физиологическими процессами старения яичка. АПФ-2 оказывает регулирующее действие на 5-гидрокситриптаминовый 3A (HTR3A) и холинергический Nicotinic Alpha 1 (CHRNA1) рецепторы. HTR3A опосредованно влияет на апоптоз через продукцию TNF-α, увеличивая секрецию серотонина. CHRNA1 в очаге воспаления взаимодействует с лейкоцитами. Можно предположить, что увеличение экспрессии АПФ-2 при воспалительной реакции в яичках, вызванной SARS‐ CoV‐2 приведет к дисфункции сперматогенеза и в целом к тестикулярной недостаточности.
Анализируя паттерн экспрессии фурина в ткани яичка, мы наблюдали повышенное содержание этой протеазы, что возможно свидетельствует об увеличении вирусной нагрузки, так как он расщепляет последовательность S-белка SARS-CoV-2, способствуя внутриклеточной инвазии. Принимая во внимание данные по секвенированию scRNA-seq из публичных карт «The Human Protein Atlas», согласно которым в норме АПФ-2 и фурин на 65–80% экспрессируются в мужских половых клетках, то с высокой долей вероятности можно утверждать, что они являются клетками-мишенями для SARS-CoV-2. Это предположение было отчасти подтверждено в одном из последних исследований, в котором при помощи секвенирования технологией Single-cell transcriptome scRNA-seq на основании протоколов «Gene Expression Omnibus» и «Sequence Read Archive» была выявлена высокая экспрессия АПФ-2 в сперматогониях, клетках Лейдига и Сертоли [7].
Подводя итоги исследования с абсолютной уверенностью можно утверждать об уязвимости тканей мужских половых желез к вирусной инфекции SARS-CoV-2, что следует из результатов ПЦР-РВ. Принимая во внимание собственные результаты и ранее полученные данные других исследователей, нами предлагаются некоторые гипотезы о таргетности отдельных тканевых структур яичек для этой инфекции, в первую очередь мужских гамет, однако данный вопрос остается по-прежнему окончательно не решенным и требует дальнейшего изучения.
Заключение. Таким образом по результатам полимеразной цепной реакции в режиме реального времени на РНК ви- руса SARS-CoV-2, оценки экспрессии АПФ-2 и фурина, можно с большой вероятностью утверждать о присутствии вируса в тканях яичка, а также о его потенциальной таргетности к мужским половым клеткам, клеткам Сертоли и Лейдига.
Список литературы Молекулярно-генетические изменения тканей яичек пациентов с COVID-19
- Kogan EA, Berezovsky YuS, Protsenko DD i dr. Patologicheskaya anatomiya infectsii vyzvannoy SARS-CoV-2. Sudebnaya Meditsina. 2020;6(2):8–30. In Russian. DOI: 10.19048/2411-8729-2020-6-2-8-30
- Hoffmann M, Kleine-Weber H, Schroeder S. SARS-CoV-2 cell entry depends on ACE2 and TMPRSS2 and is blocked by a clinically proven protease inhibitor. Cell. 2020;181:271–280
- Douglas GC, O'Bryan MK, Hedger MP et al. The novel angiotensin-converting enzyme (ACE) homolog, ACE2, is selectively expressed by adult Leydig cells of the testis. Endocrinology. 2004 Oct;145(10):4703-4711
- Fan C, Li K, Ding Y, Lu LW, Wang J. ACE2 expression in kidney and testis may cause kidney and testis damage after 2019-nCoV infection. MedRxiv. 2020. DOI: 10.1101/2020.02.12.20022418
- Li MY, Li L, Zhang Y, Wang XS. Expression of the SARS-CoV-2 cell receptor gene ACE2 in a wide variety of human tissues. Infect Dis Pov-erty. 2020;9(1):45. DOI: 10.1186/s40249-020-00662-x
- Verma S, Saksena S, Sadri-Ardekani H. ACE2 Receptor Expression in Testes: Implications in COVID-19 Pathogenesis. Biol Reprod. 2020; ioaa080. DOI: 10.1093/biolre/ioaa080
- Wang Z, Xu X. scRNA-seq profiling of human testes reveals the presence of the ACE2 receptor, a target for SARS-CoV-2 infection in spermato-gonia, Leydig and Sertoli cells. Cells. 2020;9:920
- Yang M, Chen S, Huang B, et al. Pathological Findings in the Testes of COVID-19 Patients: Clinical Implications. Eur Urol Focus. 2020;S2405-4569(20):30144-30149. DOI: 10.1016/j.euf.2020.05.009
- Pan F, Xiao X, Guo J et al. No evidence of SARS-CoV-2 in semen of males recovering from COVID-19. Fertil Steril. In press. DOI: 10.1016/j.fertnstert.2020.04.024
- Song C, Wang Y, Li W, Hu B, Chen G, Xia P, Wang W, Li C, Diao F, Hu Z, Yang X, Yao B et al. Absence of 2019 novel coronavirus in se-men and testes of COVID-19 patients. Biol Reprod. 2020. DOI: 10.1093/biolre/ioaa050
- Younis JS, Abassi Z, Skorecki K. Is there an impact of the COVID-19 pandemic on male fertility? The ACE2 connection. Am J Physiol Endo-crinol Metab. 2020;318(6):E878-E880. DOI: 10.1152/ajpendo.00183.2020
- Li D, Jin M, Bao P, Zhao W, & Zhang S. Clinical characteristics and results of semen tests among men with coronavirus disease 2019. JAMA Network Open. 2020;3(5):e208292. DOI: 10.1001/jamanetworkopen.2020.8292
- Schindell BG, Webb AL, Kindrachuk J. Persistence and Sexual Transmission of Filoviruses. Viruses. 2018;10(12):683. DOI: 10.3390/v10120683
- Wu H, Jiang X, Gao Y et al. Mumps virus infection disrupts blood-testis barrier through the induction of TNF-α in Sertoli cells. FASEB J. 2019;33(11):12528-12540. DOI: 10.1096/fj.201901089R
- Siemann DN, Strange, DP, Maharaj PN et al. Zika Virus Infects Human Sertoli Cells and Modulates the Integrity of the In Vitro Blood-Testis Barrier Model. Journal of Virology. 2017;91(22). DOI: 10.1128/jvi.00623-17
- Deen GF, Broutet N, Xu W et al. Ebola RNA Persistence in Semen of Ebola Virus Disease Survivors - Final Report. N Engl J Med. 2017; 377(15):1428-1437. DOI: 10.1056/NEJMoa1511410
- Gorchakov R, Berry RM, Patel SM et al. Optimizing PCR Detection of Zika Virus from Various Body Fluids. Am J Trop Med Hyg. 2019; 100(2):427-433. DOI: 10.4269/ajtmh.18-0755
- Govero J, Esakky P, Scheaffer SM et al. Zika virus infection damages the testes in mice. Nature. 2016; 540(7633):438-442. DOI:10.1038/nature20556
- Matusali G, Houzet L, Satie AP et al. Zika virus infects human testicular tissue and germ cells. J Clin Invest. 2018;128(10):4697-4710. DOI: 10.1172/JCI121735
- Clarke NE, Turner AJ. Angiotensin-converting enzyme 2: the first decade. Int J Hypertens 2012: 3073(15). DOI: 10.1155/2012/307315
- Donoghue M, Hsieh F, Baronas E et al. A novel angiotensin‐converting enzyme‐related carboxypeptidase (ACE2) converts angiotensin I to angiotensin 1‐9. Circ Res. 2000; 87:E1‐E9.
- Warner FJ, Lew RA, Smith AI et al. Angiotensin-converting enzyme 2 (ACE2), but not ACE, is preferentially localized to the apical surface of polarized kidney cells. J Biol Chem. 2005;280:39353–39362. DOI: 10.1074/jbc.M508914200


