Молекулярно-генетический анализ сортообразцов озимой пшеницы, выращенных в различных экологических зонах Украины
Автор: Моргун Богдан Владимирович, Степаненко Антон Игоревич, Чугункова Татьяна Владимировна
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Экология
Статья в выпуске: 3-4 т.15, 2013 года.
Бесплатный доступ
Представлены результаты исследования селекционных образцов озимой мягкой пшеницы, выращенных в лесостепной и степной зонах Украины, на наличие аллеля Glu-В1al, который определяет высокие хлебопекарные качества муки. Показано, что использование полимеразной цепной реакции для выявления инсерции в 43 п.н. в регионе MAR позволяет дифференцировать селекционные образцы по аллелям высокомолекулярных глютенинов.
Пшеница, экология, аллель glu-в1al, пцр
Короткий адрес: https://sciup.org/148202003
IDR: 148202003 | УДК: 633.11
Molecular genetic analysis of winter wheat cultivars grown in different ecological zones of ukraine
The results of the study of selection samples of winter wheat, grown in the forest-steppe and steppe zones of Ukraine, on the presence of allele Glu-B1al defining high baking quality of flour are presented. It is shown that the employment of the polymerase chain reaction for detection of the insertion of 43 bp in the MAR region allows differentiation of samples by high-molecular-weight glutenin locus of wheat.
Текст научной статьи Молекулярно-генетический анализ сортообразцов озимой пшеницы, выращенных в различных экологических зонах Украины
Проблема качества зерна является одной из важнейших при создании новых сортов озимой мягкой пшеницы. При этом экологическая составляющая выращивания растений и, в целом, климатические особенности определенных регионов оказывают существенное влияние на качество и количество растительной продукции. Наряду с экологическими аспектами природопользования, которые должны учитываться в растениеводстве, особого внимания заслуживает и генетическая составляющая сортов, во многом определяющая пищевую ценность пшеничной муки [1]. Существует достаточно большое количество генетических систем, QGpc-локусов, контролирующих качество зерна пшеницы [2, 3]. Среди них важное место по эффективности занимают QTL и генные структуры, определяющие состав высокомолекулярных субъединиц глютенинов (HMW-GS).
В настоящее время продолжается идентификация локусов, ответственных за HMW-GS у пшеницы [4, 5]. Гены, которые контролируют высокомолекулярные глютенины, находятся в проксимальных участках на длинном плече хромосом 1А, 1В, 1D пшеницы и характеризуются множественным аллелизмом [6].
Классификация мирового генофонда по аллельным вариантам высокомолекулярных глютенинов позволила охарактеризовать частоту распространения отдельных субъединиц, составляющих аллельные варианты локусов Glu-A1, Glu-B1, Glu-D1 среди 1060 сортообразцов озимой мягкой пшеницы разных стран мира.
В Украине у изученных образцов преобладал вариант Glu-В1 7+9 (частота встречаемости 65,8%), в то время как к первой категории субъединиц, которые имеют генотипически обусловленное позитивное влияние на технологические и биохимические свойства зерна, необходимо отнести 1В 7+8,
частота которой среди украинских сортов составляла примерно 21,8% [7, 8]. При ПЦР-анализе 28 сортов пшеницы из 11 стран мира также была зафиксирована большая частота субъединиц глютенина 7+9, чем высокоэффективных HMW-GS 7+8 [5]. Это свидетельствует об определенной уникальности субъединиц глютенина, которые определяют высокое качество теста.
В последние годы особое внимание исследователей, работающих в области экологических аспектов селекции, а также генетических проблем качества зерна пшеницы, привлечено к изучению аллеля Glu-B1 al , который обеспечивает наилучшие показатели хлебопекарного качества муки. Было показано, что ‘ x’ –тип гена локуса Glu-B1 al кодирует субъединицу 1Bx7OE, обусловливает её сверх экспрессию и является одним из наиболее сильных по позитивному влиянию на качество муки пшеницы среди идентифицированных Gli/Glu аллелей в мировой коллекции. Впервые он был выявлен у сорта мексиканской пшеницы Ред Ривер 68, который характеризуется высокими показателями качества муки, и по молекулярному строению представляет собой тандемную дупликацию ДНК, кодирующую биосинтез субъединицы 1Bx7 глютенина [9]. В настоящее время показано, что среди сортов озимой мягкой пшеницы, занесенных в Государственный реестр сортов растений, пригодных для распространения в Украине, 6 сортов являются носителями аллеля Glu-B1 al [10].
Все генотипы, которые несут аллель Glu-B1 al , могут быть идентифицированы биохимическими методами, а также с помощью молекулярногенетических методов по наличию инсерции в 43 п.н. в регионе MAR (matrix-attachment region) и дупликации в 18 п.н. в кодирующей области гена. Хотя, как было показано [11], последняя не является абсолютно специфичной, поскольку она была выявлена в первичной структуре ДНК других аллелей ( Glu-B1 ak , Glu-B1 b ), среди растений сорта Chinese Spring, изолятов тетраплоидной пшеницы и других материалов.
В Институте физиологии растений и генетики Национальной академии наук Украины проводится большая работа по созданию высокопродуктивных, сверхсильных по качеству сортов озимой мягкой пшеницы [12] и использование молекулярногенетических технологий является важной составляющей в генетико-селекционных программах. В данной работе представлены результаты идентификации аллеля Glu-B1 al в сортообразцах озимой пшеницы, выращенных в различных экологических зонах Украины.
МАТЕРИАЛ И МЕТОДЫ
Материалом исследований служили семена сор-тообразцов (398 номеров) озимой мягкой пшеницы, выращенные в зонах Лесостепи и Степи Украины, а также сортообразец пшеницы двуручки Древлянка и сорт Панна селекции Одесского селекционногенетического института Украинской академии аграрных наук, используемые в качестве положительного контроля при постановке полимеразной цепной реакции.
Суммарную ДНК выделяли из шрота, используя СТАВ-буфер, который обеспечивал качественный перевод ДНК в раствор с минимальными потерями. Очистка от белковой фракции достигалась двукратной экстракцией смесью хлороформ: изоамиловый спирт (24:1) с дальнейшим забором водной фазы. ДНК осаждали СТАВ-раствором 1ч. Освобождения от фракции РНК достигали путем добавления к раствору 50 мкг RNase A, инкубированием при 37°С /15мин, экстракцией смесью хлороформа и изоамилового спирта и, в итоге, осаждением высокомолекулярных нуклеиновых кислот изопропанолом. Осадок растительной ДНК промывали 70% этанолом, подсушивали и растворяли в ТЕ буфере pH 8,0, который обеспечивал оптимальные условия хранения очищенного препарата.
В качестве внутреннего контроля для ПЦР использовали праймеры к гену актина act (Gen Bank: AB181991.1). Для реакции брали 30 нг очищенной общей ДНК. Режим амплификации: первичная денатурация – 94°С/3мин и 35 циклов в режиме 94°С/30с; 57°С/30с; 72°С/39с; конечная элонгация 72°С/10мин. Продукты амплификации разделяли методом электрофореза в 1,2% агарозном геле с добавлением бромистого этидия и документировали на рабочей станции Gel-Doc (BioRad).
Для мультплексной ПЦР с целью выявления ин-серции в 43 п.н. в регионе MAR использовали праймеры MAR-F 5'-CCTCA GCATG CAAAC ATGCA GC-3' и MAR-R 5'-CTGAA ACCTT TGGCC AGTCA TGTC-3' [11] и праймеры к референтному гену пшеницы TaTM20 [13], размер ожидаемого ампликона 563 п.н и 934 п.н. Для реакции брали 30 нг ДНК. Режим амплификации: денатура- ция – 94°С/3мин и 40 циклов в режиме 94°С/30с; 61°С/30с; 72°С/1мин; конечная элонгация – 72°С/5мин. Продукты амплификации визуализировали после их электрофоретического разделения в 1,6% агарозном геле в ультрафиолетовом свете с использованием бромистого этидия как красителя.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Одним из первых этапов молекулярногенетического анализа ДНК является подтверждение наличия высокомолекулярных фракций во всех изучаемых образцах. Эти исследования были проведены и таким образом подтверждена возможность использования выделенного генетического материала для дальнейшей работы. Последующее определение качества ДНК с использованием праймеров к гену актина ( act ) показало, что все исследуемые образцы содержат ампликон длиной 507 п.н. (рис. 1) и выделенная ДНК из растений пшеницы достаточного качества для проведения основной полимеразной цепной реакции.
Результаты молекулярного скрининга образцов на наличие инсерции, характерной для аллеля al локуса Glu-B1 , выращенных в лесостепной (рис. 2а), либо степной (рис. 2б) зонах Украины, свидетельствовали об отсутствии у них различий.
Известно, что климатические особенности региона, экологические условия выращивания пшеницы оказывают влияние на показатели качества зерна. Однако наличие у определенных образцов генетически обусловленного локуса высокого качества зерна (Glu-B1 а1) позволило нам идентифицировать его независимо от зоны выращивания пшеницы. Представленная на рис. 2 часть общих результатов молекулярно-генетического анализа свидетельствует о том, что ампликон 563 п.н. присутствует практически у всех сортообразцов, включая сорт Панна, который относится к сильным пшеницам. Этот сорт пшеницы является носителем ин-серции в 43 п.н. в регионе MAR и, соответственно, гена Вх7OE [10]. Исключение составлял образец № 102, который по данным проведенного ПЦР-анализа содержит ампликон 520 п.н., выявляющий ген Вх7 [11].
Типичные результаты ПЦР-анализа на наличие локуса Glu-B1 а1 в проанализированном нами селекционном материале, полученном путем простых межсортовых, трёхлинейных, беккросных скрещиваний представлены на рис. 3. Они свидетельствуют о дифференциации селекционного материала по изучаемому гену. Присутствие в сортообразцах обоих ампликонов (520 та 563 п.н.) может быть индикатором их гетерогенности [11].
1 2 3 4 5 6 7 8 9 10 11 12
507 п.н.


500 п.н.
Рис. 1 . Электрофореграмма продуктов амплификации гена act в образцах пшеницы: 1 – 41923; 2 – 289; 3 – 103; 4 – 102; 5, 6 – негативный контроль, ДНК ячменя сорта Вакула; 7-9 - негативный контроль, ДНК рапса; 10, 11 – негативный контроль – ТЕ буфер; 12 – маркер молекулярного веса Gene Ruler™ DNA Ladder Mix (Thermo Scientific)
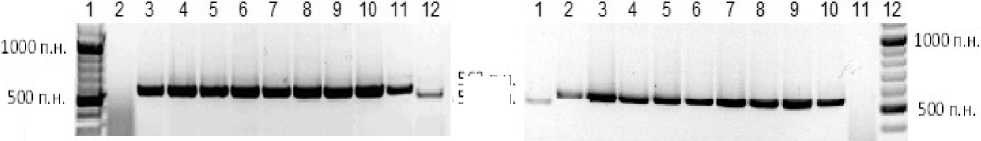
б
а
563 П.Н,
520 пл.
Рис. 2. Результаты идентификации аллеля Glu-B1al : а) 1 – маркер Gene Ruler™ DNA Ladder Mix; 2 – негативный контроль – ТЕ буфер; 3 – позитивный контроль – Панна; 4 – 107; 5 – 106; 6 –105; 7 – 104; 8 – 101; 9 – 4192; 10 – 289; 11 – 103; 12 – 102; б) 1 – 102; 2 – 103; 3 – 289;. 4 – 4192; 5 – 101; 6 – 104; 7 – 105; 8 – 106; 9 – 107; 10 – позитивный контроль – Панна; 11 – негативный контроль – ТЕ буфер; 12 – маркер молекулярного веса Gene Ruler™ DNA Ladder Mix
1 2 3 4 5 б 7 8 9 10 11 12 13 14 15 16 17 18
934 п.н.
563 п.н.
520 п.н.
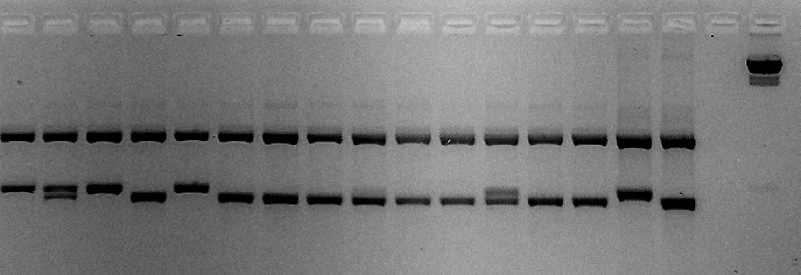
564 ц.н.
Рис. 3 . Результаты идентификации аллеля Glu-B1al : 1, 3, 5 - селекционные образцы, позитивные по аллелю Glu-B1al ; 4, 6-11, 13, 14 - селекционные образцы, негативные по аллелю Glu-B1al ; 2, 12 - селекционные образцы гетерозиготные по аллелю Glu-B1al ; 15 - позитивный контроль, Панна; 16 - негативный контроль, Древлянка; 17 - негативный контроль – ТЕ буфер; 18 –маркер молекулярного веса Lambda DNA/HindIII
В целом, анализ 398 селекционных образцов на наличие инсерции в 43 п.н. в регионе MAR свидетельствует о том, что 158 образцов (40%) являются позитивными по аллелю Glu-B1al, 196 образцов (49%) – негативными и 44 (11%) – гетерозиготными по идентифицируемому гену.
Следует отметить, что проблема повышения качества пшеничной муки приобретает определенную остроту, особенно в связи с увеличением Украиной экспорта зерна. В этой связи становится актуальным и необходимым использование в селекционных программах исходного материала с генетически обусловленными аллелями высокого качества зерна. Проведенный нами молекулярно- генетический анализ на наличие в селекционном материале озимой пшеницы аллеля Glu-B1а1 высокомолекулярных глютенинов свидетельствует о том, что выбранные методы исследования являются эффективными. Основываясь на результатах массового анализа по идентификации инсерции в 43 п.н. в регионе MAR, возможно дифференцировать вновь созданные с помощью различных методов гибридизации образцы и отбирать для дальнейшей работы генотипы, несущие ген Вх7 OE HMW-GS.
Список литературы Молекулярно-генетический анализ сортообразцов озимой пшеницы, выращенных в различных экологических зонах Украины
- Рибалка О.I., Моргун Б.В., Починок В.М. Сучаснi дослiдження якостi зерна пшеницi у свiтi: генетика, бiотехнологiя та харчова цiннiсть запасних бiлкiв//Физиология и биохимия культурных растений. 2012. Т. 44. № 1. С. 3-22.
- Крупнов В.А., Крупнова О.В. Генетическая архитектура содержания белка в зерне пшеницы//Генетика. 2012. Т. 48. № 2. С. 149-159.
- Чеботарь С.В., Благодарова Е.М., Куракина Е.А., Семенюк И.В., Полищук А.М., Козуб Н.А., Созинов И.А., Хохлов А.Н., Рыбалка А.И., Сиволап Ю.М. Генетический полиморфизм локусов, определяющих хлебопекарное качество украинских сортов пшеницы//Вавиловский журнал генетики и селекции. 2012. Т. 16. № 1. С. 87-98.
- Ravel C., Praud S., Murigneux A., Linossier L. et al. Identification of Glu-B1-1 as a candidate gene for the quantity of high-molecular-weight glutenin in bread wheat (Triticum aestivum L.) by means of an association study//Theor. Appl. Genet. 2006. V. 112. N 4. P. 738-743.
- Obreht D., Kobiljski B., Djan M., Vapa L. Identification of Glu-В1 alleles in bread wheat cultivars using PCR//Genetica. 2007. V. 39. N 1. P. 23-28.
- Gao X., Appelbee M.J., Mecuria G.T., Chalmers K.J., Mather G.T. A second ‘overexpression’ allele at the Glu-B1 highmolecular-weigth glutenin locus of wheat: sequence characterization and functional effects//Theor. Appl. Genet. 2012. V. 124. P. 333-343.
- Панченко I.А., Усова З.В., Рябчун В.К., Леонов О.Ю. Класифiкацiя свiтового генофонду озимої пшеницi за алельними варiантами високомолекулярних глютенiнiв//Селекцiя i насiнництво. 2009. Вип. 79. С. 169-180.
- Усова З.В., Панченко I.А. Рiвень показникiв якостi зерна пшеницi озимої м’якої як результат взаємодiї субодиниць високомолекулярних глютенiнiв//Селекцiя i насiнництво. 2010. Вип. 98. С. 153-161.
- Butov B., Ma W., Gale K., Cornish G., Rampling L., Larroque O., Morel M., Bekes F. Molecular discrimination of Bx7 alleles demonstrates that a highly expressed high-molecular-weight glutenin allele has a major impact on wheat flour dough strength//Theor. Appl. Genet. 2003. V. 107. P. 1524-1532.
- Злацька А.В. Iдентифiкацiя алеля Glu-В1al високомолекулярних глютенiнiв та його вплив на ознаки хлiбопекарської якостi у пшениць, придатних до поширення в Українi//Физиология и биохимия культурных растений. 2010. Т. 42. № 4. С. 315-321.
- Butow B.J., Gale K.R., Ikea J., Juhasz A. et al. Dissemination of the highly expressed Bx7 glutenin subunit (Glu-В1al allele) in wheat as revealed by novel PCR markers and RP-HPLC//Theor. Appl. Genet. 2004. V. 109. № 7. P. 1525-1535.
- Моргун В.В. Досягнення Iнституту фiзiологiї рослин i генетики НАН України (до 65-ї рiчницi вiд дня заснування)//Физиология и биохимия культурных растений. 2011. Т. 43. № 3. С. 187-211.
- Kim Y.-Y., Kim D.-Y., Shim D et al. Expression of the Novel Weat Gene TM20 Confers Enhanced Cadmium Tolerance to Bakers’Yeast//J. Biol. Chem. 2008. V. 283. N 23. P. 15893-15902.


