Молекулярно-генетический анализ верховки обыкновенной - Leucaspius delineatus (Heckel, 1843) из водоемов Республики Коми
Автор: Рафиков Р.Р., Шадрин Д.М., Пылина Я.И., Чадин И.Ф., Новоселов А.П.
Журнал: Известия Коми научного центра УрО РАН @izvestia-komisc
Рубрика: Биологические науки
Статья в выпуске: 2 (22), 2015 года.
Бесплатный доступ
Проведено молекулярно-генетическое изучение верховки обыкновенной (Leucaspius delineatus (Heckel, 1843) бассейна р. Печора. Данные секвенирования участка мтДНК, кодирующего COI, свидетельствуют о едином механизме происхождения популяций данного вида на территории Республики Коми. AFLP анализ указывает на наличие генетической дифференциации исследованных образцов северо-восточной части ареала верховки обыкновенной. Коэффициент корреляции (0.5, p-value: 0.001) между матрицами генетических и географических расстояний популяций рыб также свидетельствует об их длительном обитании в бассейне р. Печора.
Верховка обыкновенная (leucaspius delineatus (heckel, бассейн р. печора, секвенирование гена coi мтднк, aflp анализ
Короткий адрес: https://sciup.org/14992749
IDR: 14992749 | УДК: 597.551.2:591.9
Molecular-genetic analysis of sunbleak ( Leucaspius delineatus (Heckel, 1843)) in water bodies of the Komi Republic
Sunbleak - Leucaspius delineatus (Heckel, 1843) is non-commercial fish species with extremely low amount of data in the Komi Republic territory. The new findings of sunbleak in several ponds and streams in the middle course of the Pechora river allowed to expand the area of the species to the northeast. Populations of sunbleak were found in two reservoirs located near the Pechora state district power station: in the reservoir-cooler and in the floodplain lake located 14 km downstream. The reservoir-cooler of the Pechora state district power station was used for commercial fish production from 1987 till 1998. As a result of non-intentional introduction carp and bleak were naturalized in the water basin. It was hypothesized that sunbleak, as well as the specified kinds, can have non-native origin. For this purpose we studied morphological and DNA markers in three sunbleak populations: two populations from the above reservoirs and one population form Nyuvchim water basin (basin of the Vichegda river).The morphological markers (the number of vertebrae, the transverse rows of scales number, the number of lateral line scales) evidence in favor of long period of habitation of sunbleak populations in the Pechora river basin. The analysis of sequences of mitochondrial cytochrome oxidase subunit I gene testifies to the common origin of all three studied sunbleak populations. The analysis of AFLP markers showed genetic differences between three studied populations and the isolation by distance phenomenon was approved. The reservoir-cooler population had the highest polymorphism level.The results obtained in this study do not support the origin of sunbleak in the Pechora river basin as a result of unintentional introduction and are consistent with hypothesis of close connection of the Vichegda and Pechora rivers basins in the past.
Текст научной статьи Молекулярно-генетический анализ верховки обыкновенной - Leucaspius delineatus (Heckel, 1843) из водоемов Республики Коми
Верховка обыкновенная (Leucaspius delinea-tus (Heckel, 1843) относится к непромысловым рыбам семейства карповых и характеризуется невысокими линейно-весовыми параметрами. В ее аре- ал на территории России входят все реки, впадающие с юга в Балтику и некоторые озера бассейна р. Онега. В бассейнах Каспия – Волга, реки Дагестана до Кумы, Черного моря и Азова – Дон, Кубань и реки черноморского побережья [1]. В Республике Коми (РК) верховка до недавнего времени была отмечена лишь в некоторых водоемах рек Вычегда (оз. Синдорское, являющееся остатком большого приледникового водоема, существовавшего в период четвертичных оледенений на европейском Северо-Востоке) [2] и Кама (реки Летка и Кобра) [3]. Из-за её ограниченного распространения Л.С. Берг предположил, что этот вид относительно недавно проник в Северодвинский бассейн по системе каналов, связывающих его с Волго-Камским бассейном. В последующем вид был отмечен в некоторых малых реках (притоках 1 и 2 порядков), а также озерах-старицах верхнего и среднего течения р. Вычегда [4]. Недавние находки верховки в некоторых водоемах и водотоках среднего течения р. Печора позволяют расширить ее ареал на северо-восток (рис. 1) [5].
Известно, что естественным барьером для распространения данного вида рыб на азиатскую часть территории России являются Уральские горы. Однако с развитием сети рыбоводных хозяйств стал возможен инвазийный механизм расселения. В научной литературе есть сведения о непреднамеренной интродукции верховки с последующим ее саморасселением в различных водоемах Сибири [6–10]. На территории Печорской ГРЭС (ПГРЭС), расположенной в среднем течении р.Печора, в 90-х гг. прошлого столетия также действовало тепловодное рыбоводное хозяйство. В результате интродукции в водоеме-охладителе электростанции (водохранилище наливного типа, созданное на базе двух естественных водоемов) образовались локальные самоподдерживающиеся группировки вер-ховки Leucaspius delineatus (Heckel, 1843), уклейки Alburnus alburnus (Linnaeus, 1758) и карпа Cyprinus carpio (Linnaeus, 1758). В то же время более широкая география находок верховки обыкновенной в Печорском районе, а также соответствие ряда счетных признаков (количество позвонков, поперечных рядов чешуй и чешуй в боковой линии) в выборках рыб бассейна р.Печора общей географической закономерности изменения этих показателей, свидетельствуют об ее длительном обитании в изучаемом районе [5].
Исходя из вышеизложенного, цель настоящего исследования – определить степень генетической дифференциации популяций верховки обыкновенной Leucaspius delineatus (Heckel, 1843) из водоемов республики для выявления механизма их заселения. Подобный подход позволяет существенно углубить зоогеографические исследования и расширить представления о путях формирования ихтиофауны бассейнов рек всего европейского Северо-Востока России.
Материал и методы
Для оценки генетической дифференциации популяций верховки был проведен филогенетический анализ с использованием определения последовательности (секвенирования) участка митохондриального гена субъединицы 1 цитохромоксидазы (COI мтДНК) и анализа полиморфизма длин ам-плифицированных фрагментов ДНК (AFLP – Amp- lified Fragment Length Polymorphism). Проанализированы две выборки из среднего течения р. Печора: по 15 образцов мышечной ткани рыб из водоема-охладителя ПГРЭС (географические координаты: N065°06'58.5, E057° 21'13.0) и находящегося на удалении 15 км от озера в пойме р. Печора (географические координаты N065°07'57.6, E057°04'15). Из среднего течения р.Вычегда исследовано шесть образцов, пойманных в водохранилище (географические координаты: N061°23'41.5, E050°45'16.2) у пос. Нювчим, образованном на месте слияния рек Нювчим и Дендель – притоков второго порядка р. Вычегда (рис. 1). Расстояния между популяциями для матрицы географических дистанций были измерены по «дуге большого круга» по географическим координатам.
Тотальная ДНК была выделена с помощью набора FastDNA Spin Kit (QBioGene) согласно инструкциям производителя. Определение нуклеотидной последовательности амплифицированного участка мтДНК выполнено на генетическом анализаторе ABI PRISM 310 (Applied Biosystems) с использованием праймеров Fish F1: 5'-TCAACCAACCACAAA GACATTGGCAC-3' и Fish R2: 5'-TAGACTTCTGGG TGGCCAAAGAATCA-3' [11]. Выравнивание и анализ нуклеотидных последовательностей проводили в пакете программ MEGA 6.0. [12].
В AFLP анализе использовали рестриктазы EcoRI и MseI вместе с последовательностями адаптеров EcoRI и MseI. Смесь для реакции рестрикции-лигирования включала (на 10 реакций): 10 мкл T4 DNA Ligase buffer, 10 мкл NaCl (0,5 М), 5 мкл BSA (1 мг/мл), 10 мкл MseI adaptor, 10 мкл EcoRI adaptor и 10 мкл Enzyme Master Mix (на 10 реакций), состоящий из 1 мкл 10X T4 DNA Ligase buffer, 1 мкл NaCl (0,5 М), 5 мкл рестриктазы EcoRI, 1 мкл рестрикта-зы MseI, 0,5 мкл BSA (1 мг/мл), 0,5 мкл T4 DNA Ligase, 1 мкл воды без нуклеаз. Затем к 5,5 мкл смеси для реакции рестрикции-лигирования добавляли 5,5 мкл раствора ДНК (0,1 мкг/мкл) и инкубировали в течение 3 час при 37 ºС. После этого проводили преселективную амплификацию (преамплификация) с продуктом реакции рестрикции-лигирования, предварительно разбавленным в пять раз буфером ТЕ (20 ммоль TrisHCL, 0,1 ммоль EDTA, pH 8,0). Смесь для преселективной ПЦР включала: 2 мкл разбавленного продукта реакции рестрикции-лигирования, 0.5 мкл AFLP преселексив-ной пары праймеров (Applied Biosystems) и 7.5 мкл AFLP Core Mix (Applied Biosystems). Условия реакции преамплификации: 72ºС – 2 мин, 30 циклов (94 ºС -20 с, 56 ºС – 30 с, 72 ºС – 2 мин) и 60 ºС – 30 мин.
Затем проводили селективную амплификацию с продуктом реакции преамплификации, предварительно разбавленным в пять раз буфером ТЕ. Для реакции селективной амплификации были использованы три комбинации праймеров: EcoRI-AAG (меченый)/MseI-CAA, EcoRI-AGG (меченый) /MseI-CAT и EcoRI-ACG (меченый)/MseI-CTT. Смесь для селективной ПЦР включала: 1.5 мкл разбавленного продукта преселективной амплификации, 0.5 мкл EcoRI флуоресцентно меченого праймера, содержащего на своем конце три селективных нуклеотида (Applied Biosystems), 0.5 мкл MseI прайме-
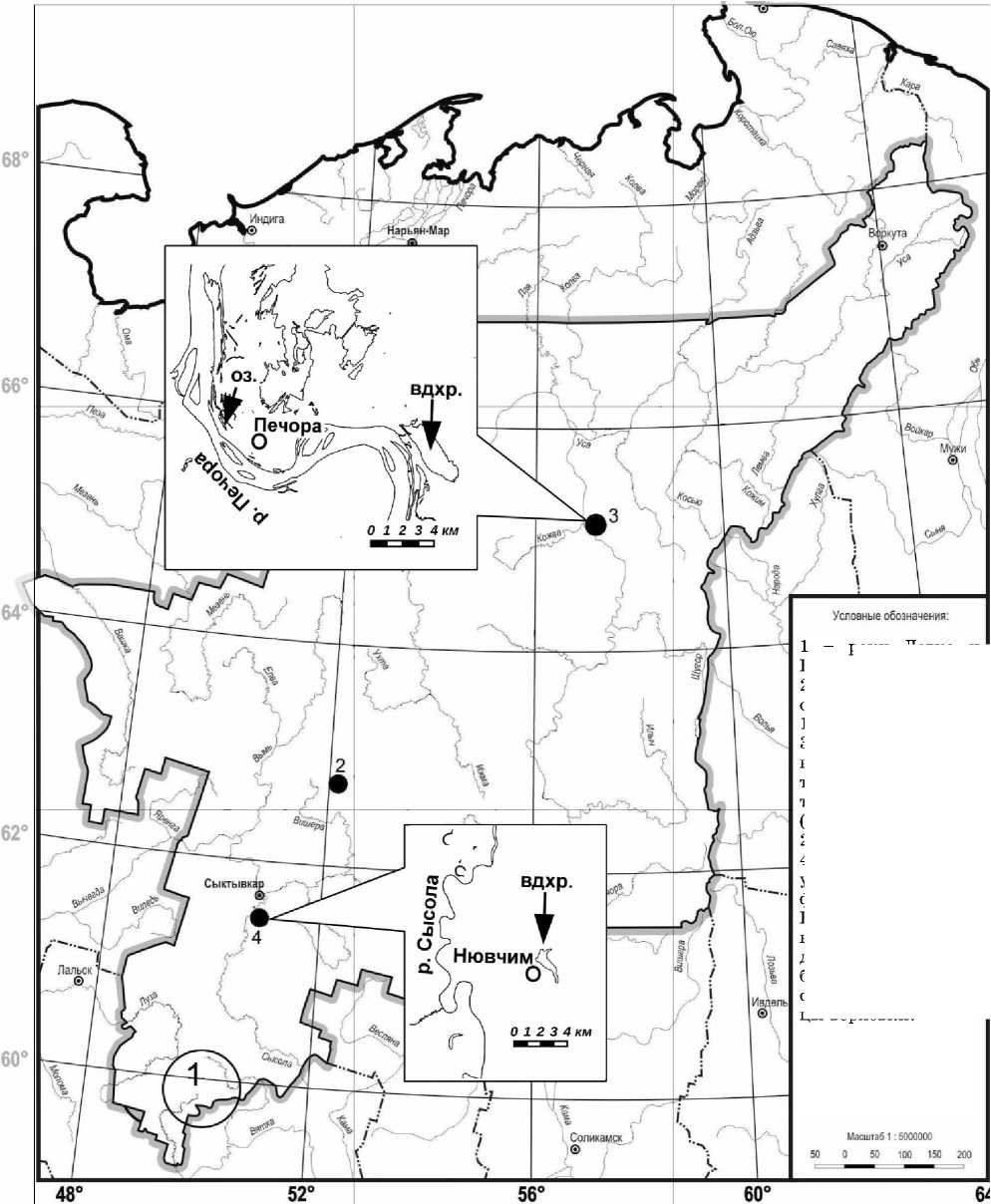
озеро Синдор-
– малые реки и
– водохранилище
– ское (Зверева и др., 1955), водоемы поймы, а также водоем-охладитель Печорской ГРЭС (Бознак, Захаров, 2009),
Рис. 1. Сведения о находках верховки обыкновенной Leucaspius delineatus (Heckel, 1843) в водоемах Республики Коми из опубликованных литературных источников.
реки Летка и Кобра (Берг, 1949),
у пос. Нювчим (Рафиков, 2012).
На выносках стрелками обозначены во доемы, в которых были выловлены исследованные образцы верховки.
ра (Applied Biosystems) и 7.5 мкл AFLP Core Mix (Applied Biosystems). Условия реакции селективной амплификации были следующими: 94 ºС – 2 мин, 10 циклов (94 ºС – 20 с, 66 ºС (-1 ºС/цикл) – 30 с, 72 ºС – 2 мин), 20 (94 ºС – 20 с, 56 ºС – 30 с, 72 ºС – 2 мин) и 60 ºС – 30 мин. Далее проводили денатурацию продукта селективной амплификации с использованием формамида (Applied Biosystems) в течение 5 мин при 95 ºС. Реакционная смесь содержала 9,25 мкл формамида, 0,25 мкл стандарта GeneScan ROX 500 (Applied Biosystems) и 0,5 мкл продукта реакции селективной амплификации. Затем полученные образцы анализировали на генетическом анализаторе ABI PRISM 3500 (Applied Biosystems). Полученные хроматограммы были обработаны с использованием внутреннего стандарта в программе GeneMapper 5.0 (Applied Biosystems) для установления длин полученных фрагментов. Затем фрагменты, различающиеся по длине менее чем на одну пару нуклеотидов (п. н.), были объединены вручную. В анализ включены фрагменты размером от 50 до 500 п. н. Наличие или отсутствие фрагментов кодировалось как «1» или «0», соответственно.
Статистический анализ данных AFLP проводили с использованием иерархической кластеризации методом Уорда на основе матрицы сходства, рассчитанной с использованием коэффициента Жаккарда в программной среде R [13]. В ней проверяли и статистическую значимость гипотезы «Iso-lation by distance» с использованием теста Мантела [14] для оценки корреляции между матрицами генетических и географических дистанций.
Кластеризацию на основе модели, описанной в работе [15], выполняли с помощью программы STRUCTURE v. 2.34 [15]. В качестве исходных данных использована бинарная матрица, содержащая сведения о 318 AFLP локусах 36 образцов верховки обыкновенной. В настройках программы было указано: не использовать данные о географическом происхождении образцов; применить «Admixture model» (модель, допускающую обмен генетической информацией между кластерами); количество итераций – 100 тыс. С такими настройками программа запускалась по 35 раз для каждого априорного значения числа кластеров (K) в диапазоне от 1 до 9. Остальные настройки были указаны в соответствии с рекомендациями авторов программы STRUCTURE для анализа доминантных маркеров [16]. Наиболее вероятное значение K (число генетически однородных кластеров) определяли методом, предложенным в работе [17]. Для численной оценки однородности результатов, полученных при независимых запусках STRUCTURE, использовали программу CLUMPP [18]. Визуализацию результатов расчета проводили с помощью программы DISTRUCT [19]. Молекулярногенетическое исследование образцов верховки выполнено на базе ЦКП «Молекулярная биология» Института биологии Коми НЦ УрО РАН (г. Сыктывкар).
Результаты исследований
В основе популяционных исследований живых организмов с помощью методов молекулярной биологии лежит выявление степени полиморфизма отдельных групп. В пределах ранга вида наиболее информативными являются рестрикционный анализ нуклеотидной последовательности ядерной ДНК и секвенирование отдельных генов мтДНК. Известно, что «не кодирующая» часть ядерного генома, ввиду меньшего селективного ограничения, более изменчива и ее скорость мутирования в два раза выше по сравнению с кодирующей [20]. Это увеличивает уровень выявляемого полиморфизма, а соответственно разрешающую способность метода и воспроизводимость полученных результатов.
Полученные последовательности участка мтДНК, кодирующего ген субъединицы 1 фермента цитохром оксидазы (COI) всех исследуемых образцов, зарегистрированы в базе данных GenBank национального центра биотехнологической информации США (KP 794941 – KP794948) [21]. Анализ указанных последовательностей выявил абсолютную идентичность их нуклеотидного состава (рис. 2). Отсутствие изменчивости данного гена в популяциях верховки обыкновенной из разных речных бассейнов республики, может указывать на быстрое расселение указанного вида. Учитывая высокую степень консервативности ген-кодирующей последовательности, расселение могло происходить несколько тысячелетий назад. По-видимому, в случае непреднамеренной интродукции (инвазийный механизм) с посадочным материалом на рыбоводное хозяйство ПГРЭС наблюдался бы некоторый нуклеотидный полиморфизм гена COI.
KP794947-Vichegda
KP794948-Vichegda
KP794946-Pechora
KP794945-Pechora
KP794944-Pechora
KP794943-Pechora
KP794942-Pechora
KP794941-Pechora
AP009307.1-France: Dombes near Leon
NC020357.1-France: Dombes near Leon
KJ.1-France: Rhone drainage
KJ 128525.1-Sweden
KJ 128524.1-Sweden
HQ961052.1-Czech Republic
HQ961053.1-Czech Republic
KJ553907.1-Turkey: Izmit drainage
I HQ961054.1-Czech Republic
HQ961055.1-Czech Republic
HQ961056.1-Czech Republic
—KJ552433.1-Alburnus alburnus France: Rhone drainage
0.0005
Рис. 2. Филогенетическое древо, построенное методом NJ (объединение ближайших соседей) на основании последовательностей COI мтДНК образцов Leucaspius delineatus (Heckel, 1843) и Alburnus al-burnus (Linnaeus, 1758) в качестве внешней группы.
При выполнении анализа длин квалифицированных фрагментов ДНК верховки три комбинации селективных праймеров позволили выявить 318 AFLP маркеров (локусов) длиной от 50 до 500 п.н. Определенные с помощью программы GenAlEx v. 6.501 популяционные показатели представлены в таблице. На основании анализа всех частот аллелей локусов AFLP 36 проанализированных образцов верховки обыкновенной из трех разноудален-
Результаты AFLP-анализа исследованных образцов, полученные с помощью программы GenAlEx v. 6.501
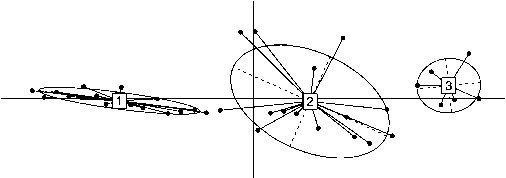
Рис. 4. Визуализация результатов анализа AFLP-маркеров Leucaspius delineatus (Heckel, 1843) из трех водоемов Республики Коми методом главных компонент. 1 – озеро пойменное (р. Печора), 2 – водоем-охладитель Печорской ГРЭС, 3 – водохранилище Нювчимское (р. Нювчим, бассейн р. Сысола).
кладу. Тем не менее, анализ главных компонент, проведенный с бинарными данными AFLP анализа в программной среде R, показал значимую обособленность исследуемых популяций (рис. 4).
Эти результаты были поддержаны анализом с применением методов байесовской статистики. С использованием алгоритма, описанного в работе [17], определили наиболее вероятное число генетических кластеров, равное 3. Это значит, что из проанализированных 36 образцов по данным AFLP анализа было выделено 3 ДНК-группы, обладающих генетическим своеобразием (рис. 5).
Результаты байесовского анализа в программе «STRUCTURE», основанного на составе AFLP-локусов, также свидетельствуют о высокой вероятности разделения исследованных рыб из пой-
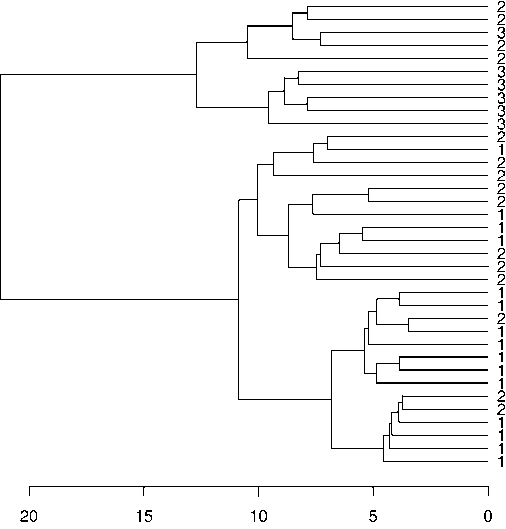
Рис. 3. Дендрограмма сходства образцов Leucaspius delineatus (Heckel, 1843), построенная на основе данных AFLP анализа (матрица сходства рассчитана с использованием эвклидова расстояния, иерархическая кластеризация выполнена с использованием метода Уорда). Происхождение образцов: 1 – озеро пойменное (р. Печора), 2 – водоем-охладитель Печорской ГРЭС, 3 – водохранилище Нювчимское (р. Нювчим, бассейн р. Сысола).
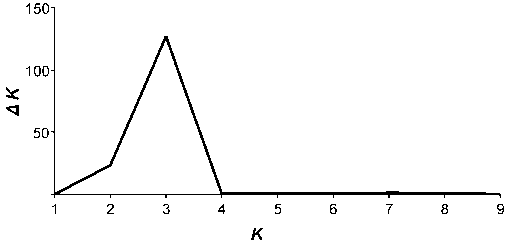
Рис. 5. Результаты байесовского анализа с помощью программы «STRUCTURE v. 2.34» состава AFLP-локусов 36 образцов Leucaspius delineatus (Heckel, 1843) различного географического происхождения. Определение наиболее вероятного числа кластеров (K) по величине Δ K.
менного озера (р. Печора) и Нювчимского водохранилища (рис.6). Часть особей, отобранных из водоема-охладителя ПГРЭС (5 экз.), могут быть классифицированы как «вычегодские», остальные – как «печорские».
Удобной количественной характеристикой при сравнении популяций является величина генетического расстояния между ними. Чаще всего используют стандартное генетическое расстояние Нея [22]. Такое генетическое расстояние между проанализированными группами (Nei Distance) варьировало от 0,04 до 0,118. Дистанция между выборками из Печорского бассейна была наименьшей. Это объясняется незначительным физическим расстоянием и свидетельствует о более близкой связи между данными группировками. Степень иден-
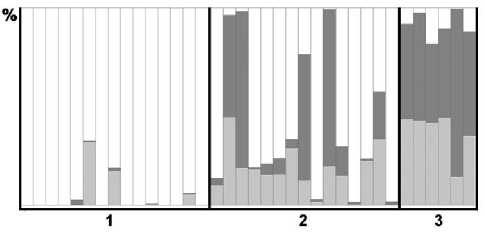
Рис. 6. Результаты байесовского анализа с помощью программы «STRUCTURE v. 2.34» состава AFLP-локусов 36 образцов Leucaspius delineatus (Heckel, 1843) различного географического происхождения. Ось абсцисс - номера выборок и код их географического происхождения (1 – озеро пойменное (р. Печора), 2 – водоем-охладитель Печорской ГРЭС, 3 – водохранилище Нювчимское (р. Нювчим, бассейн р. Сысола). Ось ординат - вероятность (%) кластеризации исследуемых образцов на группы по составу AFLP-локусов. Для подготовки рисунка использована усредненная Q-матрица, полученная с помощью программы «CLUMPP v. 1.1.2».
тичности исследованных популяций из бассейнов рек Печора и Вычегда меньше, чем в пределах Печорского бассейна. Это свидетельствует о длительном отсутствии обмена генетической информацией между популяциями вследствие давней изоляции речных бассейнов.
Обсуждение результатов
Реки северного склона Русской равнины (Печора, Вычегда) на всем своем протяжении располагаются в области покрытия льдами максимального оледенения. На территории европейского Северо-Востока России расселение верховки могло происходить в период отступания льдов максимального оледенения. Участок среднего течения р. Печора в то время был представлен тремя крупными озерами (Троицко-Печорское, Лебяжское и Усинское). По существующим предположениям, до формирования Камо-Печоро-Вычегодских водоразделов часть стока этих озер была направлена в р. Кама (р. Вель – приток р. Печора рассматривается как верховье Пракамы). Верховье р.Печора, развивавшееся изолированно со времен доледниковья, в отдельные периоды также имело сток в Каму по долинам рек Нем, Вычегда и Северная Кельтма [23].
Интересным фактом является область распространения леща в бассейне р. Печора, большая часть которого приурочена к магистральному руслу и водоемам среднего и большей части нижнего течения реки. Лещ и верховка – единственные в р.Пе-чора представители понто-каспийского фаунистического комплекса (теплолюбивые виды рыб, адаптированные к жизни в реках Понто-Каспия). По данным Г.В.Никольского [24], в теплые фазы после-ледниковья представители этого комплекса могли иметь более широкое распространение в бассейне Северного Ледовитого океана, однако вследствие изменения условий численность их значительно сократилась.
В пользу гипотезы о длительном обитании верховки обыкновенной в водоемах бассейна р.Печора также свидетельствует и результат теста Мантела, оценивающего корреляцию между матрицами генетических и географических дистанций (999 повторов; коэффициент корреляции между матрицами – 0,5; p-value: 0,001). Необходимо отметить явную гетерогенность проанализированного материала. Рыбы из пойменного озера характеризуются минимальной величиной полиморфизма, а также статистически значимо отличаются от остальных групп по таким показателям, как ожидаемая гетерозиготность (H e и uH e ), число эффективных аллелей (N e ) и информационный индекс Шеннона (I) (см. таблицу). Данный водоем расположен в пойме р. Печора и большую часть года соединяется с ней протокой, а при весеннем половодье и заливается водами реки. Возможно, его заселение небольшим числом экземпляров верховки произошло относительно недавно. Это и могло бы объяснить низкое генетическое разнообразие данной группировки (эффект основателя). По мнению авторов [25], описывающих процесс инвазийного заселения верховкой некоторых водоемов на территории Англии, основную роль в ряде случаев играли рыбаки-любители. При этом главный предполагаемый механизм – перемещение икры и молоди рыб из водоема в водоем вместе с различным снаряжением (сети, неводы, садки), используемым в процессе рыбной ловли. Необходимо отметить, что нерестовый период у данного вида рыб длится все лето (порционное икрометание) и, как показала практика, в качестве нерестового субстрата могут использоваться сетные и удилищные поплавки, дно лодки и прочие предметы. Кладка икринок имеет вид строчек шириной в 1-2 икринки и приклеена к субстрату достаточно прочно. Существует небольшая вероятность того, что при быстром переезде на другой водоем (во влажных условиях) оплодотворенные икринки действительно могут попасть в воду и продолжить свое развитие.
Основными факторами, влияющими на генетическую структуру популяций, являются генетический дрейф, поток генов и естественный отбор [26]. Для водоема-охладителя ПГРЭС установлен факт интродукции и образования устойчивых группировок уклейки и карпа. Вместе с указанными видами в этот водоем могла попасть и верховка. Однако в случае исключительно инвазийного происхождения данного вида генетическое разнообразие изучаемого материала могло быть очень низким вследствие проявления «эффекта основателя». Возможно, изменение генетической структуры вызвано привнесением дополнительного генетического материала к уже существующей популяции.
Водоем-охладитель Печорской ГРЭС характеризуется непостоянным гидрохимическим и термическим режимами, зависящими от технологических процессов электростанции [27]. Влияние измененного температурного и химического режимов проявляется на различных уровнях организации: от дефектов развития у отдельных особей разных ви- дов рыб до исчезновения типичных видов (щука, плотва, окунь) из структуры рыбной части сообщества в целом [28,29]. Устранение прямого действия отбора (прессинг хищника) при оптимальных (для верховки) температурных параметрах среды также может способствовать изменению генетического разнообразия популяций рыб.
Генетическая выборочность при небольших объемах проанализированного материала в популяционном анализе может в свою очередь повлиять на результаты исследования. Так, например, значительная доля (81 %) молекулярной дисперсии (AMOVA) приходится на внутрипопуляционную генетическую изменчивость проанализированных особей, что свидетельствует о значительной разнородности исследованного генетического материала.
Таким образом, данные секвенирования участка мтДНК, кодирующего субъединицу 1 фермента цитохромоксидазы, свидетельствуют о едином механизме происхождения популяций верховки обыкновенной. Анализ полиморфизма длин амплифи-цированных фрагментов позволяет заключить, что проанализированные выборки генетических проб верховки характеризуются явным генетическим своеобразием. Уровень изменчивости генетических и морфологических признаков данного вида, наблюдаемый при продвижении на северо-восток Республики Коми, по-видимому, отражает процесс его естественного расселения и адаптации к условиям внешней среды. Корреляция между матрицами генетических и географических расстояний также говорит в пользу предложенной нами гипотезы.
Список литературы Молекулярно-генетический анализ верховки обыкновенной - Leucaspius delineatus (Heckel, 1843) из водоемов Республики Коми
- Берг Л.С. Рыбы пресных вод СССР и сопредельных стран. М.-Л.: Изд-во АН СССР, 1949. Т. 2. С. 469-925.
- Зверева О.С., Кучина Е.С., Соловкина Л.Н. Рыбные богатства Коми АССР и пути их освоения. Сыктывкар: Коми книжн. изд-во, 1955. 106 с.
- Атлас пресноводных рыб России: в 2 т. Т. 2/Под ред. Ю.С.Решетникова. М.: Наука, 2002. 253 с.
- Рафиков Р.Р. Формирование рыбного населения искусственных водных объектов Республики Коми//Актуальные проблемы биологии и экологии: Материалы XIX Всероссийской молодежной науч. конференции (Сыктывкар, Республика Коми, Россия, 4-8 апреля 2012 г.). Сыктывкар, 2012. С. 94-96.
- Бознак Э.И., Рафиков Р.Р. О находках уклейки (Alburnus alburnus) и верховки (Leucaspius delineatus) в водоемах бассейна р. Печора//Проблемы изучения и охраны животного мира на Севере: Материалы докладов Всероссийской науч. конференции с международ. участием (Сыктывкар, Республика Коми, Россия, 16-20 ноября 2009 г.). Сыктывкар, 2009. С. 34-35.
- Интересова Е.А. Верховка Leucaspius delineatus (Cyprinidae) в водоемах юга Западной Сибири//Вопросы ихтиологии. 2012. Т. 52. № 3. С. 352-357.
- Корляков К.А., Дубчак К.А. Продукционная и паразитологическая характеристика чужеродных короткоцикловых рыб водоемов восточного склона Южного Урала//Экология. 2010. № 4. С. 312-316.
- Понкратов С.Ф. Инвазии чужеродных видов рыб в бассейн ангарских водохранилищ//Российский журнал биологических инвазий. 2013. № 4.
- Попов П.А. Характеристика ихтиоценозов водохранилищ Сибири//География и природные ресурсы. 2012. № 3. С. 77-84.
- Терещенко В.Г., Терещенко О.В. Трифонова Л.И. Формирование структуры рыбного населения водохранилища при интродукции новых видов рыб с первых лет его существования//Вопросы ихтиологии. 2004. Т. 44. №5. С. 619-631.
- Ward R.D., Zemlak T.S., Innes B.H. еt аl. Barcoding Australia’s fish species//Philosophical Transactions of the Royal Society B 360. 2005. P. 1847-1857.
- Tamura K., Stecher G., Peterson D., Filipski A., Kumar S. MEGA6: Molecular Evolutionary Genetics Analysis version 6.0.//Molecular Biology and Evolution. 2013. № 30. P. 2725-2729.
- R Core Team. R: A language and environment for statistical computing. R Foundation for Statistical Computing. Vienna, Austria, 2014.
- Mantel N. The Detection of Disease Clustering and a Generalized Regression Approach//Cancer Research. 1967. Vol. 27. № 2. P. 209-220.
- Pritchard J. K., Stephens M., Donnelly P. Inference of Population Structure Using Multilocus Genotype Data//Genetics. 2000. Vol. 155. № 2. P. 945-959.
- Pritchard J.K., Wen W., Falush D. Documentation for STRUCTURE software: version 2.3. 2010. 38 p.
- Evanno G., Regnaut S., Goudet J. Detecting the number of clusters of individuals using the software structure: a simulation study//Molecular Ecology. 2005. Vol. 14. № 8. P. 2611-2620.
- Jakobsson M., Rosenberg N.A. CLUMPP: a cluster matching and permutation program for dealing with label switching and multimodality in analysis of population structure//Bioinformatics. 2007. Vol. 23. № 14. P. 1801-1806.
- Rosenberg N.A. DISTRUCT: a program for the graphical display of population structure//Mol. Ecol. Notes. 2003. Vol. 4. № 1. P. 137-138.
- Nei M. Molecular Evolutionary Genetics. New York: Columbia University Press, 1987.
- GenBank Home. Электронный ресурс:(https://www.ncbi.nlm.nih.gov/genbank/).
- Вейр Б. С. Анализ генетических данных. М., 1995. 400 с.
- Зверева О.С. Особенности биологии главных рек Коми АССР. Л.: Наука, 1969. 279 с.
- Никольский Г.В. К истории ихтиофауны бассейна Белого моря//Зоологический журнал. 1943. Т. 22. №. 1. С. 27-32.
- Zieba G., Copp, G.H., Davies, G.D. еt аl. Recent releases and dispersal of non-native fishes in England and Wales, with emphasis on sunbleak Leucaspius delineates//Aquatic Invasions. 2010. № 5. P. 155-161.
- Алтухов Ю. П. Генетические процессы в популяциях. М.: Академкнига, 2003. 431 с.
- Бознак Э.И., Захаров А.Б. Рыбное население индустриального водоема в условиях многофакторного антропогенного воздействия//Современные проблемы водохранилищ и их водосборов: в 2 т. Т.2: Управление водными ресурсами речных водосборов. Водная экология/Труды Междунар. научно-практ. конф. (26 мая -28 мая 2009 г., г.Пермь)/Перм. гос. ун-т. Пермь, 2009. С. 220 -224.
- Рафиков Р. Р. Оценка экологического состояния водоема-охладителя Печорской ГРЭС по данным анализа флуктуирующей асимметрии//Проблемы изучения и охраны животного мира на Севере: Материалы докладов II Всероссийской науч. конференции с международ. участием (Сыктывкар, Республика Коми, Россия, 8-12 апреля 2013 г.). Сыктывкар, 2013. С. 177-179.
- Рафиков Р. Р. Особенности рыбного населения индустриального водоема в бассейне р. Печора//Экологические проблемы северных регионов и пути их решения: Материалы докладов 5-й Всероссийск. науч. конференции с международ. участием (Апатиты, Мурманская область, Россия, 24-27 июня 2014 г.). Апатиты, 2014. С. 212-215.


