Молекулярные детерминанты тройного негативного рака молочной железы
Автор: Буслаев В.Ю., Маниковская Н.С., Минина В.И.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Иммунология
Статья в выпуске: 1, 2026 года.
Бесплатный доступ
Рак молочной железы занимает второе место по распространенности среди онкологических заболеваний. В последнее время отмечается рост случаев заболеваемости и смертности раком молочной железы среди населения России. Наиболее агрессивной формой рака молочной железы является тройной негативный (трижды негативный) тип. Выполняемые исследования сфокусированы на попытках объяснить генетические и иммунологические механизмы его возникновения, прогрессии и устойчивости к терапии. Нами был выполнен систематический анализ современных данных литературы, касающихся различных факторов развития трижды негативного рака молочной железы. Поиск научных публикаций был выполнен в следующих базах данных: PubMed, Scopus, Web of Science, Embase, Cochrane CENTRAL, Google Scholar, e-library. Поиск источников осуществлялся с использованием ключевых слов: рак молочной железы, тройной негативный тип, онкогены, наследственные формы, иммунологические факторы, генетические факторы, генетический полиморфизм. Производился поиск статей на английском и русском языках. В результате в обзор было включено 83 статьи, опубликованных за последние 10 лет, включающих обсуждение различных аспектов генетической предрасположенности к формированию тройного негативного типа рака молочной железы. Сведения о генетической составляющей расширяют возможности для проведения будущих фундаментальных исследований.
Трижды негативный рак молочной железы, молекулярные детерминанты, TP53, PTEN, BRCA1, PIK3CA, EGFR, иммунное микроокружение, PD1, PD-L1, CTLA4, цитокины
Короткий адрес: https://sciup.org/147253589
IDR: 147253589 | УДК: 618.19 | DOI: 10.17072/1994-9952-2026-1-82-101
Molecular determinants of triple-negative breast cancer
Breast cancer is the second most common cancer. Recently, there has been an increase in deaths and morbidity among the population in the Russian Federation. Triple-negative breast cancer (TNBC) is the most aggressive subtype of breast cancer. The current research is focused on elucidating the genetic and immunological mechanisms underlying its development, progression, and therapy resistance. We performed a systematic analysis of current literature data concerning the different factors involved in the pathogenesis of triple-negative breast cancer. A literature search was conducted in the following databases: PubMed, Scopus, Web of Science, Embase, Cochrane CENTRAL, Google Scholar, and e-library. The search utilized keywords such as "breast cancer", "triple-negative type", "oncogenes", "hereditary forms", "immunological factors", "genetic factors", and "genetic polymorphism". The search included articles published in English and Russian. As a result, 83 articles published within the last 10 years, which discuss various aspects of genetic susceptibility to triple-negative breast cancer, were included in this review. The growing body of evidence on the genetic component of TNBC expands opportunities for future fundamental research and the development of targeted therapeutic strategies.
Текст научной статьи Молекулярные детерминанты тройного негативного рака молочной железы
Рак молочной железы (РМЖ) является самым распространенным онкологическим заболеванием среди женщин. По данным медицинской статистики за 2022 г. в мире зарегистрировано 2.3 млн. новых случаев и около 685 тыс. летальных исходов от этого вида рака [Arnold et al., 2022]. Молекулярная классификация РМЖ основана на экспрессии рецепторов эстрогена (ER), прогестерона (PR) и рецептора эпидермального фактора роста 2 типа (HER2). Выделяют: люминальный A-подтип (рецепторный статус: ER+, PR+ , HER2-, Ki-67: низкий уровень (<20%)), люминальный B-подтип (рецепторный статус: ER+, PR± (положительные или слабоположительные), HER2±, Ki-67: высокий уровень (>20%)), HER2-позитивный (рецепторный статус: ER-, PR-, HER2+) и тройной негативный (рецепторный статус: ER-, PR-, HER2-). Среди них наиболее агрессивным течением и неблагоприятным прогнозом характеризуется тройной негативный рак молочной железы (ТНРМЖ), на долю которого приходится 10–15% всех диагнозов.
Актуальность изучения ТНРМЖ обусловлена его высокой агрессивностью, склонностью к раннему рецидивированию, формированием метастазов и ограниченным арсеналом таргетных терапевтических средств ввиду отсутствия классических молекулярных мишеней (ER, PR, HER2) [Zagami, Carey, 2022]. Его биологическая уникальность также заключается в иммунологическом ландшафте [Liu et al., 2018]. По сравнению с другими молекулярными подтипами, ТНРМЖ чаще характеризуется высоким уровнем лимфоцитарной инфильтрации, повышенной экспрессией иммунных чекпойнтов (таких как PD-L1) и наличием провоспалительного цитокинового профиля [Yi et al., 2021]. Эта особенность, с одной стороны, обуславливает повышенную агрессивность и склонность к метастазированию, а с другой – открывает уникальные возможности для иммунотерапевтических вмешательств [Badve et al., 2022]. Ключевой проблемой при этом остается гетерогенность иммунного микроокружения ТНРМЖ, которая определяет вариабельность течения заболевания и ответа на лечение [Liu et al., 2018]. Существует тесная взаимосвязь между генетическими драйверами ТНРМЖ (такими как мутации в TP53, BRCA1 ) и формированием иммуносупрессивного микроокружения [Chen et al., 2018; Liu et al., 2022].
Проблема заключается в том, что, несмотря на значительный объем накопленных данных, целостное понимание сложной взаимосвязи между иммунологическими и генетическими факторами риска остается неполным. Требуется систематизация сведений о вкладе не только высокопенетрантных генов (таких как, например, BRCA1 ), но и умеренно-пенетрантных генетических вариантов, соматических мутаций в онкогенах и генах-супрессорах, а также полиморфизмов генов, контролирующих иммунный ответ и репарацию ДНК. Степень изученности иммунологических аспектов ТНРМЖ характеризуется наличием многочисленных, но зачастую разрозненных исследований, посвященных роли отдельных иммунных факторов: от экспрессии PD-L1 и CTLA-4 до провоспалительных цитокинов (IL-6, IL-8, TNF-α) и состава опухоль-инфильтрирующих лимфоцитов. Однако разрозненность этих данных и использование различных методологических подходов затрудняют формирование единой иммуно-патогенетической модели, пригодной для использования в клинической практике для совершенствования диагностики, оценки прогноза и разработки персонализированных стратегий иммунотерапии.
Цель данного систематического обзора – провести анализ современных научных данных о ключевых молекулярных детерминантах, определяющих возникновение, прогрессирование и терапевтические перспективы ТНРМЖ.
Материал и методы исследования
Настоящий систематический обзор выполнен на основе рекомендаций PRISMA (Preferred Reporting Items for Systematic Reviews and Meta-Analyses). На схеме представлена стратегия поиска научных статей для обзора (см. рисунок). В поиске использовали следующие ключевые слова: рак молочной железы, онкогены, наследственные формы, иммунологические, генетические факторы, генетический полимор- физм; breast cancer, oncogenes, hereditary forms, immunological, genetic factors, genetic polymorphism. В результате первичного поиска на момент августа 2025 г. было обнаружено 1000 статей. Критерии включения: рандомизированные клинические исследования; когорты; исследования случаев и серии случаев, в которых оценивалась генетическая предрасположенность к формированию тройного негативного типа РМЖ; исследования, опубликованные на русском или английском языке за последние 10 лет. Критерии исключения работ: РМЖ других типов; работы, опубликованные ранее 2015 г.; статьи, не прошедшие рецензирование. Большинство представленных работ касались различных аспектов лечения, разработки вакцин и изучения механизмов прогрессии данного типа РМЖ. После удаления дублирую- щихся, нерелевантных и несоответствующих критериям результатов скрининг полных текстов проводился, по меньшей мере, двумя независимыми рецензентами. На каждом этапе любые возможные расхождения разрешались путем обсуждения или достижения консенсуса с третьим экспертом.
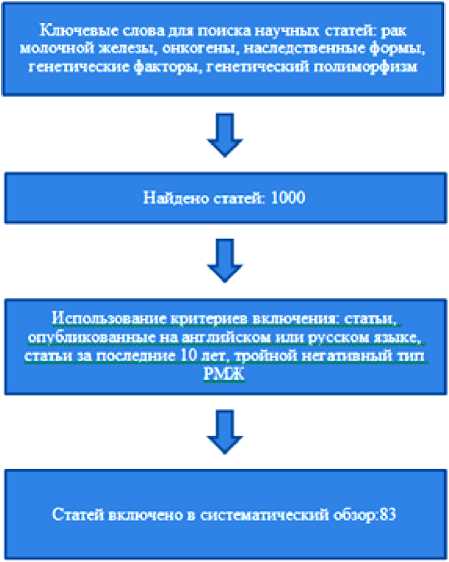
Поиск научных публикаций для систематического обзора
[Literature search for systematic review]
В результате в обзор было включено 83 научные статьи, опубликованных за последние 10 лет (в период с 2015 по 2025 гг.). В результате первичного анализа данных оказалось возможным выделить несколько основных направлений исследований в выбранной области: анализ генетических аспектов наследственных форм ТНРМЖ, изучение роли онкогенов, оценка значимости факторов иммунного ответа и генов, которые их контролируют, исследования ассоциаций герминальных вариантов различных генов в развитии ТНРМЖ с применением как GWAS, так и ген-кандидатных подходов.
Результаты и их обсуждение
Наследственные формы тройного негативного рака молочной железы
Примерно 20% пациентов характеризуются формированием наследственных форм, из них около 5– 10% имеют мутации в генах TP53, PTEN, BRCA1 и BRCA2 [Economopoulou et al., 2015]. Особенно важную роль в предопределении риска развития РМЖ, а также рака яичников играют гены BRCA1 (17q21.31) и BRCA2 (13q13.1). Белки BRCA1 (Breast Cancer Type 1 Susceptibility Protein) и BRCA2 (Breast Cancer Type 2 Susceptibility Protein) являются ключевыми эффекторами пути гомологичной рекомбинации (Homologous Recombination, HR) – наиболее точного механизма репарации двунитевых разрывов ДНК. BRCA1 – это белок, функционирующий как многофункциональный адаптер и платформа для сборки белковых комплексов. Его роль можно назвать «стратегической»: он распознает тип повреждения, рекрутирует необходимые факторы и контролирует выбор пути репарации. BRCA2 непосредственно обеспечивает ключевой этап рекомбинации. Его основная и наиболее изученная функция – регуляция работы рекомбиназы RAD51. Нарушение работы этих белков приводит к тому, что клетка вынуждена использовать альтернативные, склонные к ошибкам, пути репарации (в первую очередь, негомологичное соединение концов – NHEJ). Это обусловливает состояние геномной нестабильности и накопление хромосомных перестроек (транслокаций, делеций) и точечных мутаций. При наследовании специфических инактивирующих мутаций в генах BRCA1 и BRCA2 повышается риск развития не только РМЖ, но и других видов онкологических заболеваний. Наиболее распространенные «мажорные» мутации в BRCA1: 5382 insC, 185 delAG, 3819 del GTAAA, 3875 del GTCT, 4154 delA, 300 T>G, 2080 del A, c.2080insA, c5251 C>T, c.4675 G>A, c.5177_ 5180delGAAA. Помимо этих, описано появление множества других патогенных вариантов:
-
• нонсенс-мутации: например, c.4035A>T (p.Lys1345Ter) – образование стоп-кодона;
-
• сплайсинг-мутации: мутации в сайтах сплайсинга, нарушающие правильное «сшивание» экзонов в мРНК (например, в интронах 5, 7, 12, 18, 20, 22, 23);
-
• крупные геномные перестройки: делеции или дупликации целых экзонов (например, делеция экзонов 1–2, 1–3, 5, 13, 14–20, 17–19, 20, 21–24 и др.). Их частота может достигать 10–20% от всех мутаций в BRCA1 в некоторых популяциях, и они не обнаруживаются стандартными методами секвенирования нового поколения (NGS), требуя применения MLPA или подобных методик.
У женщин с наличием мутаций в гене BRCA1 к 70–80 годам риск развития РМЖ возрастает на 55– 72%, в случае BRCA2 – на 45–69%. Кроме того, следует отметить, что у носителей мутаций в области BRCA1 и BRCA2 РМЖ развивается в более молодом возрасте, по сравнению с теми, у кого нет мутаций. Во всей структуре РМЖ примерно 73% мутантных копий BRCA1 и BRCA2 являются ассоциированными с наследственной формой тройного негативного рака, в то время как остальные 27% случаев не несут мутаций [Domagala et al., 2017]. Генетическое тестирование BRCA1 и BRCA2 имеет большое значение для разработки стратегий терапии тройного негативного типа на ранней стадии [Gupta et al., 2025]. В этом случае также следует учитывать некоторые особенности, связанные с этнической и расовой принадлежностью. Мета-анализ высокого уровня доказательности подготовил Н. Chen с коллегами [Chen et al., 2018]. На основе обобщения результатов 537 научных публикаций авторы выявили наибольшую распространенность мутаций в BRCA1mut (OR: 3.292; 95% CI: 2.773–3.909) у женщин с тройным негативным типом [Chen et al., 2018]. BRCA2 характеризовался наличием генетических вариаций в области третьего экзона c.262_263delCT, p.Leu88AlafsTer12, что приводит к сдвигу рамки считывания и образованию нефункционального белка. Важно отметить, что распространенность мутаций в BRCA варьируется в зависимости от популяции и возраста. В то время как в общей структуре ТНРМЖ на долю носителей мутаций приходится до 20%, исследование Harahap et al. [2025] не выявило патогенных вариантов BRCA1 у женщин в постменопаузе. Это подчеркивает, что BRCA1-ассоциированный ТНРМЖ – это преимущественно заболевание молодого возраста, поэтому требуется дифференцированный подход для генетического тестирования. Хотя мутации в BRCA1 и BRCA2 приводят к сходным результатам (дефекты в репарации ДНК), их вклад в развитие ТНРМЖ неодинаков. Мета-анализ Chen et al. [2018] демонстрирует, что ассоциация BRCA1 с ТНРМЖ значительно сильнее, чем у BRCA2. Это может быть связано с дополнительными, нерепарационными функциями белка BRCA1 в клеточном цикле и транскрипционной регуляции, которые делают его утрату особенно критичной для базально-подобного фенотипа ТНРМЖ.
Ключевые аспекты патогенеза спорадического ТНМРЖ
Генетические аспекты ТНРМЖ. Патогенетически центральным элементом в развитии и прогрессии ТНРМЖ является возникновение мутаций в гене-супрессоре опухолей TP53 (Tumor Protein p53). Ген TP53 (17p13.1) кодирует транскрипционный фактор p53 – "страж генома". Роль TP53 в патогенезе ТНРМЖ первоначально подчеркивается его исключительной частотой мутирования. Если в общей структуре РМЖ мутации TP53 встречаются в 30–40% случаев [Liu et al., 2022], то при ТНРМЖ этот показатель увеличивается до 80% и выше [Yadav et al., 2015; Jin et al., 2016]. Для сравнения, частота мутаций в другом ключевом супрессоре, PTEN, значительно ниже, а мутации в онкогенах, таких как PIK3CA, встречаются примерно в 14% случаев ТНРМЖ [Chen et al., 2022]. Это делает инактивацию TP53 самым распространенным единичным генетическим событием при данном подтипе, указывая на его фундаментальную роль в биологии этих опухолей. Значимость мутаций TP53 определяется не только частотой, но и их функциональными последствиями. В ответ на повреждение ДНК, гипоксию или онкогенный стресс p53 активирует каскад транскрипционных программ, ведущих к остановке клеточного цикла (через p21), репарации ДНК, сенесценции или апоптозу. В отличие от многих других генов, мутации в TP53 при ТНРМЖ – это преимущественно миссенс-мутации (например, R175H, R248Q, R273H) в ДНК- связывающем домене. Такие мутации приводят не просто к потере функции супрессора опухоли ("loss-of-function"), но и часто наделяют мутантный белок p53 новыми, онкогенными свойствами ("gain-of-function"). Мутантный p53 не только теряет способность активировать апоптоз и останавливать клеточный цикл в ответ на повреждение ДНК, но и активно способствует инвазии, метастазированию и химиорезистентности, взаимодействуя с другими сигнальными путями. Мутации TP53 – это маркер с ясными клиническими последствиями. Значимость мутаций TP53 подтверждается их устойчивой ассоциацией с агрессивным течением болезни [Liu et al., 2022; Yadav et al., 2015]. Опухоли с мутациями TP53 часто ха- рактеризуются более высоким пролиферативным индексом (Ki-67), склонностью к раннему рецидивиро-ванию и формированию метастазов [Liu et al., 2022]. Таким образом, статус TP53 служит не только патогенетическим маркером, но и важным прогностическим фактором, позволяя стратифицировать пациентов с ТНРМЖ в группу наивысшего риска. Важно отметить, что дисфункция пути p53 является универсальным механизмом для ТНРМЖ. В случае наследственных форм (например, при синдроме Ли – Фраумени) это происходит из-за герминальных мутаций в TP53, а в спорадических случаях – из-за соматических мутаций [Liu et al., 2022]. Это подчеркивает, что инактивация этого гена является не опциональным, а, по-видимому, обязательным этапом в развитии данного агрессивного подтипа.
Анализ современных исследований позволяет утверждать, что патогенез ТНРМЖ в значительной степени определяется синергическим взаимодействием двух основных типов генетических нарушений: инактивации гена-супрессора TP53 и нарушения репарации ДНК через путь генов BRCA1/2 [Domagala et al., 2017; Chen et al., 2018]. Их совместное действие формирует уникальный биологический ландшафт этой агрессивной опухоли. Мутации TP53 и BRCA1/2 не являются независимыми событиями в патогенезе ТНРМЖ. Их можно рассматривать как элементы единой патогенетической оси: TP53 создает общий фон геномного хаоса и выживаемости поврежденных клеток, а BRCA1/2 придает этому хаосу специфическую, клинически значимую форму, определяя как крайне неблагоприятный прогноз, так и уникальные возможности для таргетного терапевтического вмешательства [Chen et al., 2018; Gupta et al., 2025]. Ключевым драйвером онкогенеза при ТНРМЖ является гиперактивация сигнального пути PI3K/AKT/mTOR, определяющего выживаемость опухолевых клеток, их устойчивость к терапии и неблагоприятный прогноз пациентов. При ТНРМЖ конститутивная активация этого пути заставляет клетку бесконтрольно расти и выживать в условиях, где нормальная клетка погибла бы. Уникальность этого пути при ТНРМЖ заключается в том, что его можно активировать двумя взаимодополняющими способами:
-
• потеря супрессора: инактивация гена PTEN (Phosphatase and TENsin homolog);
-
• активация онкогена: мутации в гене PIK3CA (PhosphatidylInositol-3-Kinase).
Ген PTEN (10q23.31) кодирует липидную фосфолипазу, катализирующую дефосфорилирование фосфа-тидилинозитол-3,4,5-трифосфата (PIP3) до PIP2. Ген PTEN не является распространённым наследственным предиктором РМЖ. Однако его инактивация (мутации, делеции, эпигенетическое сайленсирование) приводит к аккумуляции PIP3 и конститутивной активации AKT и mTOR, что стимулирует пролиферацию, выживаемость клеток и ангиогенез, одновременно ингибируя апоптоз. Данные Derkyi-Kwarteng et al. [2024], Prvanović et al. [2021] и Chen et al. [2023] последовательно описывают PTEN как опухолевый супрессор, чье выключение ведет к гиперактивации пути PI3K/AKT/mTOR и ассоциирован с синдромом Коудена. Примерно 25–50% пациентов с наличием данного синдрома могут иметь высокий риск развития РМЖ. Так как продукты гена PTEN выступают в качестве супрессоров опухолеобразований, регулируя клеточный рост, пролиферацию и выживаемость, мутации в нем нарушают эти процессы [Derkyi-Kwarteng et al., 2024]. Мутации в составе гена PTEN характеризуются аутосомно-доминантным механизмом наследования, что указывает на 50% вероятность передачи поврежденной копии гена потомкам. Утрата функций PTEN приводит к повышению экспрессии белков mTOR и PIK3 и способствуют негативному прогнозу для пациентов [Prvanović et al., 2021]. Доклинические исследования на клеточных линиях указывают на потенциальную терапевтическую мишень – ген WDHD1 , ингибирование которого может подавлять выживаемость PTEN-дефицитных клеток ТНРМЖ [Ertay et al., 2020]. Однако для подтверждения клинической значимости этого открытия требуются дальнейшие исследования. У женщин с синдромом Коудена мутации в PTEN обуславливают 25–30% риск образования ТНРМЖ [Chen et al., 2023]. PTEN относится к онкосупрессорам, нарушение функций которого могут наблюдаться не только при наследственных, но и спорадических формах ТНРМЖ. Они ассоциированы с агрессивным течением болезни, солидными опухолями и плохим прогнозом выживаемости [Chai et al., 2022]. В норме PTEN участвует в регуляции клеточного роста и выживаемости через подавление сигнального пути PI3K/AKT. Дефицит его активности также связан с образованием метастазов в лимфатических узлах, что способствует образованию более агрессивного фенотипа опухоли. Совокупный эффект дефицита активности белков P53 и PTEN приводит к повышению экспрессии фактора MEOX1, что негативно влияет на эффективность терапии ТНРМЖ [Gasparyan et al., 2020]. Статус фактора PTEN также влияет на экспрессию определенных мРНК: hsa-miR-4324, hsa-miR-125b, hsa-miR-381, hsa-miR-145 и has-miR136 [Wang et al., 2019].
Эффект, идентичный потере PTEN, – это гиперактивация PI3K/AKT/mTOR. Ключевой ген этой оси PIK3CA (3q26.32) кодирует каталитическую субъединицу p110α фосфоинозитид-3-киназы (PI3K). Активирующие миссенс-мутации в «горячих» точках (например, E545K в спиральном домене, H1047R в киназном домене) приводят к конститутивной активации киназной активности PI3K независимо от сигналов с рецепторов. Это создает эффект, аналогичный потере PTEN, – гиперактивация пути PI3K/AKT/mTOR. Поскольку мутации в гене PIK3CA могут способствовать росту опухоли, метастазированию и резистентности к химиотерапии, они также активно изучаются в контексте ТНРМЖ [Mallick, Duttaroy, Dutta, 2024]. Распространенность этих явлений для этого гистологического типа примерно равна 14% [(Chen et al., 2022]. Разработка терапии связана с применением ингибиторов, блокирующих сигнальный путь PI3K/AKT/mTOR [Hu et al., 2021]. Возможность резистентности к терапии ТНРМЖ обу- словлена мутациями, усиливающими активность PI3K/AKT/mTOR, который, в свою очередь, ингибирует апоптоз. Известно, что гиперактивация пути PI3K/AKT/mTOR смещает клеточный метаболизм в сторону аэробного гликолиза, обеспечивая быстрый приток энергии и строительных блоков для растущей опухоли (эффект Варбурга), обеспечивая ее метаболическую адаптацию. Таким образом, ось PI3K/AKT/mTOR представляет собой не просто один из многих нарушенных путей при ТНРМЖ, а своего рода «сигнальный хаб», интеграцию которого можно считать критическим событием в патогенезе данного подтипа рака. Ее гиперактивация непосредственно диктует фундаментальные свойства клеток ТНРМЖ: их выживаемость, устойчивость к лечению и метаболическую адаптацию. Ось PI3K/AKT/mTOR тесно перекрещивается с другими сигнальными каскадами, нарушенными при ТНРМЖ (например, с RAS/MAPK), создавая мощную сеть, поддерживающую опухолевый рост.
Ген KRAS (Kirsten Rat Sarcoma Viral Oncogene Homolog) является центральным молекулярным переключателем (GTP-азой) в пути RAS/MAPK, который регулирует пролиферацию и выживание клеток. В контексте ТНРМЖ его мутации, хоть и относительно редкие, вносят значительный вклад в онкогенез, влияя на агрессивность опухоли и ее микроокружение, а также создавая потенциальную уязвимость для таргетной терапии. Ген KRAS (12p12.1) кодирует белок K-Ras, который передает сигналы от рецепторов на клеточной мембране к ядру, регулируя такие процессы, как пролиферация, выживание и дифференцировка клетки. Мутации гена KRAS при ТНРМЖ редки, но значимы. Утверждение Tokumaru et al. [2020] о том, что активация пути KRAS может ассоциироваться с благоприятным иммунным микроокружением, выглядит парадоксально на фоне общепринятой роли этого онкогена в стимуляции прогрессии. Это противоречие может объясняться гетерогенностью ТНРМЖ и требует дальнейших исследований с обязательной стратификацией опухолей по иммунным подтипам.
Мутации в онкогене KRAS могут влиять на эффективность терапии и выживаемость пациентов. Самой хорошо изученной в данном контексте мутацией KRAS является G12D [Teufelsbauer et al., 2024]. Отмечено, что она может способствовать изменению микроокружения опухоли, что приводит к иммуннологическим патологиям. Несмотря на тот факт, что мутации KRAS способствуют ухудшению прогноза развития заболевания, отмечается, что повышение активности сигнального пути, ассоциированного с данным онкогеном, может увеличивать шансы выживаемости пациентов, а также стабилизирует иммунологические реакции [Tokumaru et al., 2020]. Ингибиторы сигнального пути KRAS и MEK могут также рассматриваться в качестве терапевтических средств для ТНРМЖ [Mustachio et al., 2021]. Мутантный KRAS может напрямую активировать каталитическую субъединицу p110α фермента PI3K, усиливая сигналы выживания и метаболического перепрограммирования опухоли. Это создает «сигнальный дубликат», повышающий устойчивость клетки. В то же время отмечается, что только 5% опухолей молочных желез несут мутации KRAS и до 60% характеризуются мутантным EGFR [Vodithala, Bhake., 2024].
Ген EGFR (7p11.2 ) кодирует рецептор эпидермального фактора роста (Epidermal Growth Factor Receptor), контролирующий передачу сигналов роста с поверхности клетки в ядро. При ТНРМЖ онкоген EGFR, как правило, характеризуется повышенной экспрессией. В отличие от рака легких, где часты активирующие мутации, при ТНРМЖ основными механизмами онкогенной активации EGFR являются:
-
• амплификация гена: это наиболее характерный для ТНРМЖ механизм. Повышение числа копий гена приводит к избытку рецепторов на мембране опухолевых клеток [Vodithala, Bhake, 2024]. Это создает условия для постоянного, лиганд-независимого сигналинга;
-
• сверхэкспрессия белка без генетических мутаций;
-
• аутокринная стимуляция: опухолевые клетки сами производят лиганды для EGFR , создавая петлю положительной обратной связи для собственного роста.
В литературе существуют заметные противоречия относительно прогностической значимости мутаций EGFR при ТНРМЖ. Ряд исследований связывают сверхэкспрессию или амплификацию EGFR с более агрессивным фенотипом, устойчивостью к терапии и плохой выживаемостью [Nakai, Hung, Yamaguchi, 2016]. Это объясняется тем, что EGFR активирует несколько ключевых путей выживания клеток, включая RAS/MAPK и PI3K/AKT [Song et al., 2020]. Некоторые работы парадоксальным образом предполагают, что высокая экспрессия EGFR может ассоциироваться с лучшим ответом на химиотерапию или быть маркером определенного молекулярного подтипа (например, базально-подобного), который сам по себе имеет уникальные биологические особенности [Nakai, Hung, Yamaguchi, 2016; Kim et al., 2017]. Это объясняется тем, что базально-подобные опухоли, часто экспрессирующие EGFR, могут обладать унаследованной чувствительностью к ДНК-повреждающим агентам из-за сопутствующих дефектов в системах репарации ДНК. Отмечается также диссонанс между выраженной биологической ролью EGFR in vitro и скромными результатами клинических испытаний моно-таргетных препаратов. В обзоре «A perspective on anti-EGFR therapies targeting triple-negative breast cancer» авторы разбирают причины неэффективности монотерапии против EGFR и обсуждают перспективы комбинированных подходов [Nakai, Hung, Yamaguchi, 2016]. Они указывают на необходимость сочетания ингибиторов EGFR с другими агентами для преодоления резистентности. Использование ингибиторов тирозин-киназ, моноклональных антител представляет собой перспективное направление терапии ТНРМЖ [Nakai, Hung, Yamaguchi, 2016]. Могут применяться ингибиторы m/TOR EGFR, а также может быть активирован сигнальный путь JAK/STAT3, который способствует повышению выживаемости клеток и пролиферативной активности [Song et al., 2020]. Таким образом, ген EGFR является значимым онкогенным фактором при ТНРМЖ, чья роль реализуется преимущественно через амплификацию и сверхэкспрессию белка, а не через точечные мутации. Его гиперактивация служит мощным драйвером пролиферации, выживания и метастатического потенциала опухолевых клеток, обуславливая неблагоприятный прогноз. Стратегии, направленные на одновременное блокирование EGFR и компенсаторных сигнальных путей или усиление иммунного ответа, остаются активной и перспективной областью исследований для преодоления резистентности и улучшения исходов при этом агрессивном подтипе рака.
Ген BRAF (7q34) (B-Raf Proto-Oncogene, Serine/Threonine Kinase) кодирует серин-треониновую киназу, которая и занимает ключевое положение в одном из самых важных сигнальных путей клетки – пути MAPK/ERK (Mitogen-Activated Protein Kinase / Extracellular Signal-Regulated Kinase). В раковых клетках в гене BRAF происходят активирующие миссенс-мутации, которые приводят к конститутивной (постоянной) киназной активности белка независимо от сигнала с RAS. V600E (замена валина на глутаминовую кислоту в позиции 600) является самой изучаемой мутацией в гене BRAF , которая обуславливает повышенную активность данного белка, что способствует бесконтрольному клеточному делению [Wang et al., 2021]. Мутации BRAF не считаются независимыми прогностическими индикаторами при ТНРМЖ. Их вклад затмевается более частыми нарушениями (например, в генах PI3K/AKT/mTOR или EGFR ). Некоторые исследования предполагают, что активация пути MAPK/BRAF может парадоксально ассоциироваться с благоприятными иммунными особенностями опухоли [Tokumaru et al., 2020], но это требует дальнейших подтверждений.
Мутации в гене KMT2C (7q36.1) (K-MethylTransferases 2C ), кодирующем гистоновую метилтрансфе-разу (Lysine Methyltransferase 2C), также часто ассоциированы с ТНРМЖ по причине его вовлеченности в супрессию опухолей и метастазирование. KMT2C, также обозначаемый в научной литературе как MLL3 ( Mixed-Lineage Leukemia), является метилтрансферазой, мутации в которой могут изменять активность фермента и модификацию гистонов, что может способствовать развитию метастазирования, как правило, в мозге [Seehawer et al., 2024]. KMT2C через модификацию гистонов участвует в эпигенетической регуляции экспрессии генов, вовлеченных в рост опухоли, выживаемость клеток. Мутации KMT2C часто ассоциированы с ТНРМЖ. Однако не ясно, являются ли они:
-
- драйверными событиями, непосредственно определяющими агрессивное поведение подмножества ТНРМЖ;
-
- «пассажирскими» мутациями, которые накапливаются на фоне общей геномной нестабильности, но сами по себе вносят ограниченный вклад;
-
- модификаторами, которые усиливают эффекты других, более сильных драйверных мутаций (например, в TP53 ). Многие выводы о роли KMT2C сделаны на основе исследований на клеточных линиях и модельных животных. Их перенос в клиническую практику требует валидации на крупных когортах пациентов.
Унаследованные варианты определенных низкопенетрантных генов также могут быть связаны с риском развития РМЖ, в том числе трижды негативного типа. Полногеномные исследования ассоциаций являются наиболее перспективными для выявления новых ранее неизвестных генов, которые вносят значимый вклад в развитие ТНРМЖ [Jurj et al., 2020]. Так, был обнаружен вариант rs57141087 гена TRIM37, оказывающий влияние на последствия, связанные с ТНРМЖ [Tihagam et al., 2025]. Изучение подробного геномного и транскриптомного ландшафта ТНРМЖ позволяет разрабатывать новые стратегии терапии заболевания [Jiang et al., 2019[. Пространственная транскриптомика дала возможность установить определённую степень гетерогенности ТНРМЖ [Wang et al., 2024]. Мета-анализ полнотранскриптомных данных позволяет оценить эффективность ответа на неоадювантную терапию ТНРМЖ [Zhang, Zhang, Li, 2023]. Перспективным направлением также является протеомика опухолей при развитии ТНРМЖ. Так, например, исследование количественной протеомики позволило исследовать 6306 белков в нескольких опухолях ТНРМЖ [Mariano et al., 2025].
Ген-кандидатный подход к анализу ассоциаций, реализованный в ряде исследований, также дал несколько интересных результатов. Такой подход фокусируется на генах с известной функцией (например, гены репарации ДНК, биотрансформации ксенобиотиков и др.). Исследования [Заварыкина и др., 2022; Титов и др., 2025] качественно показывают, как полиморфизмы в генах XPG (Xeroderma Pigmentosum, complementation group G), XPD (Xeroderma Pigmentosum, complementation group D), XRCC1 (X-ray Repair Cross-Complementing protein 1) и др. влияют на риск и выживаемость, причем их эффекты часто зависят от взаимодействия друг с другом и с факторами среды. При этом чрезвычайно важен этнический и популяционный контекст [Kim et al., 2017; Wang et al., 2022]. Так, в корейской популяции были найдены ассоциации с риском развития ТНРМЖ вариантов гена EGFR в 19 (L747_P753>Q) и 21 (L858R и L861Q) экзонах [Kim et al., 2017]. На примере тайваньской популяции четыре полиморфизма гена EZH2 (Enhancer of Zeste Homolog 2) (rs6950683, rs2302427, rs3757441 и rs41277434) были изучены для оценки риска ТНРМЖ, определены варианты генотипов, обуславливающих наивысший риск [Liu et al, 2022]. В Кемеровской обл. Российской Федерации были обследованы 682 женщины русской национальности, в том числе 213 больные тройным негативным раком молочной железы и 465 женщин близкого возраста, не имеющих признаков онкологических заболеваний [Титов и др., 2025]. Генетические варианты рас- сматриваются для оценки эффективности терапии ТНРМЖ. Была изучена связь генов XRCC1 (rs25487), XPG (rs17655), TP53 (rs1042522), CDKN1A1 (Cyclin-Dependent Kinase Inhibitor 1A) (rs1801270) с показателями безрецидивной и общей выживаемостью пациентов [Заварыкина и др., 2022]. Показано влияние XRCC1, XPG, TP53, CDKN1A1 на выживаемость пациентов с ТНРМЖ, принимающих терапию на основе платины [Kolyadina et al., 2023]. Полиморфные варианты генов биотрансформации ксенобиотиков также активно исследовались для получения сведений об эффективных диагностических маркерах ТНРМЖ. Отмечен вклад полиморфизмов 34 G>A и 421 C>A транспортного белка ABCG2 (ATP-Binding Cassette, Sub-family G, Member 2) в развитие риска рака. Вариант 421 C>A ассоциирован с метапластической и медулярной гистологией ТНРМЖ. Вариант CYP1B1(Cytochrome P450 Family 1 Subfamily B Polypeptide 1) 4326 C>G может использоваться для оценки выживаемости пациентов с ТНРМЖ при прохождении химиотерапии [Aziz et al., 2021]. Изучение полиморфных вариантов генов белка PXR может быть целесообразным для оценки риска ТНРМЖ [Rao, Tang, Wen, 2023].
Роль иммунных факторов в развитии ТНРМЖ . Иммунный ландшафт ТНРМЖ представляет собой динамическую и гетерогенную экосистему, где взаимодействуют многочисленные популяции иммунных клеток, определяя как агрессивность течения заболевания, так и потенциальный ответ на терапию. Ключевыми отличительными особенностями иммунного микроокружения ТНРМЖ являются: высокий уровень лимфоцитарной инфильтрации, активация иммунных чекпойнтов, дисбаланс в составе иммунных клеток, преобладание миелоидных супрессорных клеток, уникальный цитокиновый профиль, нарушение сигналинга интерферона I типа.
Важным прогностическим фактором и потенциальным предиктором ответа на иммунотерапию при ТНРМЖ является состав и плотность опухоль-инфильтрирующих лимфоцитов (TILs). К ним относятся:
-
• цитотоксические Т-лимфоциты (CD8+): высокий уровень инфильтрации CD8+ T-клеток ассоциирован с улучшенной выживаемостью и ответом на иммунотерапию [Liu et al., 2018; Badve et al., 2022]. Однако их функция при ТНРМЖ часто подавлена через механизмы иммунного чекпойнта;
-
• T-хелперы (CD4+) и T-регуляторные клетки (Treg): роль CD4+ T-клеток неоднозначна: Th1-ответ способствует активации CD8+ T-клеток, в то время как популяция Treg (FoxP3+), напротив, играет критическую роль в подавлении противоопухолевого иммунитета [Navarrete-Bernal et al., 2020]. Высокое соотношение CD8+/Treg является благоприятным прогностическим признаком;
-
• В-лимфоциты: помимо роли в гуморальном иммунитете, В-клетки выполняют функции антигенпрезентирующих клеток. Формирование третичных лимфоидных структур (TLS), содержащих В-клетки, ассоциировано с улучшенным ответом на иммунотерапию при ТНРМЖ [Conte et al., 2024]. Примечательно, что В-клетки могут усиливать IL-1β-зависимую инвазивность опухоли [Toney et al., 2025].
При развитии ТНРМЖ в организме отмечается дисбаланс в составе иммунных клеток. Цитотоксические CD8+ T-клетки часто находятся в состоянии «истощения». Регистрируется повышенное количество FoxP3+ Tregs, которые активно подавляют противоопухолевый иммунный ответ [Navarrete-Bernal et al., 2020]. В-клетки могут играть противоречивую роль: с одной стороны, участвуют в презентации антигена, с другой – могут усиливать инвазивность опухоли через продукцию IL-1β [Toney et al., 2025].
Популяция клеток миелоидного ряда играет ключевую роль в формировании иммуносупрессивной ниши. К ним относятся:
-
• опухоль-ассоциированные макрофаги (TAMs): при ТНРМЖ часто доминирует альтернативно активированный M2-фенотип, способствующий ангиогенезу и подавлению T-клеточного ответа [Liu et al., 2018];
-
• миелоидные супрессорные клетки (MDSCs): эти незрелые миелоидные клетки активно рекрутируются в опухоль под действием IL-8 [Dominguez et al., 2017] и обладают мощной супрессорной активностью в отношении T-лимфоцитов.
Работа иммунной системы связана с активацией таких иммунологических факторов, как PD-L1 (Programmed Death-Ligand 1), CTLA4 (Cytotoxic T-Lymphocyte-Associated Protein 4), PD1 (Programmed Cell Death Protein 1) . Герминальные варианты генов иммунного ответа рассматриваются в качестве важных предикторов развития РМЖ. В ряде работ обсуждаются ассоциации иммунных чекпойнтов с ТНРМЖ (PD-L1, PD-1, CTLA-4) [Navarrete-Bernal et al., 2020; Peng et al., 2020; Badve et al., 2022; Izadi et al., 2024; Li et al., 2025]. Единодушно признается, что ось PD-1/PD-L1 является главным механизмом ускользания ТНРМЖ от иммунного надзора. Иммунотерапия, нацеленная на чекпойнты, стала прорывом в лечении ТНРМЖ.
Значительную роль при ТНРМЖ играют и другие ингибиторные рецепторы, формирующие «синдром истощения» T-клеток. Это:
-
• CTLA-4: его роль выходит за рамки простого маркера. CTLA-4, экспрессируемый преимущественно Treg, конкурирует с CD28 за лиганды B7 на APC, что приводит к подавлению ранних этапов активации T-клеток [Navarrete-Bernal et al., 2020; Peng et al., 2020];
-
• LAG-3 (Lymphocyte-Activation Gene 3): его экспрессия часто ко-индуцируется с PD-1, а двойное ингибирование LAG-3 и PD-1 рассматривается как перспективная стратегия преодоления резистентности к монотерапии [Yi et al., 2021; Li et al., 2025];
-
• TIM-3 (T-cell Immunoglobulin and Mucin-domain containing-3): TIM-3 часто ко-экспрессируется с PD-1 на самых дисфункциональных клонах T-лимфоцитов, и его блокада может восстанавливать противоопухолевый иммунитет [Yi et al., 2021].
Наряду с основными иммунологическим факторами, вносящими наиболее весомый вклад в развитие ТНРМЖ (PD-L1, CTLA4, PD1), активно рассматривается роль провоспалительных цитокинов. Среди них отмечен клинический потенциал ИЛ-1B, ИЛ-6, ИЛ-8, TGF-β и фактора некроза опухоли – TNF-α. Они играют важную роль в прогрессировании ТНРМЖ и развитии метастазирования. ИЛ-6, ИЛ-8, в особенности TNF-α, участвуют в обеспечении клеточной выживаемости.
Цитокиновый коктейль, продуцируемый при ТНРМЖ, является мощным драйвером злокачественной прогрессии. IL-8 (интерлекин -8), по данным Deng et al. [2020] и Abdulkarim et al. [2024], выступает ключевым фактором ангиогенеза и эпителиально-мезенхимального перехода. Важна также его роль как мощного хемоаттрактанта для нейтрофилов, что является одним из ключевых механизмов формирования иммуносупрессивного микроокружения при ТНРМЖ. Высокие показатели экспрессии гена ИЛ-1В (2q14.1) связаны с усиленной инвазивностью, метастазированием и наихудшим прогнозом ТНРМЖ [Toney et al., 2025]. Ингибирование продукции данного фактора или предотвращение возможности его связывания с рецепторами может служить одним из направлений терапии ТНРМЖ. В случае развития данного заболевания, ИЛ-1B продуцируется с участием самих раковых клеток в составе микроокружения опухоли. Он участвует в ангиогенезе, росте опухоли и метастазировании [Wilson et al., 2023; Zhou et al., 2024]. Главным образом, активность ИЛ-1B при РМЖ состоит в образовании метастазов в области костей. Продолжаются клинические испытания по использованию ингибиторов ИЛ-1B в случае развития солидных опухолей. TNF-α [Narasimhan et al., 2022] напрямую стимулирует стволовые клетки рака, способствуя рецидивам и метастазам. В контексте ТНРМЖ крайне важна иммуносупрессивная функция TGF-β . TGF-β подавляет цитотоксическую активность CD8+ T-клеток и NK-клеток, ингибирует дифференцировку Th1-клеток и способствует дифференцировке Treg. Также он является мощным индуктором эпителиально-мезенхимального перехода (Epithelial-Mesenchymal Transition –EMT).
Цитокиновый профиль при ТНРМЖ не просто сопровождает воспаление, а активно формирует иммуносупрессивное и про-опухолевое микроокружение [Liu et al., 2018; Vecchi et al., 2022]. Их эффекты при ТНРМЖ можно систематизировать (см. табл. 1).
Таблица 1
Эффекты цитокинов при ТНРМЖ [Cytokine effects in triple negative breast cancer]
|
Цитокин / Хемокин |
Основные источники в опухоли |
Ключевые клетки-мишени и эффекты |
|
IL-8 (CXCL8) |
Опухолевые клетки, макрофаги |
Нейтрофилы/MDSC: мощный хемоаттрактант, усиливает их супрессорную активность [Dominguez et al., 2017]. Опухоль: индукция EMT и вас-кулогенной мимикрии через ось IL-8/CXCR2 [Deng et al., 2020; Abdulkarim et al., 2024]. |
|
TNF-α |
Макрофаги, T-клетки |
Опухоль: активация NF-κB → выживаемость, пролиферация, индукция стволовости [Narasimhan et al., 2022; Zafari et al., 2024; Qodir et al., 2025]. |
|
IL-6 |
Опухолевые клетки, стромальные клетки |
Опухоль: активация JAK/STAT3 → пролиферация, выживаемость, хеморезистентность [Vecchi et al., 2022; Vasiyani et al., 2025]. Иммунные клетки: поляризация макрофагов в M2-фенотип. |
|
IL-1β |
В-клетки, макрофаги |
Опухоль: усиление инвазивности [Toney et al., 2025]. Системно: участие в костном метастазировании [Zhou et al., 2024]. |
|
TGF-β |
Treg, опухолевые клетки |
Иммунные клетки: мощное подавление функции эффекторных T-клеток. Опухоль: индукция EMT и метастазирования [Liu et al., 2018]. |
Также стоит отметить, что в активации противоопухолевого иммунитета критическую роль играет сигналинг интерферона I типа (IFN-I). Этот путь активируется в ответ на неоантигены и повреждение ДНК через cGAS-STING путь [Liu et al., 2018; Vasiyani et al., 2025] и необходим для эффективного прай-мирования T-клеток и их инфильтрации в опухоль [Chen et al., 2018; Jiang et al., 2019]. Нарушение сигна-линга IFN-I является одним из ключевых механизмов развития резистентности к иммунотерапии при ТНРМЖ [Liu et al., 2018; Deng et al., 2020].
Взаимосвязь генетических событий, иммунного ответа и других факторов риска ТНРМЖ
Драйверные генетические события непосредственно диктуют правила формирования иммунного ландшафта. Мутации TP53 не только приводят к геномной нестабильности, но и могут изменять секреторный профиль опухолевой клетки, способствуя повышенной экспрессии провоспалительных цитокинов и хемокинов, которые рекрутируют супрессорные популяции [Liu et al., 2022]. Дефекты пути гомологичной рекомбинации (HRD), включая BRCA -мутации , ведут к накоплению большого количества соматических мутаций и, как следствие, неоантигенов. Это делает такие опухоли «иммунологически горячими» с высоким уровнем инфильтрующих лимфоцитов, что объясняет их повышенную чувствительность к ингибиторам иммунных чекпойнтов и ингибиторам PARP [Domagala et al., 2017; Chen et al., 2018]. Активация онкогенных путей (PI3K/AKT , RAS/MAPK ) напрямую модулирует экспрессию PD-L1 на опухолевых клетках [Tokumaru et al., 2020; Hu et al., 2021]. Кроме того, эти пути контролируют продукцию VEGF и IL-8, создавая иммуносупрессивное и про-ангиогенное микроокружение [Deng et al., 2020; Prvanović et al., 2021].
Генетические вариации в генах чекпойнтов (например, полиморфизмы PD-L1 ) [Makrantonakis et al., 2022]) изучаются как прогностические биомаркеры. Vlajnic Т. et al. [2022] и Wang et al. [2022] указывают на техническую сложность определения статуса PD-L1 из-за гетерогенности его экспрессии, что является важным практическим ограничением. Ген PD1 (2q37.3) вовлечен в регуляторные процессы иммунной системы, которые предотвращают распознавание клеток опухоли. Он является одним из компонентов сигнального пути PD1/PD-L1, который способствует выживаемости злокачественных новообразований. Перспективным направлением является разработка и применение ингибиторов данного пути (например, пембролизумаба), в основном для терапии более агрессивных форм ТНРМЖ [Li et al., 2025]. Как правило, применение блокаторов в данном случае происходит в комбинации с химиотерапией для предотвращения развития метастазирования [Jin et al., 2024]. Необходимы дополнительные исследования для выявления большего числа маркеров, ассоциированных с PD1/PD-L1. Роль гена CTLA-4 кажется более сложной, и его высокая экспрессия может, по некоторым данным [Peng et al., 2020], ассоциироваться с лучшей выживаемостью. Ген CTLA4 (2q33.2) экспрессируется как в опухолевых клетках, так и в клетках иммунитета внутри микроокружения опухоли [Navarrete-Bernal et al., 2020]. Его основная функция заключается в активации Т-клеток, он выступает в качестве посредника между микроокружением опухоли и иммунной системой [Yi et al., 2021]. CTLA4 обычно конкурирует с молекулой CD28 за связывание с CD80 и CD86, которые отвечают за активацию T-клеток. Было исследовано, что уровни экспрессии CTLA4 в составе трансформированных клеток ТНРМЖ коррелируют с параметрами выживаемости и сохраняемости опухоли. Высокая экспрессия данного фактора ассоциирована с более стабильной выживаемостью пациентов и снижением возможностей рецидивирования [Peng et al., 2020]. Инфильтрирующие в опухоль лимфоциты под контролем CTLA4 могут влиять на системный статус воспаления у пациентов, тем самым потенциально оказывать влияние на эффективность противоопухолевой терапии. Наряду с другими активаторами клеток иммунитета, CTLA4 является маркером для разработки более эффективных способов терапии ТНРМЖ. Воздействие на него с помощью ингибиторов контрольных точек является наиболее целесообразным. В настоящее время также обсуждается применение блокаторов CTLA4 с нановакцинами на основе мРНК [Lin et al., 2022].
Поскольку большое количество исследований указывают на важную роль цитокинов в развитии ТНРМЖ, исследуется прогностический и клинический потенциал полиморфных вариантов их генов. Для ИЛ-1b был изучен потенциал полиморфизмов IL-1β rs1143627, rs1799916, и rs16944 в связи с изменением риска к развитию ТНРМЖ [Sghaier et al., 2024]. Минорные аллели rs16944 показали значимую ассоциацию с патологией. Для ИЛ-8 наиболее значимым и известным полиморфным вариантов является rs4073. Он располагается в промоторном регионе гена. Отмечена роль аллеля А в формировании риска развития ТНРМЖ на примере тайваньской популяции [Wang et al., 2022].
РМЖ возникает и развивается в результате действия как внутренних, так и внешних факторов. Было показано, что от 20 до 30% случаев РМЖ связаны с неправильным образом жизни (употребление алкоголя и табака, лишний вес и ожирение, физическая инертность), с факторами окружающей среды и профессиональной деятельности. Большой интерес представляют собой исследования предрасположенности к РМЖ в условиях промышленно-развитых регионов. В частности, было показано, что повышенные концентрации полициклических ароматических углеводородов в атмосфере многократно увеличивают риск развития РМЖ [Shen et al., 2017]. Влияние поллютантов на организм женщин может выражаться на индивидуальных показателях гормонального фона. Был отмечен синергический эффект стероидных гормонов и аутоантител в прогрессировании РМЖ [Глушков и др., 2023]. Наряду с иммунологическими предикторами РМЖ в генетическом анализе могут использоваться компоненты биотрансформации ксенобиотиков [Глушков и др.,2018]. Был описан предиктивный потенциал генов репарации ДНК и клеточного цикла [Торгунакова и др., 2022]. Гены антиоксидантной защиты могут участвовать в формировании предрасположенности к определенным субтипам РМЖ (люминальный А субтип) [Тимофеева и др., 2023]. Таким образом, существует значительный интерес к роли низкопенетрантных генетических вариантов в формирование полигенного риска развития ТНРМЖ. Их эффект индивидуален и зависит от гене- тического фона и внешних факторов. Комбинация GWAS и исследований кандидатных генов максимально полно раскрывает генетическую архитектуру предрасположенности к данному виду рака.
Подводя итог выполненного аналитического обзора, можно отметить, что уровень статей, опубликованных за последние 10 лет в данной области, заметно варьировался (табл. 2).
Таблица 2
Классификация цитируемых статей в обзоре [Classification of cited articles in review]
|
Уровень доказательности |
Тип исследования |
Описание |
Авторы |
|
1a. Наивысшая надежность |
Мета-анализ и рандомизированные контролируемые испытания (РКИ) |
Систематические обзоры РКИ или крупные РКИ, предоставляющие наиболее надежные доказательства |
Chen et al., 2018; Badve et al., 2022 |
|
2b. Высокая надежность (для наблюдательных исследований) |
Когортные исследования и Пул-анализ |
Проспективные или ретроспективные наблюдения за группой пациентов (когортой) или объединенный анализ нескольких когорт |
Economopoulou et al., 2015; Liu et al., 2022; Conte et al., 2024; Yadav et al., 2015; Jin et al., 2016; Derkyi-Kwarteng et al., 2024; Prvanovic et al., 2021; Chen et al., 2023; Dominguez et al., 2017; Jiang et al., 2019; Wang et al., 2024; Zhang, Zang, Li, 2023; Mariano et al., 2025; Kolyadina et al., 2023; Jurj et al., 2020; Ti-hagam et al., 2024; Harahap et al., 2025; Arnold et al., 2022; Domagala et al., 2017; Gupta et al., 2024; Chai et al., 2022; Mallick et al., 2024; Hu et al., 2021; Musta-chio et al., 2021; Vodithala and Bhake., 2024; Nakai et al., 2016; Kim et al., 2017; Wang et al., 2021; Seehaw-er et al., 2024; Liu et al, 2022; Yeoh et al., 2023; Aziz et al., 2021; Rao, Tang, Wen, 2023; Izadi et al., 2024; Li et al., 2025; Bernal et al., 2020; Peng et al., 2020; Sghaier et al., 2024; Wang et al., 2022; Shen et al., 2017; Baranova et al., 2022; Obidiro, Battogtokh, Akala, 2023; Jin et al., 2024; Chakravarty et al., 2025; Tiwari et al., 2023; Zagami, Carey., 2022 |
|
3b. Средняя надежность (склонны к систематическим ошибкам) |
Исследования «случай – контроль» |
Сравнение группы больных с группой здоровых лиц; полезны для выявления ассоциаций, но подвержены систематическим ошибкам. |
Kim et al., 2017; Makrantonakis et al., 2022; Boguszewska-Byczkiewicz et al., 2023; Sghaier et al., 2024; Титов и др., 2025; Заварыкина и др., 2022; Liu et al, 2022; Глушков и др., 2018; Глушков и др., 2023; Тимофеева и др., 2023; Торгунакова и др., 2022 |
|
4. Низкая надежность (предварительные данные) |
Серии случаев и Описания случая |
Описания нескольких пациентов (серия) или одного пациента (case report); позволяют выдвигать гипотезы, но не доказывают их |
Harahap et al., 2025; Wang et al., 2019; Tokumaru et al., 2020; Teufelsbauer et al., 2024 |
|
5. Фундаментальные исследования (требуют клинического подтверждения) |
Доклинические исследования (in vitro / in vivo) и теоретические обзоры |
Исследования на клеточных линиях и модельных животных, фундаментальные механизмы, обзоры перспективных технологий. |
Ertay et al., 2020; Gasparyan et al., 2020; Hu et al., 2021; Deng et al., 2020; Song et al., 2020; Seehawer et al., 2024; Chakravarty et al., 2025; Tiwari et al., 2023; Vander Heiden, Cantley , Thompson, 2009; Qiao et al., 2016; Lin et al., 2022; Wilson et al., 2023; Zhou et al., 2024; Narasimhan et al., 2022; Qodir et al., 2025; Zafa-ri et al., 2024; Vasiyani et al., 2025; Vecchi et al., 2022; Toney et al., 2025; Abdulkarim et al., 2024; Rajaram et al., 2024; Andreopoulou et al., 2015; Du, Li, 2022; Li et al., 2015; Kim et al., 2021; Vlajnic et al., 2022; Wang et al., 2019 |
В таблице 2 приведена классификация статей согласно Оксфордской системе классификации уровней доказательности (Oxford Centre for Evidence-Based Medicine (CEBM) Levels of Evidence). В этих работах использовались различные методологические подходы: мета-анализы и рандомизированные контролируемые испытания, когортные исследования, «случай – контроль», серии случаев эксперименты in vitro/in 92
vivo). Можно отметить преобладание когортных исследований и мета-анализов (66.3% от всех работ), дополненных фундаментальными работами (14.5%) для объяснения механизмов. В совокупности эти работы демонстрируют переход от изучения изолированных генетических дефектов к комплексной, интегрированной парадигме, в которой ядро геномной нестабильности ( TP53, BRCA ) неразрывно связано с активацией онкогенных сигнальных путей (PI3K, EGFR) и, что наиболее важно, с формированием специфического иммунного микроокружения.
Заключение
Систематический обзор данных литературы позволил охарактеризовать вклад разных групп генов в предрасположенность к развитию данного заболевания. Ядро составляют высокопенетрантные мутации в генах-супрессорах ( BRCA1, TP53, PTEN ), ведущие к дефектам репарации ДНК и неконтролируемому росту. Драйверы прогрессии – это соматические мутации и дисрегуляция онкогенных путей (PI3K/AKT/mTOR, KRAS, EGFR ). Эти генетические и сигнальные аномалии напрямую диктуют архитектуру иммунного микроокружения, модулируя экспрессию чекпойнтов, секрецию цитокинов и хемоки-нов, а также рекрутинг и функциональное состояние иммунных клеток. Микроокружение формируется под влиянием иммунных чекпойнтов (PD-L1) и провоспалительных цитокинов (IL-8, TNF-α), которые подавляют иммунитет и стимулируют метастазирование. Индивидуальный риск модулируется множеством низкопенетрантных полиморфизмов в генах, отвечающих за репарацию ДНК, метаболизм и иммунный ответ. Остальные группы генетических факторов могут его модифицировать (в меньшей степени). Безусловно, важно учитывать вклад факторов среды, специфику изученной популяции, репродуктивную историю женщины и другие конфаундеры, способные значимо модифицировать индивидуальный риск. Перспективы лечения лежат в комбинации химиотерапии, таргетной терапии (ингибиторы PARP, PI3K, AKT, mTOR) и иммунотерапии (ингибиторы чекпойнтов). Будущее – за прецизионными подходами, включающими:
-
• комбинации иммунотерапевтических агентов , направленные на одновременное таргетирование нескольких механизмов иммунного ускользания (например, PD-1 + LAG-3);
-
• таргетинг на иммуносупрессорные клетки в микроокружении (например, ингибиторы CSF-1R для истощения TAM, блокада рецепторов хемокинов для предотвращения рекрутинга MDSC);
-
• использование технологий генетического редактирования (CRISPR/Cas9) не только для коррекции онкогенных дефектов, но и для усиления противоопухолевого иммунитета (например, редактирование T-клеток для создания более эффективных CAR-T);
-
• создание комплексных генетических и иммунных профилей для истинно персонализированного подхода к каждому пациенту с ТНРМЖ, учитывающего как драйверные мутации опухоли, так и особенности ее иммунного контекста.


