Молекулярный анализ генетического разнообразия популяций донников ( Melilotus dentatus Pers.)
Автор: Мунтян А.Н., Белова В.С., Чижевская Е.П., Румянцева М.Л., Симаров Б.В., Андронов Е.Е.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Корма и кормопроизводство: биологические основы
Статья в выпуске: 6 т.47, 2012 года.
Бесплатный доступ
Проведены молекулярно-генетические исследования популяций донника зубчатого ( Melilotus dentatus Pers.) из разных географически удаленных районов (Северный Кавказ и Казахстан). Использованный комплексный подход включал внутри- и межпопуляционный анализ по таксономически значимым молекулярным маркерам (ITS). Также выполнен анализ участка рецепторного гена nfr 5. Показано, что среди растений Melilotus dentatus Pers. имеются различия как на внутри-, так и на межпопуляционном уровне. Кроме того, наблюдается обособленность популяций донников в кластеры согласно их географическому распространению. Определено независимое распределение популяций растений донников по рецепторной части гена nfr 5 относительно кластерной структуры ITS региона.
Генетическое разнообразие, ген nfr5
Короткий адрес: https://sciup.org/142133368
IDR: 142133368 | УДК: 633.366:575.17:577.21
Molecular analysis of the genetic diversity of populations of sweet clover ( Melilotus dentatus Pers.)
In the studies of Melilotus dentatus Pers. populations from different geographically remote areas (North Caucasus and Kazakhstan), a compex approach of intra- and inter-population analysis of taxonomically important molecular markers (ITS) was used. The analysis of receptor gene nfr5 was also made. It is shown that the Melilotus dentatus Pers. plants differ at both intra- and inter-population levels. A consolidation of sweet clover’s populations to clusters is observed according to their geographic location. An independent distribution of populations on receptor part of nfr5 gene concerning cluster structure of ITS region is determined.
Текст научной статьи Молекулярный анализ генетического разнообразия популяций донников ( Melilotus dentatus Pers.)
В мировом земледелии донник как кормовая культура играет не столь большую роль в сравнении с другими бобовыми кормовыми травами. Однако к настоящему времени в результате всестороннего изучения у него выявлен комплекс хозяйственно ценных свойств. Так, донник характеризуется высокой засухоустойчивостью и одновременно повышенной зимостойкостью, а также отличается от других бобовых высокой устойчивостью к болезням и вредителям (1). Кроме того, донник зубчатый лучше поедается животными вследствие более низкого содержания кумарина (2). Способность донника произрастать на засоленных землях и солонцах позволяет использовать его для восстановления почв за счет создания солерезистентного бобово-ризобиального комплекса. Соответственно, важная задача при биорекультивационных мероприятиях — увеличение симбиотической эффективности, которая, в свою очередь, в значительной степени зависит от генотипа растения-хозяина.
Специфичность бобово-ризобиального симбиоза обеспечивается обменом сигнальными молекулами между партнерами, в результате чего запускается механизм образования специализированного органа — клубенька. В ответ на выделение корнем растения специфических индукторов — флавоноидов, азотфиксирующие бактерии начинают продуцировать сигнальные молекулы (Nod-факторы), которые инициируют процесс образования клубеньков у бобовых растений (3). Все Nod-факторы представляют собой липохитоолигосахариды. У бобовых растений имеются семь генов, предположительно участвующих в распознавании бактериальных сигналов микросимбионтов и взаимодействии (4). Особенно интересно семейство генов LYK, к которым относятся nfrl и nfr5, впервые выявленные у лядвенца японского (3, 5), SymIO и Sym2 у гороха посевного (3), а также ген NFP у диплоидной люцерны (6, 7). Продукты этих генов, кодирующих LysM-содержащую рецепторную киназу, имеют типичную для растений доменную структуру: внеклеточные LysM-домены, предположительно участвующие в рецепции Nod-фактора, трансмембранный домен и внутрикле- точный домен серин/треонин киназы.
Гены, содержащие LysM -кодирующие участки (LysM -мотивы), относятся к древней и весьма разнообразной группе, распространенной во всех царствах, кроме архей (7). Филогенетический анализ показал, что некоторые последовательности бактериальных LysM -мотивов имеют общие корни с последовательностями у грибов, растений, насекомых и животных. Это позволило предположить, что одна группа таких генов сформировалась перед дивергенцией растительного и животного миров, другая — в результате конвергентной эволюции. Структурное сходство LysM-содержа-щей протеинкиназы с пептидогликаном, представляющим собой один из компонентов клеточной стенки бактерий, служит доказательством участия рецепторных белков NFR1 и NFR5 в распознавании и передаче Nod-фактора на следующие компоненты сигнального каскада, приводящего к образованию клубеньков (7). Однако в настоящее время еще недостаточно знаний, раскрывающих происхождение и механизмы функционирования обсуждаемой группы рецепторных генов.
Существует множество молекулярно-генетических методов, позволяющих исследовать генетическое разнообразие и популяционную изменчивость сельскохозяйственных культур (8). Нашей целью был молекулярный анализ генетической изменчивости у растений донника зубчатого ( Melilotus dentatus Pers.), отобранных в разных географически удаленных районах (Приаралье и Северный Кавказ).
Методика . Семенной материал собирали в период созревания донника зубчатого (октябрь, 2000 год) на территории Республики Казахстан — сайты № 31 (49° 56' с.ш., 58° 92' в.д.) и № 57 (49° 59' с.ш., 57° 71' в.д.), а также в Краснодарском крае России (Северо-Кавказский регион) — сайт № 51 (43° 52’ с.ш., 39° 22 ' в.д.). Семена стерилизовали концентрированной серной кислотой 10 мин, тщательно промывали стерильной водой и проращивали в чашках Петри при температуре 4 °С в течение 2 сут. Для дальнейших исследований из каждой популяции отбирали по 20 проростков.
Геномную ДНК выделяли из 2-суточных проростков методом хлороформной экстракции с использованием CTAB-буфера (9). Растительный материал тщательно гомогенизировали, затем суспендировали в СТАВ и инкубировали при температуре 65 °С в течение 60 мин. После экстракции хлороформом надосадочную жидкость, содержащую ДНК, осаждали равным объемом изопропанола, после чего промывали 70 % этиловым спиртом. Образец ДНК ресуспендировали в 50 мкл деионизированной воды.
Для RAPD-фингерпринтинга (RAPD — random amplified polymorphic DNA) использовали десятичленный праймер FS-27 (5'-AGCCGGCCTT-3') (10). Амплификацию выполняли на термоциклере My Cycler («Bio Rad», США) (денатурация 3 мин при 95 °С; 40 циклов: денатурация — 30 с при 94 °С, отжиг праймеров — 30 с при 37 °С, элонгация — 3 мин при 68 °С; завершающий синтез — 3 мин при 72 °С). RAPD проводили в реакционной смеси объемом 20 мкл, содержащей 10* буфер (670 мМ Трис-HCl, pH 9,1; 166 мМ сульфат аммония, 20 мМ хлорид магния, 0,1 % Твин 20), dNTP (концентрация каждого 0,15 мМ), праймер (15 пМ), 1,5 ед. Taq-полимеразы (UAB «Fermentas», Литва) и 1 мкл геномной ДНК (1012 нг). Продукты амплификации разделяли в 2 % агарозном геле, содержащем бромистый этидий, с 0,5*TAE буфером.
При амплификации ITS региона растительной ДНК использовали праймеры ITS4 (5'-TCCTCCGCTTATTGATATGC-3') и ITS5 (5'-GGAA-GTAAAAGTCGTAACAAGG-3') (11). Амплификацию проводили в 20 мкл смеси, содержащей 10* буфер, dNTP (концентрация каждого 0,15 мМ), смесь праймеров ITS4 и ITS5 (15 пМ), 1,5 ед. Taq-полимеразы (5 ед/мкл) и 1 мкл геномной ДНК (10-12 нг) на термоциклере My Cycler («Bio Rad», США). Протокол ПЦР: денатурация 3 мин при 95 °C; 30 циклов — 30 с при 95 °C, 30 с при 55 °C, 1 мин при 72 °C; завершающая элонгация 4 мин при 72 °C. Полимеразную цепную реакцию для участка гена nfr5 осуществляли с помощью пары вырожденных праймеров — nfr5-for3 (5'-AAGTCT-TGGTTGTTAYTTGCCA-3') и nfr5-Grev3 (5'-TGCAGTCTCAGCTAATGAA-GTAC-3'). Протокол ПЦР: 3 мин при 95 °C; 30 циклов — 30 с при 94 °C, 30 с при 42 °C, 1 мин при 72 °C; 4 мин при 72 °C.
Для определения нуклеотидной последовательности продукты амплификации ДНК клонировали в векторе pTZ57R/T (UAB «Fermentas», Литва). Cеквенирование выполняли со стандартными праймерами М13 на автоматическом приборе CEQ™ 8000 Genetic Analysis System («Beckman Coulter, Inc.», C0A). Каждую последовательность анализировали в двух направлениях. Данные по определению нуклеотидных последовательностей участков ITS и nfr5 обрабатывали с помощью программного обеспечения секвенатора CEQ™ 8000 Genetic Analysis System. Выравнивание и сборку нуклеотидных и белковых последовательностей проводили с использованием программы Vector NTI Suit 8 (. При построении филогенетических деревьев пользовались программами ClustalX ( и FPQuest («Bio Rad», C0A).
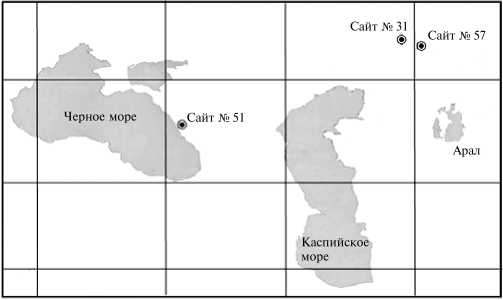
Рис. 1. Расположение мест сбора образцов семян донника Melilotus dentatus Pers., использованных в исследовании.
Результаты . Места сбора образцов донника (номера сайтов) отмечены на рисунке 1.
Для молекулярного изучения генетического разнообразия популяций донника нами использовался комплексный подход, включающий RAPD-анализ, а также определение нуклеотидной последовательности межгенных участков рибосомальной ДНК
(ITS регион). Особое внимание уделялось определению генетического разнообразия рецепторного комплекса гена nfr5 , продукты которого предположительно вовлечены в распознавании ризобиального Nod-фактора.
Начальный этап работы включал выполнение RAPD-фингерприн-тинга, а также анализ растительной ДНК с использованием таксономически значимых участков (ITS). По результатам RAPD-анализа (рис. 2) была построена дендрограмма филогенетического родства изученных образцов донника зубчатого (рис. 3), на которой проявились как внутри-, так и межпопуляционные различия. Популяции донников из Приаральского региона оказались достаточно однородными (за исключением варьирования по минорным фрагментам). При этом популяции растений из Приаралья и с Cеверного Кавказа четко различались, хотя некоторое число образцов имели идентичные RAPD-профили. Для последующего анализа ITS региона и рецепторного участка гена nfr5 из каждой популяции отобрали по три образца Melilotus dentatus Pers. с наиболее полиморфными RAPD-профилями (см. рис. 2).
A
Б
В
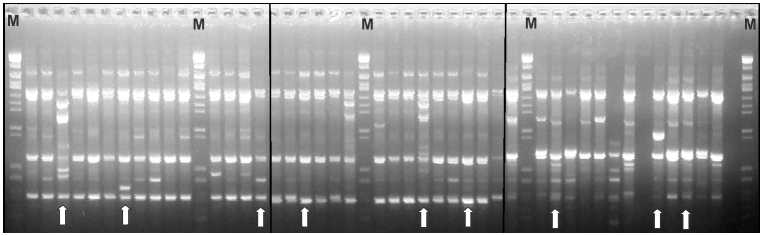
Рис. 2. RAPD-фингерпринтинг для образцов из популяций донника Melilotus dentatus Pers., отобранных в Приаралье (A и Б, соответственно сайты № 31 и № 57) и на Северном Кавказе (В, сайт № 51) . М — маркер молекулярных масс 7 /BstEII. Стрелками обозначены RAPD-профили, которые были взяты для последующего анализа ITS региона и рецепторного участка гена nfr5 .
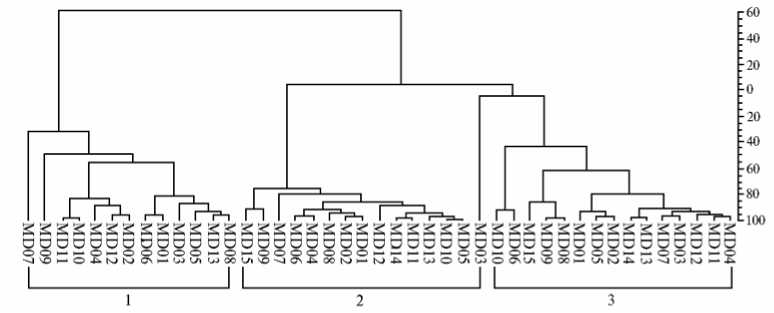
Рис. 3. Дендрограмма филогенетического родства для образцов из популяций донника Melilotus dentatus Pers. (MD) , отобранных на Северном Кавказе (1, сайт № 51) и в Приаралье (2 и 3, соответственно сайты № 31 и № 57) , по данным RAPD-фингерпринтинга.
Секвенированный внутренний транскрибируемый регион (ITS) рибосомальной ДНК включал высококонсервативную последовательность 5,8S-субъединицы РНК и два транскрибируемых участка — ITS1 и ITS2. Такие свойства, как многокопийность, небольшой размер (600-700 п.н.) и согласованная эволюция между локусами ITS1 и ITS2 (11), позволяют использовать эти спейсеры в качестве таксономически значимого молекулярного маркера в систематике высших растений (12).
У исследованных донников нуклеотидные последовательности ITS региона имели размер 687 п.н. На их основании была построена дендрограмма родства растений донника (рис. 4). При этом полученные результаты полностью совпали с данными RAPD-фингерпринтинга. В обоих случаях растения донника из Приаральского и Северо-Кавказского регионов формировали отдельные кластеры, причем степень различий соответствовала обособленности популяций.
Детальный анализ нуклеотидных последовательностей ITS региона выявил точечные замены в регионах ITS1, 5,8S и ITS2 (рис. 5). Особенно интересен участок ITS2, где все три вариабельных сайта с нуклеотидными заменами (позиции 494, 611 и 648) однозначно маркируют отличия северокавказских донников от приаральских. Согласно данным литературы, ITS1 и ITS2 регионы эволюционно сопряжены, то есть генетические изменения должны затрагивать оба спейсера. Однако наши результаты показали, что максимум полиморфных сайтов наблюдается в ITS2 (см. рис. 5).
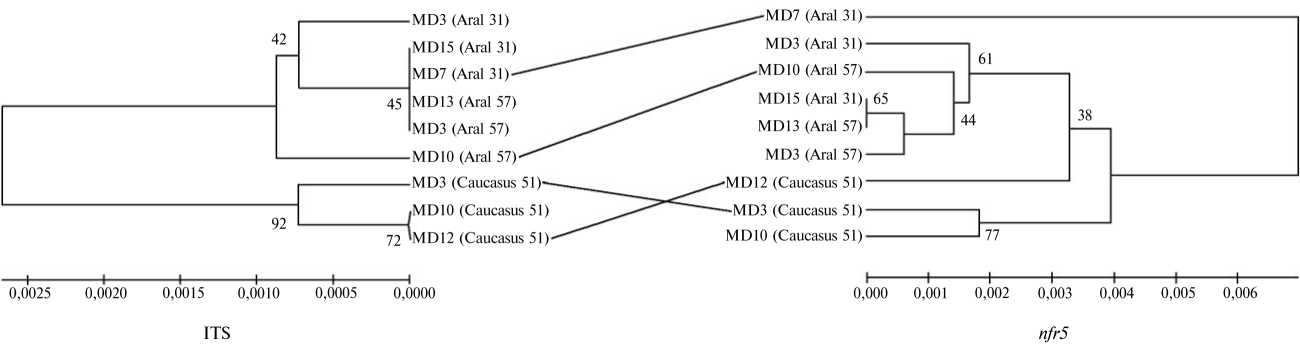
Рис. 4. Дендрограммы филогенетического родства по ITS региону (внутренний транскрибируемый регион рибосомальной ДНК) и участку гена nfr5 (рецепторный белок NFR5) для образцов из популяций донника Melilotus dentatus Pers. (MD) , отобранных на Северном Кавказе (сайт № 51 — Caucasus 51) и в Приаралье (сайты № 31 и № 57 — соответственно Aral 31 и Aral 57).
ITS1 I 5,8S ITS2
79 | 160 | 391 | 494 | 611 | 648
|
Consensus |
G |
T |
A |
T |
C |
A |
|
|
3 |
G |
T |
A |
T |
C |
A |
|
|
1 |
7 |
G |
T |
G |
T |
C |
A |
|
15 |
G |
T |
A |
T |
C |
A |
|
|
3 |
G |
C |
A |
T |
C |
A |
|
|
2 |
10 |
G |
T |
A |
T |
C |
A |
|
13 |
G |
T |
A |
T |
C |
A |
|
|
3 |
G |
T |
A |
A |
T |
T |
|
|
3 |
10 |
G |
T |
A |
A |
T |
T |
|
12 |
A |
T |
A |
A |
T |
T |
|
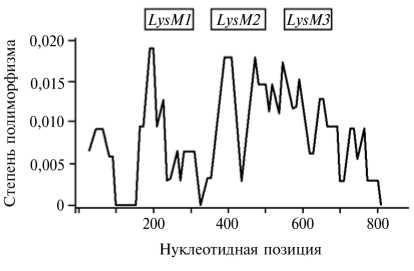
Рис. 5. Вариабельные позиции в нуклеотидных последовательностях внутреннего транскрибируемого региона ITS рибосомальной ДНК, включающего высококонсервативную последовательность 5,8S-субъединицы РНК и транскрибируемые участки ITS1 и ITS2 регионов, у образцов донника Melilotus dentatus Pers. из разных популяций: 1 и 2 —
Приаралье, сайты соответственно № 31 и № 57, 3 — Северный Кавказ, сайт № 51
(для сайтов указаны номера проанализированных образцов).
Рис. 6. Нуклеотидный полиморфизм доменной структуры рецепторного участка гена nfr5 у изученных растений донника Melilotus dentatus Pers. (независимо от их географического происхождения). LysMl , LysM2 и LysM3 — мотивы гена nfr5 , продукты которых отвечают за связывание бактериального сигнала.
На этапе молекулярногенетического анализа рецепторного гена nfr5 мы провели выравнивание полученных по следовательностей (нуклеотидной и аминокислотной) относительно рецепторного региона гена nfr5 у козлятника восточного. Для популяций донника зубчатого определили доменную структуру изучаемого участка, размер которого составил 778 п.н. Как оказалось, наибольшее число вариабельных сайтов приходятся на LysM-домены: в LysM1 и LysM2 имелись четыре, в LysM3 — три вариабельных позиции (рис. 6, 7).
LysM1 LysM2 LysM3
|
1 |
180 | |
198 |
1 235 I |
281 |
1 359 | |
402 |
\ 448 |
I 469 |
536 |
565 |
608 |
|
Consensus |
C |
C |
G |
T |
T |
A |
A |
T |
T |
A |
A |
|
3 |
C |
C |
G |
T |
T |
A |
A |
T |
T |
A |
A |
|
1 7 |
T |
T |
A |
T |
T |
G |
G |
C |
T |
G |
G |
|
15 |
C |
C |
G |
T |
T |
A |
A |
T |
T |
A |
A |
|
3 |
C |
C |
G |
T |
T |
A |
A |
T |
T |
A |
A |
|
2 10 |
C |
C |
G |
T |
C |
A |
A |
T |
T |
A |
A |
|
13 |
C |
C |
G |
T |
T |
A |
A |
T |
T |
A |
A |
|
3 |
C |
C |
G |
C |
T |
A |
A |
T |
T |
A |
A |
|
3 10 |
C |
C |
G |
T |
T |
A |
A |
T |
C |
A |
A |
|
12 |
T |
T |
G |
T |
T |
G |
A |
T |
T |
G |
A |
|
Consensus (аминокислота) |
- |
— |
Glu |
Ile |
Phe |
— |
— |
— |
Val |
Ser |
Asn |
|
Замещенная аминокислота |
— |
— |
Lys |
Thr |
Ser |
— |
— |
— |
Ala |
Gly |
Ser |
Рис. 7. Вариабельные позиции нуклеотидных последовательностей и значимые аминокислотные замены в рецепторном участке гена nfr5 у образцов донника Melilotus dentatus Pers. из разных популяций: 1 и 2 — Приаралье, сайты соответственно № 31 и № 57, 3 — Северный Кавказ, сайт № 51 (для сайтов указаны номера проанализированных образцов).
Анализ аминокислотных последовательностей показал, что в домене LysM1 число сайтов с заменами уменьшилось до 2, в LysM2 — до 1, при этом в LysM3 оно осталось прежним и равнялось 3 (см. рис. 7). Таким образом, обращает на себя внимание LysM3-домен, в котором выявлено повышение частоты несинонимичных (значимых) замен, возможно, указывающих на эволюцию анализируемого гена в рамках движущего отбора с целью создания множества модификаций растительного рецептора при взаимодействии с бактериальным сигналом.
Сопоставление дендрограмм, построенных на основании изучения нуклеотидных последовательностей в рецепторной части гена nfr5 и в ITS регионе (см. рис. 4), показало, что топология дендрограммы nfr5 уже не имеет такого однозначного сходства с RAPD- и ITS-дендрограммами, согласующимися как между собой, так и с географической приуроченностью популяций донника. Вероятно, здесь наблюдается варьирование замен в рецепторном участке гена nfr5 вне зависимости от географического происхождения растений. Возможно, это явление связано с экологической пластичностью донника в изменяющихся условиях среды, его способностью тонко реагировать на бактериальные сигналы (Nod-фактор) и адаптироваться к ним, не исключено также, что мы имеем дело с переносом генетического материала между популяциями.
Итоговые нуклеотидные последовательности участков для ITS и nfr5 у растений донника депонированы в базу данных NCBI под следую щими номерами:
(ITS_69/7-JF461307, ITS_69/2-JF461308, ITS_69/13-JF461309,
ITS_57/3-JF461310, ITS_57/14-JF461311, ITS_57/10-JF461312,
ITS_51/3-JF461313, ITS_51/16-JF461314, ITS_51/15-JF461315,
ITS_31/7-JF461316, ITS_31/3-JF461317, ITS_31/15-JF461318);
(NFR5_69/7-JF461295, NFR5_69/2-JF461296, NFR5_69/13-JF461297, NFR5_57/3-JF461298, NFR5_57/14-JF461299, NFR5_57/10-JF461300, NFR5_51/3-JF461301, NFR5_51/16-JF461302, NFR5_51/15-JF461303, NFR5_31/7-JF461304, NFR5_31/3-JF461305, NFR5_31/15-JF461306).
Итак, показано, что между растениями донника зубчатого Melilotus dentatus Pers., произрастающими в разных регионах (Приаралье и Северный Кавказ), имеются различия как на внутри-, так и на межпопуляционном уровне. Кроме того, наблюдается обособленность популяций донника в кластеры согласно их географическому распространению. При этом выявлено независимое распределение популяций по рецепторной части гена nfr5 относительно кластерной структуры по ITS региону. Примененный нами молекулярно-генетический анализ полиморфизма по симбиотическим генам позволяет получать более глубокое представление о биоразнообразии растений из этой хозяйственно значимой группы, необходимое при их использовании как генетических ресурсов в программах по биотехнологиям живых систем. Учитывая интенсивное развитие фундаментальных исследований по симбиогенетике, также интересно проследить коэволюци-онные связи между макро- и микросимбионтами.


