Молекулярный анализ микологического поражения древесины
Автор: Андронов Е.Е., Чижевская Е.П., Пинаев А.Г., Павлов С.А.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Методика
Статья в выпуске: 5 т.48, 2013 года.
Бесплатный доступ
Оценка микологического поражения образцов древесины традиционно проводится с помощью культивирования, продолжительность которого может составлять до нескольких месяцев. Нами продемонстрирована возможность применения методов молекулярной биологии для таксономического и количественного анализа при грибном поражении древесины. С использованием секвенирования библиотеки диагностического фрагмента межгенного участка ITS рибосомального оперона и ПЦР с детекцией в реальном времени обнаружено, что 75 % популяции, населяющей проанализированный образец древесины (фрагмент эксплуатируемой деревянной конструкции), относится к виду Aureobasidium pullulans. Показано, что примененный подход имеет большие преимущества перед традиционными методами микологической экспертизы, так как он универсален, доступен для большинства современных отечественных лабораторий и не зависит от культивирования. Метод характеризуется высокой скоростью выполнения анализов (3-4 сут) и довольно низкими затратами (1-2 тыс. руб. на образец). Основное достижение разработанного протокола заключается в возможности выявлять разнообразие в микробных сообществах, которое до последнего времени, по всей видимости, недооценивалось. Без существенных модификаций предложенный метод может быть перенесен в рутинную сельскохозяйственную практику для детекции грибных патогенов.
Грибное поражение, древесина, пцр с детекцией в реальном времени
Короткий адрес: https://sciup.org/142133438
IDR: 142133438 | УДК: 632.4:577.29:632.08
Molecular analysis of fungal wood decay
A conventional analysis of fungal decay of wood is based on cultivation dependent approaches and can take up to several months. Here we demonstrate a possibility of molecular methods use for taxonomical and quantitative analyses of fungal wood decay. Using the sequencing of ITS libraries and real-time PCR we showed that 75 % of fungal population of the wood sample analysed is represented by Aureobasidium pullulans specie. The approach applied has great advantages over traditional cultivation dependent approaches because of its versatility, availability and cultivation independency. The method is characterized by its high speed (3-4 days) and low cost (1000-2000 rub. per sample). Our protocol’s main achievement is the ability to identify real diversity of fungal population. The method can be transferred in routine agricultural practice for fungal pathogen detection.
Текст научной статьи Молекулярный анализ микологического поражения древесины
Проблема микологического поражения образцов древесины традиционно решается с использованием методов культивирования, продолжительность которого может составлять до нескольких месяцев. То же характерно для микологического тестирования других объектов. Однако по следнее десятилетие ознаменовано широким внедрением в практику микологического анализа методов молекулярной экологии микроорганизмов, основывающихся на исследовании общей ДНК, выделенной из различных объектов (1, 2).
Существующие молекулярные подходы по большей части основаны на детекции и анализе таксономически значимых участков генома грибов. Прежде всего это фрагменты рибосомального оперона: гены субъединиц рибосом и межгенные участки ITS и IGS (1, 3, 4).
Рис. 1. Образец пораженной древесины, представленный для анализа.
Нашей целью была разработка протокола для таксономического и количественного анализа микологического поражения образца на основе двух молекулярных подходов — анализа библиотеки клонов суммарного амплификата ITS-участка рибосомального оперона и ПЦР с детекцией в реальном времени.
Описание методики. Для исследования был представлен образец деревянной конструкции (сельский
16.552.11.7047).
дом), на котором в течение первого месяца эксплуатации было выявлено интенсивное окрашенное микологическое поражение (рис. 1).
Для выделения ДНК 100-250 мг образца (в виде опилок) разрушали перетиранием в фарфоровой ступке с добавлением абразивов. Первый этап экстракции проводили при температуре 65 ° C в СТАВ-содержащем буфере (СТАВ — 2 %; NaCl — 1,4 M; EDTA — 20 мМ), с добавлением стеклянных шариков (0,3 мм) и периодическом интенсивном встряхивании на вортексе (3 раза по 5 мин). Смесь дважды экстрагировали хлороформом, после чего суммарную ДНК осаждали изопропанолом. Окончательную очистку ДНК проводили посредством селективной сорбции на диоксиде кремния в соответствии с типовой методикой (5). Качество ДНК проверяли визуально после электрофоретического разделения по степени деградации основного массива (20-30 т.п.н.).
ПЦР выполняли со стандартными компонентами. Для амплификации участка рибосомального оперона, содержащего районы ITS1, ITS2 и ген 5,8-рРНК, применяли праймеры ITS1 и ITS4 (3). В качестве термостабильной ДНК-полимеразы использовали Taq-полимеразу («Хеликон», г. Москва). Температура отжига — 52 ° C. Матрицей служила ДНК, выделенная из исследуемого образца, в количестве 50 нг на реакцию в общем объеме 30-50 мкл. Для реамплификации клонированной в плазмиде вставки использовали стандартные праймеры M13F (-46, 22-mer, «Fermentas», Литва) и M13R (-46, 24-mer, «Fermentas», Литва), температура отжига — 55 ° C. Вместо матричной ДНК в реакционную смесь добавляли небольшое количество интактных клеток Escherichia coli , содержащих плазмиду с клонированной вставкой. При ПЦР с детекцией в реальном времени анализ выполняли на амплификаторе ICycler («Bio-Rad», США). Для определения общего количества грибной ДНК в пробе использовали праймеры 5,8S и ITS1f, условия ПЦР соответствовали опубликованным рекомендациям (6). При амплификации применяли стандартный буфер для ПЦР с добавлением SYBR green («Amresco LLC», США) до конечной концентрации 0,3* и изотиоцианата флюоресцеина («Sigma-Aldrich», США) до конечной концентрации 10 нмоль. Калибровочную кривую строили на основе серии разведений ДНК, выделенной из штамма дрожжей Saccharomyces cerevisiae 1B-D1606 (7).
Для клонирования амплифицированных фрагментов ДНК после электрофоретического разделения продуктов ПЦР полосу, содержащую необходимый фрагмент ДНК, вырезали из агарозного геля. ДНК выделяли в соответствии с обычной методикой (5) с той лишь разницей, что в первом растворе гель выдерживали при 65 ° С. Очищенный амплифициро-ванный фрагмент клонировали в Т-векторе pAL («Евроген», г. Москва). Лигирование и трансформацию проводили по стандартным методикам. Для рестрикционного анализа клонированные фрагменты реамплифи-цировали, как описано выше. К аликвоте ПЦР-буфера, содержащей 300500 нг неочищенного продукта, добавляли эквивалентный объем 1* буфера Tango («Fermentas», Литва) и 2-3 ед. эндонуклеазы MspI («Fermentas», Литва). Продукты рестрикции разделяли электрофоретически в 3 % агарозном геле. Рестрикционный анализ проводился для 40 клонов каждой из исследованных проб.
После анализа выявили группу клонов с одинаковыми рестрикционными профилями (рис. 2).
На заключительном этапе выполняли секвенирование и определение таксономического положения клонированных последовательностей ITS-участка. Три клона, представляющие основной рестрикционный тип,
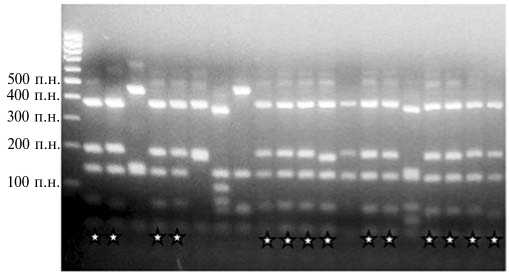
Рис. 2. Рестрикционный анализ библиотеки клонов ITS-участка грибной ДНК, выделенной из образца эксплуатируемой деревянной конструкции, представленного для исследования. На первой дорожке слева — маркер молекулярной массы («Си-бэнзим», Россия); звездочками отмечены доминантные рестрикционные типы, характеризующиеся одинаковым набором фрагментов ДНК.
подвергли циклическому секвенированию по Сэнгеру с помощью капиллярного автоматического секвенатора Beckman Coulter CEQ8000 и набора DTCS Quick Start kit («Beckman Coulter, Inc.», США) в соответствии с рекомендациями изготовителя. Секвенирование проводили с использованием реампли-фицированных фрагментов, выделенных из геля, и стандартных праймеров для секвенирования M13. Таксономическую принадлежность клонов определяли с применением программы BLASTn (8), доступной на сервере NCBI (National Center for Biotechnology Information, США).
При количественной оценке содержания общей грибной ДНК методом ПЦР с детекцией в реальном времени и пересчете на число дрожжевых клеток на 1 г субстрата в образцах было выявлено более 108 грибных клеток на 1 г субстрата. Анализ видового состава грибов в одном из образцов пораженной древесины с использованием амплификации общей последовательности ITS, клонирования и секвенирования показал, что более 75 % всей популяции составляет вид Aureobasidium pullulans. Это очень распространенный, поражающий поверхности деревянных строений аскомицет, вызывающий такой же тип поражений, как на обследованном объекте . Отдельного внимания заслуживает тот факт, что, согласно опубликованным на указанном интернет-ресурсе данным, этот гриб способен расти даже на виниловом сайдинге, используя питательные вещества, накапливающиеся на поверхностях. Таким образом, в работе была полностью решена поставленная задача — выявлен основной агент микологического поражения и оценено его количество.
Следует отметить, что описанный метод, доступный фактически любой молекулярно-биологической лаборатории, не требует много времени для идентификации грибных агентов. Так, суммарные затраты составили около 1,5 тыс. руб. и 2 человеко-дня (всего анализ продолжался 4 рабочих дня). По сравнению с методиками, основанными на культивировании, описанный прием, несомненно, представляет собой исключительно быстрый, точный, а главное, универсальный протокол для микробиологического анализа образцов различного происхождения, причем это касается не только грибов. Во Всероссийском НИИ сельскохозяйственной микробиологии с использованием аналогичных подходов проводят анализы бактериальных и архейных сообществ, населяющих различные объекты окружающей среды. Мы полагаем, что эти методы с успехом могут быть использованы и в практике сельского хозяйства.
Итак, в настоящей публикации на примере исследования образца древесины предложен быстрый и универсальный протокол, доступный большинству современных отечественных лабораторий, который обеспечивает количественный и детальный таксономический анализ популяции гри- бов, заселяющих тестируемый образец. Метод характеризуется высокой скоростью определения (3-4 сут) и довольно низкими затратами (1-2 тыс. руб. на образец). Его основное достижение заключается в возможности выявлять разнообразие микробных сообществ, которое до последнего времени, по всей видимости, недооценивалось.


