Морфофункциональное состояние кишечного барьера биомодели при введении холерных вибрионов О139 серогруппы штаммов с разным набором детерминант вирулентности
Автор: Бугоркова С.А., Осина Н.А., Бугоркова Т.В., Кутырев В.В.
Журнал: Морфологические ведомости @morpholetter
Рубрика: Краткие сообщения
Статья в выпуске: 1 т.19, 2011 года.
Бесплатный доступ
Представлены результаты сравнительной оценки реакции апудоцитов и клеток эффекторной зоны иммунной системы кишечника крольчат на заражение холерными вибрионами ctxA+, tcpA+ и ctxA-, tcpA- штаммов 0139 серогруппы. Показано, что реакция апудоцитов и клеток эффекторной зоны иммунной системы кишечника крольчат зависит от генотипа заражающих штаммов и коррелирует с характером и выраженностью морфологических изменений в кишечнике и внутренних органах животных.
Vibrio cholerae о139 се- рогруппы, эффекторная зона иммунной системы, апудоциты
Короткий адрес: https://sciup.org/143176990
IDR: 143176990
Morphofunctional condition of intestinal barrier in biomodel challenged with cholera vibrios of O139 serogroup strains possessing different sets of virulence determinants
Presented are the results of comparative assessment of reaction of apudocytes and cells of effector zone of rabbit intestine immune system on the challenge with ctxA+, tcpA+, and ctxA-, tcpAcholera vibrios of O139 serogroup strains. The reaction of apudocytes and cells of effector zone of rabbit intestine immune system was demonstrated to depend on infecting strains genotype and to correlate with character and expression of morphologic changes in intestine and internals of the animals.
Текст краткого сообщения Морфофункциональное состояние кишечного барьера биомодели при введении холерных вибрионов О139 серогруппы штаммов с разным набором детерминант вирулентности
Морфологическими эквивалентами проявления функционирования тех или иных генов холерного вибриона в макроорганизме являются нарушения, возникающие в ответ на инокуляцию микроба, в виде развития различных патологических или адаптационно-компенсаторных реакций. При моделировании холерной инфекции желудочно-кишечный тракт (ЖКТ) биомоделей обеспечивает первую линию защиты макроорганизма, выступая местом тесного взаимодействия патогена с его функциональными системами и, в первую очередь, индуктивной и эффекторной зонами иммунной [6] и нейроэндокринной системами.
В силу высокого эпидемического потенциала и склонности к быстрому распространению, холерные вибрионы О139 серогруппы долгое время признавались в качестве второго этиологического агента эпидемической холеры. Как и представители О1 серогруппы, холерные вибрионы О139 серогруппы неоднозначны в отношении эпидемического потенциала, определяемого наличием хромосомного «острова патогенности» [2]. В реализации холерного инфекционного процесса в макроорганизме ключевая роль отводится следующим детерминантам вирулентности патогена – токсин-корегулируемым пилям адгезии и холерному токсину, синтез которых кодируют соответствующие гены tcpА-F и ctxAB [10].
Цель исследования - сравнительная морфофункциональная характеристика реакции апудоцитов и клеток эффекторной зоны иммунной системы кишечника у крольчат, зараженных холерными вибрионами О139 серогруппы ctxA+, tcpA+ и ctxA-, tcpA- штаммов.
Материалы и методы исследования. В работе использовали 5 штаммов холерных вибрионов О139 серогруппы, выделенных из различных источников (табл. 1). Для выявления tcpА гена в полиимеразной цепной реакции (ПЦР) использовали олигонуклеотидные праймеры, предложенные S.P. Keasler, R.H. Hall [9], проводя амплификацию фрагмента tcpА гена с данным праймером в соответствии с авторскими рекомендациями. Идентификацию штаммов Vibrio cholerae (ctxA+) проводили с использованием тест-системы «ГенХол - для выявления ДНК V.cholerae (ctxA+) методом ПЦР» (ТУ 8895-00601898109-2007, производства ФГУЗ РосНИПЧИ «Микроб»). Работу выполняли в соответствии с инструкцией к препарату.
Экспериментальную холеру воспроизводили на крольчатах (16 особей) 7-8 дневного воз-
Таблица 1
Характеристика штаммов V. cholerae О139 серогруппы, используемых в работе
|
Штамм V.cholerae O139 |
Место выделения культуры |
Наличие основных генов, связанных с вирулентностью |
Количество животных: |
||
|
Зараженных |
Павших до: |
||||
|
36 ч |
48 ч |
||||
|
62 |
внешняя среда (река Москва), 1998 г. |
ctxA-, tcpA- |
2 |
0 |
0 |
|
МО 45 |
больной (Индия), 1992 г. |
ctxA+, tcpA+ |
4 |
4 |
0 |
|
Р16064 |
больной (г. Азов), 1993 г. |
ctxA+, tcpA+ |
4 |
3 |
1 |
|
170 |
внешняя среда (река Москва), 1999 г. |
ctxA-, tcpA- |
2 |
0 |
0 |
|
РО7 |
больной (Индия), 1992 г. |
ctxA+, tcpA+ |
4 |
2 |
1 |
% опустошен, апудоцитов + % гистохимически активных апудоцит Иан = ---------—------------------;----------------------------- % клеток в состоянии функционального покоя
раста, массой 130-150 г [8], заражая животных культурой V.cholerae О139 в дозе 1х107 КОЕ. Животных разделили на группы: 1-я группа – для заражения использовали штаммы, в геноме которых присутствовали гены ctxA, tcpA; 2-я группа – заражали культурами штаммов с отсутствующими генами ctxA, tcpA. Контрольным животным (3 особи) в аналогичных опытным условиях внутрикишечно вводили 0,2 мл 0,9 % раствора натрия хлорида. Павших и через 48 ч наблюдения усыпленных хлороформом животных вскрывали, оценивая патоморфологические изменения. Кусочки органов фиксировали в 10% водном нейтральном растворе формалина и обрабатывали по общепринятой в гистологии схеме обезвоживания и заливки материала в парафин [3]. Полутонкие парафиновые срезы кишечника и внутренних органов окрашивали гематоксилином и эозином, импрегнировали серебром по Гримелиусу, применяли сочетанную окраску альциановым синим и Шифф-реактивом [5]. Эффекторную зону иммунной системы ЖКТ, представленную лимфоидными клетками Lamina propria (собственная пластинка слизистой оболочки - СПС) и межэпителиальными лимфоцитами (МЭЛ), характеризовали, подсчитывая количество клеток на 1000 ядер энтероцитов при увеличении Х 200. Количество бокаловидных клеток (БК) и апудоцитов определяли в 10 полях зрения правильно ориентированных срезов кишечника в 10 повторах при увеличении Х 200. Секреторный профиль БК оценивали по количеству клеток, дающих голубую (кислые мукополисахариды - КМПС), красную (нейтральные мукополисахариды - НМПС) или фиолетовую (смешанные формы) окраску на 100 секреторных клеток. Морфофункциональное состояние апудоцитов определяли по изменению интенсивности окрашивания и зоне распределения продукта секреции в клетке. Индекс активности апудоцитов (Иап) вычисляли по формуле [1]:
Исследования проводили с помощью программы ДММ (версия 2.1.0.0) аппаратнопрограммного комплекса МЕКОС-Ц. Статистическую обработку данных проводили в программе Microsoft Office Excel 2003.
Результаты исследований и их обсуждение. Животные 1-ой группы в 75 % случаев пали в течение 36 ч после заражения. У них отмечали типичные для холерной инфекции изменения в подвздошной кишке и начальных отделах толстого кишечника в виде перерастяжения петель прозрачной, бесцветной, слегка опалесцирующей жидкостью (рис.).
В отличие от заражения холерными вибрионами О1 серогруппы, при гистологическом исследовании в кишечнике крольчат наблюдали проявления воспалительного характера с превалированием пролиферативно-инфильтративных процессов над явлениями отека и дистрофического поражения энтероцитов. Эти изменения в ЖКТ протекали на фоне выраженных токсических повреждений паренхиматозных органов. Не исключено, что такие особенности развития патологического процесса в макроорганизме на введение холерных вибрионов 0139 серогруппы ctxA+, tcpA+ штаммов, обусловлены особенностями строения самого микроорганизма [7]. СПС оболочки была инфильтрирована полиморфонуклеарами (ПМЯЛ) и лимфоцитами. Количество последних достигало 6,9±0,97 клеток в поле зрения среза (в контроле – 4,2±1,17). Для эффекторной зоны иммунной системы кишечника характерным было снижение в 2-2,5 раза количества МЭЛ во всех отделах кишечника на фоне почти двукратного уменьшения количества апудоцитов (табл.2), особенно в тонком кишечнике и изменение их функциональной активности, обусловленной опустошением кле- ток. Так, Иап для тонкого кишечника на введение холерных вибрионов ctxA+, tcpA+ штаммов в среднем в 10 раз превышал аналогичный показатель у контрольных животных. Бокаловидные клетки были гипертрофированы, их число на единицу площади среза увеличивалось по сравнению с контролем, характер секрета в них чаще обусловливали КМПС. Известно, что защитные функции кишечного барьера связывают с НМПС [4], а описанные изменения свидетельствуют о нарушении процессов обновления секрета в клетках.
Крольчата 2-ой группы были умерщвлены через 48 ч наблюдения. При макроскопическом исследовании у них отмечали умеренное полнокровие паренхиматозных органов, гиперемию сосудов серозной оболочки тонкого кишечника. В кишечнике регистрировали умеренное количество слизистого желтоватого содержимого с газом. При гистологическом исследовании у крольчат этой группы регистрировали признаки функционального напряжения клеток паренхимы органов. В тонкой кишке животных наблюдали умеренный отек и полнокровие сосудов подслизистой оболочки, инфильтрацию СПС оболочки и стромы ворсин ПМЯЛ и лимфоцитами. Количество последних достигало 9,6±0,94 клеток в поле зрения среза (в контроле – 4,2±1,17). Количество МЭЛ при этом умеренно повышалось, а реакция апудоцитов заключалась в некотором уменьшении числа клеток без выраженного изменения их функциональной активности (табл.). Увеличивалось количество бокаловидных клеток на единицу площади среза по сравнению с контролем, менялся характер секрета в них, чаще, чем в контроле встречались клетки со смешанным продуктом секреции.
Таким образом, изменения морфофунк-
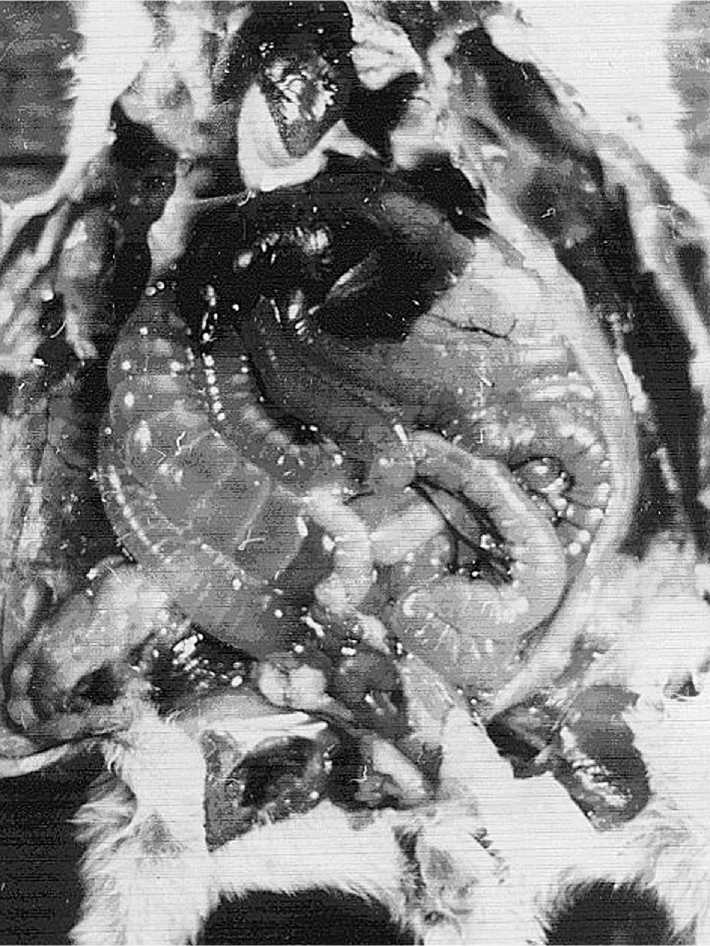
Рис. Крольчонок-сосунок. Внутрикишечное заражение холерными вибрионами О139 серогруппы ctxA+, tcpA+ штамма. 36 ч после заражения. Выраженный холерогенный эффект.
ционального состояния бокаловидных клеток, апудоцитов и элементов эффекторной зоны иммунной системы кишечника, выполняющих в макроорганизме барьерные функции, при моделировании холерной инфекции, отражали уровень повреждающего действия на эти структуры вибрионов О139 серогруппы штаммов с генотипом ctxA+, tcpA+ и направленность адаптационнокомпенсаторных реакций на введение ctxA- , tcpA- культур. Количественная характеристика барьерных структур биомодели, повышая инфор- мативность исследования, позволяет уточнять роль отдельных детерминант вирулентности в патогенезе патологического процесса.
Таблица 2
Характеристика клеток кишечного барьера крольчат-сосунков, зараженных холерными вибрионами О139 серогруппы
|
Определяемый показатель (М±m) |
Группа |
Двенадцатиперстная кишка |
Тощая кишка |
Подвздошная кишка |
Толстый кишечник |
|
Количество апу-доцитов Иап |
1-я |
4,43±0,8* 4,03 |
5,53±0,59 2,08 |
3,23±0,89* 3,41 |
2,5±0,62* 0,63 |
|
2-я |
6,2±0,69 0,95 |
6,6±1,2 0,68 |
4,7±0,91 0,94 |
3,75±0,55 0,43 |
|
|
Контроль |
8,0±1,45 0,29 |
7,8±0,39 0,46 |
6,3±0,89 0,32 |
5,4±0,56 0,35 |
|
|
Количество МЭЛ |
1-я |
- |
3,7±0,64* |
5,08±1,3* |
2,2±0,14 |
|
2-я |
- |
5,9±0,89 |
7,45±1,5 |
3,9±0,13 |
|
|
Контроль |
- |
9,4±1,32 |
12,0±2,4 |
4,2±1,17 |
|
|
Количество бокаловидных клеток |
1-я |
- |
3,7±2,14 |
7,4±1,9 |
9,3±1,44 |
|
2-я |
- |
3,4±0,19 |
5,2±0,89 |
6,7±0,32 |
|
|
Контроль |
- |
3,1±0,9 |
6,1±2,4 |
7,9±1,92 |
Примечание: * Уровень значимости различий результатов по отношению к контролю p<0,05.
Список литературы Морфофункциональное состояние кишечного барьера биомодели при введении холерных вибрионов О139 серогруппы штаммов с разным набором детерминант вирулентности
- Бугоркова С.А., Кутырев В.В., Бугоркова Т.В., Куличенко А.Н. Способ оценки качества вак цинных препаратов против холеры//Патент РФ №2301075. -Опуб. Бюл. №17, 20.06.07.
- Ерошенко Г.А. Vibrio cholerae O139: генетика и молекулярные механизмы образования возбуди теля холеры не О1 серогруппы/Г.А. Ерошенко//Проблемы особо опасных инфекций. 2006. №2 (92). -С.1518.
- Меркулов Г.А. Курс патогистологической техни ки. М.: «Медицина», 1969.367 с.
- Писарев В.Б. Бактериальный эндотоксикоз: взгляд патолога: монография/В.Б. Писарев, Н.В. Богомолова, В.В.Новочадов -Волгоград: Издво ВолГМУ, 2008.308 с.
- Саркисов Д.С. Микроскопическая техника: руководство/Д.С. Саркисов, Ю.Л. Перов. М.: «Медицина», 1996. -544 с.
- Хаитов Р.М. Иммунная система желудочно кишечного тракта: особенности строения и функ ционирования в норме и при патологии/Р.М. Хаитов, Б.В. Пинегин//Иммунология. 1997. №5. с. 47.
- Щелканова Е.Ю Новые гены Vibrio cholerae 0139 и их роль в патогенности/Е.Ю. Щелканова, Н.И. Смирнова//Проблемы особо опасных инфекций.1998. №1 (92). С. 3137.
- Dutta N.K. Experimental cholera in infant rabbit: a method for chemotherapeutic investigation/N.K. Dutta, M.K. Habbu//Brit. J. Pharmacol.1955. -V.10. P. 153159.
- Keasler S.P. Detection and biotyping Vibrio cholerae O1 with multiplex polymerase chain reaction/S.P. Keasler, R.H. Hall//Lancet.1993. V.341.P. 1661.
- Reidl J. Vibrio cholerae and cholerae:out of the water and into the host/J. Reidl, K. Klose//FEMS Microbiol. Rev. -2002. -V.26. -P. 125139.


