Морфофункциональные особенности натуральных киллеров-Т-клеток больных с опухолевыми поражениями печени
Автор: Лебединская О.В., Патютко Ю.И., Забежинский Д.А., Кузовлев Е.Н., Ахматова Н.К., Шубина И.Ж., Вершинина М.Ю., Киселевский М.В.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Экспериментальные исследования
Статья в выпуске: 3 (15), 2005 года.
Бесплатный доступ
Анализ функций натуральных киллеров-Т-клеток печени и исследование их иммунофенотипа является крайне важным в оценке роли НКТ-клеток в противоопухолевом иммунитете. Целью исследований являлось изучение фенотипа и функциональной активности мононуклеарных клеток (МНК), выделенных из интактных и парагуморальных участков печени онкологических больных в сравнении с мононуклеарами периферической крови (МНПК). НК-активность и цитотоксическую способность МНК определяли с помощью цитотоксического теста. Иммунофенотипироваыие проводили методом проточной питометрии. В результате исследований выявлено, что МНК печени, особенно выделенные из параметастатических участков, по своему иммунологическому фенотипу и цитотоксической активности существенно отличаются от МНПК тех же больных. МНК печени экспрессируют на своей поверхности и дифференцировочные антигены Т-лимфоцитов (CD3), и НК-маркеры (CD57), отличаются высоким уровнем НК-активности и способностью лидировать аутологичные опухолевые клетки, представлены молодыми (иммунобластами и про лимфоцитами) и активированными (пиронинофильными) формами лимфоцитов. Все эти показатели позволяют отнести МНК печени онкологических больных к популяции I lKT-клеток, которые могут быть использованы в иммунотерапии метастатических поражений данного органа,
Короткий адрес: https://sciup.org/14054230
IDR: 14054230
Morphological-functional characteristics of natural killers-T-cells in patients with liver cancer
The functional analysis of natural-killers-T-cells (NKT-cells) of the liver and the study of their immunologic phenotype are extremely important in the evaluation of Ihe role of NKT-cells in anti-tumor immunity. The aim of the study was to investigate the phenotype and functional activity of mononuctear cells (MNCs) released from intact and paratumoral liver sites of cancer patients as compared to mononuclear cells of peripheral blood (MCPB). NK-activity and cytostatic ability of MNCs were determined by the cytotoxic test- Immunophenotyping was carried out by the method of flow cytometry. Our results showed that liver MNCs especially released from parametastatic sites significantly differed from MCPB of the same patients by their immunologic phenotype and cytotoxic activity. Liver MNCs express both differentiated antigens-of T-lymphocytes (CD3) and NK-markers (CD57) on their surface having a high level of NK-activity and lysing autologous tumor cells. All these characteristics allow us to attribute liver MNCs of cancer patients to a population ofNKT-cells, which can be used in immunotherapy of liver metastascs.
Текст научной статьи Морфофункциональные особенности натуральных киллеров-Т-клеток больных с опухолевыми поражениями печени
Введение. Иммунная система печени включает в себя большинство компонентов врожденной иммунной системы (натуральные киллеры - НК, натуральные киллеры-Т-клетки -НКТ-клетки, дендритные клетки, макрофаги и др.) и небольшую часть эффекторов специфического иммунитета (Т-клетки). Взаимосвязь между этими двумя звеньями иммунной защиты печени до конца не изучена [4,6,12,15,16]. О роли специфических иммунокомпетентных клеток известно достаточно много, гораздо меньше сведений о других субклассах моно-нуклеарных клеток (МНК) печени, особенно об их участии в инициации иммунного ответа.
Печень является основным кроветворным органом на стадии эмбрионального развития, однако и после рождения ее гемопоэтическая функция в ряде случаев сохраняется [1]. У взрослого человека она содержит стволовые клетки (c-kit+) и является органом внетимичес-кой генерации Т-клеток, НК-клеток и даже гранулоцитов. Внетимическая генерация Т-лимфоцитов в печени происходит при участии Т-кле-точных рецепторов (TCR), включая маркеры НКТ-клеток (НК1.1 + TCR) [2, 5].
Практически все сведения о внутрипеченоч-ной активации НКТ-клеток и их взаимодействии с другими звеньями иммунной системы органа были получены в экспериментах на мышах [8, 10, 14]. НКТ-клетки составляют основную часть Т-клеточной популяции печени мышей [4, 6,9] и характеризуются как CD4+, CD4 - CD8 -(двойные негативные) ар Т-клетки (Val4/ Jal8+), CDld+ НКТ-клетки [3]. Мышиные Val4/Jal8(+) НКТ-клетки составляют 30 - 50 % от общего пула Т-лимфоцитов печени и обладают потенциальной противоопухолевой активностью [3,6,10]. Активация НКТ-клеток печени сопровождается поверхностной экспрессией CD69, усилением их цитотоксичности и выработки интерферона- т(ИФН- ) [17]. Генерация НКТ-клеток печени происходит под действием интерлейкина-12 (ИЛ-12), секретируемого антигенпрезентирующими клетками (макрофагами, купферовскими и дендритными клетками) в ответ на воздействие инфекционных и вирусных агентов, эндотоксинов, а также злокачественно трансформированных клеток [8,10,
14]. Большое количество исследований, проводимых в эксперименте на мышах, показало, что НКТ-клетки печени играют важную роль в формировании противоопухолевого иммунитета. В частности, обнаружена инфильтрация НКТ-клетками ткани печени, пораженной опухолевым процессом, особенно параметастатических участков этого органа [3, 6, 8, 10, 14 -17].
Вместе с тем литературные данные, характеризующие методы выделения НКТ-клеток из печени и крови человека, их функциональные особенности, а также иммунологический фенотип, весьма немногочисленны. В настоящее время выявлено, что основная группа НКТ-клеток человека при их выделении из здоровой и пораженной опухолью печени представляет собой Va24/Vpi 1+ НКТ-клетки [2,4, 7, 9, 11, 12]. В отличие от мышиной, печень здорового человека содержит небольшое количество НКТ-клеток (0,5 % CD3+), в периферической крови их еще меньше (0,02 %) [9]. Большинство Va24+ НКТ-клеток печени человека экспрессируют \ф1 1-цепь, что отличает их от НКТ-клеток крови. Вариантами НКТ-клеток являются Т-лимфоциты, несущие на своей поверхности CD4+CD8+, CD4 - CD8 -, а также НК-клетки с высоким уровнем экспрессии таких маркеров, как CD56, CD 161 и/ или CD69 [2, 4, 12]. Некоторые исследователи, основываясь на данных иммунофенотипи-рования, разделяют НКТ-клетки на «классические» (CDld-рестриктированные) и «неклассические», которые экспрессируют на своей поверхности различные Т-клеточные рецепторы и генерация которых не зависит от наличия на их поверхности CD Id [9, 11, 12]. Очевидным является то, что НКТ-клетки охватывают более гетерогенную популяцию Т-лимфоцитов, чем считалось изначально. Дальнейший анализ функций НКТ-клеток печени и исследование их иммунофенотипа и морфологии является крайне важным в оценке роли НКТ клеток в противоопухолевом иммунитете.
Целью исследования являлось изучение морфологических особенностей, иммунофенотипа и функциональной активности мононукле-арных клеток (МНК), выделенных из пораженной опухолевым процессом печени онкологичес- ких больных, в сравнении с мононуклеарами периферической крови (МНПК).
Материалы и методы
Характеристика обследованных больных. В исследование включены 10 больных в возрасте от 15 до 67 лет (мужчин - 7, женщин - 3) с опухолевым поражением печени (табл. 1).
Таблица 1
Распределение больных по локализации первичного очага
|
Локализация первичного очага |
Кол-во больных |
|
Гепатоцеллюлярный рак печени (ГЦР) |
2 |
|
Колоректальный рак |
5 |
|
Рак молочной железы |
1 |
|
Рак почки |
1 |
|
Полииеоплазия: рак сигмовидной кишки+меланома кожи спины (метастазы рака сигмовидной кишки в печень) |
1 |
Выделение МНПК. МНПК выделяли из стабилизированной гепарином (25 Ед/мл) периферической крови на градиенте фиколла («Pharmacia», плотностью 1,077 г/см3), центрифугированием при 400 g в течение 30 мин. Лимфоидные клетки, образовавшие интерфазное кольцо, собирали пипеткой и трехкратно отмывали в среде 199. После каждой отмывки в 10 -кратном объеме среды клетки осаждали центрифугированием при 200 g.
Выделение МНК из интактноп и парату-моральноп областей печени. Из фрагментов печени, полученных после резекции этого органа, была получена клеточная суспензия. Гепатоциты отделяли от МНК путем центрифугирования при 50 g в течение 5 мин. МНК выделяли с помощью центирифугирования в градиенте фиколла («Pharmacia», плотностью 1,077 г/см3) по описанной выше методике. Клетки отмывали 2 раза средой 199 и ресуспендировали в полной культуральной среде (RPMI-1640 с добавлением 10 % эмбриональной телячьей сыворотки, 2 мМ глютамина, стрептомицина с пенициллином по 5000 МЕ/мл).
Получение опухолевых клеток из опухолевого узла печени. Из метастатического узла получали суспензию опухолевых клеток, которую затем дважды отмывали в растворе Хен-кса и ресуспендировали в полной культуральной среде.
Цитологическое исследование. Из взвеси МНК, полученных из различных участков пораженной опухолью печени, готовили мазки, которые фиксировали метиловым спиртом и окрашивали эозином азуром-2 по Романовскому-Гимза, метиловым зеленым пиронином по Браше на РНК с контрольной обработкой РНКазой. Фотографирование меченых клеток и окрашенных мазков производили с использованием системы Axio Vision 4 (Carl Zeiss, Германия).
Цитотоксический тест. НК-активность определяли на линии К-562, клетки которой культивировали в полной культуральной среде при 37°С в атмосфере 4 % СО 2 . Для определения противоопухолевой активности (цитотоксичности) МНК печени использовали аутологические опухолевые клетки. Опухолевые клетки (1хЮ4 в 1 мл) инкубировали в культуральной среде с МНК (в соотношении 1:5) в плоскодонных 96-луночных микропланшетах (Costar, Франция) 18 часов. Затем в лунки добавлялся витальный краситель МТТ (Sigma, США) и по оптической плотности, измеряемой на мультискане МСС-340 (Labsystem, Финляндия), рассчитывали процент лизиса опухолевых клеток (процент цитотоксичности).
Проточная цитометрия (FACS-анализ). Определение экспрессии поверхностных маркеров МНК проводили при помощи моноклональных антител против соответствующих ан- I тигенов (Caltag Laboratories, США), результаты учитывали методом проточной цитофлюорометрии на проточном цитометре FACScan (Becton Dickinson, США). На МНК исследовали уровни экспрессии дифференцировочных антигенов CD3, CD4, CD8, CD16; активационных антигенов CD25, CD38, HLA-DR; молекул ад- I гезии CD57, CD58. Гейт (окно) популяции клеток устанавливали на основе комбинации прямого и бокового светорассеяния и размера клеток. При учете результатов подсчитывали 10.000 клеток в гейте. Статистическая обработка материала проведена при помощи программного пакета WinMDI 2.8.
Морфофункциональные особенности натуральных киллеров-Т-клеток больных
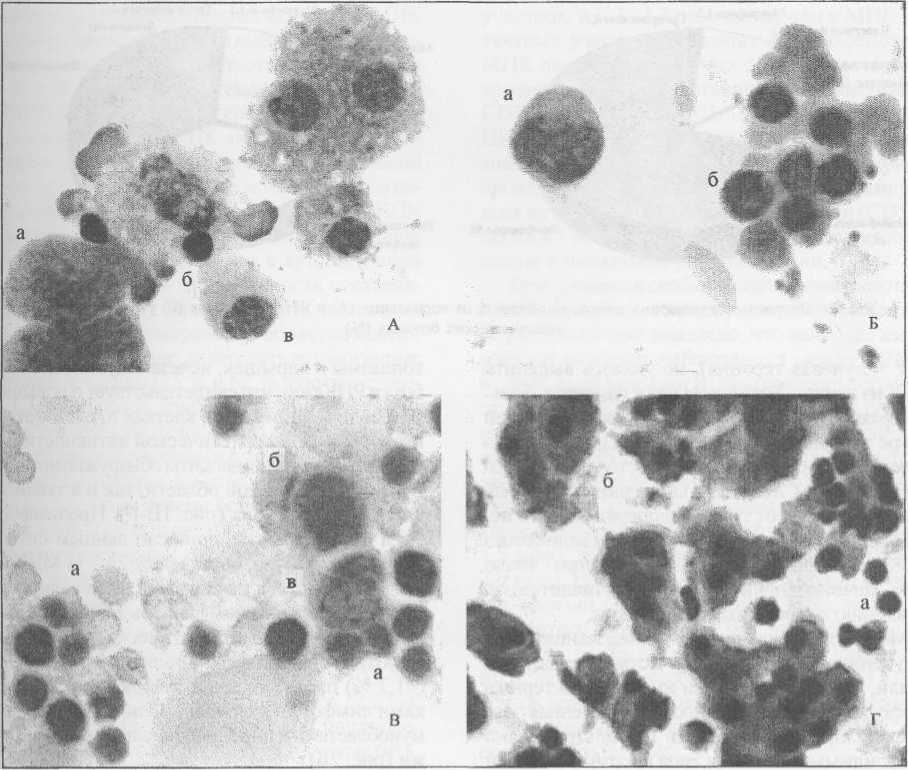
Рис. 1. НКТ в мазках взвеси клеток, взятых из интактного, параметастатического и метастатического участков печени больных:
A. Клетки интактного участка печени онкологического больного: а) гепатоциты, б) лимфоцит, в) макрофаг. Окраска эозин-азуром по Романовскому-Гимза, ок. 10, об. 100;
Б. Инфильтрация активированными лимфоцитами и властными формами параметастатической области печени онкологического больного: а) иммунобласт, б) активированные лимфоциты и пролимфоциты. Окраска эозин-азуром по Романовскому-Гимза, ок. 10, об. 100;
B. Пиронинофильные лимфоциты (а), властные формы (б) и дендритные клетки (в) в параметастатическом участке печени.
Окраска метиловым зеленым-пиронином по Браше, ок. 10, об. 100;
Г. Пиронинофильные лимфоциты (а), окружающие опухолевые клетки (б), в области метастаза печени. Окраска метиловым зеленым-пиронином по Браше, ок. 10, об. 40
Результаты и обсуждение
У первичных больных без предварительно проводимой в предоперационном периоде химио-и лучевой терапии удалось выделить 5 - 6x106 МНК из 1 см3 печени. При этом в паратумораль-ной области количество клеток в 1,5 - 2 раза пре- вышало их число в интактных участках печени. У пациентов, получивших в предоперационном периоде курс химио- и лучевой терапии, количество МНК печени составляло не более 1x10е МНК на 1 см3. У больной раком молочной железы с метастазами в печень, предварительно получившей 4 курса химиотерапии (по схеме
О.В. ЛЕБЕДИНСКАЯ, Ю.И. ПАТЮТКО, Д.А. ЗАБЕЖИНСКИЙ, Е.Н. КУЗОВЛЕВ, Н.К. АХМАТОВА

Рис. 2. Состав мононуклеарных клеток, выделенных из нормальных (А) и метастатических (Б) участков печени онкологических больных (%)
CAF + лучевая терапия), не уцалось выделить МНК из печени. В то время как у пациента, больного раком почки, получавшего перед операцией 1 курс иммунотерапии (Интрон А), количество выделенных из печени МНК составляло 10x106 МНК на 1 см3. Следовательно, количество МНК в печени зависит от типа предоперационного лечения: при химио- и лучевой терапии количество МНК минимальное, при иммунотерапии - число МНК печени значительно увеличивается по сравнению с нелечеными больными.
Морфо-гистохимические исследования МНК, полученных из различных участков печени, показали, что данные клетки имеют характерные морфологические особенности. Пораженная опухолевым процессом печень инфильтрирована лимфоидными клетками типа пролимфоцитов и иммунобластов (наиболее многочисленных в параметастатических областях), которые взаимодействуют с макрофагами и дендритными клетками (рис. 1А-Б). Среди мононуклеаров выявляется значительное количество лимфоцитов, имеющих яркую пиронинофильную окраску ци- топлазмы и ядрышек, исчезающую после обработки РНКазой, что свидетельствует о повышенном содержании РНК в клетках и, следовательно, их высокой синтетической активности. Пи-ронинофильные лимфоциты обнаруживаются как в параметастической области, так и в ткани метастатического узла (рис. 1В-Г). Пролимфоциты и иммунобласты, согласно данным цитологического анализа, составляют 24,7 % МНК интактных участков печени, при этом количество пиронинофильных лимфоцитов достигает 15,7 % (рис. 2А). В параметастатической области абсолютное большинство мононуклеарных клеток (91,3 %) представлено активированными клетками лимфоидного ряда: пролимфоцитами, иммунобластами и пиронинофильными лимфоцитами (рис. 2Б).
Сравнительное исследование цитотоксической активности МНК, выделенных из интактного и паратуморального участков печени, выявило, что при тестировании на НК-чувствительной линии К562 они не имеют достоверных отличий (табл. 2). В то же время по отношению к аутологичным
Таблица 2
Цитотоксическая и НК-активность МИК печени и периферической крови онкологических больных с метастазами в печень (%)
опухолевым клеткам киллерная активность МНК из паратуморальной области выше цитотоксической активности МНК интактного участка печени (62 % и 25 %, соответственно).
МНПК больных характеризуются достоверно меньшим уровнем НК-активности по сравнению с МНК печени и соответствуют степени цитотоксической активности мононуклеаров периферической крови здоровых доноров. МНПК больных практически не обладают киллерной способностью по отношению к аутологичным опухолевым клеткам (их активность составляет в среднем 11 %). При этом МНК интакгной и, особенно, паратуморальной областей печени способны эффективно лизировать аутологичные опухолевые клетки (25 % и 62 %, соответственно). Следовательно, наибольшую цитотоксическую активность по отношению к аллогенным и аутологичным опухолевым клеткам демонстрируют мононуклеары, выделенные из паратумо-ральных участков печени больных.
Сравнительное исследование иммунофено-типамононуклеарных лейкоцитов, выделенных из двух различных областей печени онкологических больных (табл. 3) показало, что процентное содержание клеток, экспрессирующих на своей поверхности дифференцировочные антигены CD4 (9,1 % и 10,4 %), CD8 (42,2 % и 50,9 %), CD3 (60,5 % и 79,9 %), CD16 (10,4 % и 12,2 %), примерно одинаково в интактном и паратумо-ральном участках. Однако следует отметить, что интенсивность флюоресценции при детектировании данных молекул на поверхности МНК, выделенных из параметастатических участков, в 1,2 -1,3 раза выше, чем у МНК интактных участков. Различия иммунофенотипа МНК двух исследованных областей печени по уровню экспрессии активационных антигенов CD25 (5,7 % и 6,6 %), CD38 (42,2 % и 35,9 %) и НК-маркера CD57 (31,9 % и 37,1 %) также незначительны. В то же время число мононукле-аров паратуморальной области, экспрессирующих на поверхности молекулы адгезии (CD58), почти в 3 раза превышает их процентное содержание в интактном участке печени.
При сравнении особенностей иммунофенотипа МНПК больных и мононуклеаров пораженной опухолью печени выявлено, что наиболее выраженные различия наблюдаются между МНПК и МНК, выделенными из паратуморального участка (табл. 3). Как следует из табл. 3 и гистограмм (рис. 3,4), у МНК пораженной метастазами печени по сравнению с мононуклеарными лейкоцитами периферической крови онкологических больных значительно повышены уровни экспрессии дифференцировочного маркера CD8 (в 1.5 раза), активационных антигенов CD38 (в 2.5 раза), НК-маркера CD57 (в 1,7 раза) и моле кул адгезии CD58 (в 4,6 раза). В то же время процентное содержание CD4+ клеток, напротив, у МНПК почти в 4 раза превышает таковую у МНК печени. Количество CD3+, CD 16+ и CD25+ клеток примерно одинаково как в популяции мо-нонуклеарных лейкоцитов крови, так и МНК, вы деленных из печени.
Таким образом, МНК печени онкологических больных по иммунологическому фенотипу и уровню НК-активности существенно отлича-
Таблица 3
Характеристика иммунологического фенотипа МНК, выделенных из печени и периферической крови онкологических больных
|
CD-маркер |
Уровень экспрессии антигенов на поверхности мононуклеарных лейкоцитов, % |
|||
|
Интактный участок печени(1) |
Паратуморальная область печени (2) |
Периферическая кровь (3) |
Достоверность различий между группами |
|
|
CD3 |
60,5±14,0 |
79,9±24,0 |
76,9±18,0 |
р|2> 0,05; р,3> 0,05; р2,> 0,05 |
|
CD4 |
9,1±1,7 |
10,4±4,4 |
36,6±13,0 |
р 12> 0,05; р „< 0,05; р2,< 0.05 |
|
CD8 |
42,2±4,7 |
50,9±12,0 |
35,0±12,0 |
Р u > 0,05; р ,3 > 0,05; р у > 0,05 |
|
CD16 |
10,4±4,2 |
12,2±1,1 |
19,1 ±6,0 |
|
|
CD25 |
5,7±1,7 |
6,6±1,4 |
4,5±1,6 |
|
|
CD38 |
42,2±12,0 |
35,9±4,3 |
13,8±2,7 |
р, > 0,05; р,3< 0,05; р23< 0,05 |
|
CD57 |
31,9±5,2 |
37,1 ±4,9 |
24,3±3,4 |
р|2> 0,05; р,3> 0,05; р„>0,05 |
|
CD58 |
24,0±9,0 |
71,5±19,0 |
15,6±3,8 |
р, <0,05;р,,>0,05;р,,>0,01 |
О.В. ЛЕБЕДИНСКАЯ, Ю.И. ПАТЮТКО, Д.А. ЗАБЕЖИНСКИЙ, Е.Н. КУЗОВЛЕВ, Н.К. АХМАТОВА h MNK h«pam2 СОЗ h MNK hapam2 CD6
li MNK hepam2 CD38
hMNKhepam2CD6B
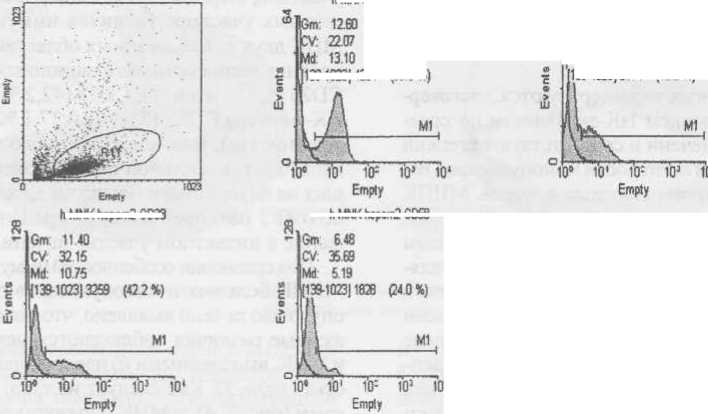
Рис. 3. Иммунологический фенотип МИК, выделенных из интактного участка печени онкологических больных (уровень экспрессии СОЗ, CD8, CD38, CD58)
139-102314264 60 5%)
Gm: 924
CV 32.16
Md. 8.20
139-1023] 2574 (422%)
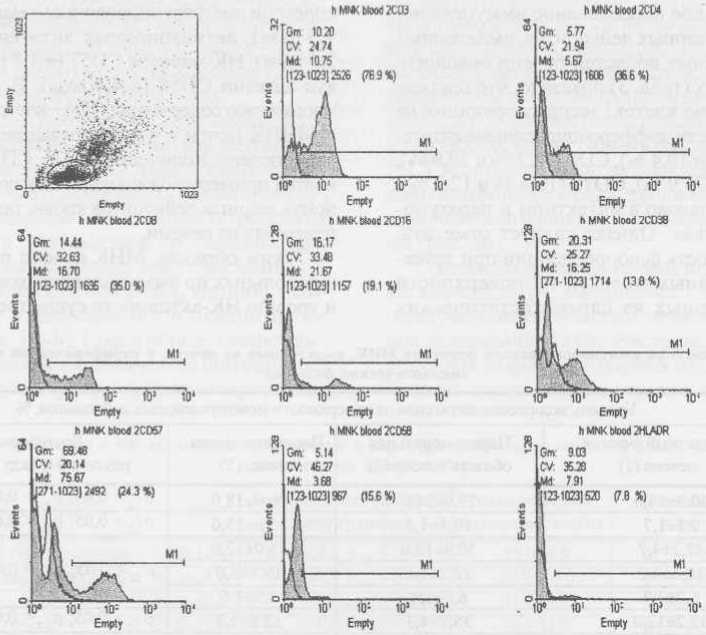
Рис. 4. Иммунологический фенотип МНК, выделенных из периферической крови онкологических больных (уровень экспрессии СОЗ, CD4. CD8, CD38, CD57, СО 58, HLA-DR)
ются от МНПК тех же больных. Исходя из наших данных, они являются преимущественно CD3+ Т-лимфоцитами, но, в отличие от МНПК, активно экспрессируют на своей поверхности антигены натуральных киллеров (CD57). Морфологически популяция МНК пораженной метастазами печени, особенно в паратумораль-ных областях, состоит в основном из молодых и синтетически активных клеток лимфоидного ряда, что свидетельствует о процессах бласт-трансформации, дифференцировки и активации лимфоцитов, приводящих, по-видимому, к формированию субпопуляции НКТ-клеток.
Эта субпопуляция лимфоцитов характеризуется высокой НК-активностью, повышенной экспрессией молекул адгезии (что обеспечивает их фиксацию в области поражения и взаимодействие с антигенпрезентирующими дендритными и с опухолевыми клетками), увеличенным количеством активационных антигенов на поверхности. Печень-ассоциированные лимфоциты обладают достоверно большей цитотоксической активностью по отношению к аутологичным опухолевым клеткам, чем лимфоциты периферической крови больных. Следовательно , результаты наших исследований подтверждают экспериментальные данные о наличии в пораженной опухолевом процессом печени особой субпопуляции НКТ-клеток, которые могут быть использованы для целей иммунотерапии онкологических заболеваний, осложненных метастазированием в печень [3].


