Морфологические изменения холедоха при стентировании по поводу механической желтухи
Автор: Лебедев С. С., Паклина О. В., Тинькова И. О., Греков Д. Н., Тавобилов М. М., Карпов А. А., Дроздов П. А., Маер Р. Ю.
Журнал: Московский хирургический журнал @mossj
Рубрика: Общая хирургия
Статья в выпуске: 2 (80), 2022 года.
Бесплатный доступ
Введение. Нами проведен сравнительный морфологический анализ состояния стенки холедоха при имплантации пластикового и нитинолового стента на различных строках после стентирования.Материалы и методы. В исследование включен 91 пациент, которому выполнена панкреатогастродуоденальная резекция по поводу периампулярной карциномы в отделении гепатопанкреатобилиарной хирургии Боткинской больницы с 2014 по 2020 годы. Из них 56 пациентов были ранее стентированы с использованием пластикового стента, 35 - нитинолового. Гистологическую структуру стенки холедоха исследовали в зависимости от вида стента (пластиковый или нитиноловый) и сроков его имплантации (14-30 сут., 31-60 сут., 61 и более суток).Результаты. При использовании обоих типов стентов в стенке ОЖП развиваются необратимые морфологические изменения, но характер их различен. При использовании пластиковых стентов изменения происходят во всех слоях стенки и характеризуются атрофией слизистой и фиброзированием протока. При металлических стентах в слизистой развиваются гиперпластические процессы, выраженность которых пропорциональна длительности нахождения стента в просвете ОЖП. Гиперплазированная слизистая протока прорастает стент, суживает или полностью обтурирует просвет протока, создавая дополнительные возможности для образования биопленок, при этом мышечный слой протока сохраняет свою структуру.Заключение. Время функционирования пластиковых стентов меньше нитиноловых, развивающиеся фиброзно-атрофические изменения стенки ОЖП при их имплантации меньше влияют на просвет протока и отток желчи, чем гиперпластические процессы при нитиноловых стентах, что делает обоснованным использование пластиковых стентов предпочтительным.
Пластиковый билиарный стент, нитиноловый билиарный стент
Короткий адрес: https://sciup.org/142234864
IDR: 142234864 | УДК: 006.617-089 | DOI: 10.17238/2072-3180-2022-2-35-42
Morphological changes in the choledochus during stenting for mechanical jaundice
Introduction. We have performed a comparative morphological analysis of the state of the choledochal wall when plastic and nitinol stent are implanted at different stages after stenting.Materials and methods. The study included 91 patients who underwent pancreatogastroduodenal resection for periampullary carcinoma at the Department of Hepatopancreatobiliary Surgery, Botkin Hospital from 2014 to 2020. Of these, 56 patients were previously stented using a plastic stent and 35 were stented using a nitinol stent. The histological structure of the choledochal wall was studied depending on the type of stent (plastic or nitinol) and the timing of its implantation (14-30 days, 31-60 days, 61 days and more).Results. When both types of stents are used, irreversible morphological changes develop in the ductus wall, but their nature is different. When plastic stents are used the changes occur in all layers of the wall and are characterized by mucosal atrophy and ductal fibrosis. With metal stents hyperplastic processes develop in the mucosa, the severity of which is proportional to the duration of the stent placement in the ductus lumen. Hyperplastic mucosa of the duct infiltrates the stent, narrows or completely obstructs the ductal lumen, creating additional opportunities for biofilm formation, while the muscular layer of the duct retains its structure.Conclusion. The functioning time of plastic stents is shorter than that of nitinol stents, the developing fibrotic-atrophic changes of the ductus wall when they are implanted have less influence on the ductus lumen and bile outflow than hyperplastic processes in nitinol stents, which makes reasonable the use of plastic stents preferable.
Текст научной статьи Морфологические изменения холедоха при стентировании по поводу механической желтухи
Билиарное стентирование является глубоко разработанным и высокоэффективным методом разрешения механической желтухи [1]. Однако срок функционирования билиарных стентов ограничен. Обструкция стента приводит к рецидиву механической желтухи и холангита, что существенно снижает качество жизни пациентов. В связи с этим, предпринималось большое количество исследований, направленных на увеличение времени функционирования билиарных стентов. Независимо от способа выполнения стентирования, все проведенные сравнительные исследования не дали значимых результатов в вопросе увеличения времени функционирования стента, кроме увеличения диаметра пластикового стента или использования саморасширяющегося металлического стента [2]. При этом направление научного поиска в основном было сосредоточено на разработке той или иной модификации билиарного стента. С другой стороны, вопрос о морфологических изменениях стенки холедоха и их влиянии на время функционирования стента крайне мало изучен.
Нами проведен сравнительный морфологический анализ состояния стенки холедоха при имплантации пластикового и нитинолового стента на различных строках после стентирования с целью определения возможных путей улучшения результатов билиарной декомпрессии.
Материал и методы
В исследование включен 91 пациент, которому выполнена панкреатогастродуоденальная резекция по поводу периампу- лярной карциномы в отделении гепатопанкреатобилиарной хирургии Боткинской больницы с 2014 по 2020 годы. Из них 56 пациентов были ранее стентированы с использованием пластикового стента, 35 – нитинолового. Среднее время стояния пластикового стента составило 76,5±2,7 сут. (от 3 до 145 сут.), нитинолового стента – 98,8±11,3 сут. (от 14 до 344 сут.).
Гистологическую структуру стенки холедоха исследовали в зависимости от вида стента (пластиковый или нитиноловый) и сроков его имплантации (14–30 сут., 31–60 сут., 61 и более суток). Данные о количестве исследованных гистологических образцов представлены в таблице 1. Хирургическое лечение после декомпрессии было выполнено на разных сроках, что позволило оценить динамику, характер и выраженность морфологических изменений.
При гистологическом исследовании соблюдали максимальную стандартизацию всех подготовительных и аналитических этапов с использованием линейки роботизированного оборудования (Microm International GMbH, Германия). Срезы для гистологического исследования толщиной 3 мкм окрашивали гематоксилином и эозином. Описательное исследование гистологических препаратов выполняли под микроскопом Axio Scope A1 (Carl Zeiss Microimaging GMbH, Германия). Основная часть морфологического исследования выполнена после создания электронной галереи изображений с помощью полуавтоматического сканера микропрепаратов Pannoramic® Flash Desk Dx (3DHISTOTECH, Венгрия), что позволяло максимально стандартизовать режимы морфометрического исследования. Использовалось увеличение сканирующего объектива х20.
Таблица 1
Количество исследованных гистологических препаратов в зависимости от вида стента и сроков его имплантации
Table 1
Number of investigated histological preparations depending on the type of stent and the timing of its implantation
|
Вид стента Type of stent |
Длительность стояния стента Stent retention time |
||
|
14–30 сут. 14–30 days |
31–60 сут. 31–60 days |
61 и более сут. 61 days and more |
|
|
Пластиковый plastic |
20 |
21 |
15 |
|
Нитиноловый nitinol |
23 |
4 |
8 |
Результаты исследования
В норме слизистая оболочка желчного протока формирует плоские складки и покрыта эпителием, идентичным по морфологии эпителию главного протока поджелудочной железы. В общем желчном протоке всегда присутствуют так называемые мешочки Биля – небольшие лунки эпителия, погруженные стенку протока. Дно мешочка обычно окружено и связано с группами маленьких, разветвленных или простых желез – перибилиарные железы. Перибилиарные железы выстланы кубовидным или низко-цилиндрическим муцин-содержащим эпителием и окружены уплотненной стромой. Для эпителия экстрапеченочных желчных протоков характерно наличие в клетках лизосом и включений желчных пигментов – это считается доказательством резорбтивной, то есть всасывательной, функции эпителия протоков. В эпителии нередко встречаются бокаловидные клетки. Как правило, их количество резко увеличивается при заболеваниях желчных путей, при этом также отмечается компенсаторная гиперплазия самих желез. Собственная пластинка желчных протоков богата эластическими волокнами, расположенными продольно и циркулярно. Характерное групповое расположение перибилиарных желез помогает микроскопически отличить общий желчный проток от главного протока поджелудочной железы, так как его дренирующие боковые ветви не окружены простыми железами.
При анализе гистологической структуры общего желчного протока (ОЖП) при стентировании выявлен ряд закономерностей. Патологические изменения в стенки общего желчного протока отражали хроническое воспаление, на первых этапах вызванное его длительной обструкцией, а после декомпрессии стентом, по сути, продолжительным нахождением вдавленного инородного тела (пластиково- го или металлического) в слизистую протока. Поэтому микроскопически оценивали не только характер и выраженность воспалительной инфильтрации, а также сохранность архитектоники слизистой, наличие эрозий, язв, участков гиперплазии, атрофию собственных желез протока, степень фиброзирования (склерозирования) его стенки (таблица № 2).
При сравнительном анализе морфологических изменений стенки ОЖП в группах до 30 суток следует отметить, что воспалительные процессы преобладали над фибропластическими, особенно при нитиноловых стентах. В данной группе ни в одном из проанализированных случаев не развился фиброз стенки протока. При пластиковых стентах фиброз всей стенки протока был отмечен только в 5/20 случаях, который сопровождался полной атрофией перибилиарных желез. Эрозии и язвы при выраженном воспалении были характерны для двух групп. При нитиноловых стентах отмечались гиперпластические процессы в слизистой, что объяснялось сетчатой структурой стента.
Например, при длительности стояния пластикового стента 14 дней (рис. 1) стенка ОЖП структурно была сохранена, воспалительные процессы преобладали над фибропластическими. Воспалительная инфильтрация носила лимфоплазмоцитарный характер и группировалась вокруг перибилиарных желез. Просветы части желез были расширены. Мышечный слой практически не вовлекался в воспаление и, как следствие, не подвергался разрушению. Несмотря на выраженность воспалительной инфильтрации, видимых язв слизистой не просматривалось. В прилежащей паренхиме поджелудочной железы отмечался отек междольковой соединительной ткани и коллапс части ацинусов.
Таблица 2
Гистологические изменения стенки общего желчного протока при стентах на разных сроках
Table 2
Histological changes of common bile duct wall with stents at different terms
|
Тип повреждения Type of injury |
Пластиковый стент Plastic stent |
Нитиноловый стент Nitinol stent |
|
14-30 сут. (N20) 14-30 days (N20) |
14-30 сут. (N23) 14-30 days (N23) |
|
|
Воспаление: Inflammation: выраженное expressed умеренное/слабое medium/weak |
15 5 |
22 1 |
|
Слизистая (эпителий): Mucosa (epithelium): эрозии/язвы erosions/ulcers |
20 |
15 |
|
0 |
7 |
|
|
гиперплазия hyperplasia |
5 |
0 |
|
атрофия желез glandular atrophy |
||
|
Фиброз: Fibrosis: |
||
|
нет или фокальный no or focal |
0 |
15 |
|
собственной пластинки слизистой intrinsic mucosal plate |
15 |
7 |
|
всей стенки про- |
5 |
0 |
|
тока |
||
|
the entire duct wall |
||
|
31–60 сут. (N 21) |
31–60 сут. (N 4) |
|
|
31–60 days (N 21) |
31–60 days (N 4) |
|
|
Воспаление: Inflammation: |
||
|
выраженное expressed |
16 |
4 |
|
умеренное/слабое medium/weak |
5 |
0 |
|
Слизистая (эпителий): Mucosa (epithelium): |
21 |
3 |
|
эрозии/язвы erosions/ulcers |
0 |
1 |
|
гиперплазия hyperplasia |
15 |
0 |
|
атрофия желез glandular atrophy |
Продолжение Таблицы 2
|
Фиброз: Fibrosis: |
0 |
4 |
|
|
нет или фокальный no or focal |
6 |
0 |
|
|
собственной пластинки слизистой intrinsic mucosal plate |
15 |
0 |
|
|
всей стенки протока the entire duct wall |
|||
|
61 сут. и более (N |
61 сут. |
и более (N 8) |
|
|
15) |
61 days |
or more (N |
|
|
61 days or more (N 15) |
15) |
||
|
Воспаление: Inflammation: |
|||
|
выраженное expressed |
5 |
7 |
|
|
умеренное/слабое medium/weak |
10 |
1 |
|
|
Слизистая (эпителий): |
|||
|
Mucosa |
|||
|
(epithelium): |
8 |
6 |
|
|
эрозии/язвы erosions/ulcers |
0 |
8 |
|
|
гиперплазия hyperplasia |
15 |
0 |
|
|
атрофия желез glandular atrophy |
|||
|
Фиброз: Fibrosis: нет или фокальный no or focal |
0 |
8 |
|
|
собственной пластинки слизистой |
3 |
0 |
|
|
intrinsic mucosal plate |
12 |
0 |
|
|
всей стенки протока the entire duct wall |
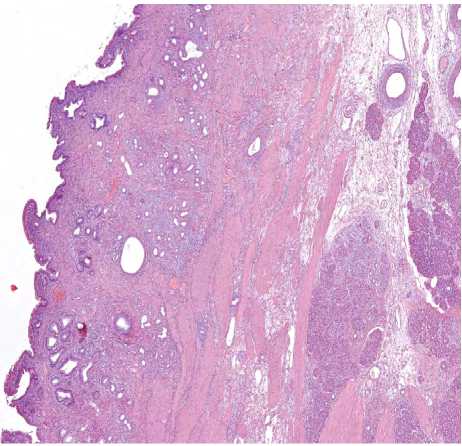
Рис. 1. Стенка ОЖП, пластиковый стент, длительность 14 дней: слизистая протока сохранена, отмечается эктазия собственных желез. Воспалительная инфильтрация преимущественно в слизистой, частично вовлекает мышечную оболочку. В прилежащей паренхиме признаки обструктивного панкреатита
Fig. 1. Common bile duct wall, plastic stent, duration 14 days: mucosa of the duct is preserved, ectasia of own glands is noted. Inflammatory infiltration predominantly in the mucosa, partially involving the muscularis.
In the adjacent parenchyma there are signs of obstructive pancreatitis
При сравнительном анализе морфологических изменений стенки ОЖП в группах от 31 до 60 суток следует отметить, что в группе нитиловых стентов воспалительные процессы также преобладали над фибропластическими и также не развивался фиброз всей стенки протока. При пластиковых стентах фиброз всей стенки протока был отмечен в 15/21 случаях и сопровождался полной атрофией перибилиарных желез. Эрозии и язвы при выраженном воспалении были характерны для двух групп.
Например, при длительности стояния пластикового стента 28 дней (рис. 2) стенка ОЖП была структурно изменена, за счет выраженного фиброза с атрофией слизистой и мышечного слоя. В данном случае фибропластические процессы преобладали над воспалением. Отмечалось полное исчезновение складок и мешочков слизистой. Просматривались единичные группы желез с метаплазированным высоким цилиндрическим эпителием. Мышечный слой замещался плотным коллагеновым фиброзом. Эрозии в слизистой носили неглубокий характер.
При сравнительном анализе морфологических изменений стенки ОЖП в группах от 61 суток и более следует отметить, что в группе нитиловых стентов, несмотря на продолжительность нахождения стента в протоке, воспалительные процессы преобладали над фибропластическими. При пластиковых стентах склероз всей стенки протока развился в 12/15 случаях и сопровождался полной атрофией перибилиарных желез. По мере склерозирования стенки воспалительные процессы уменьшались. Воспалительная инфильтрация носила подэпи- телиальный очаговый характер и была представлена лимфоцитами и плазматическими клетками.
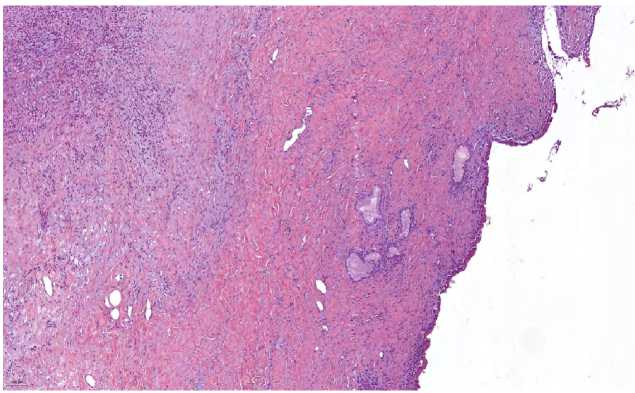
Рис. 2. Стенка ОЖП, пластиковый стент, длительность 28 дней: слизистая протока разрушена и атрофированная. Стенка полностью коллагенизирована. Скудная воспалительная инфильтрация в подэпителиальном слое
Fig. 2. Common bile duct wall, plastic stent, 28 days duration: the mucosa of the duct is destroyed and atrophied. The wall is completely collagenized. Scarce inflammatory infiltration in the subepithelial layer
В качестве примера, аналогичные изменения отмечали при пластиковом стенте длительностью 64 дня (рис. 3). В результате длительного стояния стента в стенке ОЖП сформировался пролежень с глубокой язвой и полным фиброзированием стенки протока. Следует отметить, что в данном случае прилежащая ацинарная ткань поджелудочной железы также подверглась атрофии и склерозу. Дно пролежня ОЖП полностью покрыто детритом.
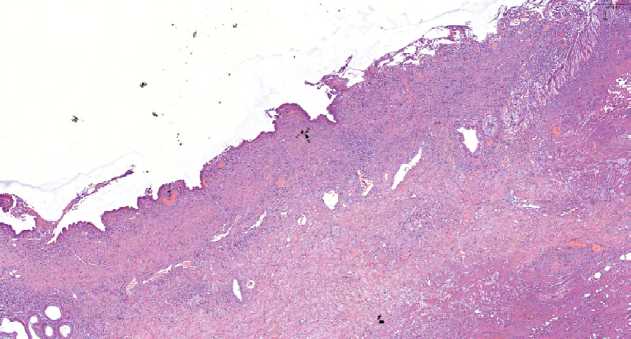
Рис. 3. Стенка ОЖП, пластиковый стент, длительность 64 дней: слизистая протока разрушена и атрофированная. Стенка полностью коллагенизирована.
Скудная воспалительная инфильтрация в подэпителиальном слое
Fig. 3. Common bile duct wall, plastic stent, 64 days duration: the mucosa of the duct is destroyed and atrophied. The wall is completely collagenized. Scarce inflammatory infiltration in the subepithelial layer
Вероятно, в процессе длительного стояния стента из пластика, между ним и стенкой ОПЖ формируются пустоты или «карманы», как результат изъязвления и уплотнения стенки протока. Подобные «карманы» заполнены детритом и желчью, что в свою очередь дополнительно способствует дальнейшему углублению сформированного пролежня в стенке, дальнейшей хронизации воспаления, атрофии морфофункциональных структур протока и развитию необратимого склероза стенки протока и прилежащей паренхимы железы.
В случаях стентирования холедоха при ампулярной карци- номе, в участках подрастания или врастания в стенку протока опухолевых желез, формировались глубокие клиновидные язвы, которые в свою очередь также создавали углубления или карманы, способствующие скоплению желчи в смеси с тканевым детритом между негибкой стенкой пластикового стента и изменяющейся в процессе воспаления и склерозирования стенкой ОЖП (рис. 4).
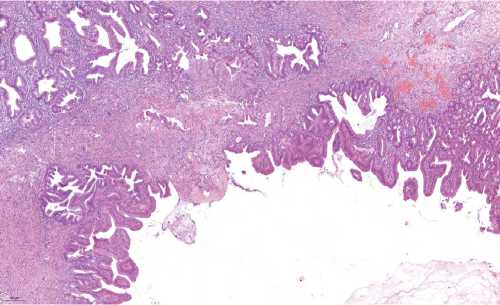
Рис. 4. Стенка ОЖП, пластиковый стент, длительность 49 дней: а) в протоке выраженное воспаление, вовлекающее все оболочки протока, фокус аденокарциномы подрастает со стороны паренхимы сдавливая проток с обеих сторон; б) клиновидная язва в области подрастания карциномы, заполненная детритом
Fig. 4. Common bile duct wall, plastic stent, 49 days duration: a) pronounced inflammation in the duct, involving all duct membranes, adenocarcinoma focus is growing from the parenchyma side squeezing the duct from both sides; b) wedge-shaped ulcer in the area of carcinoma overgrowth, filled with detritus
Макроскопически нитиноловые стенты плотно фиксированы к внутренней поверхности ОЖП. Благодаря сетчатой структуре стента в первую очередь сохраняется слизистая протока и, следственно, ее функция. Конечно, в условиях обструкции воспаление протоков является неотъемлемой частью всего патологического процесса протоковой системы, но при декомпрессии протоков важен не только факт оттока желчи, но и сохранность функции эпителиального покрова.
При нитиноловых стентах во всех исследованных случаях слизистая протока была сохранена на всех сроках хирургического вмешательства. При нитиноловых стентах архитектоника ОЖП была также сохранна. Поверхностный контур слизистой протока носил мозаичный характер, наряду с вдавленными участками просматривались гиперплазированные участки, выступающие в просвет сетки. Во всех случаях воспалительные процессы преобладали над фибропластическими. Воспалительная инфильтрация носила лимфоплазмоцитарный характер группировалась под эпителием и вокруг перибилиарных желез. Эрозивные изменения затрагивали только верхушки складок эпителия. Также псевдоэрозии слизистой могли возникнуть в результате ее механического повреждения при извлечении стента из протока в условиях выраженного воспаления (рис. 5).
При нитиноловых стентах мышечный слой порционно был вовлечен в воспаление без разрушения и склерозирования. В прилежащей паренхиме железы отмечалась только частичная атрофия ацинусов.
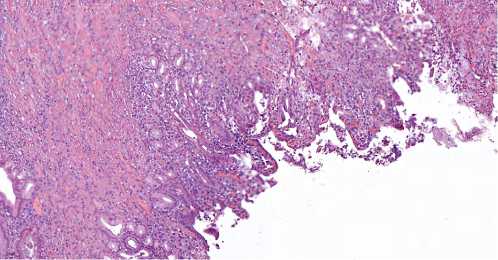
Рис. 5. Стенка ОЖП, нитиноловый стент, длительность 48 дней: воспалительная инфильтрация преимущественно в слизистой, перибилиарные железы сохранены и гиперплазированы Fig. 5. Common bile duct wall, nitinol stent, 48 days duration: inflammatory infiltration predominantly in the mucosa, peribiliary glands preserved and hyperplasia
Обсуждение
В многочисленных исследованиях морфологическим изменениям стенки ОЖП при его стентировании тем или иным типом стента не уделяли особого внимания. В клинической практике наибольшее значение при дренировании желчных путей имеет вероятность окклюзии стента, в результате образования биопленки или бактериальной колонизации, а также возможность его санации и замены при длительном стоянии. Поэтому, исследователи сосредоточились на изменениях конструкции стента, различных покрытиях, разработке антирефлюксного клапана, а также длине и положении стента в холедохе. Проведенные исследования не дали значимых результатов в вопросе увеличения времени функционирования стента, кроме имплантации пластикового стента большего диаметра или использования саморасширяю-щегося стента. Гораздо меньше внимания в научной литературе уделено структурным изменениям стенки ОЖП при инплантации билиарных стентов. Очевидно, что морфологические изменения в стенки протока отражают общепатологические реакции тканей на импланты: воспаление, изъязвления, грануляции или фиброз, неясна только динамика изменений во времени и их выраженность. Экстрапанкреатическая система желчных протоков долгое время считался довольно простой системой, предназначенной для транспортировки желчи. Наличие многочисленных периби-лиарных желез, расположенных вместе с протоковой системой, не находило должной интерпретации [1]. Y. Nakanuma полагает, что ПБЖ, выделяя специфические панкреатические ферменты (α-амилазу, трипсин и липазу), способны принимать участие в переваривании белков и липидов и играть важную роль в физиологии жёлчи [2]. Недавние исследования подчеркивают функцию перибилиарных желез как дополнительной ниши стволовых клеток-предшественников гепатобилиарной системы, играющих огромную роль в ее регенерации [3]. Уникальная способность стволовых клеток перибилиарных желез дифференцироваться как в клетки жёлчных протоков, так и в клетки печени и поджелудочной железы может быть связана с тем, что в ходе эмбрионального развития эпителиальные клетки этих органов имеют общее происхождение из эпителия двенадцатиперстной кишки [4].
Согласно полученным данным, фибропластические и атрофические изменения стенки общего желчного протока были более выражены при использовании пластикового стента. В результате анализа микроскопических изменений стенки холедоха выявлено, что на первых двух неделях преобладают признаки хронического или острого воспаления, а ближе к 4 неделям начинает формироваться фиброз стенки с атрофией слизистой и мышечного слоя. Площадь фиброзных изменений находится в прямой зависимости от длительности нахождения имплантированного пластикового стента в просвете общего желчного протока.
В случаях использования нитиноловых стентов в стенке холедоха гиперпластические процессы преобладали над фиброзными, сохранялись все слои и компоненты стенки протока до 50 дней и более, при этом хроническое воспаление в слизистой носило персистирующий характер. Данный факт возможно объяснить сетчатой структурой стента и, как следствие, сохранением резервных клеток перибилиарных желез, которые в свою очередь участвуют в регенерации слизистой протока, поддерживая ее эпителий в функциональном состоянии. Прорастание нитинолового стента слизистой холедоха не защищает его внутреннюю поверхность от образования биопленок или колонизации бактерий, а также от окклюзии его просвета, но защищает от полного фиброзирования всех слоев ОЖП как это происходит при использовании пластикового стента. Однако процесс гиперплазии слизистой холедоха напрямую зависит от длительности нахождения в его просвете непокрытого саморасширяющегося стента. И можно смело утверждать, что через 60 суток гиперплазия слизистой носит необратимый характер и может способствовать окклюзии стента (как путем механического сужения просвета, так и вторично – за счет образования биопленки). Степень гипертрофии слизистой может быть разной и, по всей видимости, возможно, связана с индивидуальными особенностями организма.
Заключение
Таким образом, понимание морфологических изменений стенки ОЖП позволяет нам утверждать, что с ними также мо- гут быть связаны процессы, которые способствуют окклюзии билиарных стентов. При использовании обоих типов стентов с течением времени в стенке ОЖП развиваются необратимые морфологические изменения, но характер их различен. При использовании пластиковых стентов основные метаморфозы происходят во всех слоях стенки и характеризуются атрофией слизистой и фиброзированием протока, по сути проток превращается в фиброзную «трубку», сохраняя при этом просвет для оттока желчи. При металлических стентах в слизистой развиваются гиперпластические процессы, выраженность которых пропорциональна длительности нахождения стента в просвете ОЖП. Гиперплазированная слизистая протока прорастает стент, сужает или полностью обтурирует просвет протока, создавая дополнительные возможности для образования биопленок, при этом мышечный слой протока сохраняет свою структуру.
Все это позволяет сделать вывод о том, что несмотря на то, что время функционирования пластиковых стентов короче в сравнении с нитиноловыми, развивающиеся фиброзно-атро фические изменения стенки ОЖП при их имплантации меньше влияют на просвет протока и отток желчи, чем гиперпластические процессы при нитиноловых стентах, что делает обоснованным использование пластиковых стентов предпочтительным.
Список литературы Морфологические изменения холедоха при стентировании по поводу механической желтухи
- Boulay BR, Parepally M. Managing malignant biliary obstruction in pancreas cancer: choosing the appropriate strategy. World J Gastroenterol., 2014, № 20(28), рр. 9345-9353. https://doi.org10.3748/wjg.v20.i28.9345.
- Шабунин А.В., Тавобилов М.М., Лебедев С.С., Карпов А.А. Механизмы окклюзии билиарных стентов и возможные способы ее профилактики. Хирургия. Журнал им. Н.И. Пирогова, 2020. № 5. С. 70-75.
- Nakanuma Y, Hoso M, Sanzen T, Sasaki M. Microstructure and development of the normal and pathologic biliary tract in humans, including blood supply. Microsc Res Tech., 1997, № 15, рр. 552-570.
- Carpino G., Cardinale V., Onori P. et al. Biliary tree stem/progenitor cells in glands of extrahepatic andintraheptic bile ducts: an anatomical in situ study yielding evidence of maturational lineages. J. Anat., 2012, № 220(2), рр. 186-199.
- Lanzoni G, Cardinale V, Carpino G. The hepatic, biliary, and pancreatic network of stem/progenitor cell niches in humans: a new reference frame for disease and regeneration. Hepatology, 2016, № 64, рр. 277-286.
- Carpino G., Cardinale V., Onori P. et al. Biliary tree stem/ progenitor cells in glands of extrahepatic andintraheptic bile ducts: an anatomical in situ study yielding evidence of maturational lineages. J. Anat., 2012, № 220(2), рр. 186-199.


