Морфологические изменения элементов гистогематического барьера слизистой оболочки полости рта при красном плоском лишае
Автор: Акмалова Г.М., Мусина Ляля Ахияровна, Чуйкин Сергей Васильевич
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 2 т.24, 2016 года.
Бесплатный доступ
Гистологическими и электронно-микроскопическими методами установлено, что при красном плоском лишае в слизистой оболочке полости рта выявляются патологические изменения эпителия с деструкцией базальной мембраны и склероз собственной пластинки слизистой с разрушением элементов гистогематического барьера в виде редукции сосудистого русла и атрофии малых слюнных желез и их протоков.
Красный плоский лишай, гистогематический барьер, слюнные железы
Короткий адрес: https://sciup.org/143177103
IDR: 143177103
Morphological histohematic barrier element changes of the mouth mucous membrane in case of lichen Rubber planus
It was established by histological and electron-microscopical methods that there had been revealed pathological changes of the epithelium in the mouth mucous membrane in case of lichen rubber planus. Those changes were chatacterized of the basal membrane destruction and sclerosis of proper mucous plate followed by the destruction of the histohematic barrier elements in the form of the bloodstream reduction and atrophy of minor salivary glands and their ducts.
Текст научной статьи Морфологические изменения элементов гистогематического барьера слизистой оболочки полости рта при красном плоском лишае
Введение. Красный плоский лишай (КПЛ) – это хроническое воспалительное заболевание многофакторной природы, поражающее покровные ткани - кожу и слизистые оболочки, в том числе и полости рта [1, 2, 3]. Эрозивно-язвенные формы КПЛ слизистых рассматриваются как преканцерозы [4, 5]. При воспалительных заболеваниях одним из важнейших звеньев па- тогенеза являются изменения гемато - тканевых отношений, направленных на восстановление нарушенного гомеостаза, важную роль в котором выполняют гистогематические барьеры (ГГБ). Известно, что в слизистой оболочке ротовой полости также благодаря ГГБ происходит избирательный направленный обмен веществ, в том числе, и микроэлементов между кровью и внутренним содержимым слюнных желез [6]. Несомненно, переход метаболитов, медиаторов, ферментов, гормонов через ГГБ должен зависеть и от функциональных и морфологических нарушений составляющих его компонентов [7]. Подробных исследований по выявлению структурных изменений всех элементов, входящих в ГГБ, при КПЛ слизистой оболочки полости рта не проводилось. Цель исследования - выявить особенности морфологических изменений элементов гистогематического барьера слизистой оболочки полости рта при красном плоском лишае.
Материал и методы исследования. У 29 пациентов с эрозивно-язвенной формой красного плоского лишая слизистой оболочки полости рта исследовали биопсии тканей с пораженных участков (с диагностической целью с согласия пациентов). Кусочки тканей фиксировали в 10% растворе забуференного формалина по Лилли, обезвоживали и заливали в парафин по стандартной методике. Гистологические срезы окрашивали гематоксилином и эозином. Изучали и фотографировали под световым микроскопом DMD 108 (Leica, Германия).
Для электронно-микроскопического изучения кусочки тканей фиксировали в растворе 2% глютарового альдегида на фосфатном буфере Миллонига (рH 7,2-7,4) с постфиксацией в 1% растворе четырехокиси осмия на том же буфере. Обезвоживали и заливали в эпон-812 по общепринятой методике. Ультратонкие срезы получали на ультрамикротоме («LKB-III», Швеция), контрастировали 2% водным раствором уранилацетата и раствором цитрата свинца по Рейнольдсу. Срезы изучали в электронном микроскопе «JEM-1011» (JEOL, Япония) при увеличении от ×2500 до ×10000.
Результаты исследования и их обсуждение. Известно, что морфологический субстрат ГГБ в слизистой оболочке полости рта составляют эндотелиальные клетки капилляров, секреторные клетки малых слюнных желез, эпителиальные клетки выводных протоков слюнных желез, сопровождающие их миоэпителиальные клетки, а также внеклеточный матрикс собственной пластинки слизистой из коллагеновых и эластических волокон, заполненный гелеподобным веществом, во многом определяющим транспортные процессы в интерстициальном пространстве [6]. Анализ гистологических препаратов биопсий пациентов при КПЛ и результаты электронной микроскопии выявили множественные признаки нарушения избирательной проницаемости и активного транспорта веществ, вследствие изменения структуры составляющих элементов ГГБ слизистой оболочки полости рта.
Нельзя игнорировать при КПЛ нарушение структуры покрывающего слизистую оболочку эпителиального слоя, выполняющего барьерную функцию. Кроме разрушения межклеточных контактов между эпителиальными клетками были выявлены выраженные патологические изменения базальной мембраны, заключающиеся в разрыхлении, во фрагментации или полной ее деструкции (рис. 1). В зонах разрушения базальной мембраны эпителиальный слой полностью отрывался от стромальной пластинки.
Сохранившаяся зона базальной мембраны под базальными клетками эпителия представляла собой участки тонкофибриллярного вещества в виде неравномерных полос умеренной электронной плотности. Базальные клетки в норме играют роль камбиальных элементов эпителия и обеспечивают прочную связь между эпителием и подлежащей собственной пластинкой слизистой. На препаратах как результат компенсаторной реакции, выражающейся в пролиферативной активности и ускоренной дифференцировке эпителиоцитов, выявлялась атипичная стратификация эпителия (рис. 2).
В цитоплазме эпителиальных клеток отмечались дистрофические изменения в виде вакуолизации митохондрий. В шиповидных клетках увеличивалось количество тонофиламентов и рибосом, появлялось значительное количество кератогиалиновых гранул, указывающих на нарушение экзоцитоза, обеспечивающего барьерную функцию эпителия. Межклеточные контакты полностью нарушались, эпителиальные клетки, разъединяясь, теряли свои характерные формы
(рис. 3). На границе шиповатого и базального слоев встречались единичные клетки Лангерганса, мигрирующие трансэпителиально сегментоядерные лейкоциты и лимфоциты, формирующие локальные группы иммунокомпетентных клеток. Выявлялись признаки акантолиза. Здесь же определялись скопления лимфоцитов вперемежку с эритроцитами.
Исследовать непосредственно основную часть концевых секреторных отделов малых слюнных желез, анатомически находящихся в мышечной оболочке щеки, не представилось возможным. Стараясь не причинить пациентам большие повреждения тканей, а особенно мышечных слоев, маленьких размеров (1х1х1мм) биоптаты были взяты для исследования с поверхностных слоев слизистой оболочки. Единичные слюнные железы, выявляющиеся до мышечной оболочки, непосредственно в собственной пластинке слизистой, были атрофированы, отделены друг от друга прослойками плотной соединительной ткани (рис. 4). Секреторные клетки желез четко не дифференцировались, а большинство их ядер были сморщены, находились в стадии пикноза.
Остальные элементы, входящие в состав ГГБ, это эндотелиоциты сосудов, эпителиальные клетки, выстилающие выводные протоки слюнных желез, сопровождающие их миоэпителиальные клетки и внеклеточный матрикс собственной пластинки слизистой, также имели выраженные изменения. В собственной соединительнотканной пластинке слизистой оболочки определялись признаки разрыхления и разволокнения базальной мембраны сосудов, отек сосудистой стенки, а также периваскулярные отеки. Выявлялись грубые нарушения сосудистого барьера, это геморрагическое пропитывание стромы, кровоизлияния, полиморфная клеточная инфильтрация. Определялось множество клеток: лимфоцитов, плазматических клеток, секреторных и фагоцитарных макрофагов, тучных клеток, фибробластических клеток разной степени зрелости. Признаки нарушения микроциркуляции проявлялись также в расширении или сужении просвета капилляров за счет выбухания эндотелиоцитов в просвет сосуда (рис. 5). Большинство эндотелиоцитов выглядели гиперхромными, ядра были нехарактерные с сильно изрезанными краями. В цитоплазме часто определялись вакуолизация и деструкция митохондрий, появлялось большое количество микровыростов цитоплазмы в результате сокращения эндотелиоцитов, увеличивалось количество остаточных телец в их цитоплазме.
В отдельных слюнных протоках выстилающие эпителиальные клетки были набухшими, между ними и миоэпителиальными клетками определялись отечные участки (рис.6). В других
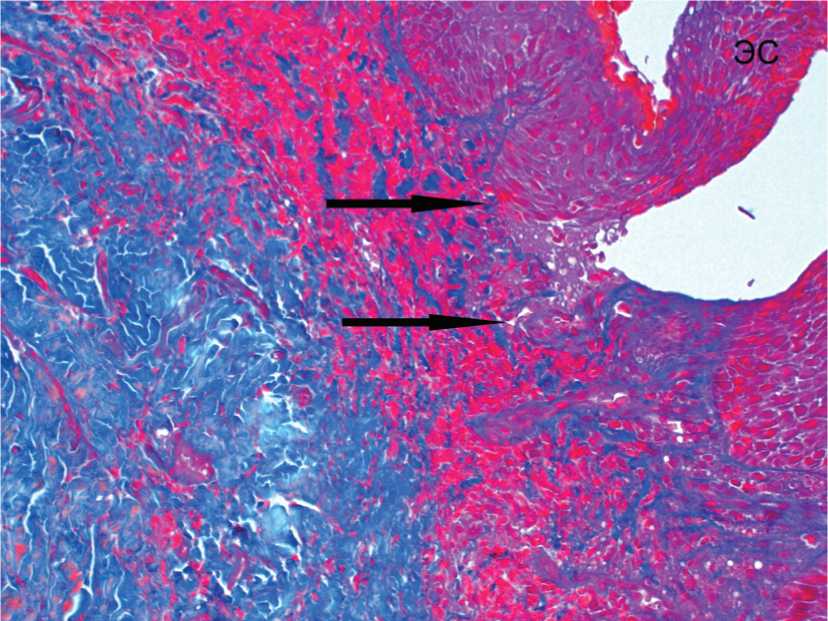
Рис. 1. Разрушение базальной мембраны (↑) и отделение эпителиального слоя (ЭС) от собственной пластинки слизистой оболочки полости рта при КПЛ. Биопсия. Пациентка Ф. Окраска по Маллори. Ув. 200.
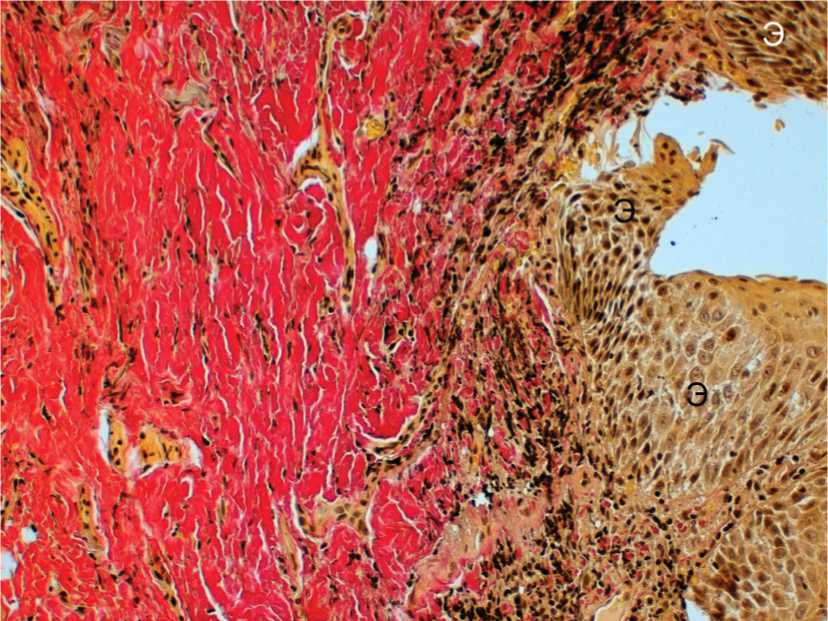
Рис. 2. Атипичная стратификация эпителия (Э) слизистой оболочки полости рта при КПЛ. Биопсия. Пациентка Ф. Окраска по Ван-Гизону. Ув. 200.
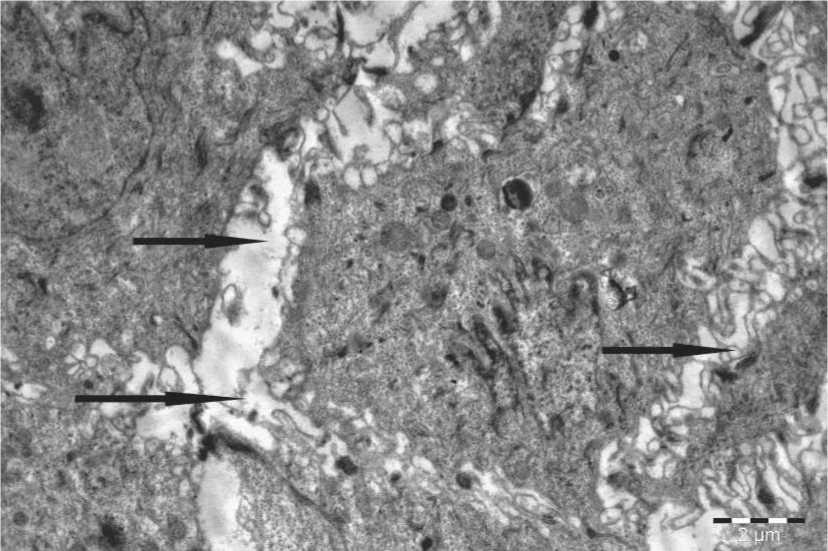
Рис. 3. Нарушение межклеточных контактов (↑) между эпителиальными клетками в слизистой оболочке полости рта при КПЛ. Биопсия. Пациентка Ф. Электронная микрофотография.
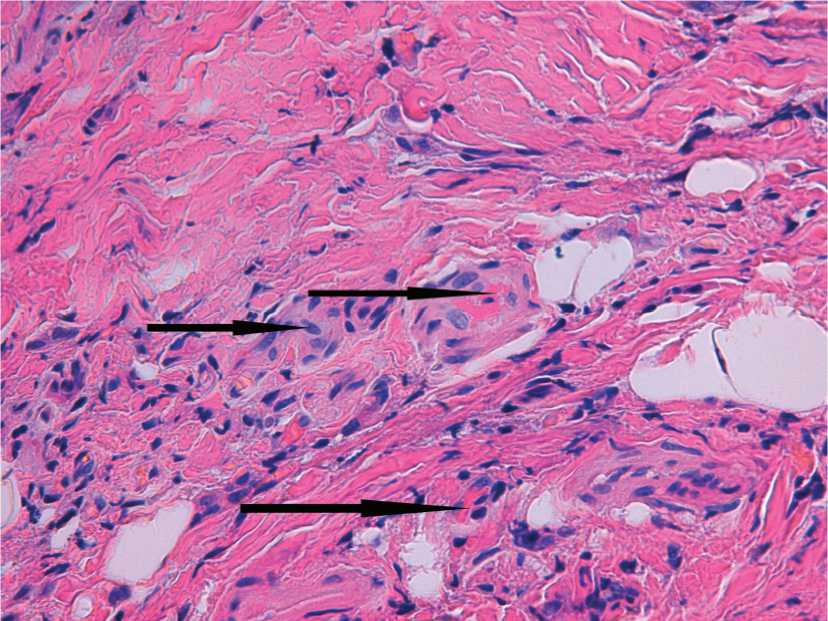
Рис. 4. Атрофирующиеся концевые отделы малых слюнных желез (↑) между прослойками соединительной ткани в слизистой оболочке полости рта при КПЛ. Биопсия. Пациентка Ф. Окраска гематоксилином и эозином. Ув. 200.
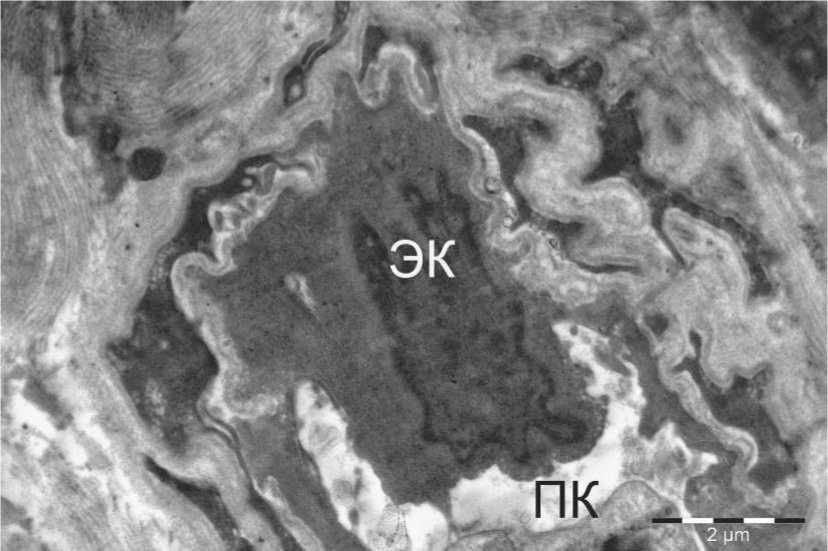
Рис. 5. Сужение просвета капилляра (ПК) за счет выбухания эндотелиоцита (ЭK) в собственной пластинке слизистой оболочки полости рта при КПЛ. Биопсия. Пациентка Ч. Электронная микрофотография.
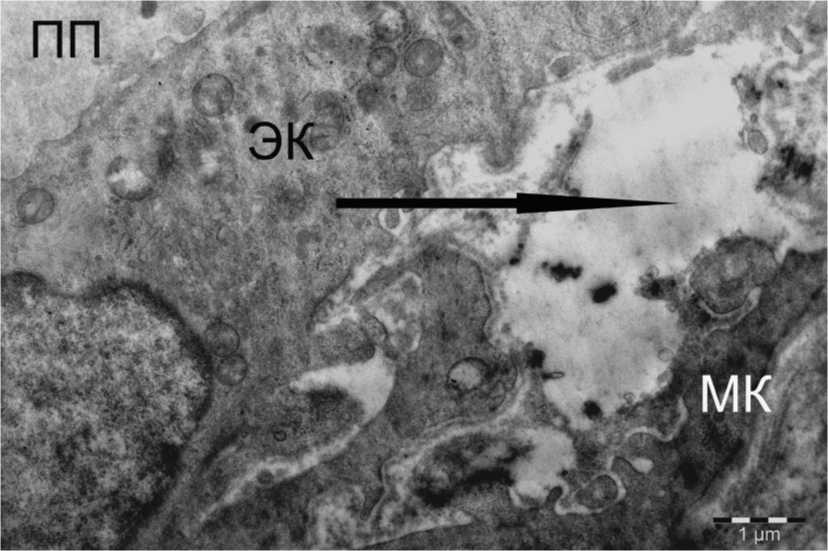
Рис. 6. Отек (↑) между выстилающей проток эпителиальной клеткой (ЭК) и миоэпителиальной клеткой (МК) в собственной пластинке слизистой оболочки полости рта при КПЛ. ПП – просвет протока. Биопсия. Пациентка Т. Электронная микрофотография.
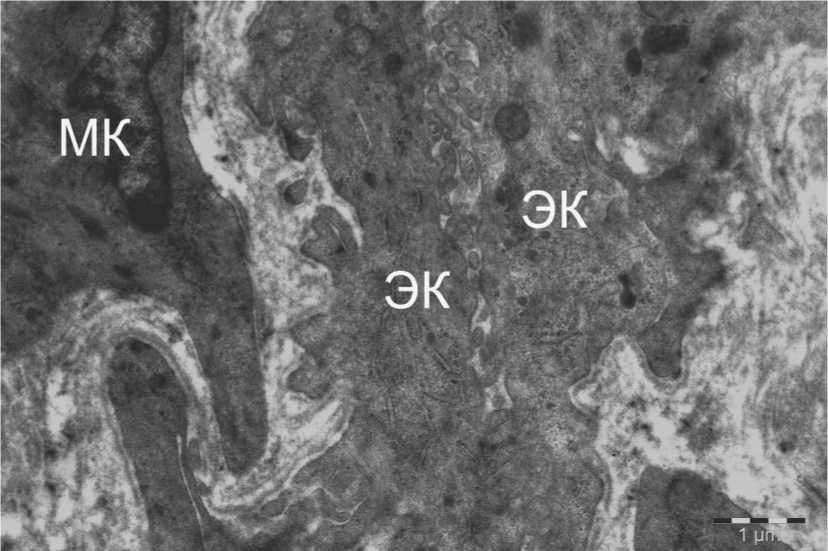
Рис. 7. Сужение просвета слюнного протока с формированием атипичных выростов (↑) цитоплазмы эпителиальных клеток (ЭК) в просвет в собственной пластинке слизистой оболочки полости рта при КПЛ. МК -миоэпителиальная клетка Биопсия. Пациентка Т. Электронная микрофотография.
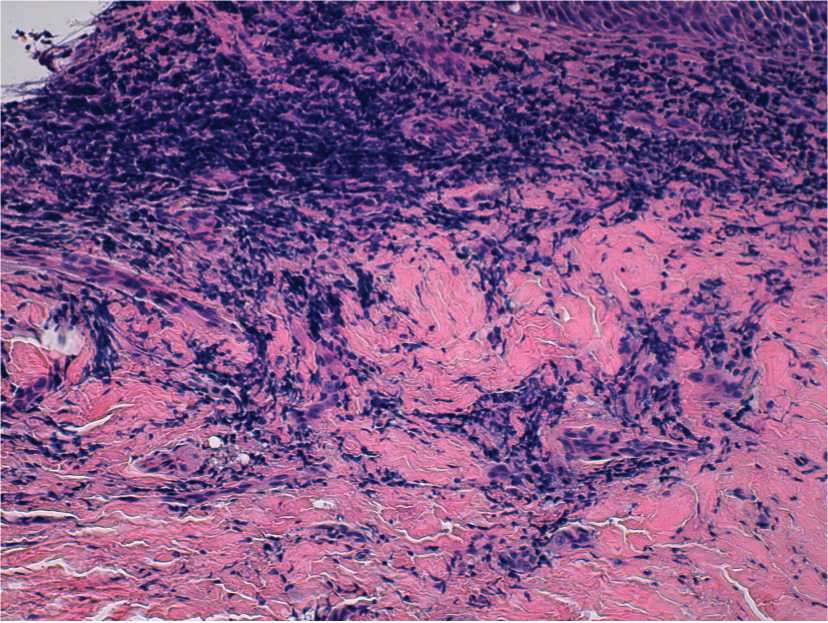
Рис. 8. Склерозирование соединительнотканной пластинки слизистой олочки полости рта при КПЛ. Биопсия. Пациентка Ф. Окраска гематоксилином и эозином. Ув. 100.
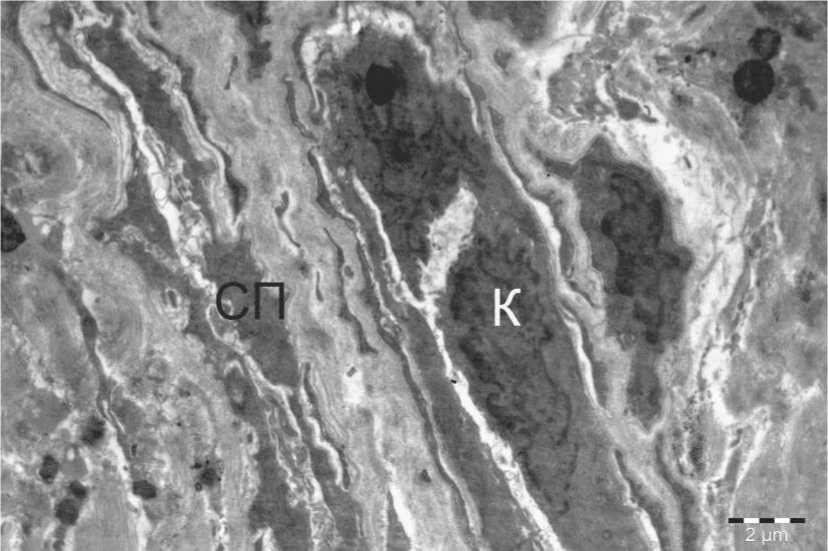
Рис. 9. Кровеносный сосуд (К) и слюнной проток (СП) с признаками атрофии в склерозированной ткани собственной пластинки слизистой оболочки полости рта. Биопсия. Пациентка Ф. Электронная микрофотография.
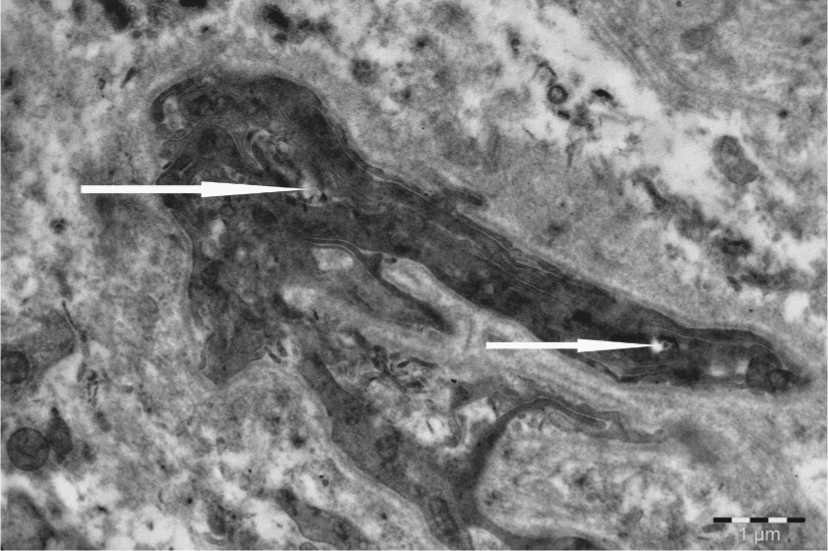
Рис. 10. Полное сужение просвета сосуда (↑) в склерозированной ткани собственной пластинки слизистой оболочки полости рта. Биопсия. Пациентка Ф. Электронная микрофотография.
протоках резко сужались просветы, а эпителиальные клетки в них формировали множественные атипичные для них выросты цитоплазмы, которые слущивались в просвет (рис.7). Цитоплазма эпителиальных клеток выглядела гиперхромной, также как и у миоэпителиальных клеток вокруг них. Миоэпителиоциты теряли «корзинчатую» форму, становились более вытянутыми и узкими, ядра в них сильно уменьшались в размерах, отдельные сморщивались.
В условиях сосудисто-тканевой проницаемости и пропитывания соединительной ткани плазменными белками, в условиях деструкции волокнистых структур и сложных межклеточных коопераций, ведущих к развитию воспалительных процессов хронического характера, обычно возникает внеклеточный диспротеиноз, обязательно влекущий за собой склероз соединительной ткани, проявляющийся как адаптивно-компенсаторная реакция направленная на восстановление нарушенного гомеостаза в тканях [8]. Подобные признаки процесса склерозирования собственной пластинки слизистой оболочки полости рта выявлялись и на гистологических препаратах биопсий при ПКЛ (рис.8). На ультраструктурном уровне соединительная ткань стромы имела вид, характерный для грубой рубцовой ткани. Коллагеновые волокна были беспорядочно и довольно плотно упакованы вперемежку с большим количеством фибробластических клеток разной степени зрелости. Аморфного основного вещества между фибриллами было меньше, чем в норме.
В склерозированной строме слизистой оболочки полости рта при КПЛ многие сосуды гиали-низировались, подвергались атрофии, также как и близлежащие слюнные протоки (рис.9). Эпителиальные клетки, выстилающие стенки слюнных протоков, уплотнялись, были осмиофильными. Многие атрофированные сосуды и слюнные протоки превращались в узкие трубочки с резко суженным просветом (рис.10).
Результаты проведенных морфологических исследований указывают на то, что при КПЛ нарушение структуры большинства составляющих элементов ГГБ, а именно - редукция сосудистого русла, атрофия малых слюнных желез и их протоков, склеротические изменения стромы собственной пластинки слизистой оболочки полости рта, ведут к снижению транспорта электролитов и компонентов плазмы в эпителиальный слой слизистой, и являются причиной дистрофических и деструктивных изменений тканей в области поражения. По комплексу патоморфологических проявлений описываемых процессов в слизистой оболочке полости рта, сводящихся к деструкции базальной мембраны и акантолизу, выраженной лимфоцитарной и фибробластической инфиль- трации стромы и эпителия, компенсаторной пролиферации эпителиоцитов и компонентов экстрацеллюлярного матрикса, приводящих к дизрегуляции в эпителиально-стромальных взаимоотношениях, КПЛ можно рассматривать как местное проявление системной аутоиммунной реакции. При этом, несомненно, разрушение структурных элементов ГГБ является одним из ключевых звеньев патогенеза заболевания.
Заключение.
Таким образом, при КПЛ выявляются патологические изменения эпителия с деструкцией базальной мембраны и собственной пластинки слизистой оболочки полости рта с разрушением элементов ГГБ. Нарушение сосудисто-тканевой проницаемости и геморрагическое пропитывание стромы с развитием воспалительных процессов хронического характера приводят к склерозу соединительнотканной пластинки слизистой оболочки, сопровождающегося редукцией сосудистого русла, атрофией малых слюнных желез и их протоков.
Список литературы Морфологические изменения элементов гистогематического барьера слизистой оболочки полости рта при красном плоском лишае
- Munde A.D. Demographic and clinical profile of oral lichen planus: A retrospective study / A.D.Munde, R.R. Karle, P.K.Wankhede, S.S.Shaikh, M.Kulkurni //Contemp. Clin.Dent. - 2013. - № 4. - Р.181-185.
- Payeras M.R. Oral lichen planus: Focus on etiopathogenesis Review/M.R.Payeras, K.Cherubini, M.A.Figueiredo, F.G. // Salum. Archives of Oral Biology. - 2013. -Vol. 58, № 9. - Р.1057-1069.
- Srinivas K. Oral lichen planus - Review on etiopathogenesis / K. Srinivas, K. Aravinda, P.Ratnakar, N. Nigam, S.Gupta //Natl. J. Maxillofac.Surg. - 2011. - №2. - Р.15-16
- Shirasuna K. Oral lichen planus: Malignant potential and diagnosis Review/K.Shirasuna // Oral Science International. - 2014. - Vol.11, № 1. - P. 1-7.
- Sugerman P.B. Oral lichen planus: causes, diagnosis and management/ P. B. Sugerman, N.W. Savage // Aust. Dent. J. - 2002. - Vol.47, №4. -P.290-297.
- Петрович Ю.А. Гематосаливарный барьер/Ю.А. Петрович, Р.П. Подорожная, С.М. Киченко// Российский стоматологический журнал. - 2004. - № 4. - С. 39-45.
- Биохимия тканей и жидкостей полости рта: учебное пособие/Т.П. Вавилова. - М.: ГЭОТАР-Медиа, 2012. - 208 с.
- Шехтер А. Б. Воспаление, адаптивная регенерация и дисрегенерация (анализ межклеточных взаимодействий) / А.Б. Шехтер, В.В.Серов // Архив патологии. - 1991. - Т.53, №7. -С.7-14.


