Морфологические изменения кровеносного русла пищевода при компенсированном алкогольном циррозе печени
Автор: Куликов С.В., Углова П.Е.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Статья в выпуске: 1 (69), 2021 года.
Бесплатный доступ
С целью изучения морфологических изменений сосудов пищевода при алкогольном циррозе печени, а также определения значения этих изменений в развитии компенсации нарушенной гемодинамики были исследованы кусочки нижней трети пищевода от 25 мужчин в возрасте 25-50 лет. В качестве контроля использовали материал от 10 лиц такого же возраста, погибших в результате травм. С помощью ряда гистологических, морфометрических и статистических методик показано, что при развитии венозной гиперемии в пищеводе «включаются» реакция Бейлиса - Остроумова и вено-артериальная реакция. Кроме того, в сосудистом бассейне пищевода происходит образование компенсаторных регуляторных структур в виде мышечно-фиброзных и фиброзных пучков вен, а также пучков интимальной мускулатуры и мышечно-эластических сфинктеров артерий. Кроме того, часть артерий этого органа ремоделируются в «замыкающие». Вся эта сосудистая перестройка противодействует резкому нарастанию венозного давления в области портокавального анастомоза пищевода, тем самым уменьшая риск развития аррозивного пищеводного кровотечения.
Алкогольный цирроз печени, пищевод, сосуды, морфология, компенсация
Короткий адрес: https://sciup.org/142227860
IDR: 142227860 | УДК: 616.13/.16:616.329:[616.36-004:616.89-008.441.13]
Morphological changes in the blood bound of the esophagus with compensated alcoholic cirrhosis of the liver
In order to study morphological changes in esophageal vessels in alcoholic cirrhosis of the liver, as well as to determine the significance of these changes in the development of compensation for impaired hemodynamics, pieces of the lower third of the esophagus were examined from 25 men aged 25-50 years. As a control, we used material from 10 persons of the same age who died as a result of injuries. With the help of a number of histological, morphometric and statistical techniques, it has been shown that with the development of venous hyperemia in the esophagus, the Beilis-Ostroumov reaction and the veno-arterial reaction are turned on. In addition, the formation of compensatory regulatory structures in the form of muscle-fibrous and fibrous bundles of veins, as well as bundles of intimate muscles and muscular-elastic sphincters of the arteries occurs in the vascular system of the esophagus. In addition, some of the arteries of this organ are remodeled into “guard” ones. All this vascular remodeling counteracts a sharp increase in venous pressure in the area of the portocaval anastomosis of the esophagus, thereby reducing the risk of developing arrosive esophageal bleeding.
Текст научной статьи Морфологические изменения кровеносного русла пищевода при компенсированном алкогольном циррозе печени
Алкогольный цирроз характеризуется перестройкой структуры печени и ее ангиоархитектоники, что приводит к формированию синдрома портальной гипертензии с открытием портокавальных анастомозов [2, 7, 8, 9].
Наиболее важную роль в патологии играет соединение непарной и полунепарной вен с венозными коллекторами пищевода и кардии, подвергающиеся варикозной трансформации и разрыву, что ведет к острой кровопотере [1, 2, 3, 6].
Между тем у некоторых больных с циррозом печени сравнительно долго не появляется пищеводного кровотечения, что, вероятно, связано с возникновением более выраженных компенсаторных сосудистых реакций, препят- ствующих появлению фатального осложнения. Следует отметить, что в литературе довольно подробно представлены особенности ремоделирования вен пищевода в условиях портальной гипертензии [1, 2, 3].
В то же время несколько поверхностно описываются их компенсаторные структуры, а также нет полной ясности в трактовке механизмов, обеспечивающих коррекцию изменившегося гемодинамического режима [1, 3].
Кроме того, ангиоморфологами вовсе не уделяется внимание состоянию артерий этого органа в условиях венозного застоя пищевода [1, 3]. Однако артериальное русло способно эффективно корригировать нарушения гемодинамики в органах и тканях [4, 5].
ЦЕЛЬ РАБОТЫ
Определить патоморфологические изменения сосудистого бассейна пищевода при циррозе печени алкогольного генеза, а также определить механизмы сосудистой адаптации к возникающим дисциркуляторным расстройствам в органе.
МЕТОДИКИ ИССЛЕДОВАНИЯ
С целью изучения патоморфологии кровеносного бассейна пищевода исследован секционный материал, полученный в патологоанатомическом отделении ГБУЗ ЯО «Областная клиническая больница», от 15 мужчин в возрасте от 25 до 50 лет, имевших цирроз печени алкогольной этиологии, который подтверждался анамнестическими данными (стаж употребления алкоголя более 10 лет) и морфологическими маркерами. Основными причинами смерти явились лобарная пневмония, острый панкреатит, острое нарушение мозгового кровообращения и другие заболевания, не связанные с осложнениями цирроза печени в виде пищеводного кровотечения. У них наблюдались минимальные проявления портальной гипертензии в виде незначительного накопления асцитической жидкости и отсутствия варикозно-расширенных вен передней брюшной стенки.
Таким образом, в подобных случаях алкогольный цирроз печени фигурировал в патологоанатомическом диагнозе в рубрике «сопутствующее», либо «фоновое» заболевание, как одно из проявлений хронической алкогольной интоксикации. В качестве контроля использовали аутопсийный материал из танатологического отделения ГУЗ ЯО «Ярославское областное бюро судебно-медицинской экспертизы» от 10 мужчин такого же возраста, умерших от причин насильственного характера. Фрагменты нижней части пищевода фиксировали в 10%-м нейтральном формалине и заливали в парафиновые блоки. В работе был использован комплекс гистологических и морфометрических методик. В частности, применяли окраску гематоксилин-эозином, по Масону и фукселином по Харту. Морфометрическое исследование кровеносного русла осуществляли окуляр-микрометром типа МОВ-1-15х, с помощью которого измеряли следующие параметры: наружный диаметр сосудов (попавших в поперечный срез), толщина стенки вен (в участках наибольшей толщины), средней оболочки (медии) артерий, мышечно-фиброзных пучков вен, а также интимы артерий крупного и среднего калибра. Артерии и вены на уровни ветвления были разделены в соответствии с ранее разработанной методикой [4, 5]. В дополнение к этому подсчитывали численность артерий, обладавших ин-тимальной мускулатурой и сфинктерами. Цифровой материал обрабатывали с помощью программы STATISTICA с использованием t-критерия Стьюдента. Полученные данные считали достоверными, если ошибка средней не превышала 5 % (р < 0,05).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
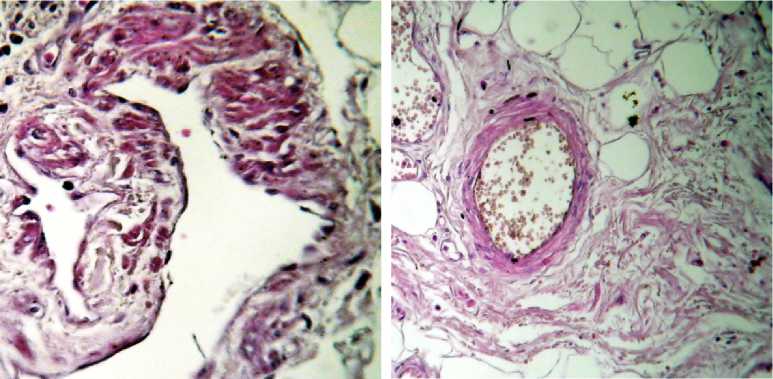
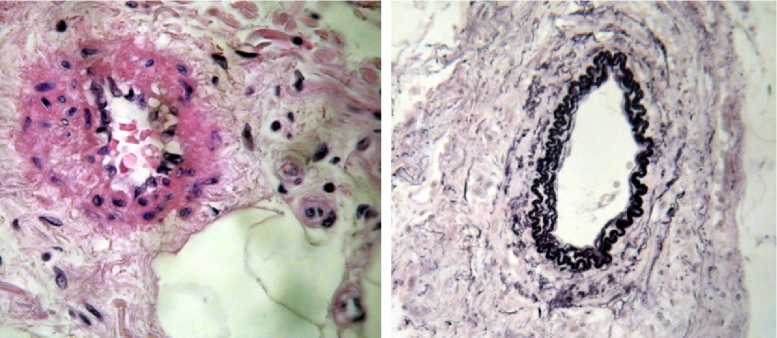
При алкогольном циррозе печени слизистая оболочка пищевода имела серый цвет с синюшным оттенком, который придавали извилистые, узловатые вены, формировавшие хорошо заметный сосудистый рисунок. Многослойный плоский эпителий слизистой оболочки этого органа на большом протяжении подвергался атрофии, реже утолщался в результате гиперплазии клеток базального слоя, образующих акантотические тяжи и проникающие в соединительную ткань собственной пластинки, нередко формируя выраженную эпителиальную сеть. Клетки эпителия часто находились в состоянии гидропической дистрофии с переходом в балонную дистрофию. В слизистой оболочке выявлялись очаговые густые лимфоцитарные инфильтраты, являющиеся морфологическим признаком хронического эзофагита. Собственная пластинка слизистой оболочки и подслизистая основа пищевода имели значительно большую толщину, чем в контрольной серии, за счет отека соединительной ткани, расширения лимфатических коллекторов и венозной гиперемии. В полнокровных венах отмечались признаки стаза и нередко тромбоза. Следует отметить, что среди расширенных вен встречались сосуды, стенки которых оказывались утолщенными в результате наличия крупных гладкомышечных клеток и многочисленных эластических волокон. Кроме того, часть венозных стенок оказывалась утолщенной неравномерно, вследствие разрастания колагеновых волокон или мощных пучков из миоцитов (рис. см. а). Артерии сопротивления, к которым относятся мелкие артерии и артериолы, также имели гипертрофированную стенку, по сравнению с контролем, из-за большего количества лейомиоцитов в их средней оболочке (рис. см. б, в). В дополнение к этому внутренний диаметр артерий пищевода уменьшался, эндотелиальные клетки интимы принимали вытянутую форму, располагаясь перпендикулярно к просвету, а их цитоплазма становилась светлой, вакуолизированной, что указывает на наличие гидропической дистрофии (рис. см. в).
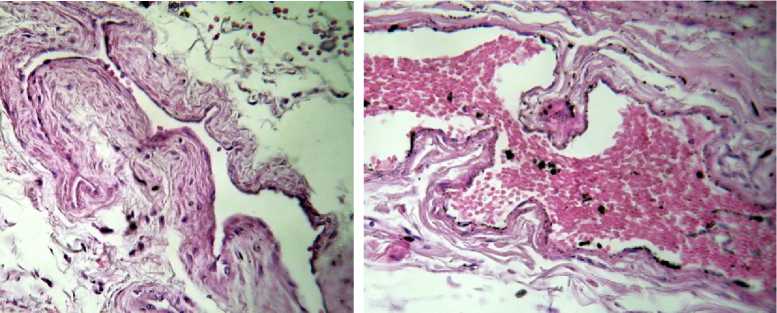
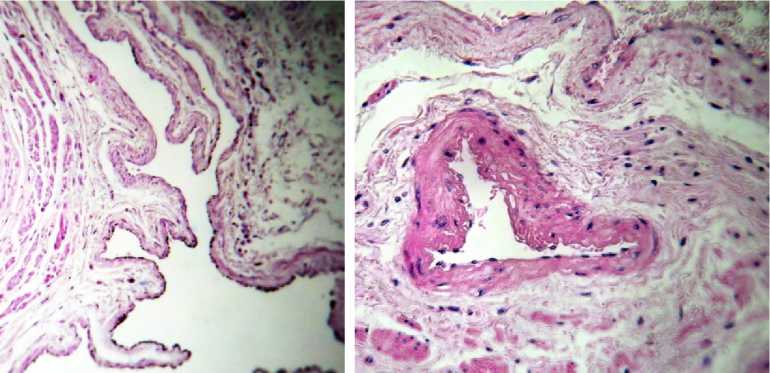
В кровеносном русле пищевода, кроме описанных выше структурных изменений, появлялись особые регуляторные структуры, практически не встречающиеся в контрольной серии, играющие важную роль в компенсации нарушенного кровообращения. К ним относятся: мышечно-фиброзные и фиброзные пучки вен, а также интимальная косопродольная мускулатура и мышечно-эластические сфинктеры артерий. Мышечно-фиброзные пучки имели вид уплощенных, широких выступов, состоящих из переплетающихся гладкомышечных клеток и коллагеновых волокон, приводящих к значительному сужению просвета, который принимал извилистые и щелевидные очертания (рис. см. д) Фиброзные образования, в одних случаях, имели округлую или неправильную форму, располагаясь на тонкой ножке, напоминая, полипы (рис. см. е). Они были образованы в результате инвагинации периваскулярной соединительной ткани и части стенки вены в просвет, который на продольном срезе приобретал «зубчатоооб-разный» контур (рис. 1 е). Такие вены принимали характерную для рассматриваемой патоло- гии варикозную трансформацию вследствие чередования участков сужения и расширения. В других случаях фиброзные структуры имели большую длину, углубляясь в просвет на достаточно большие расстояния, и довольно причудливую форму, раздваиваясь на вершинах и имея сходство с «щупальцами» (рис. см. ж).
Микроскопическое исследование показало, что в интиме артерий, кроме мощного продольного слоя гладких мышц, располагающегося по всему периметру, визуализировались группы гладкомышечных клеток, образующих пучки, выступающие в просвет сосуда (рис. см. з). Внутренняя эластическая мембрана, в зоне формирования таких миогенных образований, разделялась на отдельные волокна, окутывая их сверху и снизу. Кроме того, в устьях боковых ветвей, отходящих от более крупных артериальных стволов, встречались особые мышечные структуры – мышечно-эластические сфинктеры, представляющие собой валики, покрытые расслоенной эластической мембраной. Оба вида артериальных мышечных структур изнутри были выстланы эндотелием.
а б
в г
д
е
ж
з
Рис. Морфологические изменения кровеносного русла пищевода в контроле (б) и при компенсированном алкогольном циррозе печени (а, в–з). Окраска: а, б, в, д–з – гематоксилин-эозином, г – фукселином по Харту.
Увеличение: а–з – об. 20, ок. 10:
а – неравномерное утолщение стенки мелкой вены (слева) и вены среднего калибра (справа) за счет образования пучков из гладких миоцитов; б – нормальная мелкая артерия; в – стенка мелкой артерии с резким утолщением средней оболочки за счет гиперплазии гладких миоцитов; сужение просвета с «частоколообразной» ориентацией эндотелия, находящегося в состоянии гидропической дистрофии; г – усиленная складчатость и расщепление внутренней эластической мембраны мелкой артерии на несколько пластинок; д – несколько уплощенных мышечно-фиброзных пучков, вдающихся в просвет вены среднего калибра с резким сужением ее просвета; е – фиброзные полиповидные образования, значительно выступающие в просвет крупной вены, образованные в результате инвагинации периваскулярной соединительной ткани;
ж – «щупальцеобразные» тонкие фиброзные пучки, глубоко вдающиеся в просвет крупной вены;
з – два пучка интимальной гладкой мускулатуры мелкой артерии
С помощью морфометрического исследования объективизированы описанные выше качественные изменения кровеносного бассейна пищевода в условиях портальной гипертензии, свойственной алкогольному циррозу печени.
В частности, толщина медии артерий крупного и среднего калибра увеличивалась – в 1,4 (р < 0,001) раза, а мелкого калибра и артериол, относящихся к сосудам сопротивления, – в 1,3 (р < 0,05) раза, по сравнению с контролем. Толщина интимы крупных и средних артерий так же, как и медия, увеличивалась в 1,3 (р < 0,05) раза. В дополнение к вышеперечисленному численность артерий, имеющих интимальные пучки и сфинктеры, увеличивалось в 3 раза, по сравне- нию с контрольной серией. Толщина стенки крупных, средних и мелких вен возрастала в 2 (р < 0,001) раза, а венул – в 1,5 (р < 0,001) раза по отношению к контролю. Аналогичная тенденция отмечалась и в отношении толщины мышечно-фиброзных пучков крупных вен – она возрастала в 2 (р < 0,001) раза.
ЗАКЛЮЧЕНИЕ
Наши исследования позволили установить, что при алкогольном циррозе печени, в условиях портальной гипертензии, наблюдается венозная гиперемия нижней трети пищевода, отражающая сброс крови в портокавальном направлении, которая предопределяет развитие выраженных морфологических изменений веноз-ного и артериального русла этого органа и образование в них разнообразных регуляторных структур. В частности, в ответ на переполнение пищеводных вен кровью происходит рефлекторное сокращение гладких миоцитов их стенки с последующим развитием гипертрофии. Данные изменения являются сущностью универсальной реакции Бейлиса – Остроумова, направленной на предотвращение венозной регургитации. Кроме того, в венах пищевода происходит образование регуляторных структур, способных активно или пассивно участвовать в движении крови к правым камерам сердца. Речь идет о мышечно-фиброзных и фиброзных пучках. Первые структуры, обладая гладкой мускулатурой, выполняющую контрактильную функцию, обеспечивают активное продвижение венозной крови. Вторые, способствующие варикозной трансформации, в силу отсутствия миоцитов, не играют активной роли, но, вероятно, выполняют роль клапанов, предотвращающих ретроградную циркуляцию. Кроме ремоделирования вен пищевода, вызванного повышением давления крови в них, отмечается структурная перестройка и артерий, которая выражается, во-первых, в развитии гипертрофии гладких миоцитов, их средней оболочки, а во-вторых, в формировании продольного, так называемого «функционального», ин-тимального слоя.
Сокращение гладкомышечных элементов медии сопровождается повышением тонуса артерий с увеличением сопротивления кровотоку. Артерии с мощным продольным слоем гладких миоцитов называются «замыкающими», вследствие того, что сокращение интимальных мышечных клеток приводит к окклюзии их просвета, полностью блокируя кровоток на каком-либо участке органа.
Указанные изменения артерий, в ответ на венозный застой, лежат в основе, так называемой вено-артериальной реакции. Она является трафаретной и возникает рефлекторно в тех случаях, когда наблюдается увеличение венозного давления, которое инициирует повышение сопротивления кровотоку с уменьшением притока артериальной крови [4,5]. Так же, как в венах, в артериях пищевода образуются специальные сосудистые регуляторы: пучки инти-мальной мускулатуры и мышечно-эластические сфинктеры. Функциональная роль их заключается в коррекции нарушенного кровообращения и перераспределения потоков артериальной крови. Появление пучков, а также продольной мускулатуры в интиме связывают с миграцией гладких миоцитов из медии в интиму через «окна» во внутренней эластической мембране, возникающей также стандартно при различных гемодинамических растройствах [5].
Данная структурная перестройка в кровеносном русле пищевода сопровождается адаптацией к гемодинамическим расстройствам, противодействует резкому нарастанию венозного давления, тем самым уменьшая риск развития аррозивного пищеводного кровотечения.
Список литературы Морфологические изменения кровеносного русла пищевода при компенсированном алкогольном циррозе печени
- Волков, А. В. Морфологические особенности перестройки венозного и лимфатического русел пищевода в условиях портальной гипертензии. -Текст: непосредственный / А. В. Волков, Г. М. Рынгач, В. А. Головнев // Бюллетень СО РАМН. - 2004. - Т. 111, № 1. - С.115 - 119.
- Гарбузенко, Д. В. Патогенез портальной гипертензии при циррозе печени. - Текст: непосредственный / Д. В. Гарбузенко // Рос. журн. гастроэнтерол., гепатол., колопроктол. - 2002. - Т. 12, № 5. - С. 23 - 29.
- Патоморфологические и морфометрические особенности венозного русла кардиоэзофагальной зоны в условиях портальной гипертензии. - Текст: непосредственный / А. В. Жура, В. В. Климович, Т. Э. Владимирская, И. А. Швед // Вестник хирургической гастроэнтерологии. - 2010. - № 2. -С. 20 - 24.
- Куликов, С. В. Структурные преобразования мочевого пузыря и его сосудистой системы у мужчин пожилого и старческого возраста. - Текст: непосредственный / С. В. Куликов, И. С. Шорманов, А. С. Соловьев // Экспериментальная и клинческая урология. - 2020. - № 2. - С. 124 - 130.
- Шорманов, С. В. Изменение строения печени при экспериментальной коарктации аорты и стенозе легочного ствола. - Текст: непосредственный / С. В. Шорманов, Ю. В. Новиков, С. В. Куликов // Морфология. - 2014. - Т. 146, № 6. - С. 72 - 76.
- Arakawa, M. Pathomorphology of esophageal and gastric varices. - Direct text / M. Arakawa, T. Masuzaki, K. Okuda // Semin. Liver Dis. - 2002. -Vol. 22, № 1 - P. 73 - 82.
- Franchis, R. Evolving consensus in portal hypertension; Report of the Baveno IV Consensus Workshop on methodology of diagnosis and therapy in portal. hypertension. - Direct text / R. Franchis // J. Hepatology. - 2005. - Vol. 43, № 1. - P. 167 - 176.
- The role of non-invasive markers in predicting esophageal varicose veins and variceal bleeding in patients with alcoholic liver cirrhosis from central India. - Direct text / H. G. Kothari, S. J. Gupta, N. R. Gaikwad [et al.] // Turk J. Gastroenterol. -2019. - Vol. 30, № 12. - P. 1036 - 1043.
- Purdad, F. Manifestations and complications associated with liver cirrhosis. - Direct text / F. Purdad // Curr Med Res Opin Review. - 2015. - Vol. 31, № 5. -P. 925 - 937.


