Морфологические изменения нейронов гранулярного слоя зубчатой извилины при стресс-индуцированной депрессии и возможность фармакологической коррекции новым производным глутаминовой кислоты
Автор: Экова М.Р., Смирнов А.В., Тюренков И.Н., Волотова Е.В.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Статья в выпуске: 1 (65), 2020 года.
Бесплатный доступ
Были проведены морфометрическое исследование изменений в гранулярном слое зубчатой извилины крыс в возрасте 12 месяцев при моделировании депрессии и оценка возможности фармакологической коррекции выявленных изменений нейроглутамом. В гранулярном слое зубчатой извилины определяли: площади ядер, цитоплазмы и перикарионов нейронов, ядерно-цитоплазматическое отношение, относительные площади ядер, цитоплазмы и перикарионов нейронов, относительную площадь нейропиля. У крыс с экспериментальной депрессией, по сравнению с контрольной группой, отмечалось увеличение относительной площади нейропиля и снижение всех остальных морфометрических параметров. Применение нейроглутама продемонстрировало корректирующее действие.
Зубчатая извилина, депрессия, стресс, нейрон, крыса
Короткий адрес: https://sciup.org/142225938
IDR: 142225938 | УДК: 616-091.8
Morphological changes of the neurons of the granular layer of the geared sign in stress-induced depression and the possibility of pharmacological correction by the new derivative of glutamin acid
Were conducted morphometric study of changes in the granular layer of the dentate gyrus of rats at the age of 12 months when modeling depression and assessing the possibility of pharmacological correction of the revealed changes with neuroglutam. In the granular layer of the dentate gyrus, the following areas were determined: areas of nuclei, cytoplasm and pericarion of neurons, nuclear-cytoplasmic ratio, relative areas of nuclei, cytoplasm and pericarions of neurons, relative area of neuropil. In rats with experimental depression, compared with the control group, an increase in the relative area of the neuropil and a decrease in all other morphometric parameters were noted. The use of neuroglutam demonstrated a corrective effect.
Текст научной статьи Морфологические изменения нейронов гранулярного слоя зубчатой извилины при стресс-индуцированной депрессии и возможность фармакологической коррекции новым производным глутаминовой кислоты
Депрессия относится к наиболее распространенным психическим заболеваниям, характеризуется высокой частотой рецидивов и низким уровнем ответа на лечение антидепрессантами [8]. Одной из основных причин депрессии является хронический стресс. Однако молекулярные механизмы, лежащие в основе патофизиологии депрессии до конца не изучены. Согласно нейрогенной гипотезе, депрессия связана с нарушением процесса нейрогенеза в зубчатой извилине гиппокампа [15]. Исследования на животных показывают, что нейрогенез у взрослых играет роль в обучении и памяти [7], регуляции гипоталамо-гипофизарно-надпочечниковой (ГГН) оси в ответ на стресс [15] и терапевтических эффектах антидепрессантов [13]. Нарушение регуляции ГГН оси при хроническом стрессовом воздействии приводит к чрезмерному выделению глюкокортикоидных гормонов, которые негативно влияют на процесс нейрогенеза, подавляя пролиферацию, дифференцировку и выживание клеток [16]. Нейроны зубчатой извилины особенно чувствительны к патогенным эффектам глюкокортикоидов, поскольку экспрессируют как высокоаффинные минералокортикоидные (МР), так и низкоаффинные глю- кокортикоидные рецепторы (ГР) [15]. ГР были также идентифицированы в делящихся клетках-предшественниках субгранулярной зоны зубчатой извилины [8]. Помимо прямого влияния на нейрональные клетки-предшественники, стресс может также играть косвенную роль в регуляции нейрогенеза в зубчатой извилине путем увеличения уровня внутриклеточного эндогенного супрессора P27KIP1, который ингибирует пролиферацию клеток [9]. Большое значение в регуляции нейрогенеза и нейропластичности отводится нейротрофическиму фактору мозга (BDNF), так как повышение глюкокортикоидов приводит к снижению его уровня в гиппокаме [4]. Кроме того, при стрессе происходит сверхактивация рецептора N-метил-D-аспарагиновой кислоты в зрелых гранулярных нейронах зубчатой извилины с последующим эксайтотоксиче-ским действием глутамата [8]. Таким образом, исследование морфологических изменений в зубчатой извилине может способствовать формированию новых терапевтических мишений в лечении депрессии.
ЦЕЛЬ РАБОТЫ
Заключалась в морфометрическом исследовании изменений в гранулярном слое зубчатой извилины крыс в возрасте 12 месяцев при моделировании депрессии и оценке возможности фармакологической коррекции выявленных изменений β-фенильным производным глутаминовой кислоты – нейроглутамом (соединение под лабораторным шифром РГПУ-135).
МЕТОДИКА ИССЛЕДОВАНИЯ
Исследование выполнено на 30 нелинейных крысах-самцах в возрасте 12 месяцев, 10 из которых составили контрольную группу, 10 – группу с экспериментальной депрессией и 10 – группу животных с экспериментальной депрессией, получавших соединение с лабораторным шифром РГПУ-135. Исследуемое соединение вводили внутрибрюшинно за 1 час до моделирования депрессивного состояния в дозе 26 мг/кг. 1-я и 2-я группы животных получали соответственно массе эквивалентный объем физиологического раствора. При содержании животных, моделировании депрессивного состояния и выведения их из эксперимента руководствовались Правилами проведения работ с использованием экспериментальных животных, Хельсинской декларации (1975 г., 2000 г.). Экспериментальное моделирование депрессии у животных вызывали путем мягкого стрессового воздействия в течение 7 дней (ежедневно по 30 минут). Действие стрессоров, таких как виб- рация, громкий звук и пульсирующий яркий свет, осуществлялось в специальной камере, содержащей 6 изолированных отсеков и было непредсказуемым для животных. Данная модель приводит к развитию у животных стойкого депрессивного состояния и имеет сходство с клинической картиной депрессии [4]. Эвтаназию животных проводили с использованием «Гильотины для крыс» (AE0702, производитель «Open Science»). Головной мозг фиксировали в нейтральном забуференном 10%-м формалине. Парафиновые срезы изготавливали во фронтальной плоскости, окрашивали гематоксилином и эозином, тионином по методу Ниссля и изучали на уровне от –2,40 до –3,96 мм относительно брегмы [10] с использованием микроскопа «Axio Lab. A1» (Carl Zeiss Microscopy GmbH, Германия). Фотодокументирование осуществляли камерой «AxioCam 105 color» (Carl Zeiss Microscopy GmbH, Германия). С помощью модуля Image Analysis программы ZEN 1.1.2.0 (Carl Zeiss Microscopy GmbH, Германия) в гранулярном слое зубчатой извилины определяли следующие морфометрические параметры: площади ядер, цитоплазмы и перикарионов нейронов, ядерно-цитоплазматическое отношение (ЯЦО), относительные площади ядер, цитоплазмы и перикарионов нейронов, относительную площадь нейропиля.
Статистическую обработку данных проводили с помощью программы Statistica 8.0 (StatSoft, USA). Обобщенные данные представляли в виде медианы (Me) с указанием интерквартильного интервала (Q1-Q3), где Q1 – 25 процентиль, Q3 – 75 процентиль. Различия между группами оценивали по критерию Краскела – Уоллиса с последующим множественным сравнением групп между собой с использованием критерия Дана и считали статистически значимыми при p < 0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
У животных всех экспериментальных групп слои зубчатой извилины четко определялись топографически и соответствовали цитоархитек-тоническим особенностям, описанным в литературе для крыс [14]. Гранулярный слой зубчатой извилины у контрольной группы животных был образован плотно расположенными близкими к округлой форме перикарионами нейронов, встречались единичные нейроны с гиперхрома-тозом цитоплазмы и сморщиванием (рис., А). Абсолютные и относительные морфометрические показатели нейронов представлены в таблице. При воздействии комбинированного стресса выявлены как качественные изменения нейронов гранулярного слоя зубчатой извилины крыс, описанные нами ранее [3], так и количественные. Качественные признаки повреждения были представлены участками очаговых выпа- дений нейронов, явлениями хроматолиза, полиморфными изменениями ядер: отмечалось как набухание, так и пикноморфные изменения (рис., Б).
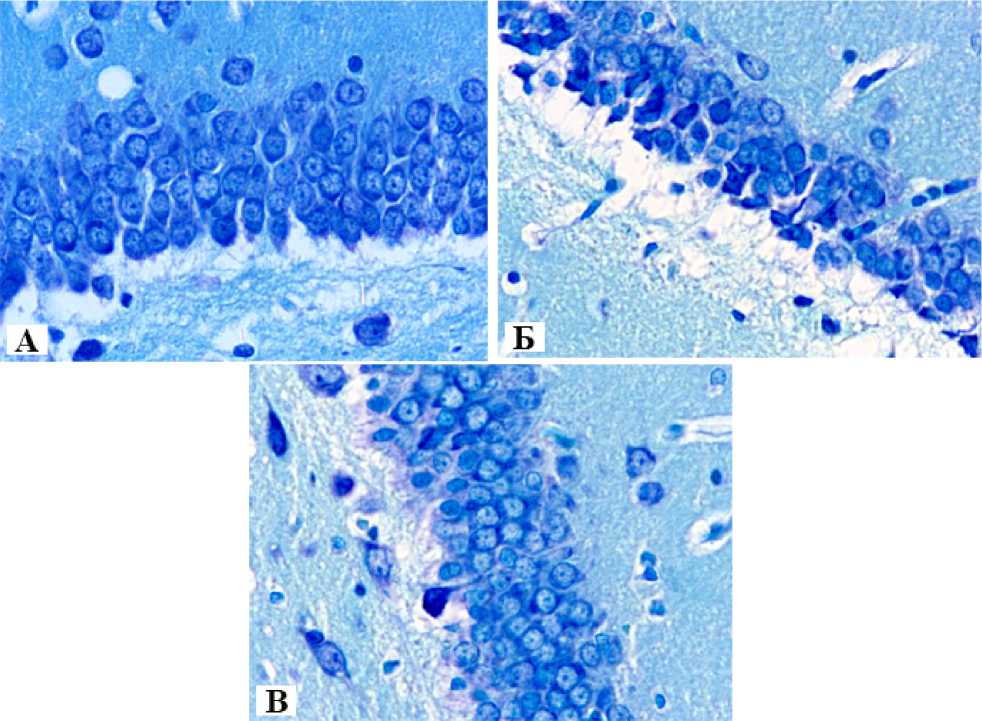
Рис. Морфологические изменения в гранулярном слое зубчатой извилины крыс при стресс-индуцированной депрессии:
А – 1 группа, контроль; Б – 2 группа, депрессия; В – 3 группа, депрессия + нейроглутам. Окраска тионином по методу Ниссля. Ув. ×400
Наличие повреждений в гранулярном слое зубчатой извилины подтверждалось изменениями морфометрических параметров нейронов. Оценка абсолютных показателей у крыс с экспериментальной депрессией продемонстрировала достоверное уменьшение (р < 0,05) на 30,1 % площади ядер, на 13,9 % площади цитоплазмы и на 21,3 % площади перикарионов нейронов, а также снижение ЯЦО на 11,1 % (р < 0,05) по сравнению с контрольной группой (см. табл.).
Достоверные различия обнаруживались в снижении относительных площадей ядер на 34,4 % (р < 0,05), цитоплазмы на 17,9 % (р < 0,05), перикарионов нейронов на 23,9 % (р < 0,05) и увеличении относительной площади нейропиля на 27,5 % (р < 0,05) в гранулярном слое зубчатой извилины у животных 12 месяцев, подвергнутых воздействию комбинированного стресса по сравнению с контролем (см. табл.).
При фармакологической коррекции экспериментальной депрессии у крыс нейроглутамом в гранулярном слое зубчатой извилины наблюдалась гистологическая картина близкая к контрольной группе животных. Большинство нейронов характеризовалось ядрами и перикарионами близкими к округлым по форме (рис., В), хотя встречались сморщенные нейроны и нейроны с гиперхромией цитоплазмы, удельное количество последних снижалось [3], по сравнению со стрессированными животными без фармакологической коррекции.
Применение нейроглутама продемонстрировало достоверное повышение только абсолютных морфометрических показателей нейронов гранулярного слоя зубчатой извилины крыс по сравнению с животными без лечения: увели- чение площадей ядра на 16,4 % (р < 0,05), цито- нейронов на 21 % (р < 0,05), ЯЦО снижалось на плазмы на 20,7 % (р < 0,05), перикарионов 12,5 % (р < 0,05) (см. табл.).
Изменение морфометрических параметров нейронов гранулярного слоя зубчатой извилины крыс, Ме (Q1–Q3)
|
Морфометрические показатели |
Гранулярный слой зубчатой извилины |
||
|
Контроль |
Депрессия |
Депрессия+ нейроглутам |
|
|
Площадь ядер нейронов, мкм2 |
29,6 (24,1–35,3) |
20,7* (14,7–29,3) |
24,1# (17,8–30,3) |
|
Площадь перикарионов нейронов, мкм2 |
60,6 (50,5–71,9) |
47,7* (38,8–61,1) |
57,7# (46,9–68,6) |
|
Площадь цитоплазмы перикарионов нейронов, мкм2 |
30,9 (24,6–38,7) |
26,6* (21,8–33,0) |
32,1# (26,6–39,6) |
|
ЯЦО, число |
0,9 (0,7–1,2) |
0,8* (0,6–1,0) |
0,7# (0,5–0,9) |
|
Относит. площадь ядер нейронов, % |
25,9 (20,3–31,8) |
17,0* (14,6–21,2) |
15,4 (12,0–17,6) |
|
Относит. площадь перикарионов нейронов, % |
53,5 (46,1–61,8) |
40,7* (35,0–48,3) |
34,7 (32,1–39,5) |
|
Относит. площадь цитоплазмы перикарионов нейронов, % |
27,9 (25,6–31,4) |
22,9* (18,9–26,3) |
20,1 (17,5–22,5) |
|
Относит. площадь нейропиля, % |
46,5 (38,2–53,9) |
59,3* (51,5–65,0) |
65,3 (60,5–67,9) |
Различия достоверны при p < 0,05: * по сравнению с животными группы Контроль, # по сравнению с животными группы Депрессия (критерий Краскела – Уоллиса с посттестом Дана).
В ходе проведенного нами морфометрического исследования установлено, что при мягком стрессовом воздействии, которое вызывает у животных депрессивные симптомы, отмечаются атрофические изменения нейронов гранулярного слоя зубчатой извилины, которые сочетаются с обратимыми и необратимыми процессами [3]. Данные изменения могут приводить к уменьшению объёма гранулярного слоя, что было продемонстрировано в исследованиях на грызунах, подвергшихся хроническому стрессу [11, 12].
Важно отметить, что в моделях депрессии у грызунов лечение антидепрессантами индуцирует увеличение снижения объема гранулярного слоя зубчатой извилины [6, 11]. Нами было показано, что при фармакологической коррекции экспериментальной депрессии у крыс нейроглутам способствовал уменьшению атрофических изменений в нейронах, что подтверждает его антидепрессантное и нейропро-текторное действия, выявленные ранее [1, 2].
ЗАКЛЮЧЕНИЕ
Таким образом, полученные нами данные свидетельствуют о том, что при моделировании стресс-индуцированной депрессии у крыс в возрасте 12 месяцев в гранулярном слое зубчатой извилины отмечаются атрофические изменения нейронов, которые характеризуются снижением абсолютных и относительных морфометрических показателей, таких как площади ядра, цитоплазмы, перикарионов нейронов, ядерно-цитоплазматическое отношение, а также повышение относительной площади нейропиля. Применение β-фенильного производного глутаминовой кислоты – нейруглатама (РГПУ-135) оказывает корректирующее нейропротек-торное воздействие, поскольку способствует снижению атрофических изменений нейронов, вследствие увеличения абсолютных морфометрических параметров, по сравнению с животными с экспериментальной депрессией.
Исследование выполнено при финансовой поддержке РФФИ и Администрации Волгоградской области в рамках научного проекта № 19-415-340004\19.
Список литературы Морфологические изменения нейронов гранулярного слоя зубчатой извилины при стресс-индуцированной депрессии и возможность фармакологической коррекции новым производным глутаминовой кислоты
- Дозозависимое влияние гидрохлорида b-фенил-глутаминовой кислоты (нейроглутама) на поведение животных / И. Н. Тюренков [и др.] // Бюллетень экспериментальной биологии и медицины. - 2014. - Т. 158, № 8. - С. 196-201.
- Нейропротекторное действие фенибута и нейроглутама при экспериментальной ишемии головного мозга на фоне измененной иммунореактивности / Е. В. Волотова [и др.] // Экспериментальная и клиническая фармакология. - 2016. - Т. 79, № 4. - С. 18-25.
- Характеристика морфологических изменений зубчатой извилины при фармакологической коррекции депрессивного состояния у крыс зрелого возраста / А. В. Смирнов [и др.] // Медицинский вестник Северного Кавказа. - 2019. - Т.14, № 4. - С. 668-671.
- A depressive state in rats in chronic combined stress induced by combined stresses of different modalities / I. N. Tyurenkov [et al.] // Neuroscience and behavioral physiology. - 2015. - Vol. 45, № 5. - P. 542-549.
- Adlard, P. A. Voluntary exercise protects against stress-induced decreases in brain-derived neurotrophic factor protein expression / P. A. Adlard, C. W. Cotman // Neuroscience. - 2004. - Vol. 124, № 4. P. 985-992.
- Chronic fluoxetine induces the enlargement of perforant path-granule cell synapses in the mouse dentate gyrus / Y. Kitahara [et al.] // PLoS One. - 2016. -Vol. 11. - e0147307.
- Deng, W. Adult-born hippocampal dentate granule cells undergoing maturation modulate learning and memory in the brain / W. Deng // J. Neurosci. -2009. Vol. 29, № 43. - P. 13532-13542.
- Enhancement of hippocampal plasticity by physical exercise as a polypill for stress and depression: A review / A. Li [et al.] // CNS Neurol. Disord. Drug Targets. - 2019. - Vol. 18, № 4. - P. 294-306.
- Heine, V. M. Increased P27KIP1 protein expression in the dentate gyrus of chronically stressed rats indicates G1 arrest involvement / V. M. Heine // Neuroscience. - 2004. - Vol.129, № 3. - P. 593-601.
- Paxinos, G. The rat brain in stereotaxic coordinates. 6th ed. / G. Paxinos, C. Watson. - New York (NY): Elsevier Academic Press, 2007.
- Repeated social defeat-induced depression-like behavioral and biological alterations in rats: involvement of cholecystokinin / C. Becker [et al.] // Mol. Psychiatry. - 2008. - Vol.13. - P. 1079-1092.
- Stress and loss of adult neurogenesis differentially reduce hippocampal volume / T. J. Schoenfeld [et al.] // Biol. Psychiatry. - 2017. - Vol. 82. - P. 914-923.
- Surget, A. Drug-dependent requirement of hippocampal neurogenesis in a model of depression and of antidepressant reversal / A. Surget // Biol. Psychiatry. - 2008. - Vol. 64, № 4. - P. 293-301.
- The hippocampus book / P. Andersen [et al.]. - Oxford University Press, 2007. - 832 p.
- Umschweif, G. The dentate gyrus in depression [Electronic resource] / G. Umschweif, P. Greengard, Y. Sagi // European Journal of Neuroscience. - Access mode: https://onlinelibrary.wiley.com/doi/abs/ ?af=R
- DOI: 10.1111/ejn.14640
- Wong, E. Y. Raised circulating corticosterone inhibits neuronal differentiation of progenitor cells in the adult hippocampus / E. Y. Wong, J. Herbert // Neuroscience. - 2006. - Vol.137, № 1. - P. 83-92.


