Морфологические изменения нейронов хвостатого ядра крыс, склонных к формированию алкогольной зависимости
Автор: Гуров Д.Ю., Туманов В.П., Смирнов А.В., Снигур Г.П., Григорьева Н.В., Быхалов П.С., Хлопонин П.А., Самусев Р.П.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Рубрика: Обзорные статьи
Статья в выпуске: 2 (62), 2019 года.
Бесплатный доступ
В работе проведен анализ морфологических изменений в хвостатом ядре крыс, склонных и несклонных к формированию алкогольной зависимости, отобранных с использованием метода определения алкогольной мотивации, основанный на определении уровня общей неспецифической реактивности организма. Парафиновые срезы толщиной 4-6 мкм окрашивали гематоксилином и эозином, тионином по методу Ниссля, проводили иммуногистохимические реакции с использованием моноклональных антител против рецепторов-2 глутамата (GLUR2). В хвостатом ядре крыс, предрасположенных к алкогольной зависимости, выявлены морфофункциональные различия в структурной организации, достоверно большая объемная плотность перикарионов нейронов, по сравнению с животными, несклонными к алкоголизации. При иммуногистохимическом исследовании обнаружена более высокая степень экспрессии иммунореактивного материала в перикарионах нейронов хвостатого ядра крыс, склонных к формированию алкогольной зависимости, что свидетельствует о наличии иммунофенотипических различий и метаболизма в глутаматцептивных нейронах неостриатума.
Крыса, хвостатое ядро, алкоголь, предрасположенность
Короткий адрес: https://sciup.org/142224335
IDR: 142224335 | УДК: 616-091.8
Morphological changes in neurons of caudate nucleus of rats predisposed to alcohol dependence
We analyzed morphological changes in caudate nucleus of rats, predisposed and not predisposed to formation of alcohol dependence, selected using the method of determining alcohol motivation, based on determining level of total nonspecific reactivity of the organism. Paraffin sections 4-6 pm thick were stained with hematoxylin and eosin, thionin by Nissl's method, immunohistochemical reactions were performed using monoclonal antibodies against glutamate receptors 2 (GLUR2). In caudate nucleus of rats predisposed to alcohol dependence, morphofunctional differences in structural organization, a significantly greater volumetric density of perikaryon neurons, compared with animals not predisposed to alcoholization, were revealed. In predisposed to alcohol dependence rats immunohistochemical study revealed a higher degree of immunoreactive material expression in neuron perikarya of caudate nucleus, which indicates the presence of immunophenotypic differences and metabolism in glutamateceptive neurons of neostriatum.
Текст научной статьи Морфологические изменения нейронов хвостатого ядра крыс, склонных к формированию алкогольной зависимости
В связи с ростом интереса к проблеме формирования алкогольной зависимости исследование различных отделов ЦНС с позиций конституционально обусловленного влечения к алкоголю и лечению хронической алкогольной зависимости остается актуальным [5].
Механизмы алкогольной аддикции связаны как с изменением локального уровня ацетальдегида в мозге, возникающим при употреблении алкоголя, так и c генетически детерминированной активностью систем метаболизма этанола и ацетальдегида в печени и в головном мозге.
Результаты различных исследований указывают на то, что феномен предпочтения эта- нола животными и предрасположенность к потреблению алкоголя у людей имеют генетически обусловленную структурную основу и могут быть связаны с интенсивностью обмена алкоголя в организме, зависят от активности ферментных систем метаболизма спиртов и альдегидов, являющихся мощными регуляторами уровня ацетальдегида в клетке [6, 10].
В морфогенезе алкогольной болезни головной мозг, структуры стриопаллидарной системы в частности, играют существенную роль в интегративном взаимодействии различных отделов центральной нервной системы, обеспечивая поддержание мышечного тонуса, контроль произвольных движений [4, 7].
При длительной алкоголизации развиваются нарушения нейромедиаторного обмена, усиленный синтез катехоламинов, высвобождение дофамина в префронтальной коре, экс-трастриатальное связывание и глутаматергиче-ская передача через метаботропные глутаматные рецепторы [7].
Существующие гипотезы рассматривают развитие атрофических изменений в подкорковых областях головного мозга при хроническом алкоголизме как результат влияния алкоголя, его метаболитов, при этом коморбидная патология способна активировать протективные механизмы; с другой стороны, коморбидная патология при хронической алкогольной зависимости способствует формированию в подкорковых областях изменений воспалительного характера на фоне существующей атрофии ткани, маскируя клинические проявления алкогольинду-цированной субкортикальной атрофии [9].
Таким образом, исследование морфологических изменений в подкорковых ядрах, в частности, nucleus caudatus у животных, склонных и несклонных к формированию алкогольной зависимости, является актуальным с учетом роли стриопаллидарной системы в поддержании мышечного тонуса, экстрапирамидного контроля движений, участии в формировании мотивационного поведения и связанных с ним эмоций [12].
ЦЕЛЬ РАБОТЫ
Исследовать морфологические изменения нейронов в хвостатом ядре крыс, склонных и несклонных к формированию алкогольной зависимости.
МЕТОДИКА ИССЛЕДОВАНИЯ
В работе нами использован метод определения алкогольной мотивации, основанный на определении уровня общей неспецифической реактивности организма (УОНРО) – интегративного генетически обусловленного показателя, отражающего степень общей чувствительности организма к различным экзогенным воздействиям («Способ определения предрасположенности к алкоголизации у лабораторных крыс» № 204120726/14 (022241 от 06 июля 2004 г.). При отборе крыс с различными уровнями начальной алкогольной мотивации использовали 180 белых крыс-самцов весом 180–220 г. Все экспериментальные животные были выведены в питомнике ФКУЗ «Волгоградский научно-исследовательский противочумный институт». Важное внимание при проведении экспериментальной части исследования было уделено вопросам содержания, отбора, группировки животных, что позволило выполнить за- планированные научные задачи. Содержание экспериментальных животных осуществляли в стандартных клетках Т-3 (Чехия). Кормление осуществлялось по стандартному лабораторному рациону со свободным доступом к воде, при температуре воздуха в виварии 18–22 °С, относительной влажности воздуха – 50–60 %.
Наиболее приемлемым для распределения животных по УОНРО является подход, основанный на определении болевой (ноцицептивной) чувствительности посредством дозированного электроболевого воздействия [1]. В результате тестирования было установлено, что средний порог вокализации в группе «короткоспящих» животных составил (17,4 ± 1,1) В и был достоверно ниже, чем в группе «долгоспящих» животных, где этот показатель составил (26,2 ± 0,8) В (P ± 0,05). Таким образом, «короткоспящие» животные, потенциально склонные к приему алкоголя, отличались большей чувствительностью к действию электробо-левого стресса (высокий уровень УОНРО).
Результаты теста послужили основанием для отбора 15 крыс с коротким сном, средняя продолжительность анестезии этанолом у которых была (45,6 ± 3,9) минуты, и 17 крыс с длительным сном продолжительностью (184,3 ± 11,4) минут. «Длительноспящие» животные имеют отрицательную алкогольную мотивацию по сравнению с «коротко спящими» крысами, у которых предрасположенность к алкогольной зависимости высокая [1, 4].
После эутаназии производили вскрытие животного и осмотр внутренних органов на предмет патологических изменений. Вскрывали череп, извлекали головной мозг и быстро проводили забор материала, который помещали в 10%-й раствор нейтрального формалина. После фиксации в формалине в течение 48 часов образцы тканей обезвоживали и заливали в парафин. С парафиновых блоков готовили срезы толщиной 4–6 мкм. Их окрашивали по хорошо разработанным и описанным ранее методикам гематоксилином и эозином, тионином по методу Ниссля [2, 8].
Иммуногистохимическое исследование проводили на парафиновых срезах толщиной 4 мкм, которые помещали на адгезивные стекла и инкубировали во влажной камере с первичными моноклональными антителами против рецепторов глутамата (GLUR-2, клон 6C4, Thermo Fisher Scientific, USA) в разведении 1:75 при комнатной температуре в течение 30 минут, использовали полимерную визуализирующую систему, рекомендованную в соответствии с протоколом фирмы-производителя [3]. По завершении проведения иммуногиcтохимичеcкой реакции для лучшей визуализации ядер в нерв- ных клетках головного мозга производили до-краcку гематоксилином.
Фотодокументирование производили с использованием цифровой фотокамеры Canon (Japan) светового микроскопа Axiostar plus (Карл Цейc, Германия) с объективами х10, х40.
Статистическую обработку данных проводили с использованием пакетов программ Statistica 6,0 (StatSoft, USA). Различия между группами оценивали при помощи непараметрического критерия Манна-Уитни (Mann-Whitney, U-test) и считали статистически значимыми при p < 0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
При морфологическом исследовании крыс, склонных к формированию алкогольной зависимости, в хвостатом ядре обнаруживается увеличение плотности расположения нейронов в ростральной области и постепенное её снижение в каудальном направлении. Нейроны располагаются внутри нечетко отграниченных областей, окруженных пучками нервных воло- кон. При окраске по Нисслю обнаруживаются пузырьковидные округлые ядра в центральной части перикариона нейрона, реже встречаются нейроны с ядрами овальной формы. Ядрышко, как правило, выражено, расположено в центральной части ядра, в некоторых случаях эктопировано. Цитоплазма перикарионов большинства нейронов умеренно базофильна.
У крыс, не склонных к формированию алкогольной зависимости плотность расположения нейронов меньше (см. табл.), в состав группы входит в среднем около десяти нейронов. Перикарионы большинства нейронов имеют полигональную форму и меньшие размеры по сравнению с перикарионами крыс, склонных к формированию алкогольной зависимости. При окраске по методу Ниссля в нейронах хорошо определяется центрально расположенное крупное круглое ядро с базофильной нуклеолеммой и центральным достаточно крупным ядрышком. Цитоплазма перикариона слабо базофильная. Гранулы базофильной субстанции не визуализируются в большинстве перикарионов.
Морфометрические показатели хвостатого ядра крыс с различной конституциональной алкогольной мотивацией, (M ± m)
|
Показатели |
Экспериментальные группы крыс |
|
|
несклонные к формированию алкогольной мотивации |
склонные к формированию алкогольной мотивации |
|
|
Объёмная плотность перикарионов нейронов, % |
16,6 ± 0,9 |
19,8 ± 1,06* |
|
Объёмная плотность ядер нейронов, % |
6,6 ± 0,7 |
7,2 ± 0,7 |
|
Объёмная плотность цитоплазмы перикарионов нейронов, % |
10,0 ± 0,9 |
12,6 ± 0,8* |
|
Объёмная плотность нейропиля, % |
83,4 ± 1,8 |
80,2 ± 1,4* |
|
Средний объём перикарионов нейронов, мкм3 |
654,2 ± 32,2 |
769,3 ± 41,1* |
|
Средний объём ядер нейронов, мкм3 |
342,9 ± 14,6 |
355,3 ± 19,2 |
|
Средний объём цитоплазмы перикарионов нейронов, мкм3 |
345,3 ± 18,9 |
414,0 ± 31,7* |
|
Ядерно-цитоплазматическое отношение |
0,99 ± 0,08 |
0,85 ± 0,07 |
|
Объемное отношение перикарионов нейронов к нейропилю |
0,20 ± 0,03 |
0,25 ± 0,02* |
* р < 0,05.
При морфометрическом исследовании хвостатого ядра обнаружено, что объёмная плотность перикарионов нейронов у крыс, несклонных к формированию алкогольной зависимости, составляет (16,6 ± 0,9) % (табл.), что на 3,2 % ниже по сравнению с животными, склонными к алкоголизации, у которых данный морфометрический показатель составляет (19,8 ± 1,06) % (при р < 0,05). Объёмная плотность цитоплазмы перикарионов нейронов у крыс, несклонных к формированию алкогольной зависимости, составляет (10,0 ± 0,9) % (табл.), что на 2,6 % ниже по сравнению с животными, склонными к алкоголизации, у которых данный морфометрический показатель составляет (12,6 ± 0,8) % (при р < 0,05).
Средний объем перикарионов нейронов у крыс, несклонных к формированию алкогольной зависимости, составляет (654,2 ± 32,2) мкм3, что на 15 % ниже по сравнению с животными, склонными к алкоголизации (табл.), у которых данный морфометрический показатель составляет (769,3 ± 41,1) мкм3 (при р < 0,05). Изменение данного параметра сопровождается значимым снижением среднего объёма цитоплазмы перикарионов нейронов у крыс, несклонных к формированию алкогольной зависимости, который составляет (345,3 ± 18,9) мкм3, что на 16,6 % ниже по сравнению с животными, склонными к алкоголизации, у которых данный морфометрический показатель составляет (414,0 ± 31,7) мкм3 (при р < 0,05).
При иммуногистохимическом исследовании хвостатого ядра крыс, склонных к формированию алкогольной зависимости, с использованием моноклональных антител к рецепторам-2 глутамата (GLUR2) обнаруживается низкая степень экспрессии иммунопозитивного материала в перикарионах нейронов среднего размера (рис. 1). Им-мунопозитивный материал распределен равномерно в цитоплазме перикарионов. Значительная часть нейронов обладает иммунонегативной цитоплазмой перикарионов. Кроме того, определяется слабопозитивная реакция в нейропиле. При иммуногистохимическом исследовании nucleus caudatus крыс, несклонных к формированию алкогольной зависимости, обнаружены глутамат-цептивные нейроны, обладающие слабой степенью экспрессии иммунореактивного материала при использовании моноклональных антител к рецепторам-2 глутамата (GLUR2).
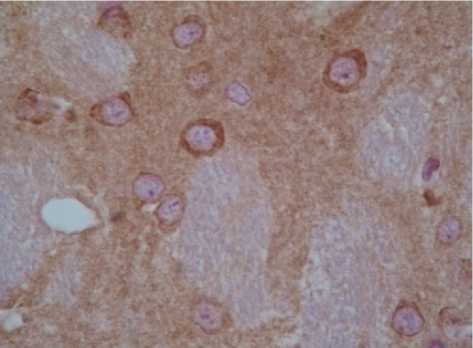
Рис. 1. Строение вентрального отдела хвостатого ядра крыс, склонных к формированию алкогольной мотивации. Иммуногиcтохимичеcкая реакция с моноклональными антителами против рецепторов-2 глутамата (GLUR2), докраcка гематоксилином. Ув. х 400
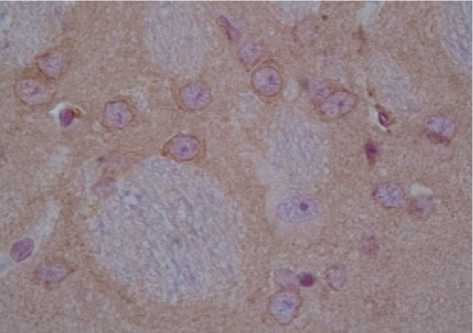
Рис. 2. Строение вентрального отдела хвостатого ядра крыс, несклонных к формированию алкогольной мотивации. Иммуногиcтохимичеcкая реакция с моноклональными антителами против рецепторов-2 глутамата (GLUR2), докраcка гематоксилином.
Ув. х 400
Обнаруживаемая иммуногистохимическая картина свидетельствует о существовании внутри популяции нейронов средних размеров в хвостатом ядре крыс, несклонных к формированию алкогольной зависимости, глутаматцеп-тивных нейронов, обладающих меньшей степенью экспрессии рецепторов глутамата (GLUR-2) по сравнению с группой крыс, склонных к формированию алкогольной зависимости.
ЗАКЛЮЧЕНИЕ
Морфологические различия в организации подкорковых структур головного мозга у крыс с различной предрасположенностью к формированию алкогольной зависимости неразрывно связаны с особенностями нейрохимического обмена, активности различных медиаторных систем и количественного распределения рецепторов на нейронах, что создает определенное пространственно-временное состояние отдельных областей головного мозга и влияет на их вклад в формирование аддиктивного поведения.
В головном мозге крыс, склонных к формированию алкогольной мотивации, нами обнаружены морфофункциональные отличия в передних отделах хвостатого ядра, которые выражаются в различиях структурной организации на тканевом, клеточном и молекулярном уровнях, в том числе достоверно большей объемной плотностью перикарионов нейронов и объемной плотностью цитоплазмы перикарионов нейронов по сравнению с животными, несклонными к формированию алкогольной мотивации, и, соответственно, меньшей объёмной плотностью нейропиля, что сочетается с более высокими объемными параметрами нейронов (объём перикарионов нейронов, объём цитоплазмы перикарионов нейронов).
При хронической алкогольной интоксикации различные типы нейромедиаторов могут оказывать синергичное и антогонистичное воздействие на нейроны [4]. Считается, что нарушения в дофаминергической передаче тесно связаны с глутаматергической системой. Этот феномен особенно важен, поскольку помимо основной роли возбуждающего нейромедиатора, глутамат может проявлять нейротоксические свойства [5]. При гиперактивации глутама-тергической передачи происходит интенсивное поступление ионов кальция в клетку индуцирующего процессы образования активных форм кислорода, а также активацию протеинкиназ. Следствием этих процессов может стать глута-матиндуцированное повреждение и гибель нейронов [7], которая сопровождается атрофическими изменениями в подкорковых ядрах [12].
При иммуногистохимическом исследовании с использованием первичных антител против рецепторов-2 глутамата (GLUR2) обнаружена высокая степень экспрессии иммунореактивного материала в перикарионах нейронов хвостатого ядра крыс, склонных к формированию алкогольной зависимости, что свидетельствует, с одной стороны, о наличии иммунофе-нотипических различий и метаболизма в глута-матцептивных субкортикальных нейронах, с другой стороны, о потенциально большем риске повреждения и гибели нейронов у крыс, склонных к формированию алкогольной мотивации, хотя уже при моделировании хронической алкогольной интоксикации у крыс в некоторых отделах головного мозга, в супраоптических ядрах, обнаруживается низкая экспрессия метаболических глутаматных рецепторов [11].
Список литературы Морфологические изменения нейронов хвостатого ядра крыс, склонных к формированию алкогольной зависимости
- Мулик А. Б. Оптимизация медико-биологического эксперимента in vivo / А. Б. Мулик - Волгоград, 2003. - 212 с.
- Особенности структурных изменений головного мозга при моделировании алиментарного дефицита магния // А. В. Смирнов [и др.], Современные проблемы науки и образования. - 2013. - № 4.
- Петров, С. В. Руководство по иммуногистохимической диагностике опухолей человека / С. В. Петров, Н. Т. Райхлин // Казань. - 2012. - 624 с.
- Писарев, В. Б. Вариабельность структур центральной нервной системы и ее роль в развитии патологических процессов / В. Б. Писарев, А. В. Смирнов, Д. Ю. Гуров // Волгоград, Изд-во ВолГУ. - 2006. -192 с.
- Azevedo, C. A. Neuromodulation Therapies for Alcohol Addiction: A Literature Review / C. A. Azevedo, A. Mammis // Neuromodulation. - 2018. -Vol. 21 (2). - P. 144-148.
- Ceramide pathways modulate ethanol-induced cell death in astrocytes / M. Pascual [et al.] // J. Neurochem. - 2003. - № 6. - P. 1535-1545.
- Cerebral dopaminergic and glutamatergic transmission relate to different subjective responses of acute alcohol intake: an in vivo multimodal imaging study/ G. Leurquin-Sterk [et al.] // Addict Biol. - 2018. -Vol. (3). - P. 931-944.
- Ermilov V. V. The role of р-amyloidopathy in the pathogenesis of age-related macular degeneration in correlation with Alzheimer's disease // Neuro-degenerative diseases. - 2017. - Vol. 17. - S1. -P. 606.
- Fein, G. Subcortical volumes are reduced in shortterm and long-term abstinent alcoholics but not those with a comorbid stimulant disorder / G. Fein, D. Fein // Neuroimage Clin. - 2013. - Vol. 3. -P. 47-53.
- Genotypic differences in ethanol sensitivity in two tests of motor incoordination / J. C. Crabbe [et al.] // J. Appl. Physiol. - 2003. - № 4. - P. 1338-1351.
- Muram, S. Presynaptic G Protein-Coupled Receptors Differentially Modulate Spontaneous Glutamate Release in the Supraoptic Nucleus / S. Muram, T. M. Rowe, M. Hirasawa // J. Neuroendocrinol. - 2016. - Vol. 28 (4).
- Resting state synchrony in long-term abstinent Alcoholics: Effects of a current major depressive disorder diagnosis / G. Fein [et al.] // Alcohol. - 2017. -Vol. 59. - P. 17-25.


