Морфологические изменения внутренних органов у крыс при длительном избыточном потреблении углеводов и жиров
Автор: Чернышева Мария Борисовна, Макарова Мария Александровна, Цветков Иван Сергеевич
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 3 т.22, 2014 года.
Бесплатный доступ
Проведено исследование внутренних органов крыс после длительного (20 недель) избыточного потребления углеводов и жиров. Рацион опытных животных включал обогащенный жиром стандартный корм и 20% раствор фруктозы вместо питьевой воды. Показано, что в отсутствии увеличения массы тела и повышения уровня глюкозы и триглицеридов, у крыс развивается жировая дистрофия печени, липоматоз поджелудочной железы и коронообразные структуры в жировой ткани.
Ожирение, метаболический синдром, крысы, рацион с высоким содержанием жиров и углеводов
Короткий адрес: https://sciup.org/143177004
IDR: 143177004
Morphological changes of the internal organs of rats after long-term excessive consumption of carbohydrates and fats
A study of the internal organs of rats after long-term (20 weeks) excessive consumption of carbohydrates and fats was realized. The diet of experimental animals consisted of standard feed, enriched with fat, and 20% fructose solution instead of drinking water. It was shown that in the absence of weight gain and raised glucose and triglyceride levels the rats developed fatty liver disease, lipomatosis of the pancreas and crown-like structures in adipose tissue.
Текст научной статьи Морфологические изменения внутренних органов у крыс при длительном избыточном потреблении углеводов и жиров
Введение. Ожирение - это хроническое полиэтиологическое заболевание, к причинам развития которого, в первую очередь, следует отнести высококалорийное питание, а именно, избыточное потребление жиров и углеводов, превышающее энергетические затраты организма, а также генетическую предрасположенность и прогрессирующую распространенностью заболеваний эндокринной системы и органов пищеварения [1]. Ожирение характеризуется избыточным накоплением жировой ткани и прогрессирует при естественном течении, после окончания курса лечения высока вероятность рецидива [2]. На фоне ожирения развивается метаболический синдром - совокупность метаболических, гормональных и клинических нарушений, являющихся факторами высокого риска развития сердечно-сосудистых, хронических воспалительных и онкологических заболеваний [3].
При ожирении в жировых депо увеличивается количество нейтрального жира, он откладывается в подкожной клетчатке, в большом сальнике, брыжейке и эпикарде. Также жировая ткань появляется в органах, где она обычно почти не встречается, например, в поджелудочной железе и стенках правого желудочка сердца. При ожирении развивается жировая дистрофия печени, липоматоз поджелудочной железы и ожирение сердца [4].
В литературе представлены сведения о структурных и морфофункциональных изменениях внутренних органов при ожирении и метаболическом синдроме у человека. Что касается их моделирования у лабораторных животных, то, напротив, в них, как правило, приводятся данные только о лабораторных биохимических показателях [5-9].
Ожирение и метаболический синдром у лабораторных животных можно вызвать с помощью специального рациона с высоким содержанием углеводов, жиров, углеводов и NaCl и рационы, имитирующие пищевые предпочтения человека, например, «диета кафетерия» [10]. Наиболее адекватным и простым методом моделирования ожирения является использование корма с высоким содержанием и углеводов, и жиров [5,6,7]. Показано, что обогащение рациона жирами различного происхождения способствует развитию ожирения, инсулинорезистентности и стеатоза печени [11, 12]. По данным литературы [6, 10] рацион экспериментальных животных обогащают жирами на 10-60% по калорийности, наиболее распространенным вариантом считается рацион с высоким (30-40%) содержанием жира. Для обогащения рациона углеводами в эксперименте используют сахарозу, глюкозу и фруктозу. Однако, для моделирования ожирения наиболее эффективна именно фруктоза. Даже за очень короткий срок (1-2 недели) у крыс, потребляющих фрук- тозу, развиваются проявления метаболического синдрома такие, как инсулинорезистентность и триглицеридемия [13].
Цель исследования - выявить морфологические изменения внутренних органов при длительном избыточном потреблении углеводов и жиров у крыс линии Спрэйг-Доули
Материал и методы исследования. В работе были использованы две группы половозрелых самцов крыс Спрейг-Доули (питомник «Столбовая») массой тела 226-236г. на начало эксперимента. Всех экспериментальных животных содержали в стандартных условиях освещения и температурного режима при свободном доступе к пище и воде. Экспериментальные животные контрольной группы (n=3) получали стандартный корм ПК-120-1 (ООО «Лабораторснаб») и обычную питьевую воду. Экспериментальные животные опытной группы (n=7) - рацион, включающий обогащенный жиром на 30% по калорийности стандартный корм ПК-120-1 и 20% раствор фруктозы в питьевой воде. Эксперимент длился 20 недель.
В течение всего эксперимента измеряли массу тела у крыс обеих групп. Животных выводили из эксперимента передозировкой диэтилового эфира. Проводили гистологическое исследование внутренних органов, которые в первую очередь вовлекаются в патологический процесс при ожирении - сердце, печень, поджелудочная железа и жировая ткань, окружающая придаток яичка. Органы фиксировали в жидкости Буэна, заливали в парафин, изготавливали гистологические срезы толщиной 5-7 мкм и окрашивали их гематоксилином и эозином.
Проводили забор крови, получали сыворотку, в которой определяли уровень глюкозы и триглицеридов (наборы Human GmbH 10260 и 10720P) на автоматическом биохимическом анализаторе Mindray BS (Китай).
Результаты исследования и их обсуждение. После окончания эксперимента показатели массы тела у крыс контрольной и опытной групп не различались (табл.). По данным биохимического исследования у животных опытной и контрольной групп статистически значимых различий содержания в сыворотке крови глюкозы и трилицеридов не выявлено (табл.).
При морфологическом исследовании печени балочное и дольковое строение сохранено у всех животных контрольной группы. Гепатоциты с мелкой базофильной зернистостью. По ходу балок диффузно рассеяные неэпителиальные клеточные элементы, неравномерное полнокровие синусоидных капилляров и вен. В опытной группе у всех крыс балочное и дольковое строение печени было также сохранено. В центрах долек - гепатоциты с мелкой базофильной зернистостью, а в периферических - с мелкокапельной и среднекапельной жировой дистрофией (Рис. 1).
Поджелудочная железа у всех животных
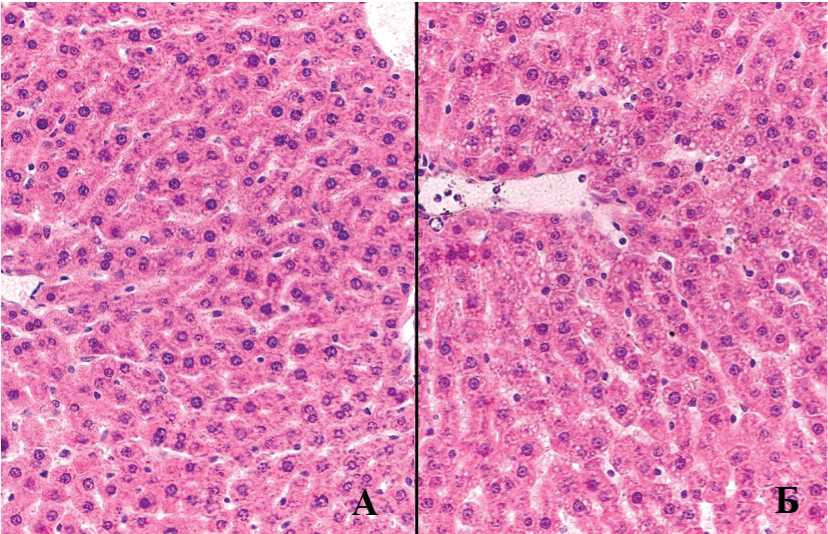
Рис. 1. Печень крыс контрольной (А) и опытной групп (Б). А) гепатоциты с мелкой базофильной зернистостью. Б) гепатоциты с мелко- и среднекапельной дистрофией. Окраска гематоксилином и эозином. Ув. 400
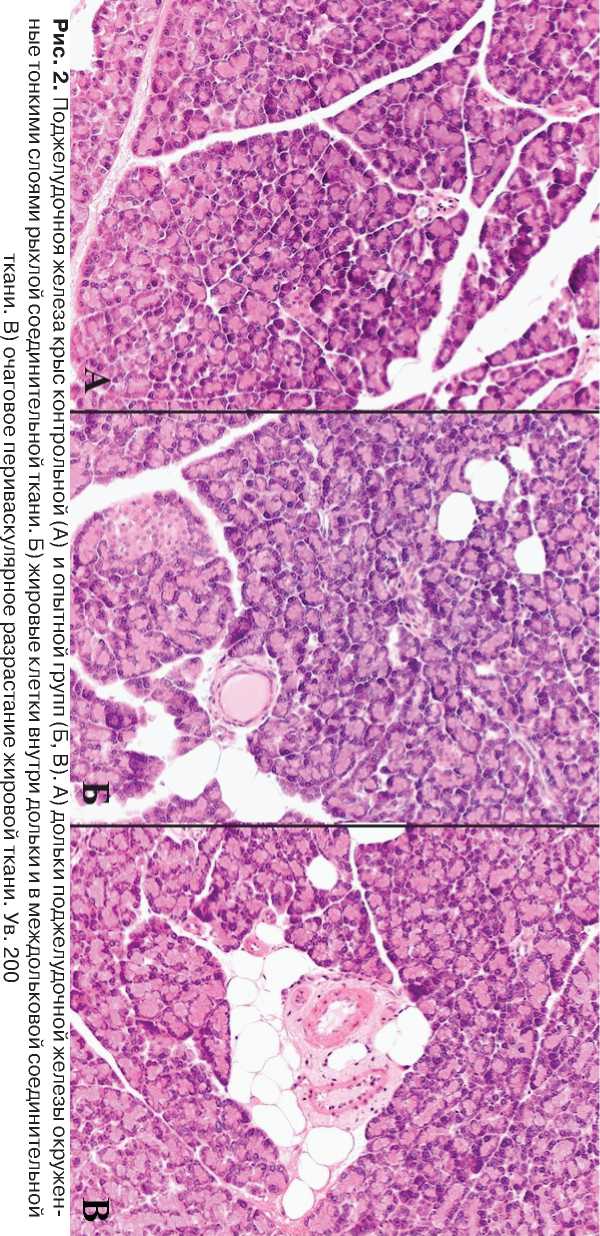
контрольной группы с тонкими прослойками соединительной ткани, строение серозных ацинусов и выводных протоков не нарушено. Единичные островки Лангерганса представлены эндо-криноцитами с нормохромными ядрами и окружены тонкими волокнами. Прилежащая жировая ткань имела равномерно ячеистый вид, короноподобные структуры (crown-like structures), характерные для ожирения, отсутствовали. В опытной группе в отличие от контрольной у 5 из 7 животных встречались единичные в препарате разрастания жировой ткани (липоматоз) внутри долек и вокруг сосудов (рис. 2.).
В контрольной группе у всех животных жировая ткань, прилежащая к придатку яичка, была представлена дольками, состоявшими из крупных клеток, плотно примыкающих друг к другу, с эксцентрично расположенными уплощенными ядрами. По сравнению с контрольной - у 5 из 7 животных опытной группы в препаратах встречались короноподобные структуры, представленные скоплениями макрофагов, окружающими адипоциты (рис. 3).
При моделировании ожирения исследователи чаще всего используют крыс Спрейг-Доули, в связи с тем, что эта линия отличается выраженными индивидуальными различиями. По данным литературы [5-9] при длительном (от 3 до 6 месяцев) избыточном употреблении углеводов и жиров у 50% животных развивается ожирение и метаболический синдром - значительно увеличивается масса тела и висцерального жира, повышается уровень инсулина, триглицеридов и холестерина, возникает инсулинорезистент-ность и нарушенная толерантность к глюкозе.
В нашем эксперименте показатели массы тела у животных опытной группы, при употреблении ими в течение 20 недель избыточного количества углеводов и жиров, не отличались от
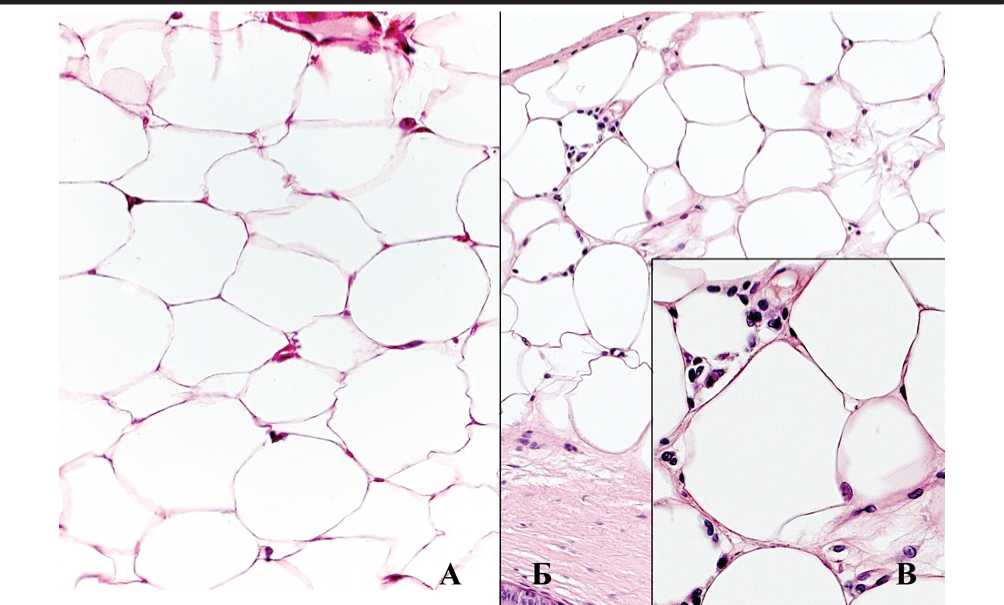
Рис. 3. Жировая ткань, окружающая придаток яичка, у крыс контрольной (А) и опытной групп (Б, В). А) – адипоциты сферической и многоугольной форм, жировая капля окружена цитоплазмой, ядро уплощено. Б), В) короноподобные структуры - скопления макрофагов, окружающих адипоциты. Ув.: А, Б - 200; В - 400.
Таблица.
Масса тела экспериментальных животных и биохимические показатели сыворотки крови у крыс опытной и контрольной группы
Заключение. Таким образом, при дли- тельном избыточном потреблении углеводов и жиров, при отсутствии увеличения массы тела и повышения уровня глюкозы и триглицеридов, развивается жировая дистрофия печени, липоматоз поджелудочной железы и коронообразные структуры в жировой ткани.
Список литературы Морфологические изменения внутренних органов у крыс при длительном избыточном потреблении углеводов и жиров
- Acosta A., Camilleri M. Gastrointestinal Morbidity in Obesity//Acad. Sci. 2014. V.1311. P. 42-56.
- Гинзбург М.М. Ожирение и метаболический синдром. Влияние на состояние здоровья, профилактика и лечение. Самара.: Парус, 2000. 160с.
- Ройтберг Г.Е. Метаболический синдром. М.: МЕДпресс-информ, 2007. 224 с.
- Струков А.И., Серов В.В. Патологическая анатомия. - М.: Медицина, 1979. 527с.
- Levin B.E., Dunn-Meynell A.A., Balkan B., Keesey R.E. Selective breeding for diet-induced obesity and resistance in Sprague-Dawley rats //American Journal of Physiology - Regulatory, Integrative and Comparative Physiology. 1997. V.273. Р.725-730.
- Ghibaudi L., Cook J., Farley C., Heek M., Hwa J.J. Fat Intake Affects Adiposity, Comorbidity Factors, and Energy Metabolism of Sprague-Dawley Rats // Obesity Research. 2002. V.10. N.9.
- Ricci M.R., Levin B.E. Ontogeny of diet-induced obesity in selectively bred Sprague-Dawley rats // American Journal of Physiology - Regulatory, Integrative and Comparative Physiology. 2003. V.285. Р.610-618.
- Deng J.Y., Huang J.P., Lu L.S., Hung L.M. Impairment of cardiac insulin signaling and myocardial contractile performance in high-cholesterol/fructose-fed rats// Am J Physiol Heart Circ Physiol. 2007. V. 293(2)
- Axelsen L.N., Lademann J.B., Petersen J.S., Holstein-Rathlou N.H., Ploug T., Prats C., Pedersen H.D., Kjølbye A.L. Cardiac and metabolic changes in long-term high fructose-fat fed rats with severe obesity and extensive intramyocardial lipid accumulation //Am J Physiol Regul Integr Comp Physiol. 2010. V. 298(6)
- Angelova P., Boyadjiev N. A review on the models of obesity and metabolic syndrome in rats // Trakia Journal of Sciences. 2013. V. 1. P. 5-12.
- Grundy S.M., Brewer H.B., Cleeman J.I., Smith S.C., Lenfant C. Definition of Metabolic Syndrome Report of the National Heart, Lung, and Blood Institute // American Heart Association Conference on Scientific Issues Related to Definition Circulation. 2004. V.109. P. 433-438
- Buettner R., Parhofer K., Woenckhaus M., Wrede C., Kunz-Schughart L., Scholmerich J. and Bollheimer L. Defining high-fat-diet rat models: metabolic and molecular effects of different fa t types // Journal of Molecular Endocrinology. 2006. V. 36. P. 485-501.
- Selder J., Chen, Y. D., Cully M. and Reaven, G., Hyperinsulinemia in fructose-induced hypertriglyceridemia in rat // Metabolism. 1980. V. 4. P. 303-305.


