Морфологические критерии эффективности комплексной терапии венозных трофических язв нижних конечностей, включающей обработку анолитом нейтральным АНК и лазерным излучением
Автор: Чернеховская Н.Е., Шишло В.К., Чомаева А.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Экспериментальные и лабораторные исследования
Статья в выпуске: 4 (32), 2013 года.
Бесплатный доступ
Нелинейным белым крысам создавали модель инфицированной кожной раны путем скарификации эпидермиса в области наружной поверхности бедра с последующим нанесением культуры золотистого стафилококка L500 (штамм 13407), выделенного у больного сепсисом. Через сутки констатировали признаки воспаления. Животные были разделены на 4 группы: 1-я группа - интактные животные; 2-я группа - животные с моделью воспаления; 3-я группа - животным орошали раневую поверхность анолитом нейтральным АНК ежедневно, 3 раза в день; 4-я группа - обрабатывали рану лазерным излучением от гелий-неонового лазера УФЛ-01 «Ягода», работающий на длине волны 633 нм, мощность на выходе - 15-20 мВт. Экспозиция облучения равна 200 с. Обработку раневой поверхности проводили ежедневно, 3 раза в день. Обработка инфицированной раны ано- литом нейтральным АНК способствовала эпителизации раны через 10±1,4 сут., тогда как в контрольной группе животных раны эпителизировались через 21±1,6 сут. Это свидетельствует о том, что анолит нейтральный АНК стимулирует потенцию фибробластов к их интенсивному делению, что в конечном итоге ускоряет образование грануляционной ткани в ране. Обработка инфицированной раны низкоинтенсивным лазерным излучением способствует повышению митотической активности эпителиоцитов и фибробластов в 3 раза и очищению и эпителизации инфицированной раны через 16±1,2 сут. от начала лечения.
Венозная трофическая язва, анолит нейтральный анк, лазерное излучение
Короткий адрес: https://sciup.org/142211104
IDR: 142211104 | УДК: 615.47:616-085
Текст научной статьи Морфологические критерии эффективности комплексной терапии венозных трофических язв нижних конечностей, включающей обработку анолитом нейтральным АНК и лазерным излучением
Высокая частота неудовлетворительных результатов лечения больных хронической венозной недостаточностью нижних конечностей с венозными трофическими язвами объясняется тем, что при этой патологии происходят изменения микроциркуляторного русла, удлиняются фазы воспаления и регенерации, тормозится пролиферация фибробластов и снижается синтез ДНК, РНК, гликопротеидов и коллагена, что в свою очередь задерживает формирование грануляционной ткани и эпителизацию язв [1, 3, 4, 5, 12, 15] В течение последних 10–15 лет созданы принципиально новые виды медицинского оборудования, позволяющие повысить эффективность местного лечения ран. Эти аппараты работают на принципах квантовой техники – лазерные и плазменные установки, которые позволяют уничтожать в ране патогенные микроорганизмы и снизить опасность побочных явлений и осложнений [10, 11, 14].
В последнее время в клиническую практику постепенно начинает внедряться анолит нейтральный АНК. Технология электрохимической активации – это новая область прикладной электрохимии. Явление электрохимической активации воды было открыто в 1975 г. инженером В.М. Бахиром [2]. Сущность явления электрохимической активации состоит в том, что разбавленные растворы минеральных солей (к ним относится и обычная питьевая соль) в результате анодной или катодной (униполярной) обработки в диафрагменном электрохимическом реакторе переходят в метастабильное состояние, характеризующееся аномальной физико-химической активностью, которая постепенно убывает во времени (релаксирует). Именно в период релаксации ЭХА-среды проявляют свои главные технологические качества [16].
Электрохимическая обработка маломинерализованных водных растворов в первую очередь связана с превращени- ем разбавленных растворов хлорида натрия (менее 5 г/л) в экологически чистые активированные моющие, дезинфицирующие и стерилизующие растворы преимущественно для медицины и пищевой промышленности. Для их синтеза разработаны и серийно производятся установки типа СТЭЛ различных модификаций.
Актуальность использования электрохимически активированных растворов обусловлена их следующими свойствами: выраженным дезинфицирующим и стерилизующим эффектами, низкой стоимостью получаемых растворов, технологической простотой их получения, быстрым сроком самоокупаемости установок, производящих ЭХА-растворы [7, 9].
Данные об активации биоэнергетических и синтетических процессов в клетке под воздействием лазерного излучения объясняют то положительное влияние, которое оказывает когерентный свет на процессы физиологической и репаративной регенерации [8, 13]. Способность к регенерации является одним из основных свойств живого. Однако при определенных условиях процессы регенерации могут нарушаться. Лазерное излучение обеспечивает физиологический режим регенерации тканей, ограничивающий процессы рубцевания
Основу процесса регенерации после повреждения составляют клетки соединительной ткани [6]. У животных фазы раневого процесса не всегда соответствуют тем фазам, которые описаны у человека. Вот почему в нашей работе мы в основном сделали акцент на изучение пролиферативной активности основных клеточных популяций, которые являются важнейшими в ходе репаративной регенерации тканей.
Целью работы явилось изучение влияния анолита нейтрального АНК и лазерного излучения на пролиферативную активность эпителиоцитов кожи и фибробластов в условиях экспериментальной инфицированной раны.
Материал и методы
Экспериментальным животным – нелинейным белым крысам линии Вистар (1-я группа – интактные животные) создавали модель инфицированной кожной раны путем скарификации эпидермиса в области наружной поверхности бедра с последующим нанесением культуры золотистого стафилококка L500 (штамм 13407), выделенного у больного сепсисом (2-я группа – животные с моделью раневой инфекции). Через сутки констатировали признаки воспаления. Экспериментальным животным 3-й группы, сразу же после создания модели воспаления, проводили обработку раневой поверхности анолитом нейтральным АНК, который распыляли на рану через пульверизатор в течение 3-х минут 3 раза в день, ежедневно. Обработку раневой поверхности животным 4-й группы проводили с помощью лазерного излучения. В качестве источника когерентного лазерного излучения использовали гелий-неоновый лазер УФЛ-01 «Ягода», работающий на длине волны 633 нм, мощ- ность на выходе – 15–20 мВт. Экспозиция облучения равна 200 с. Обработку раневой поверхности проводили 3 раза в день, ежедневно.
В дальнейшем через 3, 5 и 7 суток от начала эксперимента с помощью иммуногистохимических методов исследовали клетки фибробластического ряда и получили следующие результаты.
Иммуногистохимическое исследование клеток фибробластического ряда, под которым подразумеваются клетки от малодифференцированных до зрелых [17], показало их интенсивное деление при воздействии анолита нейтрального АНК (рис., табл. 1).
Как видно из таблицы 1, интенсивность пролиферативных процессов клеток фибробластического ряда у контрольной группы животных составляет 1,71±0,11 кл. В условиях экспериментального воспаления количество пролиферирующих клеток у 2-й группы животных на 3-и сутки увеличилось по сравнению с интактными животными и составило 2,13±0,1 кл., а затем продолжало нарастать
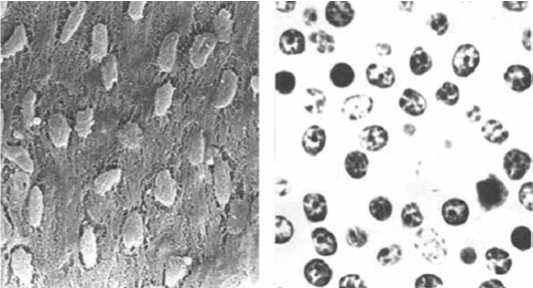
а
б
Интенсивное деление клеток фибробластического ряда, под воздействием анолита нейтрального АНК: а – СЭМНП, ×240; б – полутонкий срез, ×240
Таблица 1
Пролиферативная активность клеток фибробластического ряда при обработке анолитом нейтральным АНК экспериментальной инфицированной раны
На 2-е сутки после воздействия анолита нейтрального АНК на инфицированную кожную рану наблюдалось очищение раны, а с 3-х суток – появление грануляций в дне. Это свидетельствует о том, что анолит нейтральный АНК стимулирует потенцию фибробластов к их интенсивному делению, что в конечном итоге ускоряет образование грануляционной ткани в ране.
Во всех эпителиальных тканях любого происхождения (экто-, эндо- и мезодермального) существуют ростковые или стартовые зоны. В многослойных эпителиях, к которым принадлежит эпителий кожи, стартовые зоны расположены в базальном слое. Эти клетки мало специализированы, и поэтому они сохранили способность делиться. В процессе пролиферации образующиеся новые клетки продвигаются по направлению к поверхности эпителиального пласта и по мере продвижения специализируются для выполнения защитных функций. Достигнув поверхности, они теряют способность к делению [18], В результате механических повреждений или воспалительной реакции в ходе раневого процесса условия к делению клеток становятся более благоприятными, поскольку в результате указанного процесса возникает нарушение контактного торможения клеток. В связи с этим в ходе экспериментальной работы мы исследовали пролиферативную активность базальных эпителиоцитов многослойного плоского ороговевающего эпителия кожи в области раны.
Исследование пролиферативной активности эпителиоцитов интактных животных, так же как и клеток фибробластического ряда, показало их низкую активность (табл. 2).
В области краев раны в условиях модели раневой инфекции заметно увеличение потенции клеток эпителиального пласта, их деление, но нарастает оно значительно медленнее к 7-м суткам, чем популяции фибробластов в ранее приведенном исследовании.
При ежедневном орошении анолитом нейтральным АНК раневой поверхности заметно побуждение клеток базального слоя эпителия к делению. Как показало исследование эпителиальных клеток, анолит нейтральный АНК ускоряет процессы регенерации инфицированной раны. Так, уже на 3-и сутки в сравнении с 1-ой и 2-ой группами животных отмечено увеличение количества клеток эпителиального пласта более чем в 2 раза (5,17±1,13), а затем происходило нарастание массы эпителия к 7-м суткам (12,51±1,34).
Раны в основной группе животных полностью эпи-телизировались к 10-м–11-м суткам. В группе контроль-
Таблица 2
Пролиферативная активность эпителиоцитов при воздействии анолита нейтрального АНК в условиях экспериментальной раневой инфекции
После воздействия лазерного излучения на инфицированную кожную рану в 4-й группе животных, начиная с 3-х суток, наблюдали очищение раны, а с 5-х суток – появление грануляций в дне раны. Увеличилось количество эпителиоцитов и фибробластов в зоне раневой поверхности. Так, в контрольной группе животных митотическая активность эпителиоцитов через 3 суток была 1,71±0,11, в основной группе – 3,17±0,13, а через 7 суток – 5,51±0,34. Количество фибробластов по сравнению с контрольными животными (2,13±0,11) увеличилось в два раза (4,41±0,52), продолжало нарастать и к 7-м суткам составило 6,91±1,06. Раны в основной группе животных полностью эпителизировались к 16-м – 17-м суткам.
Выводы
-
1. При воздействии анолита нейтрального АНК на экспериментальные гнойные раны митотическая активность эпителиоцитов повышалась через 7 сут. в 7,3 раза, а количество фибробластов – в 3,2 раза по сравнению с показателями у контрольных животных.
-
2. Обработка инфицированной раны анолитом нейтральным АНК способствовала эпителизации раны через 10±1,4 сут., тогда как в контрольной группе животных раны эпителизировались через 21±1,6 сут. Это свидетельствует о том, что анолит нейтральный АНК стимулирует потенцию фибробластов к их интенсивному делению, что в конечном итоге ускоряет образование грануляционной ткани в ране.
-
3. Обработка инфицированной раны низкоинтенсивным лазерным излучением способствует повышению митотической активности эпителиоцитов и фибробластов в 3 раза и очищению и эпителизации инфицированной раны через 16±1,2 сут. от начала лечения.
Список литературы Морфологические критерии эффективности комплексной терапии венозных трофических язв нижних конечностей, включающей обработку анолитом нейтральным АНК и лазерным излучением
- Амбулаторная ангиология. Руководство для врачей/Под ред. А.И. Кириенко, В.М. Кошкина, В.Ю. Богачева. М.: ЛИТТЕРРА, 2007. 328 с.
- Бахир В.М. Электрохимическая активация и технические электрохимические системы на основе проточных электролитических модульных элементов ПЭМ//Электрохимическая активация. 2-й Международный симпозиум. М., 1999. С. 10-15.
- Белов Ю.В. Руководство по сосудистой хирургии с атласом оперативной техники. М.:МИА, 2011. 464 с.
- Бендерский Ю.Д., Киршин А.А., Морозов А.А. Наш опыт лечения тяжелых трофических расстройств у больных посттромбофлебитической болезнью нижних конечностей в сочетании с сахарным диабетом II типа//Сердечно-сосудистые заболевания. Приложение. XI ежегодная сессия НЦ Сердечно-сосудистой хирургии им. А.Н. Бакулева РАМН. М., 13-15 мая 2007. С. 70.
- Берченко Г.Н. Морфологические аспекты заживления осложненных ран. Автореф..дис. д-ра мед. наук. М., 1997. 43 с.
- Волкова О. В., Шахламова В. А., Миронова А. А. Атлас сканирующей электронной микроскопии клеток, тканей и органов. М.: Медицина, 1987.
- Девятов В.А., Петров С.В., Янгилев Ф.Ш.и др. Экономическая оценка результатов лечения гнойных хирургических заболеваний и ран с применением активированных электрохимическим методом водных растворов//Электрохимическая активация. 2-й Международный симпозиум. М., 1999. С. 133-135.
- Дуванский В.А. Физические и физико-химические методы в комплексном лечении гнойных ран и трофических язв. Автореферат дис..докт. мед. наук. М., 2002. 30 с.
- Леонов Б.И., Бахир В.М., Вторенко В.И. Электрохимическая активация в практической медицине//Электрохимическая активация. 2-й Международный симпозиум. М., 1999. С. 15-23.
- Марахонич Л.А., Вережан Ю.М., Вигриянов Ю.П. и др. Применение воздушно-плазменных потоков и монооксида азота в лечении гнойной хирургической инфекции, трофических язв, пролежней//NO-терапия: теоретические аспекты, клинический опыт и проблемы применения экзогенного оксида азота в медицине. М., 2001. С. 113 -114.
- Москаленко В.И. Комплексное лечение огнестрельных ранений с использованием оксида азота и лимфогенных методов (клинико-экспериментальное исследование). Дис.докт. мед. наук. М., 2006. 238 с.
- Савельев В.С., Кириенко А.И., Богачев В.Ю. Венозные трофические язвы. Мифы и реальность//Флеболимфология. 2000. №11. С. 5-10.
- Толстых П.И., Клебанов Г.И., Шехтер А.Б. Антиоксиданты и лазерное излучение в терапии ран и трофических язв. М.: Издательский дом «Эко», 2001. 240 с.
- Толстых П.И., Луцевич Э.В., Толстых М.П. и др. На рубеже нового тысячелетия -традиционные догмы и ориентации на современные лечебные технологии в профилактике нагноений ран и лечении трофических язв//Мат. итогов научной работы за 2000 год: Сб. науч.тр. М., 2001. С. 65-66.
- Толстых П.И., Тамразова О.Б., Павленко В.В., Кулешов И.Ю., Толстых М.П. Длительно незаживающие раны и язвы. Патогенез, клиника, лечение. М.: Дипак, 2009. 168 с.
- Электрохимическая активация: история, состояние, перспективы//Под ред. профессора В.М. Бахира. Академия медико-технических наук РФ. М., 1999. С. 5-9.
- Дейл М. М., Джон К. Формен. Руководство по иммунофармакологии. М.: Медицина, 1998. 332 с.
- Хэм А., Кормак Д. Гистология. М.: Мир, в 5 т., 1983.


