Морфологические особенности брахиоцефальных артерий у пациентов с гипоплазией дуги аорты
Автор: Сойнов Илья Александрович, Синельников Ю.С., Кливер Е.Э., Корнилов И.А., Ничай Н.Р., Горбатых А.В., Кулябин Ю.Ю., Горбатых Ю.Н.
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Врожденные пороки сердца
Статья в выпуске: 4 т.19, 2015 года.
Бесплатный доступ
Цель Оценить особенности морфологии и характер структурных изменений стенки левой подключичной артерии у новорожденных и младенцев с коарктацией и гипоплазией дуги аорты. Материал и методы В исследование включили 27 пациентов с гипоплазией дуги аорты в возрасте 64 (27; 89) дней, средней массой тела 3,6±1,1 (1,8-6,9) кг, оперированных в центре детской хирургии ННИИПК им. акад. Е.Н. Мешалкина в 2013-2014 гг. Всем пациентам выполняли хирургическую коррекцию гипоплазии дуги аорты без искусственного кровообращения с модифицированной реверсивной пластикой лоскутом левой подключичной артерии. Интраоперационно осуществляли забор фрагмента левой подключичной артерии с целью определения степени васкуляризации, соотношения эластина и коллагена. Сравнивали результаты с показателями контрольной группы, которую составили образцы левой подключичной артерии у пациентов (п = 27) аналогичного возраста, умерших после операции по поводу врожденных пороков сердца без гипоплазии дуги аорты. Результаты Обнаружили достоверные различия в содержании тонких коллагеновых и эластических волокон у пациентов с гипоплазией дуги и пациентов с нативной аортой. Особенностями являются достоверно большее содержание тонких коллагеновых и меньшее содержание эластических волокон в стенке подключичной артерии у пациентов с гипоплазией дуги аорты. Заключение Морфология подключичной артерии у детей с гипоплазией дуги характеризуется увеличением количества коллагеновых и уменьшением эластических волокон, что обусловлено пролиферацией гладких миоцитов, миофибробластов, фибробластов и изменением их соотношения. Данные особенности определяют изменения эластических характеристик сосудистой стенки - повышение ригидности.
Гипоплазия дуги аорты, морфология, эластичность
Короткий адрес: https://sciup.org/142140697
IDR: 142140697
Morphological features of brachiocephalic arteries in patients with aortic arch hypoplasia
Objective. The study was designed to assess the morphology and structural changes in the walls of the left subclavian artery in neonates and infants with coarctation and aortic arch hypoplasia. Methods. The study included 27 patients with hypoplasia of the aortic arch at the age of 64 (27; 89) days, average body weight of 3.6±1.1 (from 1.8 to 6.9 kg), who were operated at the Center of Pediatric Surgery of Academician Ye. Meshalkin Research Institute of Circulation Pathology in the period from 2013 to 2014. All patients underwent off-pump surgery of hypoplasia of the aortic arch by using modified reverse plasty with a patch from the left subclavian artery. The patch was taken intraoperatively to determine the ratio of elastin and collagen. The results were compared with those of the control group. Results. Significant differences were found in the content of collagen and elastic fibers in patients with aortic arch hypoplasia. Patients with hypoplasia had a significantly higher content of thin collagen and a lower content of elastic fibers in the wall of the subclavian artery. Conclusion. The morphology of the subclavian artery in children with aortic arch hypoplasia is characterized by an increase of collagen and a decrease of elastic fibers due to the proliferation of smooth muscle cells, myofibroblasts, fibroblasts and the change in their relationship. These features determine the changes in elastic characteristics of the vascular wall, i.e. increased rigidity.
Текст научной статьи Морфологические особенности брахиоцефальных артерий у пациентов с гипоплазией дуги аорты
Гистологические показатели стенки левой подключичной артерии
Цель – оценить особенности морфологии и характер структурных изменений стенки левой подключичной артерии у новорожденных и младенцев с коарктацией и гипоплазией дуги аорты.
Материал и методы
В исследование включили 27 пациентов с гипоплазией дуги аорты в возрасте 63,6±89,6 (1–281) дня, средней массой тела 3,6±1,1 (1,8–6,9) кг, оперированные в центре детской хирургии ФГБУ «ННИИПК им. акад. Е.Н. Мешалкина» в 2013–2014 гг. Всем пациентам выполняли хирургическую коррекцию гипоплазии дуги аорты без искусственного кровообращения с модифицированной реверсивной пластикой лоскутом левой подключичной артерии. Интраоперационно осуществляли забор фрагмента левой подключичной артерии с целью определения степени васкуляризации, соотношения эластина и коллагена. Сравнивали результаты с показателями контрольной группы, которую составили образцы левой подключичной артерии у пациентов (n = 27) аналогичного возраста, умерших после операции по поводу врожденных пороков сердца без гипоплазии дуги аорты.
Фрагменты подключичных артерий, взятых интраоперационно у больных с гипоплазией дуги аорты и на аутопсии у пациентов без патологии аорты, фиксировали в 10% растворе формалина на фосфатном буфере и заливали в парафин. Подготовили срезы толщиной 4 мкм на микротоме фирмы Microm HM 550 и окрашивали гематоксилин-эозином по методу Ван Гизона с комбинированной докраской эластики орсеином, также устанавливали РAS-реакции методом импрегнации срезов серебром по Гомори и методом Пикро Маллори (Picro Mallory Trichromica). Обзорную гистологию проводили с помощью программно-микроскопного комплекса, который включал световой микроскоп Imadger M2 (ZEISS, Германия), цифровую видеокамеру AxioCam НRc и компьютер Pentium 4. Иммуногистохимическое окрашивание гистологических препаратов выполнили на автоматическом иммуногистостейнере Benchmark XT Ventana с помощью мышечного актина (Actin Muscle (HUC-1)), гладкомышечного миозина (Myosin, Smooth Muscle (SMMS-1)) и системы визуализации ultraView Universal DAB Detection Kit (Roche). При стереомор-фометрическом исследовании изучали степень васкуляризации, соотношение эластина и коллагена, а также изменение их соотношения в стенке неизмененной подключичной артерии и подключичной артерии у пациентов с гипоплазией дуги аорты.
Статистический анализ
Статистическую обработку проводили с использованием пакета прикладных программ Stata 13. Оценивали нормальность распределения признака с помощью гистограммы распределения признака, а также критериев Колмогорова – Смирнова, Лиллиефорса и Шапиро – Уилка. Для описательной статистики нормально распределенных количественных признаков использовали параметрические методы: вычисление средних значений и средних квадратических отклонений. Для количественных признаков с неправильным распределением, а также качественных (порядковых и номинальных) признаков применяли непараметрические методы – вычисления медиан и соответствующий интервал между 75-м и 25-м процентилями. При сравнении двух независимых групп использовали t-критерий Стьюдента для признаков с гауссовским распределением и U-критерий Манна – Уитни для признаков с неноминальным распределением. Значение не более 0,05 считали статистически достоверным.
Результаты
При гистологическом исследовании васкуляризации стенки подключичной артерии у детей с гипоплазией дуги аорты не обнаружили достоверной разницы по этому показателю с контрольной группой ( таблица ).
Содержание тонких коллагеновых волокон в стенке подключичной артерии у пациентов контрольной груп-
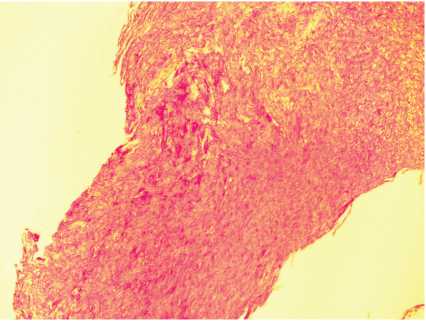
Рис. 1. Фрагмент подключичной артерии у пациентов с гипоплазией дуги аорты (гипоэластоз с образованием «плешей»). Окраска по Ван Гизону. Увеличение х 180
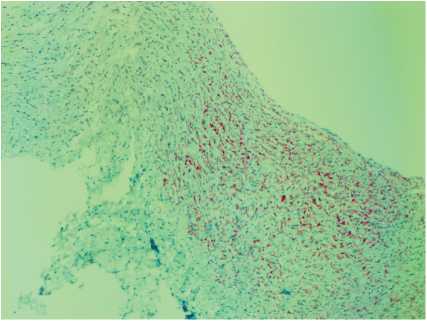
Рис. 2. Неравномерное распределение миозина в стенке подключичной артерии у пациентов с гипоплазией дуги аорты. Иммуногистохимическая окраска с использованием Myosin, Smooth Muscle (SMMS-1). Увеличение х 180
пы было достоверно ниже, чем в артерии у пациентов с гипоплазией дуги (p<0,05), а содержание эластических волокон в стенке нормальной подключичной артерии, напротив, выше (p<0,05). В то же время в обеих группах наблюдалась тенденция к уменьшению количества эластических волокон с течением времени (p<0,05). В стенке подключичной артерии у пациентов с гипоплазией аорты также отмечен гипоэластоз вплоть до развития «плешей» (рис. 1). Увеличение тонких коллагеновых волокон в образцах артерии у пациентов с гипоплазией дуги указывает на нарушение синтеза гладких миоцитов (рис. 2), фибробластов, миофибробластов на фоне текущего повреждения клеточно-волокнистых структур с развитием во внутренней и средней оболочках подключичной артерии миксоматозной мышечно-фиброзной ткани (рис. 3), представленной пролиферирующими клеточными элементами, вокруг которых развивается рыхлая соединительная ткань, содержащая тонкие коллагеновые волокна.
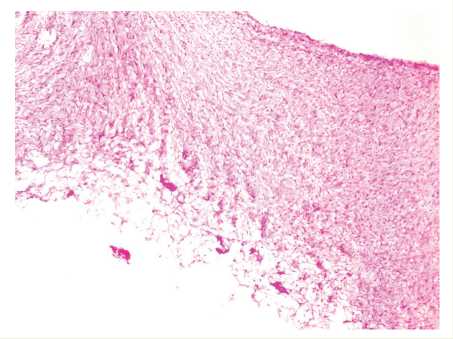
Рис. 3. Участки миксоматозной мышечно-фиброзной ткани. Окраска: гематоксилин-эозином. Увеличение х 180
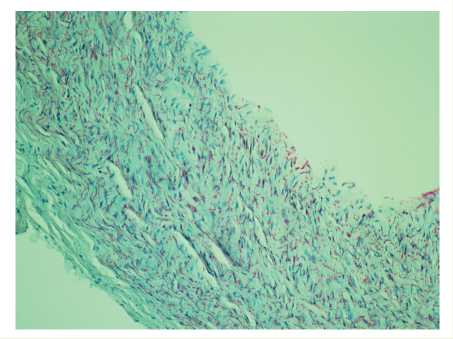
Рис. 4. Интрамуральные сосуды адвентициальной и медиальной оболочек подключичной артерии. Иммуногистохимическая окраска с использованием Аctin Muscle (HUC-1). Увеличение х 180
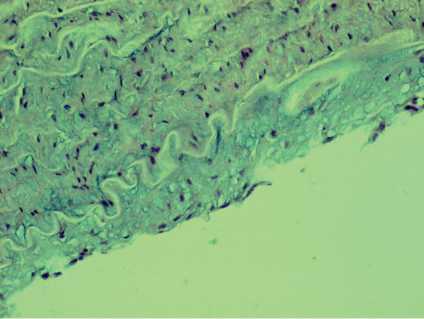
Рис. 5. Скопления липидов и пенистых клеток в интимальном слое. Окраска Picro Mallory Trichromica.
Увеличение х 280
Новообразование сосудов капиллярного типа в адвентициальной оболочке подключичной артерии у пациентов с гипоплазией дуги аорты происходит из собственных сосудов при участии эндотелиальных и гладкомышечных клеток, адвентициальных фибробластов и протекает с уменьшением количества интрамуральных сосудов (рис. 4).
В единичных случаях со стороны интимы обнаружили скопления липидов и пенистых клеток, что указывает на ранние гистологические признаки атеросклероза у данной категории больных (рис. 5).
Обсуждение
Подключичная артерия, как и любой сосуд эластического типа, имеет эластико-коллагеновый каркас, основная функция которого – передача пульсовой волны и превращение пульсирующего тока крови в более равномерный. При врожденной обструктивной патологии дуги аорты происходит нарушение эластико-коллагено-вого каркаса, что приводит к сосудистой дисфункции [9, 10], которая в свою очередь у пациентов после коррекции гипоплазии дуги аорты может влиять на долгосрочный прогноз. 30% пациентов с этой патологией имеют риск раннего возникновения артериальной гипертензии, аневризм аорты и брахиоцефальных сосудов, ишемической болезни сердца и ишемического инсульта [3]. Впервые сосудистую дисфункцию описали в 1985 г., что явилось прорывом в понимании патологического процесса [11]. Выявили патологическую сосудистую реактивность предплечья и нормальную реактивность сосудов голени у детей с обструктивной патологией аорты. Как правило, такие пациенты имеют морфофункциональные нару- шения крупных артерий. До сих пор остается неясной причина вышеуказанных осложнений: патология гладких миоцитов, волокнистых структур или их сочетание [1, 2, 5]. Многие авторы сосредотачиваются на морфологических изменениях самой аорты, не уделяя должного внимания брахиоцефальным сосудам [5, 7]. На наш взгляд, проблема носит комплексный характер. Как и в других морфологических исследованиях артерий эластического типа у пациентов с обструктивной патологией дуги аорты, мы обнаружили увеличение коллагеновых волокон и снижение эластических вплоть до их полного отсутствия. Такие изменения эластико-коллагенового состава приводят к повышенной жесткости и сниженной растяжимости артерии. Даже после устранения обструкции на уровне дуги соотношение эластических и коллагеновых волокон не изменяется, продолжая снижаться с течением времени. В норме у детей раннего возраста также имеется физиологическое снижение эластина [12], однако оно чередуется с увеличением эластических волокон, что не происходит у детей с обструктивной патологией аорты, даже если она была коррегирована в младенчестве. Такие изменения в стенке сосудов эластического типа предрасполагают к системной артериальной гипертензии [1, 4, 10].
Также мы обнаружили повреждения клеточно-волокнистых структур с развитием во внутренней и средней оболочках подключичной артерии миксоматозной мышечно-фиброзной ткани, представленной пролиферирующими клеточными элементами, а также патологию vasa vasorum. Подобные изменения описаны при аневризмах аорты [13–15], поэтому обструктивная патология дуги аорты – возможный фактор риска образования аневризм.
Как и Тодоров С.С., изучавший морфологию различных сегментов аорты [7], мы обнаружили ранние признаки атеросклероза. Meyer A.A. и соавторы показали, что дегенеративные и пролиферативные изменения в брахиоцефальных артериях и аорте приводят к ранней инвалидности больных и высокой летальности в общей популяции пациентов с обструктивной патологией дуги аорты [15].
Заключение
Морфология подключичной артерии у детей с гипоплазией дуги характеризуется увеличением коллагеновых и уменьшением эластических волокон, что обусловлено пролиферацией гладких миоцитов, миофибробластов, фибробластов и изменением их соотношения. Данные особенности определяют изменения физических характеристик сосудистой стенки (повышение ригидности). Во внутреннем и среднем слоях артерии отмечается гиперплазия гладких миоцитов, 7. миофибробластов, фибробластов с формированием мышечно-фиброзной ткани. В адвентиции уменьшается количество интрамуральных сосудов, развиваются кровоизлияния. Все вышеуказанные изменения в комплексе обусловливают снижение эластичности и приводят к развитию гемодинамических нарушений.
Список литературы Морфологические особенности брахиоцефальных артерий у пациентов с гипоплазией дуги аорты
- Сойнов И.А., Синельников Ю.С., Горбатых А.В. Ничай Н.Р., Иванцов С.М., Корнилов И.А., Кшановская М.С., Горбатых Ю.Н. Артериальная гипертензия у пациентов после коррекции коарктации и гипоплазии дуги аорты//Патология кровообращения и кардиохирургия. 2015. Т. 19. № 2. С. 102-113.
- Синельников Ю.С., Кшановская М.С., Горбатых А.В., Иванцов С.М., Прохорова Д.С. Гипоплазия дуги аорты//Патология кровообращения и кардиохирургия. 2013. № 3. С. 68-72.
- Toro-Salazar О.Н., Steinberger J., Thomas W., Rocchini A.P., Carpenter B., Moller J.H. Long-term follow-up of patients after coarctation of the aorta repair//Am. J. Cardiol. 2002. Vol. 89. P. 541-547.
- Синельников Ю.С., Кшановская M.C., Прохорова Д.С. и др. Хирургическая коррекция коарктации аорты, всегда ли оправданы ожидания?//Сибирский медицинский журнал. 2013. Т. 28. № 4. С. 55-58.
- Machii М., Becket A. Hypoplastic aortic arch morphology pertinent to growth after surgical correction of aortic coarctation//Ann. Thorac. Surg. 1997. Vol. 64. P. 516-20.
- Прохорова Д.С., Нарциссова Г.П., Горбатых Ю.Н., Синельников Ю.С., Субботин Д.В. Сравнительная оценка эластических свойств аорты у новорожденных с коарктацией аорты до и после хирургической коррекции//Патология кровообращения и кардиохирургия. 2011. № 2. С. 17-20.
- Тодоров С.С. Патоморфологическая характеристика изменений аорты при коарктации у детей первого года жизни//Вестник ВолГМу. 2009. № 3. С. 73-76.
- Синельников Ю.С., Горбатых Ю.Н., Горбатых А.В., Иванцов С.М., Стрельникова М.С., Чащин О.В., Прохорова Д.С., Литасова Е.Е. Хирургическое лечение коарктации с гипоплазией дистального отдела дуги аорты у новорожденных//Патология кровообращения и кардиохирургия. 2011. № 3. С. 9-12.
- Горбатых Ю.Н., Синельников Ю.С., Сойнов И.А. и др. Хирургическая коррекция аномалий дуги аорты у младенцев в условиях искусственного кровообращения//Хирургия. 2015. № 8. С. 18-21.
- O'Sullivan J.J. Late hypertension in patients with repaired aortic coarctation//Curr. Hypertens. Rep. 2014. Vol. 16. P. 421-26.
- Gidding S., Rocchini A., Moorehead C., Schork M., Rosenthal A. Increased forearm vascular reactivity in patients with hypertension after repair of coarctation//Circulation. 1985. Vol. 71. P. 495-9.
- Machii M., Becker A.E. Morphologic features of the normal aortic arch in neonates, infants, and children pertinent to growth//Ann. Thorac. Surg. 1997. Vol. 64. P. 511-5.
- Тодоров С.С. Клинико-морфологическая характеристика изменений аорты при синдроме Марфана у детей и взрослых//Детские болезни сердца и сосудов. 2010. № 1. С. 52-57.
- Новикова Е.Г., Титова Г.П., Таланкина И.Е. Морфологические изменения стенки аорты при расслаивающей аневризме//Архив патологии. 2013. № 6. С. 3-9.
- Новикова Е.Г., Таланкина И.Е. Морфологические особенности возрастных изменений в стенке аорты при расслаивающейся аневризме//Архив патологии. 2015. № 1. С. 18-23.
- Meyer А. A., Joharchi M.S., Kundt G., Schuff-Werner Р., Steinhoff G., Kienast W. Predicting the risk of early atherosclerotic disease development in children after repair of aortic coarctation//Eur. Heart J. 2005. Vol. 26. P. 617-22.


