Морфологические особенности миокарда при экспериментальном сахарном диабете и его фармакологической коррекции мефаргином
Автор: Тюренков Иван Николаевич, Смирнов Алексей Владимирович, Бакулин Дмитрий Александрович, Великородная Юлия Ивановна
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Статья в выпуске: 4 (76), 2022 года.
Бесплатный доступ
При экспериментальном моделировании сахарного диабета обнаружено развитие фиброзирования и гипертрофии миокарда левого желудочка сердца, что рассматривается как морфологическое проявление диабетической кардиомиопатии. Наблюдаемое под влиянием мефаргина снижение степени выраженности патологических изменений в миокарде левого желудочка выражается в снижении доли соединительной ткани и периваскулярного фиброза, снижению выраженности гипертрофии, что реализуется, по-видимому, благодаря протективному влиянию препарата на эндотелий кровеносных сосудов миокарда.
Сахарный диабет, кардиомипатия, мефаргин
Короткий адрес: https://sciup.org/142236027
IDR: 142236027 | УДК: 616-005.4:611.813.14:616-092.9
Morphological features of the myocardium in experimental diabetes mellitus and its pharmacological correction with mefargin
In experimental modeling of diabetes mellitus, the development of fibrosis and hypertrophy of the myocardium of the left ventricle of the heart was found, which is considered as a morphological manifestation of diabetic cardiomyopathy. The decrease in the severity of pathological changes in the myocardium of the left ventricle observed under the influence of mefargin is expressed in a decrease in the proportion of connective tissue and perivascular fibrosis, a decrease in the severity of hypertrophy, which is realized, apparently, due to the protective effect of the drug on the endothelium of myocardial blood vessels.
Текст научной статьи Морфологические особенности миокарда при экспериментальном сахарном диабете и его фармакологической коррекции мефаргином
Заболеваемость и смертность от сахарного диабета (СД) представляет собой мировую медицинскую проблему, согласно прогнозу ВОЗ и данным Международной диабетической федерации (IDF) распространенность СД достигнет 10,4% (642 миллиона) к 2040 г. Диабетические макро- и микроангиопатии играют ведущую роль в развитии диабетических кардиальных осложнениях, диабетической кардиомиопатии (ДКМП) и хронической сердечной недостаточности, в т.ч. включаясь в общий патогенез коморбидной патологии [1,4,6].
В основе связи диабета и сердечной недостаточности лежит не только осложнение СД в виде ишемии миокарда, но и метаболические нарушения, такие как токсичность глюкозы и липотоксичность на фоне инсулинорезистентности, дисфункции эндотелия сосудов, нарушения микроциркуляции, и капиллярная недостаточность [8].
Показано, что запущенное гипергликемией нарушение обмена веществ при СД может вести к эндотелиальной дисфункции, окислительному стрессу, нарушению проницаемости стенок капилляров, за счет процессов гликирования белков, что приводит к нарушению обмена веществ [5].
На более поздних стадиях диабетической кардиомиопатии обнаруживается гипертрофия ЛЖ и прогрессирующая диастолическая и систолическая дисфункция сердца, сопровождающейся снижением фракции выброса и сердечной недостаточностью. Кроме того, длительное воздействие окислительного стресс приводит к запуску механизмов хронического воспаления и фиброзированию миокарда [6].
Диабетические кардиальные осложнения приводят к острой необходимости эффективного лечения. Однако классические сахароснижающие методы лечения в целом оказывают нейтральное влияние на смертность от сердечно-сосудистых заболеваний при диабете и иногда даже усугубляют сердечную недостаточность [10].
Разработанный препарат мефаргин, проявляющий выраженные эндотелиопротективные свойства, улучшающий эндотелиальную функцию за счет повышения выработки NO эндотелием, представляет собой новый класс эндоте-лиопротективных средств, которые могут быть использованы при комплексном лечении СД на фоне применения противодиабетических препа- ратов [2].
Цель. Оценить морфологические особенности миокарда при экспериментальном сахарном диабете и его фармакологической коррекции ме-фаргином.
Методика исследования
Экспериментальное исследование проведено на 30 белых беспородных лабораторных крысах-самках, в возрасте 12 мес. Животные содержались в условиях вивария (ГОСТ Р 518492001) со свободным доступом к питьевой воде и пище (ООО «Лабораторкорм», Москва). В качестве патологии была выбрана экспериментальная модель, рекомендованная для изучения отдаленных последствий сахарного диабета, в которой с целью формирования осложнений СД используют крыс со стрептозотоциновым диабетом длительностью 6 месяцев. Стрепто-зотоцин-индуцированный СД моделировали однократным внутрибрюшинным введением растворенного в цитратном буфере (0,1 М, рН 4,5) стрептозотоцина («Sigma», США) в дозе 60 мг/ кг после 48-часовой пищевой депривации. В исследование брали животных с уровнем тощако-вой (забор корма за 4 часа до измерения) гликемии ≥ 15 ммоль/л через 3 дня и 6 месяцев после инъекции [3]. Для измерения уровня гликемии использовали глюкометр Contour TS и соответствующие тест-полоски (Bayer). Кровь для измерений забирали при пункции подъязычной вены. Лечение начинали через 6 месяцев после моделирования СД. Исследуемое производное ГАМК – мефаргин вводили перорально в течение 30 дней в дозе 20 мг/кг. Группе негативного контроля вводили физиологический раствор (крысы с СД без лечения). В качестве позитивного контроля использовали крыс без СД (интактных) той же партии животных.
После курсового лечения у наркотизированных (хлоралгидрат, 400 мг/кг, внутрибрюшинно) животных проводили забор образцов тканей левого желудочка сердца. Образцы тканей левого желудочка сердца проводили у наркотизированных (хлоралгидрат, 400 мг/кг, внутрибрюшинно) животных. Материал фиксировали в течение 24 часов в 10% растворе нейтрального забу-ференного формалина (pH 7,4), обезвоживали и заливали в парафин по общепринятой гистологической методике. На роторном микротоме изготавливали срезы толщиной 4-5 мкм. Окра- шивали парафиновые срезы гематоксилином и эозином, трихромом по Массону.
Гистологические срезы фотографировали цифровой камерой AxioCam 305 color (Carl Zeiss Microscopy GmbH, Германия) на базе микроскопа AxioImager A2 (Carl Zeiss Microscopy GmbH, Германия) с использованием объективов х10, х20, х40. Средний диаметр кардиомиоцитов (мкм) определяли помощью морфометрического метода исследования в произвольно выбранных областях левого желудочка с использованием программного обеспечения Zeiss Zen Pro 2.3 2021 (Carl Zeiss Microscopy GmbH, Германия).
Статистическую обработку данных проводили с использованием пакета программы «Statistica 10.0» (USA). Проверку выборки на нормальность проводили с помощью теста Колмогорова-Смирнова. Сравнение двух независимых выборок проводили непараметрическим методом (парный тест Манна-Уитни). Сравнение трех и более независимых выборок проводили непараметрическим методом (критерий Краске-ла-Уоллиса с посттестом Данна). Гипотезу о существовании различий между выборками принимали при уровне р<0,05.
Результаты и их обсуждение
У животных с сахарным диабетом, не получавших лечения, была выявлены дистрофические изменения в кардиомицитах и гипертрофия миокарда левого желудочка. Преобладали гипертрофированные кардиомиоциты, встречались участки с клетками, диаметр которых близок к норме, встречались отдельные мышечные клетки с признаками отека.
Было выявлено увеличение доли фиброзной соединительной ткани в миокарде. По сравнению с интактным контролем (рисунок 1) в миокарде крыс с экспериментальным сахарным диабетом отмечалось фиброзирование, увеличение доли соединительной ткани в периваскулярном и интерстициальном компартментах. Определялось очаговое выраженное капиллярное и венозное полнокровие, незначительный периваскулярный и интерстициальный отек. В некоторых случаях более выраженный очаговый фиброз миокарда наблюдался в субэндокардиальных отделах, был менее выражен в миокарде правого желудочка и сопровождался умеренно выраженной лимфоидной инфильтрацией областей фиброза (рисунок 2).
При проведении морфометрического исследования отмечалось статистически значимое увеличение среднего диаметра кардиомиоцитов на 74,1% (при p<0,001) по отношению к группе интактного контроля. Средний диаметр кардиомиоцитов левого желудочка у животных с сахарным диабетом составил 16,55±3,04 мкм (ме- диана 16,40 [14,11783; 18,42735]), аналогичный показатель у интактных крыс - 9,51±1,89 мкм (медиана 9,41 [8,32797; 10,74161]).
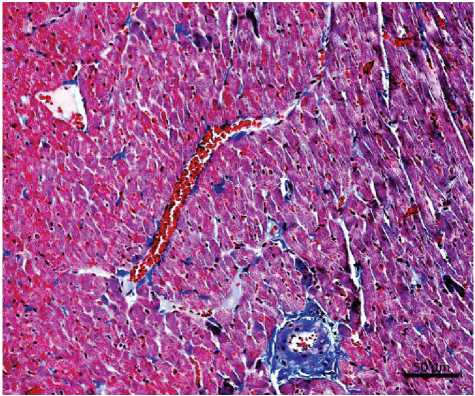
Рисунок 1. Строение миокарда левого желудочка интактной крысы.
Окраска трихромом по Массону.
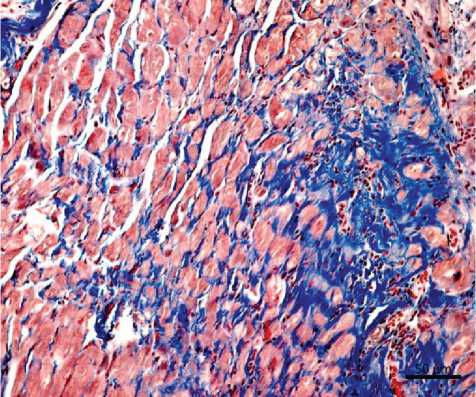
Рисунок 2. Строение миокарда левого желудочка крысы с экспериментальным сахарным диабетом.
Окраска трихромом по Массону.
У животных, получавших мефаргин, было отмечено менее выраженное фиброзирование миокарда за счет меньшего разрастания периваскулярной соединительной ткани, по сравнению с группой сахарного диабета. В кардиомиоцитах определялась хорошо выраженная поперечная исчерченность, наряду с наличием дистрофических изменений. Наблюдалось умеренное фиброзирование в периваскулярных отделах.
При проведении морфометрического исследования у животных с сахарным диабетом, получавших мефаргин, отмечалось статистически
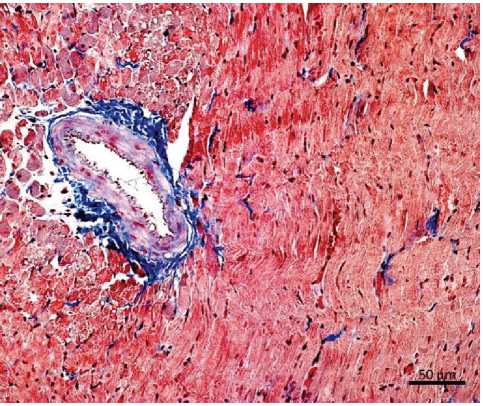
Рисунок 3. Строение миокарда левого желудочка крысы с экспериментальным сахарным диабетом, получавших мефаргин.
Окраска трихромом по Массону.
значимое снижение среднего диаметра кардиомиоцитов на 22,0% (при p<0,001) по отношению к группе животных с сахарным диабетом без лечения, однако было выявлено увеличение среднего диаметра кардиомиоцитов на 35,8% (при p<0,001) по отношению к группе интактного контроля. Средний диаметр кардиомиоцитов левого желудочка у животных с сахарным диабетом, получавших мефаргин, составил 12,91±2,39 мкм (медиана 12,73 [11,06113; 14,28153]).
Обнаруженная морфологическая картина свидетельствует о развитии очагового фиброза и гипертрофии миокарда левого желудочка сердца при экспериментальном СД. Протектив-ное влияние мефаргина на миокард левого желудочка, по нашему мнению, реализуется посредством протективного влияния препарата на эндотелий кровеносных сосудов миокарда, что способствуют снижению доли соединительной ткани и периваскулярного фиброза, снижению выраженности гипертрофии. Считается, что эндотелиальная дисфункция является ключевым фактором в развитии ДКМП и реализуется посредством влияния на эндотелий ряда патогенных факторов: гипергликемии, снижения уровня оксида азота, оксидативного стресса, ПОЛ, активации механизмов воспаления и повреждения барьерных функций [7], протекция эндотелия сосудов сердца может способствовать большей сохранности миокарда и снижению выраженности ДКМП при сахарном диабете, что подтверждает результаты нашего исследования. Однако исследования фиброза миокарда при моделировании ДКМП утверждают, что повреждение эндотелия способствует снижению степени ангиогенеза и фиброза в миокарде при СД [9].
ЗАКЛЮЧЕНИЕ
Таким образом, при экспериментальном моделировании СД обнаружено развитие фиброзирования и гипертрофии миокарда левого желудочка сердца, что рассматривается как морфологическое проявление ДКМП. Наблюдаемое под влиянием мефаргина снижение выраженности патологических изменений в миокарде левого желудочка, по нашему мнению, реализуется посредством протективного влияния препарата на эндотелий кровеносных сосудов миокарда. Изучение роли эндотелиальной дисфункции в патогенезе ДКМП требует дальнейшего углубленного анализа молекулярных механизмов.
Работа выполнена при финансовой поддержке гранта РНФ № 21-15-00192
Список литературы Морфологические особенности миокарда при экспериментальном сахарном диабете и его фармакологической коррекции мефаргином
- Патологическая анатомия коронавирусной инфекции в современных условиях /А.В. Смирнов, А.И. Бисинбекова, Н.В. Григорьева [и др.] // Волгоградский научно-медицинский журнал. 2021. № 4. С. 5-11.
- Роль NO-ергической системы в регуляции углеводного обмена и развитии сахарного диабета /Д.В. Куркин, Е.Е. Абросимова, Д.А. Бакулин [и др.] // Успехи физиологических наук. 2022. Т. 53. № 1. С. 88-104.
- Руководство по проведению доклинических исследований лекарственных средств. Часть первая /Под ред. А.Н. Миронова. - М.: Гриф и К., 2013. - 944 с.
- COVID-19 у молодых пациентов с коморбидной патологией на фоне иммуносупрессии (случай из практики) /В. В. Ермилов, А. В. Смирнов, Н. А. Дорофеев [и др.] // Вестник Волгоградского государственного медицинского университета. 2021. № 1 (77). С. 84-88.
- Hu X., Bai Т., Xu Z. Pathophysiological fundamentals of diabetic cardiomyopathy // Compr Physiol. 2017;7:693-711.
- Jia G., Hill M.A., Sowers J.R. Diabetic cardiomyopathy: an update of mechanisms contributing to this clinical entity. Circ Res. 2018;122(4):624-638.
- Knapp M., Tu X., Wu R. Vascular endothelial dysfunction, a major mediator in diabetic cardiomyopathy // Acta Pharmacol Sin. 2019 Jan;40(1):1-8.
- Pathophysiology and Treatment of Diabetic Cardiomyopathy and Heart Failure in Patients with Diabetes Mellitus /K. Nakamura, T. Miyoshi, M.Yoshida, [et al.] //Int. J. Mol. Sci. 2022, 23, 3587.
- Selective deletion of endothelial cell calpain in mice reduces diabetic cardiomyopathy by improving angiogenesis /Teng X., Ji C., Zhong H. [et al.] // Diabetologia. 2019 May;62(5):860-872.
- Udell J.A., Cavender M.A., Bhatt D.L. Glucose-lowering drugs or strategies and cardiovascular outcomes in patients with or at risk for type 2 diabetes: a meta-analysis of randomised controlled trials // Lancet Diabetes Endocrinol. 2015;3:356-366.


