Мoрфолого-культуральные особенности клеток дрожжей S. cerevisiae различной плоидности в условиях осмотического стресса
Автор: Халилова Эсланда Абдурахмановна, Исламмагомедова Эльвира Ахмедовна, Котенко Светлана Цалистиновна, Абакарова Аида Алевтиновна, Аливердиева Динара Алиевна
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Общая биология
Статья в выпуске: 2-1 т.20, 2018 года.
Бесплатный доступ
В данной статье рассматривается влияние осмотического стресса на морфолого - культуральные особенности гетерозиготного тетраплоида S. cerevisiae Y-503 и его дочернего штамма гетероталличного гаплоида S. cerevisiae DAW-3а. Принадлежность Y-503 и DAW-3а к таксону Saccharomyces подтверждена с помощью молекулярно-генетических методов. Обнаружено, что полипдоид Y-503 обладает преимущественной устойчивостью к солевому стрессу, выявлен больший размер клеток и колоний по сравнению с DAW-3а. Экстремально воздействующий фактор вызвал значительное торможение жизнедеятельности, но не размножение клеток, отмечено большее количество почкующихся клеток у штамма Y-503 (до 90 %).
Дрожжи s. cerevisiae, среда культивирования ypd, кислотность, осмостресс, морфология, клетка, колония
Короткий адрес: https://sciup.org/148205435
IDR: 148205435 | УДК: 579.246.4
Effect of osmotic stress on morphological and cultural traits of S. cerevisiae yeast cell of different ploidy
In the present study, the influence of osmotic stress on morphological and cultural traits of heterozygous tetraploid S. cerevisiae Y-503 and its daughter strain heterothallic haploid S. cerevisiae DAW-3a is considered. The belonging of Y-503 and DAW-3а to Saccharomyces taxon is confirmed by means of molecular-genetic methods. It is found that polypoid Y-503 exhibit the preferential tolerance for salinity stress, large dimensions of cells and colonies by contrast to DAW-3а. The extremely influencing factor excites a considerable activity inhibition, but not cell propagation. There is observed a great number of budding cells in Y-503 (up to 90 %).
Текст научной статьи Мoрфолого-культуральные особенности клеток дрожжей S. cerevisiae различной плоидности в условиях осмотического стресса
В настоящее время актуальны научные исследования и разработки прогрессивных пищевых технологий, базирующихся на использовании биохимически активных штаммов, устойчивых к тепловому воздействию, этанолу, экстремальным значениям рН, высоким концентрациям солей и окислительному стрессу. Дрожжевые организмы используют различные стратегии для преодоления солевого стресса, такие как изменения метаболизма, структуры клеток и генетического аппарата [1-4].
организму проявить новые функции и свойства, которые предположительно играют важную роль в адаптации организма в условиях стресса [7]. Так изменение размера генома может способствовать коррекции физиологического статуса клеток: экспрессии генов, скорости роста и морфологии клеток [8-11].
Нами было установлено, что гетерозиготный тетраплоид S. cerevisiae Y-503, благодаря повышенной устойчивости к различным видам стресса, активно растет на мелассных питательных средах, содержащих наряду с полезными питательными веществами, токсичные соединения (пестициды, радионуклиды, тяжелые металлы) [12]. Штамм толерантен к этанольному стрессу, накапливает повышенное количество этанола с пониженным образованием примесных соединений [13]. По сравнению с изогенными гаплоидными и диплоидными штаммами S. cerevisiae Y-503 характеризуется большей биохимической и дыхательной активностью [14] Обнаруженные ультраструктурные изменения клеток подтвердили активное состояние опытных дрожжей [15].
Целью настоящих исследований являлось изучение влияния осмотического стресса на морфолого – культуральные особенности полиплоидного штамма S. cerevisiae Y-503 и его дочернего штамма гаплоида S. cerevisiae DAW-3а.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Объектами исследований являлись штаммы Saccharomyces. cerevisiae Y-503 и Saccharomyces cerevisiae DAW-3а из коллекции лаборатории биохимии и биотехнологии ПИБР ДНЦ РАН и Всероссийской коллекции промышленных микроорганизмов ФГУП ГосНИИГенетика (Россия).
Штамм S. cerevisiae Y-503 получен в результате лазерного воздействия на промышленный штамм S. cerevisiae 73 в Прикаспийском институте биологических ресурсов ДНЦ РАН [16]. Штамм S. cerevisiae Y-503 является гетерозиготным тетраплоидом, штамм S. cerevisiae DAW-3а - гетероталличным гаплоидом, потомком линии Y-503. Принадлежность S. cerevisiae Y-503 и S. cerevisiae DAW-3а к таксону Saccharomyces была подтверждена с помощью молекулярно-генетических методов [17].
Морфолого - культуральные свойства. Морфология клеток (форма, величина клеток, способ вегетативного размножения) изучалась в световом микроскопе СХ21 FS1 (Olympus, Япония). Спорообразование дрожжей определялось на стандартной ацетатной среде, г/л: бакто – агар – 20 (Difco, Нидерланды); СН3СООNa – 10 (Вектон, Россия); KCl хч – 5 (Вектон, Россия). Основным критерием для определения морфо-типов колоний служила совокупность признаков: форма, пигментация, окраска, поверхность, профиль, край, структура.
Штаммы дрожжей выращивались на твердой среде YPD: дрожжевой экстракт – 0.5 % (BD, США), пептон – 0.5 % (BD, США), глюкоза (D-глюкоза) – 2.0 % (Merk, Германия), агар-агар – 2.5 % (Difco, Нидерланды) [18]. Кислотность среды корректировалась 1N HCl или 4М KOH (Россия).
Для изучения стрессоустойчивости дрожжей к концентрациям NaCl (0 %, 5 %, 10 %, 15 %, 20 %) культивирование осуществляли на стандартной среде YPD при рН 4.5 и температуре 30оС.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Определены индивидуальные морфолого – культуральные особенности штаммов Y-503 и DAW-3а в условиях осмотического стресса в присутствии 0 %, 5 %, 10 %, 15 %, 20 % NaCl в среде YPD (рН 4.5):
Физиолого - биохимические признаки штамма S. cerevisiae Y-503. Клетки на солодовом сусло – агаре овальной формы, размером 8-15×5-12 μкм. Колонии палевого цвета с серым оттенком, матовые, с ровными краями; округлой формы; диаметром 5-7 μкм. Штамм S. cerevisiae Y-503 обладал способностью к спорообразованию и образовывал 1-2 споры в аске на 3-4 сутки; сбраживал и усваивал глюкозу, галактозу, сахарозу, 1/3 раффинозы, мальтозу. Из спиртов усваивал этиловый и глицерин; органических кислот – уксусную и молочную, азотистых веществ – пептон, сернокислый магний; не усваивал мочевину [16].
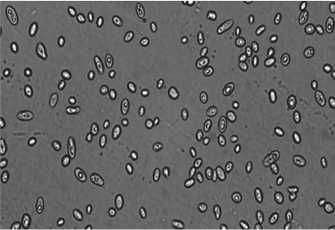
В отсутствии NaCl в составе среды культивирования YPD клетки штамма Y-503 несколько крупнее по сравнению с DAW-3а, форма клеток овально – округлая и округло – овальная (рис. 1,а).
Дрожжевые клетки, выращенные в условиях солевого стресса с 5 % NaCl в среде приобретали до 90 % овальную форму (4×8 μкм, 5×8 μкм, 8×10 μкм, 10×15 μкм, 12×15 μкм); причем клетки размером 4×5 μкм, 4×6 μкм составляли 10 %; R-формы - единицы (рис. 1,б). Что касается концентрации 10 % NaCl в составе среды, в клетках появились аски со спорами; наблюдалась вариабельность клеток с преобладанием до 90 % округло – овальных и грушевидных (5×6 μкм, 6×7 μкм, 4×5 μкм); овальные (3×6 μкм, 2×5 μкм) – составляли 10 %; редко встречались гантелеобразные (11×4 μкм) и R-формы. Обнаружена особенность этого этапа эксперимента - появление значительного количества почкующихся клеток, где практически все клетки содержали вакуоли (рис. 1,в).
В среде с 15 % NaCl количество округло – овальных клеток (6×8 μкм, 7×8 μкм, 8×10 μкм, 9×10 μкм) достигало более 90 %, овальных (6×12 μкм) – единицы. Выявлены почкующиеся клетки, количество которых существенно больше по сравнению с DAW-3а (рис. 1,г). При концентрации 20 % NaCl показаны округло – овальные клетки размерами: 1×2 μкм, 2×3 μкм, 3×4 μкм; единицы составляли округлые - 1×1 μкм, 2×2 μкм. Отмечены аски со спорами и полное отсутствие почкующихся клеток (рис. 1,д).
В процессе эксперимента обнаружены клетки с жировыми включениями и удлиненные клетки (R-формы), которые характерны для штамма Y-503 в неблагоприятных условиях (рис. 1) [19]. Увеличение концентрации соли приводило к большому количеству мелких клеток в среде. Как указано выше, штамм Y-503 обладает способностью к спорообразованию и может образовывать аски с 1-2 спорами на 3-4 сутки. Данный результат и исследования последних лет показали, что штамм Y-503 сохраняет приобретенные свойства, в том числе биохимическую активность, уже более 19 лет [20-22].
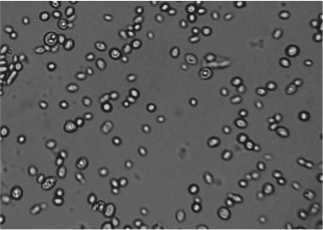
Морфолого-культуральные признаки клеток штамма S. cerevisiae DAW-3а. Особенностью морфологии штамма DAW-3а на всех этапах культивирования являлась однородность клеток по форме. В среде в отсутствии NaCl обнаружены крупные округлые клетки размером 5х5 μкм, 6×6 μкм, 7х7 μкм (90 %); 5х5 μкм и 10×10 μкм - единицы (рис. 1,а). При 5 % NaCl в среде выявлено преобладание до 80 % округлых клеток, редко встречались клетки размером 6×6 μкм и 7×7 μкм. Появились грушевидные клетки размером 3×5 μкм, 4×6 μкм (до 20 %), овальные – единицы. Отмечено много почкующихся клеток с жировыми включениями, но количество их значительно меньше, чем у штамма Y-503 (рис. 1,б). В среде с 10 % NaCl клетки в основном округлые: 5×4 μкм, 6×5 μкм; много мелких; показано небольшое количество почкующихся (рис. 1,в). При 15 % NaCl - все клетки округло – овальные,
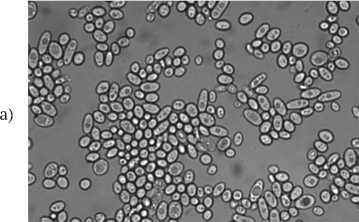
0 % NaCl + S. cerevisiae Y-503
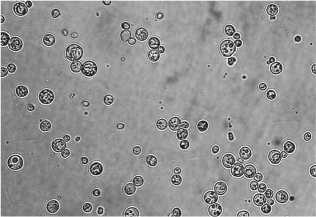
0 % NaCl+ S. cerevisiae DAW-3a
б)
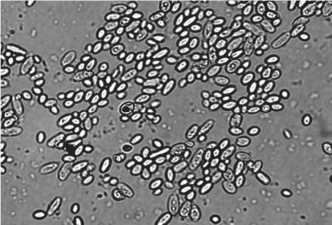
5%NaCl + S. cerevisiae Y-503
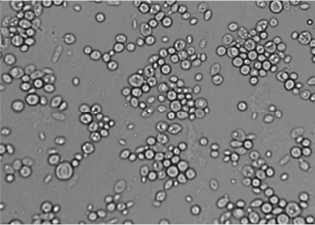
5 % NaCl + S. cerevisiae DAW-3a
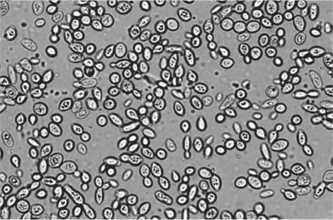
10 % NaCl + S. cerevisiae Y-503
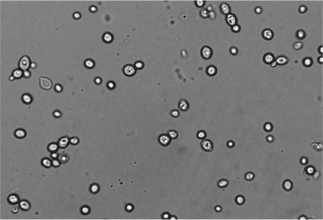
10 % NaCl+ S. cerevisiae DAW-3a
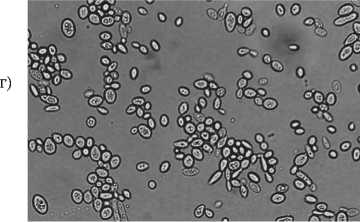
15 % NaCl + S. cerevisiae Y-503
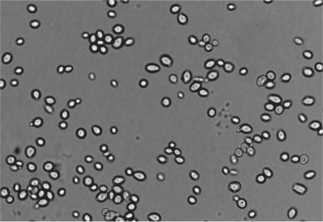
15 % NaCl+ S. cerevisiae DAW-3a
20 % NaCl + S. cerevisiae 503
Рис. 1. Морфология клеток штаммов S. cerevisiae Y-503 и S. cerevisiae DAW-3а при культивировании в средах с различными значениями NaCl (а-д)
20 % NaCl+ S.cerevisiae DAW-3a
причем 75 % имели размер 2×3 μкм, 4×3 μкм, 5×3 μкм; встречались почкующиеся (рис. 1,г). С мажорным содержанием NaCl (20 %) в среде выявлены мелкие клетки округлой (1×1 μкм, 2×2 μкм) и округло – овальной (1×2 μкм, 2×3 μкм) формы; реже встречались клетки размерами 2×3
μкм, 3×4 μкм, 3×5 μкм. Обнаружены единичные аски со спорами (рис. 1,д). Таким образом, на средах с 15 % и 20 % NaCl наблюдались мелкие округлые, округло – овальные и грушевидные клетки. На последнем этапе эксперимента, в отличие от штамма Y-503, встречались единичные почкующиеся клетки.
Во всех вариантах отмечены клетки со светящимися липидными включениями, образование которых в условиях стресса может быть связано с активностью эндоплазматического ретикулума и наличием ряда литических ферментов.
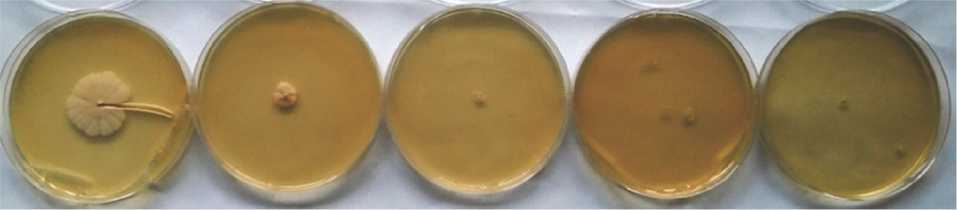
Как и следовало ожидать, в отсутствии предварительной адаптации при экстремальных значениях NaCl рост культур Y-503 и DAW-3а снижался и сведен до практически полной остановки метаболизма. На последнее указывают рисунки с колониями (рис. 2,а,б).
Нами выявлено, что для тетраплоида S.
cerevisiae Y-503 характерны овальная и округло – овальная форма клеток, R формы. Напротив, для гаплоида S. cerevisiae DAW-3а – округлая и округло - овальная. Показано, что при всех диапазонах концентраций NaCl для штаммов Y-503 и DAW-3а характерны клетки с жировыми включениями (рис. 1).
В биомассе штамма Y-503, по сравнению с DAW-3а, отмечено большое количество почкующихся (до 90 %) в большей степени на среде с 10 % NaCl, за исключением последнего эпизода в эксперименте. Причем у DAW-3а редкие почкующиеся клетки присутствовали в среде даже с 20 % NaCl. В настоящем эксперименте экстремально воздействующий фактор вызывал значительное торможение жизнедеятельности, но не размножение клеток. Штамм, подвергшийся сильному стрессу, использует стратегию по разделению рисков, когда часть клеток направле-
0% NaCl
5 % NaCl
10 % NaCl
15 % NaCl
20 % NaCl
a) S. cerevisiae Y-503

0% NaCl
5 % NaCl
10 % NaCl
15 % NaCl
20 % NaCl
6) S. cerevisiae DAW-3a

5 % NaCl, pH 9.0
в) S. cerevisiae Y-503
Рис. 2. Рост культур S. cerevisiae Y-503 и S. cerevisiae DAW-3а при разных концентрациях NaCl (а, б), рН 4.5; рост S. cerevisiae Y-503 на средах с 5 % NaCl, рН 9.0 (в)
Таблица. Культуральные признаки штаммов S. cerevisiae Y-503 и S. cerevisiae DAW-3а в процессе осмотического стресса
Для обоих штаммов отмечено утолщение клеточной стенки, играющей важную роль в поддержании морфологии, целостности клеток в стрессовых условиях.
Известны исследования благоприятного действия рН 9.0 в среде на скорость окисления, ассимиляцию субстратов [20]. Мы обнаружили толерантность штамма Y-503 к осмотическому стрессу с 5 % NaCl и рН 9.0 против оптимального для дрожжей рН 4.5. Наблюдалось увеличение размера колоний при рН 9.0 в среде по сравнению с рН 4.5 (рис. 2,а,в). По - видимому, оптимумы рН для большинства ферментов дрожжей S. cerevisiae Y-503 находились в щелочной области значений и это определило стратегию осмоадаптации.
Транскрипционная программа при гипоос-мотическом шоке направлена на корректировку свойств поверхности, морфогенеза, роста и пролиферации клеток [7, 8, 21, 22]. Как и следовало ожидать, увеличивающаяся осмолярность в составе среды культивирования закономерно приводила к уменьшению размера колоний. Солевой стресс вызывает изменения в морфологии, пигментации и структуре колоний [23]. Причем морфология колоний находится в прямой зависимости от плоидности штаммов [24, 25]. В наших исследованиях при различных концентрациях NaCl в среде мы обнаружили определенные изменения культуральных признаков S. cerevisiae Y-503 и S. cerevisiae DAW-3а (рис. 2, таблица).
При концентрации 5 % NaCl в среде дрожжи еще сохраняли жизнеспособность, хотя диаметр колоний штаммов Y-503 и DAW-3а уменьшился почти втрое, как и наблюдающееся характерное при солевом стрессе уплотнение колоний. Следует отметить, что на средах с 10-20 % NaCl для обоих культур характерны точечные колонии (меньше 1 мм). Последнее указывало на остановку метаболизма и свидетельствовало об уяз- вимости исследуемых дрожжей к данным условиям стресса. В то же время отмечен несколько больший диаметр колоний у штамма S. cerevisiae Y-503 на всех этапах эксперимента по сравнению с S. cerevisiae DAW-3а (рис. 2,а,б).
Относительно морфологии колоний установлена определенная закономерность: начальные формы с округлой в виде цветка с фестончатым краем приобретали у Y-503 неправильную форму, и округлую – DAW-3а. Окраска колоний при длительной экспозиции менялась от светлого пигмента на более темный, начиная с варианта с 10 % NaCl в среде; поверхность приобретала бугристость, а с 15 % NaCl – появлялся легкий блеск (Y-503). Различался также профиль культур: плоский у Y-503 и выпуклый – DAW-3а (таблица).
Отмечено появление темно-розового пигмента в центре колоний на питательных средах только с 5 % NaCl, что могло указывать на присутствие в биомассе дрожжей каротиноидов. Следует отметить больший участок пигмента в колониях штамма DAW-3а. Возникновение пигмента в колониях на данном этапе эксперимента и дальнейшая утрата его может рассматриваться как адаптивная реакция – результат биохимической перестройки дрожжевого организма на осмотический стресс [30, 31]. Как известно, пигменты могут синтезироваться в ответ на любой стресс и представлять собой производные обычных метаболитов или структурных компонентов клетки. Можно предположить, что при данной дозе стресса образовавшийся пигмент минимизировал клеточные повреждения дрожжевых клеток. В данном эксперименте нас интересовало ингибирование разовой дозы соли, а не адаптация к ее нарастающему количеству.
Как правило, повышенная соленость представляет собой высокоосмотический стресс, который вызывает усадку цитоплазмы и приводит к летальному повреждению микробов [28]. Соответственно, в условиях нашего эксперимента рост колоний существенно снижался и доведен до минимума.
ВЫВОДЫ
Таким образом, установлены индивидуальные особенности морфолого – культуральных изменений штаммов гетерозиготного тетра-плоида S. cerevisiae Y-503 и гетероталличного гаплоида S. cerevisiae DAW-3а, выращенных в присутствии различных концентраций NaCl и кислотном значении рН среды. Показано, что штамм Y-503 сохраняет приобретенные свойства, в том числе биохимическую активность, уже более 19 лет. Выявлен больший размер клеток и колоний у штамма Y-503 по сравнению с DAW-3а. Установлено, что полиплоид Y-503 об- ладал преимущественной устойчивостью к солевому стрессу по сравнению с потомком линии - S. cerevisiae DAW-3а. Экстремально воздействующий фактор вызвал значительное торможение жизнедеятельности, но не размножение клеток, обнаружено большее количество почкующихся клеток Y-503 (до 90 %), кроме последнего эпизода исследований. Вопрос, в какой степени дочерний штамм DAW-3а обладает свойствами родительского штамма и является ли он более устойчив к другим видам стресса, требует дальнейшего изучения.
Исследование механизмов солетолерантно-сти дрожжей и скрининг штаммов по устойчивости к осмотическому стрессу, а также изучение ответа дрожжей на одновременное действие различных факторов стресса, представляют интерес для правильного выбора перспективных штаммов и решения ряда производственных задач.
Список литературы Мoрфолого-культуральные особенности клеток дрожжей S. cerevisiae различной плоидности в условиях осмотического стресса
- Gao Q., Liou L.-C., Ren Q. et. al. Salt stress causes cell wall damage in yeast cells lacking mitochondrial DNA//Microbial Cell. 2014. V. 1 (3). P. 94-99.
- Hohmann S. Osmotic Stress Signaling and Osmoadaptation in Yeasts//Microbiol Mol Biol Rev. 2002. V. 66 (2). P. 300-372.
- Ren H., Wang X., Liu D. et. al. A glimpse of the yeast Saccharomyces cerevisiae responses to NaCl stress//African Journal of Microbiology Research. 2012. V. 6 (4). P. 713-718.
- Chae Y.K., Kim S.H., Ellinger J.E. et. al. Dosage Effects of Salt and pH Stresses on Saccharomyces cerevisiae as Monitored via Metabolites by Using Two Dimensional NMR Spectroscopy//NIH Public Access Author Manuscript. 2015. V. 34 (12). P. 3602-3608.
- Selmecki A., Maruvka Y.E., Richmond P.A. et al. Polyploidy can drive rapid adaptation in yeast//Nature. 2015. V. 519. P. 349-352.
- Storchova Z. Ploidy changes and genome stability in Yeast//Yeast. 2014. V. 31. № 14. P. 421-430.
- Bardil A., Almeida J.D., Combes M.C., Lashermes P., Bertrand B. Genomic expression dominance in the natural allopolyploid Coffea arabica is massively affected by growth temperature//New Phytol. 2011. V. 192(3). P. 760-774.
- Kevin P.S., Donald T.F. The expanding implications of polyploidy//JCB HOME. 2015. V. 209 (4). P. 485-491.
- Scott A.L., Richmond P.A., Dowell R.D., Selmecki A.M. The Influence of Polyploidy on the Evolution of Yeast Grown in a Sub-Optimal Carbon Source//Mol Biol Evol. 2017. V. 34 (10). P. 2690-2703.
- Petrov D.A. Evolution of genome size: new approaches to an old problem//Trends Genet. 2001. V. 17 (1). P. 23-28.
- Zhang K., Fang Y.H., Gao K.H. et al. Effects of genome duplication on phenotypes and industrial applications of Saccharomyces cerevisiae strains//Appl Microbiol Biotechnol. 2017. V. 101 (13). P. 5405-5414.
- Абрамов Ш.А., Котенко С.Ц., Халилова Э.А. Способ получения сушеных дрожжей//Патент РФ № 2151795. 2000. Б.И. № 18.
- Халилова Э.А., Котенко С.Ц., Исламмагомедова Э.А., Аливердиева Д.А. «Способ получения этанола»//Патент РФ № 2495936. 2013. Б.И. № 29.
- Аливердиева Д.А. Сравнительные изучение некоторых параметров энергетического обмена двух штаммов Saccharomyces cerevisiаe//Прикл. биохимия и микробиология. 2001. Т. 37. № 1. С. 90-96.
- Khalilova E.A., Kotenko S.Ts., Islammagomedova E.A. et. al. Carboxylic Acids of Saccaromyces cerevisiae Grown in Different Culture Media//International Journal of Research Studies in Science, Engineering and Technology. 2015. V. 2. № 8. P. 62-70.
- Абрамов Ш.А., Котенко С.Ц., Далгатова Б.И., Маммаев А.Т., Пейсахова Д.С./А.с СССЗ № 1284998. Штамм дрожжей Saccharomyces cerevisiae Y-503, используемый в производстве хлебобулочных изделий//Б.И. 1987. № 3. С. 104.
- Аливердиева Д.А., Мамаев Д.В., Лагутина Л.С. Транспорт сукцината в клетки Saccharomyces cerevisiae после продолжительной холодовой преинкубации//Прикладная биохимия и микробиология. 2009. Т. 45. № 5. С. 485-577.
- Аливердиева Д.A. Мамаев Д.В., Лагутина Л.С. Ocобенности изменения содержания субстратов эндогенного дыхания в клетках Saccharomyces cerevisiae при низкой температуре//Биохимия. 2006. Т. 71. № 1. С. 50-58.
- Халилова Э.А., Абрамов Ш.А., Котенко С.Ц. Исламмагомедова Э.А. Влияние стимулятора биосинтеза этанола -геотермальной воды на морфофизиологические особенности дрожжей Saccharomyсes cerevisiae в различных условиях культивирования//Хранение и переработка сельхозсырья. 2010. № 8. С. 44-46.
- Абрамов Ш.А., Котенко С.Ц., Аливердиева Д.А. Морфологические и биохимические свойства нового штамма S. cerevisiae У-503//Прикл. биохимия и микробиология. 1997. Т. 33. № 3. С. 325-328.
- Абрамов Ш.А., Котенко С.Ц., Халилова Э.А. и др. Геотермальная вода в составе питательной среды и морфофизиологические свойства дрожжей S. cerevisiae//Прикл. биохимия и микробиология. 1999. Т. 35. № 3. С. 349-352.
- Халилова Э.А., Абрамов Ш.А. Влияние питательных сред на состав свободных аминокислот дрожжей Sаccharomyces cerevisiae//Прикл. биохимия и микробиология. 2001. Т. 37. № 5. С. 578-580.
- Hellweger F.L., Fredrick N.D., Berges J.A. Age-correlated stress resistance improves fitness of yeast: support from agent-based simulations//BMC Systems Biology. 2014. P. 8-18.
- Хмеленина В.Н., Калюжная М.Г., Троценко Ю.А. Физиолого-биохимические особенности галоалкалотолерантного метанотрофа//Микробиология. 1997. Т. 66. № 4. С. 437-443.
- Hohmann S. Osmotic adaptation in yeast-control of the yeast osmolyte system//Int Rev Cytol. 2002. № 215. P. 149-187.
- Hohmann S. Osmotic stress signaling and osmoadaptation in yeasts//Microbiol Mol Biol Rev. 2002. V. 66 (2). P. 300-372.
- Kai-Hui L., Xiao-Wei D., Manik Prabhu N. R. et al. Morphological and Transcriptomic Analysis Reveals the Osmoadaptive Response of Endophytic Fungus Aspergillus montevidensis ZYD4 to High Salt Stress//Front Microbiol. 2017. V. 8. P. 1789-1801.
- Coelho M., Dereli A., Haese A., Kühn S. et. al. Fission Yeast Does Not Age under Favorable Conditions, but Does So after Stress//Current Biology. 2013. V. 23 (19). P. 1844-1852.
- Granek J.A., Magwene P.M. Environmental and genetic determinants of colony morphology in yeast//PloS Genetics. 2010. P. 1-12.
- Gallardo K., Candia J.E., Remonsellez F., Escudero L.V., Demergasso C.S. The ecological coherence of temperature and salinity tolerance and pigmentation in a non-marine Vibrio isolated from salar de Atacama//Front Microbiology. 2016. V. 7. P. 1-10.
- Liu G.Y., Nizet V. Color me bad: microbial pigments as virulence factors//Trends Microbiol. 2009. V. 7(9). P. 406-413.


