Морфометрическое исследование пирамидного слоя гиппокампа крыс при экспериментальном моделировании стеноза общих сонных артерий
Автор: Медников Д.С., Смирнов А.В., Тюренков И.Н., Куркин Д.В., Волотова Е.В., Бакулин Д.А.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Статья в выпуске: 2 (70), 2021 года.
Бесплатный доступ
Представлены результаты программного морфометрического анализа пирамидного слоя гиппокампа крыс с моделируемым стенозом общих сонных артерий. Наиболее выраженные изменения выявлены в СА1 пирамидного слоя гиппокампа, где достоверно увеличивалось количество нейронов с признаками повреждения как в гиппокампе правого, так и левого полушарий. Помимо этого, в СА1 пирамидного слоя гиппокампа левого полушария выявлено достоверное снижение удельной плотности перикарионов пирамидных нейронов.
Гиппокамп, крыса, стеноз общих сонных артерий
Короткий адрес: https://sciup.org/142229377
IDR: 142229377 | УДК: 616-005.4:611.813.14:616-092.9
Morphometric analysis of the pyramidal layer of the hippocampus of rats n the carotid arteries stenosis experimental modeling
The issue demonstrates the results of software morphometric analysis of the pyramidal layer of the hippocampus of rats with simulated stenosis of the carotid arteries. We have identified most pronounced changes in CA1 of the pyramidal layer of the hippocampus, where the number of neurons with signs of damage in both the hippocampus of the right and left hemispheres significantly increased. In addition, in CA1 of the pyramidal layer of the hippocampus of the left hemisphere, a significant decrease in the specific density of pyramidal neurons perikarya was revealed.
Текст научной статьи Морфометрическое исследование пирамидного слоя гиппокампа крыс при экспериментальном моделировании стеноза общих сонных артерий
Гиппокамп – парная структура головного мозга, входящая в состав лимбической системы и принимающая участие в пространственной ориентации, механизмах обучения и памяти, а также играющая важную роль в формировании эмоций и реакции на стресс [1, 2]. Кроме того, уникальная структурная пластичность гиппокампа связана с непрерывным на протяжении всей жизни нейрогенезом в зубчатой извилине. Подавление нейрогенеза в этой области служит причиной когнитивных дисфункций, таких как поведенческие и мнестические нарушения, расстройств эмоциональной сферы и снижения способности к обучению [1, 3]. Вместе с тем гиппокамп является одной из наиболее уязвимых структур головного мозга при различных повреждающих воздействиях, в том числе при церебральной ишемии [4, 5]. Несмотря на усилившийся в последние годы интерес к изучению гиппокампа, многие аспекты повреждения и компенсаторноприспособительных процессов, а также потенци- альная возможность фармакологической коррекции и влияния на нейропротекцию в этой области остаются во многом неизученными. Церебральный атеросклероз и хроническая ишемия головного мозга – самая распространенная причина дисциркуляторной энцефалопатии и доля хронических расстройств в группе цереброваскулярных болезней (ЦВБ) имеет отчетливую тенденцию к росту в связи с растущей заболеваемостью артериальной гипертензией в сочетании с атеросклерозом, сахарным диабетом, постарением населения и относительно успешной борьбой с острыми формами ЦВБ [5, 6].
Таким образом, ЦВБ остается актуальной не только медицинской, но и социальной проблемой.
ЦЕЛЬ РАБОТЫ
Качественными и количественными методами описать особенности изменений в пирамидном слое гиппокампа крыс при эксперимен- тальном моделировании стеноза общих сонных артерий.
МЕТОДИКА ИССЛЕДОВАНИЯ
Исследование выполнено на 25 белых аутбредных крысах-самцах (ФГУП ПЛЖ «Рап-полово», Ленинградская область) в возрасте 7– 8 месяцев. Животные были разделены на две группы: 1-я – контрольные крысы (n = 10), 2-я – крысы с моделируемым нарушением кровообращения (n = 15). Содержание животных соответствовало правилам лабораторной практики (GLP) и Приказу МЗ РФ № 267 от 19.06.2003 г. «Об утверждении правил лабораторной практики». Стеноз общих сонных артерий моделировался путем частичного ограничения кровотока с помощью наложения лигатур. Наркотизированное животное (хлоралгидрат, интраперитонеально, 400 мг/кг) фиксировали, область шеи выбривали, обрабатывали 0,05%-м раствором хлоргексидина биглюконата. Далее выделяли сосудисто-нервный пучок, образованный общей сонной артерией и блуждающим нервом, который орошали 2%-м раствором лидокаина. После выделения сонной артерии под нее подводили три лигатуры, располагаемые на расстоянии 2–3 мм друг от друга. Параллельно артерии закрепляли иглу (29G 1/2) от шприца (SFM Hospital Products GmbH, Германия), к которой привязывалась сонная артерия и которая затем убиралась таким образом, чтобы лигатуры оставались на заданном расстоянии. В результате описанных выше манипуляций кровоток по сонным артериям ограничивался в головном мозге на 40–50 % от изначальных значений. Оценку уровня локального кровотока (ЛМК, у. е.) осуществляли до и после стенозирования сонной артерии в двух точках, в месте сразу после наложения лигатур и в проекции средней мозговой артерии. После операции рану послойно ушивали, обрабатывали 0,05%-м раствором хлоргексидина биглюконата и 5%-м раствором йода, животных переносили в домашние клетки. Через 20 дней после операции оценивалось психоневрологическое состояние, сохранность рефлексов, поведение и двигательная активность [5]. На 22-е сутки животных выводили из эксперимента с применением в качестве наркоза хлоралгидрата (400 мг/кг, интраперитонеально), декапитировали гильотинным методом («Гильотина для крыс» AE0702, производитель «Open Science»), получали образцы головного мозга. Образцы головного мозга животных фиксировали в 10%-м растворе формалина, приготовленном на 0,2 mМ фосфатном буфере с дальнейшей гистологической проводкой и изготов- лением серийных парафиновых срезов толщиной 5 мкм, которые окрашивали по стандартным методикам гематоксилином и эозином, ти-онином по Нисслю. Исследование микропрепаратов проводилось с помощью микроскопа «Axio Lab. A1» (Carl Zeiss Microscopy GmbH, Germany), фотодокументирование осуществляли камерой «AxioCam 105 color» (Carl Zeiss Microscopy GmbH, Germany). Исследовали основные морфометрические параметры пирамидного слоя гиппокампа правого полушария: ширину пирамидного слоя, средние площади перикарионов нейронов, средние площади ядер нейронов, удельную плотность (УП) перикарионов нейронов, а также удельное количество (УК) нейронов с признаками повреждения. К признакам повреждения относили гиперхро-мию ядра и цитоплазмы, веретеновидное сморщивание перикариона нейрона, деформацию перикариона нейрона в сочетании с гиперхроми-ей ядра и цитоплазмы, а также гипохромию клетки (клетки-тени) [7]. Статистическую обработку данных проводили с использованием пакетов программ MS Office Excell 2007 (Microsoft Inc., США), Statistica 6,0 (StatSoft, USA). Обобщенные данные представляли в виде медианы (Me) с указанием интерквартильного интервала [Q1;Q3], где Q1 – 25 процентиль, Q3 – 75 процентиль. Различия между группами оценивали по критерию Манна – Уитни (Mann – Whitney, U-test) и считали статистически значимыми при p < 0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
При патоморфологическом исследовании пирамидного слоя гиппокампа крыс из 2-й группы несколько более выраженные изменения выявлены в правом полушарии, где УК пирамидных нейронов с признаками повреждения достоверно увеличивалось в СА1 на 23 % (p < 0,001) и в СА3 на 8,7 % (p < 0,01) по сравнению с контрольной группой (рис. 1). В пирамидном слое гиппокампа левого полушария УК нейронов с признаками повреждения достоверно увеличился на 8,5 % (p < 0,001) (рис. 2). Таким образом, УК пирамидных нейронов с признаками повреждения составило в гиппокампе правого полушария крыс 2-й группы 31,2 [22,4; 41] % и 15 [8,2; 22,1] % в СА1 и СА3 соответственно, а в СА1 гиппокампа левого полушария УК поврежденных нейронов составило 23,4 [17,1; 38,4] %. Среди пирамидных нейронов с признаками повреждения доминировали тотально гиперхромные с веретеновидно сморщенными перикарионами (рис. 3). Кроме того, встречались единичные клетки-тени. Перицеллюлярный и периваскулярный отек при этом носил умеренный характер, встречались единичные диапедезы эритроцитов и эритроцитарные стазы в просвете сосудов микроциркуля-торного русла.
Признаки атрофических процессов были более выражены в левополушарном гиппокампе крыс с моделируемым стенозом сонных артерий, где достоверное снижение средней площади перикарионов пирамидных нейронов выявлено в СА1 и СА4 на 33,2 мкм2 (p < 0,001) и на 69,2 мкм2 (p < 0,001) соответственно по сравнению с контролем.
Помимо уменьшения средней площади перикарионов пирамидных нейронов, в СА4 гиппокампа левого полушария крыс 2-й группы обнаружено достоверное уменьшение средней площади ядер на 36,2 мкм2 (p < 0,01) по сравнению с контролем.
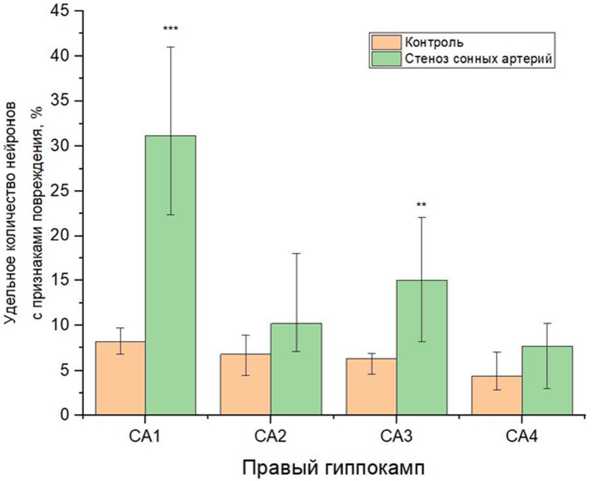
Рис. 1. Изменение удельного количества нейронов с признаками повреждения в пирамидном слое гиппокампа правого полушария крыс с моделируемым стенозом сонных артерий:
*** – р < 0,001, ** – р < 0,01 – различия достоверны по сравнению с контрольной группой (использован критерий Манна – Уитни)
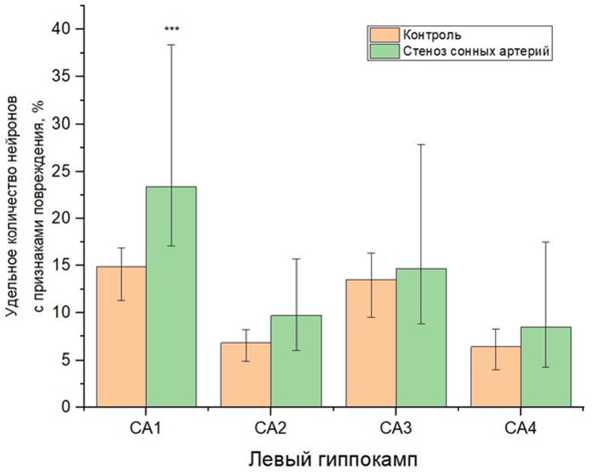
Рис. 2. Изменение удельного количества нейронов с признаками повреждения в пирамидном слое гиппокампа левого полушария крыс с моделируемым стенозом сонных артерий:
*** – р < 0,001 – различия достоверны по сравнению с контрольной группой (использован критерий Манна – Уитни)
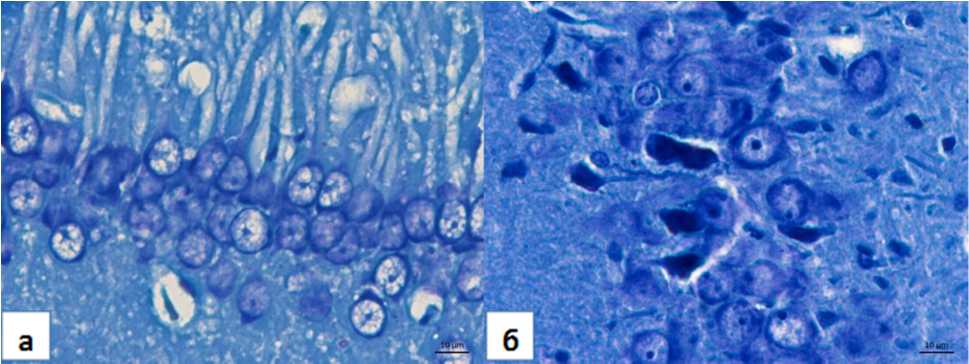
Рис. 3. Пирамидный слой СА1 гиппокампа левого полушария крысы из группы контроля (а) и крысы из группы моделируемого стеноза сонных артерий (б). Увеличение числа пирамидных нейронов с признаками повреждения (б). Окраска тионином по методу Ниссля. Ув. х400
Для СА2 пирамидного слоя гиппокампа как левого, так и правого полушарий головного мозга крыс из 2-й группы были характерны схожие с СА1 микроциркуляторные расстройства в виде умеренного периваскулярного и перицеллюлярного отека, полнокровия и единичных диа-педезов эритроцитов. Однако при морфометрическом исследовании достоверных отличий в значениях УК нейронов с признаками повреждения от контроля выявлено не было, как не было выявлено и достоверных отличий от контроля в значении удельной плотности (УП) перикарионов нейронов.
Необходимо отметить, что достоверное снижение УП перикарионов нейронов выявлено только в СА1 гиппокампа левого полушария животных 2-й группы, где этот показатель составил 36,1 [29,4; 40,4] % (табл. 1). Среди пирамидных нейронов, несущих признаки повреждения в СА2 гиппокампа как левого, так и правого полушарий головного мозга крыс с моделируемым стенозом сонных артерий, преобладали тотально гиперхромные в сочетании с веретеновидно деформированным перикарионом. Пирамидные нейроны без признаков повреждения характеризовались близкой к округлой форме, с центрально расположенным ядром и четко визуализировавшимся ядрышком.
В нейрональном составе отмечались единичные клетки-тени и единичные двуядрышковые нейроны. СА4 пирамидного слоя гиппокампа крыс 2-й группы демонстрировал наименее выраженные признаки повреждения среди всех зон и наименьшие значения УК поврежденных нейронов, которое не изменялось достоверно по сравнению с контролем (табл). При этом, в СА4 наблюдались подобные остальным зонам сосудистые нарушения, выражающиеся в умеренном перицеллюлярном и периваскулярном отеке и полнокровии микроциркулятор-ных сосудов.
Важной особенностью выявленных нами признаков повреждения нейронов в пирамидном слое левого и правого гиппокампа является доминирование тотально гиперхромных нейронов в сочетании с веретеновидной деформацией перикариона. В соответствии с современными взглядами, гиперхромия ядра и цитоплазмы расцениваются как признаки обратимого повреждения и выражают состояние сниженной функциональной активности нейрона в условиях гипоксии, в отличие от клеток-теней, которые считаются необратимо поврежденными [5, 8].
В свою очередь, выявленное нами достоверное увеличение УК нейронов с признаками повреждения в СА1 и СА3 правого, а также СА1 левого гиппокампа соотносятся с данными современной литературы, описывающих эти зоны как более уязвимые при различных воздействиях, в том числе при ишемии [8, 9].
Имеются данные, указывающие на значительную вариабельность организации нейро-глио-сосудистых комплексов как между зонами гиппокампа одного полушария, так и гиппокампа правого и левого полушарий, что, по нашему мнению, объясняет асимметричность выявленных изменений. Так, сообщается о большей степени васкуляризации СА1 и СА3 по сравнению с СА2 и СА4, кроме того, описаны отличия в функциональной активности и метаболические особенности пирамидных нейронов разных зон гиппокампа [10, 11].
Морфометрические параметры гиппокампа крыс при моделировании стеноза общих сонных артерий
|
Параметр |
Группа 1 (контроль) |
Группа 2 (стеноз сонных артерий) |
||||||
|
СА1 |
СА2 |
СА3 |
СА4 |
СА1 |
СА2 |
СА3 |
СА4 |
|
|
Левый гиппокамп |
||||||||
|
Удельное количество гиперхромных нейронов, % |
14,9 [11,3; 16,9] |
6,8 [4,9; 8,2] |
13,5 [9,5; 16,3] |
6,4 [4,0; 8,3] |
23,4 [17,1; 38,4]*** |
9,7 [6,0; 15,7] |
14,7 [8,8; 27,9] |
8,5 [4,3; 17,5] |
|
Средняя площадь перикариона нейрона, мкм2 |
107,6 [95,4; 115,5] |
94,4 [87,3; 102,2] |
118,2 [99,4; 129,6] |
149,5 [137,7; 171,3] |
74,4 [59,8; 93]** |
89,6 [61; 106,2] |
104,1 [79,7; 135,9] |
80,3 [55,1; 112,6]*** |
|
Средняя площадь ядра нейрона, мкм2 |
70,1 [59,8; 82,5] |
62,1 [59,1; 70,8] |
78,3 [64,4; 91,8] |
89,3 [77,7; 96,2] |
56,9 [39,8; 68,4] |
58,1 [43,7;70,5] |
76,8 [51,6; 90,2] |
53,1 [40,9; 75]** |
|
Средняя площадь цитоплазмы, мкм2 |
36,1 [34; 48,8] |
32,8 [25,1; 39,4] |
38,9 [31,3; 46,6] |
59,4 [51,2; 65,3] |
18,1 [13,7; 25,8] ** |
30,4 [22,2; 40] |
28,9 [19,3; 36,7] |
28,4 [19,5; 38,6] *** |
|
Удельная плотность перикарионов, % |
45,3 [41,6; 48,5] |
39 [29,0; 43,4] |
39,5 [31,1; 46,3] |
38,9 [31,5; 42,2] |
36,1 [29,4; 40,4]* |
41,3 [35,8; 44,6] |
38,3 [26,9; 43,3] |
40,8 [35,5; 43] |
|
Удельная плотность нейропиля, % |
54,7 [49,2; 59] |
61 [53,7; 66,8] |
60,5 [54,5; 63,8] |
61,1 [52,7; 69,3] |
63,9 [55,3; 70,6] |
58,7 [52,9;63] |
61,7 [54,1; 68,4] |
59,2 [52,8; 69,3] |
|
Отношение относительной площади перикарионов нейронов к нейропилю, число |
0,8 [0,6; 0,9] |
0,6 [0,5; 0,8] |
0,7 [0,6; 0,8] |
0,6 [0,5; 0,8] |
0,6 [0,5; 0,6] * |
0,7 [0,7; 0,8] |
0,6 [0,6; 0,7] |
0,7 [0,7; 0,7] |
|
Ширина пирамидного слоя, мкм |
44,3 [41,4; 47,9] |
47,1 [42,5; 55,3] |
55,8 [50,2; 60,3] |
50,2 [45,5; 53,7] |
39,8 [35,1; 43,7] |
42,6 [37,9; 47] |
59,7 [53,2; 68,1] |
48,3 [43,1; 55,7] |
|
Ядерно- цитоплазматическое отношение, число |
1,9 [1,7; 2] |
1,9 [1,7; 2,1] |
2 [1,8; 2,1] |
1,5 [1,4; 1,6] |
3,1 [2,8; 3,6] ** |
1,9 [1,6; 2,1] |
2,7 [2,4; 3,1] * |
1,9 [1,7; 2] * |
|
Правый гиппокамп |
||||||||
|
Удельное количество гиперхромных нейронов, % |
8,2 [6,8; 9,7] |
6,8 [4,5; 8,9] |
6,3 [4,6; 9] |
4,4 [2,9; 7,0] |
31,2 [22,4; 41]*** |
10,2 [7,1; 18] |
15 [8,2; 22,1]** |
7,7 [3; 10,2] |
|
Средняя площадь перикариона нейрона, мкм2 |
97,5 [91; 103,7] |
89,6 [82,4; 94,4] |
120,2 [110,3; 142,3] |
111,9 [100,5; 122,6] |
86,5 [69,9; 104] |
81,2 [71,6; 98,3] |
108,2 [89;132,4] |
89,3 [61,8; 95]** |
|
Средняя площадь ядра нейрона, мкм2 |
76,3 [66,5; 83] |
72,3 [55,6; 77,7] |
89,4 [77,6; 108,8] |
88,9 [81,3; 94] |
54,5 [37,1; 77,6] |
56,5 [41,2; 70,8] |
72,9 [58,4; 90,6] |
60,2 [44,7; 78,8]* |
|
Средняя площадь цитоплазмы, мкм2 |
20,8 [15,8; 27,1] |
17,6 [14,9; 22,6] |
30,9 [26,2; 41,3] |
22,5 [14,9; 26,4] |
31,1 [20,5; 38,2] ** |
25,2 [17,7; 31] |
34,4 [23,8; 41,1] |
30 [19,4; 39,6] |
|
Удельная плотность перикарионов, % |
33,3 [31,3; 41] |
34,5 [31; 37,7] |
33,8 [30,1; 37,5] |
28,6 [22,4; 30,7] |
37,6 [33,8; 45,9] |
39 [29,1; 43,5] |
35,8 [30,1; 37,8] |
36,4 [27; 40,1] |
|
Удельная плотность нейропиля, % |
66,7 [60,1;71] |
65,5 [55,8; 69,7] |
66,2 [61; 73,5] |
71,4 [63,4; 79,6] |
62,4 [57,2; 69] |
61 [56,9; 64,2] |
64,2 [56,3; 67,1] |
63,6 [55,5; 71,6] |
|
Отношение относительной площади перикарионов нейронов к нейропилю, число |
0,5 [0,4; 0,7] |
0,5 [0,4; 0,6] |
0,5 [0,3; 0,6] |
0,4 [0,3; 0,6] |
0,6 [0,5; 0,7] |
0,6 [0,6; 0,7] |
0,6 [0,5; 0,6] |
0,6 [0,5; 0,6] |
|
Ширина пирамидного слоя, мкм |
41,2 [37,8; 46,9] |
42 [38,1; 47,8] |
57,3 [51,8; 62,3] |
45,3 [42,2; 49,2] |
40,2 [35,8; 43,6] |
41 [34,8; 45,7] |
55,8 [50,4; 59] |
43,5 [40,9; 49,8] |
|
Ядерно- цитоплазматическое отношение, число |
3,7 [3,5; 3,8] |
4,1 [3,9; 4,4] |
2,9 [2,8; 3,1] |
4 [3,7; 4,1] |
1,8 [1,6; 2,1] *** |
2,2 [2; 2,3] *** |
2,1 [1,8; 2,3] ** |
2 [1,8; 2,1] *** |
Примечание: * – р < 0,05 – различия достоверны по сравнению с контрольной группой (использован критерий Манна – Уитни); ** – р < 0,01 – различия достоверны по сравнению с контрольной группой; *** – p < 0,001 – различия достоверны по сравнению с контрольной группой. Данные представлены в виде медианы с указанием интерквартильного размаха (Me [Q1; Q3]).
ЗАКЛЮЧЕНИЕ
Таким образом, при экспериментальном моделировании стеноза общих сонных артерий в пирамидном слое гиппокампа крыс отмечается несимметричное повреждение с более выраженным повреждением в правом полушарии, где в СА1 и СА3 достоверно увеличивалось удельное количество нейронов с признаками повреждения. При этом, как в СА1 пирамидного слоя гиппокампа левого полушария, так в СА1 и СА3 пирамидного слоя гиппокампа правого полушария признаки повреждения носили преимущественно обратимый характер на фоне умеренных сосудистых нарушений. В СА1 пирамидного слоя гиппокампа левого полушария головного мозга крыс с моделируемым стенозом общих сонных артерий выявлены процессы атрофии, выражающиеся в снижении удельной плотности и средней площади перикарионов нейронов.
Список литературы Морфометрическое исследование пирамидного слоя гиппокампа крыс при экспериментальном моделировании стеноза общих сонных артерий
- Cameron, H. A. Adult neurogenesis: beyond learning and memory / H. A. Cameron, L. R. Glover. – Text (visual) : unmediated //Annu. Rev. Psychol. – 2014. – Vol. 66, № 3. – P. 53 – 81.
- Montagrin, A. The social hippocampus / A. Montagrin, C. Saiote, D. Schiller. – Text (visual) : unmediated // Hippocampus. – 2018. – Vol. 28, № 9. – P. 672 – 679.
- Mitogen and stress-activated protein kinase 1 negatively regulates hippocampal neurogenesis / O. I. Olateju, L. More, J. S. C. Arthur, B. G. Frenguelli. – Text (visual) : unmediated // Neuroscience. – 2021. – Vol. 452, № 1. – P. 228–234.
- Нарушения мозгового кровообращения: диагностика, лечение, профилактика / З. А. Суслина, Т. А. Гулевская, М. Ю. Максимова, В. А. Моргунов. – Москва : Медпресс-информ, 2016. – 536 с. – Текст : непосредственный.
- Особенности экспрессии AIF в гиппокампе крыс при экспериментальном моделировании стеноза общих сонных артерий / А. В. Смирнов, Д. С. Медников, И. Н. Тюренков [и др.]. – Текст : непосредственный. Волгоградский научно-медицинский журнал. – 2020. – Т. 56, № 2. – С. 36 – 40.
- Функциональные и морфологические изменения в пирамидном слое гиппокампа крыс при энцефалопатии, вызванной длительными воздействиями гравитационных перегрузок / И. Н. Тюренков, А. В. Смирнов, Д. С. Медников [и др.]. – Текст : непосредственный // Российский физиологический журнал им. И. М. Сеченова. – 2019. – Т. 105, № 3. – С. 339 – 349.
- Морфологические изменения и особенности экспрессии сериновой рацемазы в гиппокампе крыс при многократном воздействии отрицательных гравитационных перегрузок / Д. С. Медников, А. В. Смирнов, М. В. Шмидт [и др.]. – Текст : непосредственный // Морфология. – 2018. – Т. 153, № 1. – С. 16 – 22.
- Бонь, Е. И. Морфофункциональные нарушения в гиппокампе крыс после субтотальной ишемии / Е. И. Бонь, Н. Е. Максимович, С. М. Зиматкин. – Текст : непосредственный // Вестник Смоленской государственной медицинской академии. – 2018. – Т. 17, № 1. С. 24 – 29.
- Морфометрическое исследование гиппокампа правого полушария крыс при моделировании гипертензивной энцефалопатии / А. В. Смирнов, М. В. Шмидт, Д. С. Медников [и др.]. – Текст : непосредственный // Волгоградский научно-медицинский журнал. – 2016. – Т. 52, № 4. – С. 7 – 11.
- Шаповалова, В. В. Структурно-функциональная реорганизация гиппокампа правого и левого полушарий и функциональная межполушарная асимметрия в постреанимационном периоде / В. В. Шаповалова, В. В. Семченко. – Текст : непосредственный // Медицинский вестник Башкортостана. – 2009. – Т. 4, № 2. – С. 169 – 173.
- Нейро-глио-сосудистые комплексы головного мозга после острой ишемии / А. С. Степанов, В. А. Акулинин, А. В. Мыцик [и др.]. – Текст : непосредственный // Общая реаниматология. – 2017. – Т. 13, № 6. – С. 6 – 17.


