Мультидисциплинарный подход к лечению злокачественной опухоли сердца
Автор: Шумаков Д.В., Дудаков В.А., Зыбин Д.И., Ващенко А.В., Гегенава Б.Б., Терешина А.А., Ивашкин Б.В., Курносов С.А., Капранов М.С., Попов М.А.
Журнал: Московский хирургический журнал @mossj
Рубрика: Клинические случаи
Статья в выпуске: 4 (74), 2020 года.
Бесплатный доступ
Введение: параганглиомы - редкие нейроэндокринные новообразования с частотой встречаемости в общей популяции 0,001-0,01%, которые возникают из мозгового вещества надпочечников и внепочечных вегетативных параганглиев соответственно. Параганлиомы сердца являются чрезвычайно редкими первичными нейроэндокринными опухолями, составляющими менее 1% всех новообразований сердца. Клинически важными является их расположение, поскольку они могут нарушать работу сердца. Для параганглиом сердца больших размеров с инвазией миокарда, потенциально может возникнуть необходимость в реконструкции или трансплантации сердца.Материалы и методы: представленный опыт из-за клинической многофакторности включил в себя несколько вариантов этапного лечения. Обсуждение: в нашем случае, учитывая секрецию катехоламинов, синдром слабости синусового узла, высокий риск кровотечения, а также фрагментацию опухоли, первым этапом планировалось достичь обратного развития опухоли при помощи эмболизации спиралями афферента, питающего опухоль сердца. Однако ввиду нескольких источников кровоснабжения образования, данная методика лечения не привела к должному эффекту. В связи с этим была выбрана тактика открытого хирургического удаления образования с реконструкцией камер сердца. По данным послеоперационной биопсии были получены данные о параганглиоме.Заключение: данный опыт показывает значимость мультидисциплинарного и персонифицированного подхода к лечению пациентов в условиях многопрофильного стационара.
Параганглиома сердца, злокачественная опухоль сердца, эндоваскулярная хирургия, эмболизация опухоли сердца, кардиохирургия
Короткий адрес: https://sciup.org/142229619
IDR: 142229619 | УДК: 616.12-089.84 | DOI: 10.17238/issn2072-3180.2020.4.88-91
Текст научной статьи Мультидисциплинарный подход к лечению злокачественной опухоли сердца
Параганглиомы—редкие нейроэндокринные новообразования с частотой встречаемости в общей популяции 0,001–0,01%, которые возникают из мозгового вещества надпочечников и внепочечных вегетативных параганглиев соответственно. Параганлиомы связаны с феохромоцитомой надпочечников, так как обе имеют нейроэктодермальное происхождение. Хотя большинство параганглиом являются спорадическими, и до 40% их могут быть связаны с наследственным синдромом [1, 3]. Локальное прогрессирование заболевания может привести к тяжелым клиническим проявлениям из-за воздействия параганглиом на окружающие структуры, поэтому рекомендуется хирургическое вмешательство [4].
Параганглиомы средостения встречаются редко, примерно 200 случаев описаны в литературе и составляют лишь 2% всех катехоламин-секретирующих опухолей [4, 5].
Параганлиомы сердца являются чрезвычайно редкими первичными нейроэндокринными опухолями сердца, составляющими менее 1% всех новообразований сердца [1, 2]. Клинически важными является их расположения, поскольку они могут нарушать работу сердца. Есть и другие новообразования, которые следует учитывать при дифференцировки диагноза, включая доброкачественные опухоли, такие как миксомы, липомы, гамартомы и рабдомиомы и злокачественные опухоли, такие как саркомы и лимфомы [1].
Иссечение опухоли является основным методом лечения таких пациентов, однако при этом возникают опасные осложнения из-за удаления части сердца [1–5]. Следует соблюдать осторожность из-за потенциальной избыточной секреции катехоламинов во время операции. Одним серьезным хирургическим осложнением является кровотечение, так как эти опухоли имеют высокую васкуляризацию и их кровоснабжение происходит из коронарных артерий [1]. Вторым частым осложнением являться высвобождение катехоламинов при манипуляциях с опухолью, что может привести к коллапсу кровообращения [1].
Для параганглиом сердца больших размеров с инвазией миокарда, потенциально может возникнуть необходимость в реконструкции или трансплантации сердца [1].
Материал и методы
Клиническая характеристика пациента
Пациента С., 47 лет, с декабря 2019 г. стало беспокоить учащенное сердцебиение с перебоями в работе сердца, сопровождающиеся головокружениями и дискомфортом за грудиной. Тогда же и обратился к врачам по месту жительства с предварительным диагнозом: «Пароксизмальная форма фибрилляции предсердий». При холтеровском мониторировании сердца выявили персистирующую форму фибрилляции-трепетания предсердий, желудочковую экстрасистолию 2 класса по Лауну. При мультиспиральной компьютерной томографии у пациента выявили тромб в полости правого предсердия. Пациент был направлен на консультацию в ГБУЗ МО МОНИКИ им. М.Ф. Владимирского.
При амбулаторном обследовании и проведении инструментальных методов исследования, включая трансторакальную эхокардиографию (Эхо-КГ), магнитно-резонансную томографию сердца (МРТ сердца) (Рис. 1) и мультиспиральную компьютерную томографию (КТ) (Рис. 1), был поставлен предварительный диагноз: гемангиома сердца. С данным диагнозом пациент был госпитализирован в отделение кардиохирургии для взрослых для дополнительных обследований и определения тактики лечения.
На электрокардиограмме (ЭКГ) — синусовый ритм с ЧСС 85уд/мин; АВ-блокада I степени; горизонтальное направление электрической оси сердца; RR — 0,68 с, PQ — 0,26 с, QRS — 0,09 с, QT — 0,30 с.
При чреспищеводной Эхо-КГ определялось объемное образование правого предсердия (67×54 мм), высоко расположенное в верхней и медиальной стенках правого предсердия, внутри образования прослеживается кровоток, не исключается сдавление верхней полой вены и правой ветви легочной вены.
С диагностической целью и определением дальнейшей тактики была проведена коронарная ангиография (КАГ), на которой выявлено объемное образование правого предсердия, кровоснабжающееся афферентом от правой коронарной артерии.
Результаты общего и биохимического анализов крови были без отклонений от нормы.
Проведенные обследования подтверждали вероятность того, что у пациента гемагиома сердца. Кардиоконсилиумом было принято решение о проведении эндоваскулярного вмешательства по эмболизации афферента, отходящего от ПКА и кровоснабжающего образование правого предсердия.
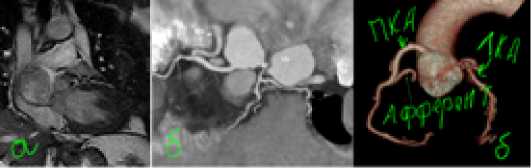
Рис. 1. Лучевая диагностика по месту жительства.
(а) МРТ сердца, (б) МСКТ сердца
Этапы эндоваскулярного вмешательства
Схема анестезиологического пособия для пациента включала в себя премедикацию, местную анестезию зоны пункции и в/в седацию с анестезией. Для выполнения данной операции был выбран правый трансрадиальный доступ с применением проводникового катетера 6 Fr, который был установлен в устье правой коронарной артерии. Коронарный проводник был проведен в дистальные отделы афферентного сосуда, по которому далее заводился микрокатетер Progreat 0,021’’. Затем была выполнена имплантация пяти выталкиваемых спиралей Hilal: две спирали — 6Х5 мм, три — 4Х7 мм. На контрольных ангиограммах отмечалась полная окклюзия основного афферента, остаточное минимальное контрастирование образования за счет дополнительного афферента малого калибра, отходящего от проксимальной трети основной афферентной артерии (Рис. 2).
Жалобы, которые беспокоили пациента до операции стали менее значимыми на первые сутки после вмешательства.
На ЭКГ синусовый ритм с ЧСС 87 уд/мин; АВ-блокада I степени; горизонтальное направление электрической оси сердца; морфология QRST по сравнению с предыдущей ЭКГ до вмешательства без существенной динамики.
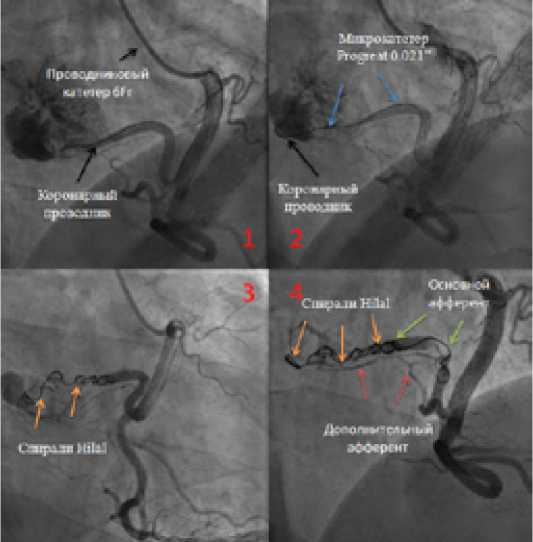
Рис. 2. Этапы эндоваскулярного вмешательства
Послеоперационный период
При трансторакальной Эхо-КГ стало отмечаться уменьшение размеров образования правого предсердия.
МРТ сердца с контрастированием в раннем послеоперационном периоде подтвердила уменьшение размеров образования (42×43×46 мм) по сравнению с предыдущим исследованием (46×50×47 мм) до операции (Рис. 3).
Пациент С. был выписан на 11-е сутки после проведенной операции под наблюдение врача-кардиолога по месту жительства.
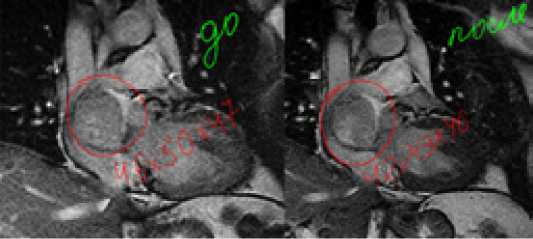
Рис. 3. МРТ сердца с контрастированием до и после эмболизации опухоли
Обследование пациента через 4 месяца
Из-за введенных карантинных мер в Российской Федерации по распространению коронавирусной инфекции COVID-19, госпитализация пациента для проведения обследований в динамике была перенесена на неопределенный срок.
После снятия карантинных ограничений, пациент был госпитализирован с жалобами на учащенное сердцебиение с перебоями в работе сердца, сопровождающиеся головокружениями и дискомфортом за грудиной.
На электрокардиограмме — суправентрикулярный ритм, тахикардия с ЧСС 117–120 уд/мин; АВ-блокада I степени; горизонтальное направление электрической оси сердца; гипертрофия левого желудочка; метаболические изменения миокарда желудочков; RR — 0,50-0,51 с, PQ — 0,26 с, QRS — 0,08 с, QT — 0,30 с.
При трансторакальной Эхо-КГ сохранялось редуцированное образование правого предсердия (34×24 мм).
При МРТ сердца с контрастированием не было отмечено динамики в уменьшении размеров образования при сравнении с предыдущим исследованием в раннем послеоперационном периоде (Рис. 4).
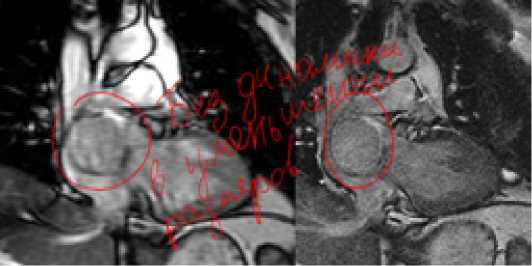
Рис. 4. МРТ сердца через 4 месяца после эмболизации опухоли
При ангиографическом исследовании изменений правой коронарной артерии не наблюдалось. В среднем ее сегменте отходил основной афферент, кровоснабжающий образование в правом предсердии, в просвете которого располагались эмболи-зирующий материал — спирали, которые несколько замедляли кровоток по нему. От проксимальной трети основного афферента отходил дополнительный афферент, диаметром около 2 мм, посредством которого также осуществлялось кровоснабжение образования (Рис. 5).
В дальнейшем был проведен кардиоконсилиум, в заключении которого из-за отсутствия положительной динамики состояния пациента показано проведение открытой хирургическое операции по удалению и гистологическому исследованию образования.
В середине июля 2020 г. пациенту было выполнено оперативное вмешательство в объеме удаления новообразования сердца с реконструкцией крыши левого предсердия, межпредсердной перегородки и стенки правого предсердия заплатами из аутоперикарда, обработанными раствором глутарового альдегида. Операция выполнялась из стандартного стернотомического доступа. После перикардиотомии при ревизии средостения было выявлено опухолевидное образование в полости правого предсердия с переходом на устье верхней полой вены и крышу левого предсердия (Рис. 6).
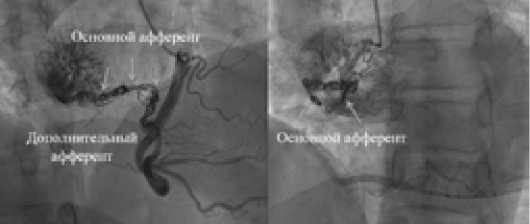
Рис. 5. Ангиографическое исследование. Состояние после эндоваскулярной эмболизации новообразования
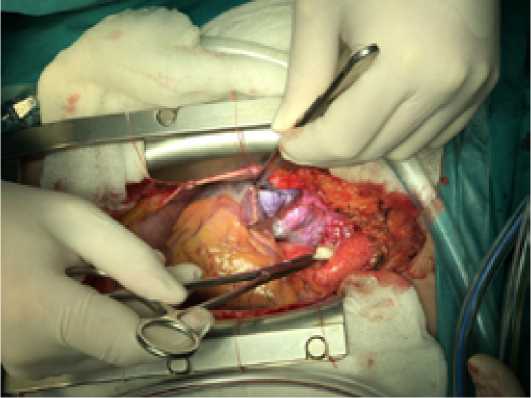
Рис. 6. Интраоперационное фото новообразования (между аортой и ВПВ)
Для удобства манипуляций верхняя полая вена выделена на всем протяжении до правого венозного угла. Подключение аппарата искусственного кровообращения по схеме: аорта–по-лые вены с канюляцией верхней полой вены в месте впадения безымянной вены. В условиях полного искусственного кровообращения на работающем сердце выполнена правая атриотмия с ревизией полости правого предсердия: опухоль прорастает верхнюю часть стенки правого предсердия, вторичную межпредсердную перегородку с субокклюзией устья верхней полой вены и распространяется на крышу левого предсердия. Решено выполнить радикальное удаление опухоли сердца. Выделена ветвь правой коронарной артерии, питающая новообразование, прошита, перевязана и пересечена. В условиях умеренной гипотермии 34 °С и фармако-холодовой кардиоплегии раствором «КУСТОДИОЛ» 2000 мл опухоль выраженной плотности размерами 5×4×4 см была удалена единым блоком в пределах здоровых тканей с формированием дефектов вторичной межпредсердной перегородки, правого предсердия и крыши левого предсердия (Рис. 7).
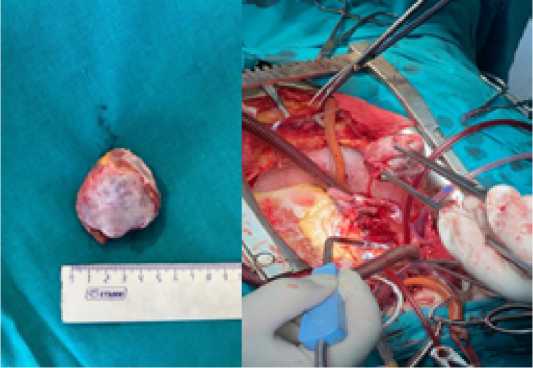
Рис. 7. Удаленная опухоль
При удалении образования выявлена ветвь из бассейна огибающей ветви левой коронарной артерии, кровоснабжающая опухоль, которая была прошита и пересечена. Выполнена реконструкция камер сердца заплатами из аутоперикарда, предварительно обработанными раствором глутарового альдегида. Первая заплата наложена на крышу левого предсердия с переходом на вторичную межпредсердную перегородку, фиксирована обвивным атравматическим швом пролен 4/0 (Рис. 8).
Второй заплатой, фиксированной обвивным атравматическим швом пролен 4/0, выполнена реконструкция стенки правого предсердия и устья верхней полой вены (Рис. 9).
Восстановление сердечной деятельности через однократную электрокардиоверсию. Стандартное завершение операции. Время ИК составило 120 мин., время окклюзии аорты – 95 мин. Ранний послеоперационный период протекал удовлетворительно. ИВЛ 10 часов. Симпатомиметическая поддержка 6 часов. На вторые сутки пациент был переведен в отделение кардиохирургии для взрослых. Проводилась антибактериальная, кардиометаболическая и антиаритми-ческая терапия.
На Эхо-КГ после удаления образования—умеренное увеличение правых камер сердца. ФВ 60%. Левые камеры сердца не расширены, умеренная гипертрофия миокарда. Диастолическая дисфункция 1 тип. Жидкости в перикарде и плевральных полостях не выявлено. На ЭКГ — эктопический средний правопредсердный ритм с ЧСС 80 уд/мин. Через две недели пациент был выписан в удовлетворительном состоянии.
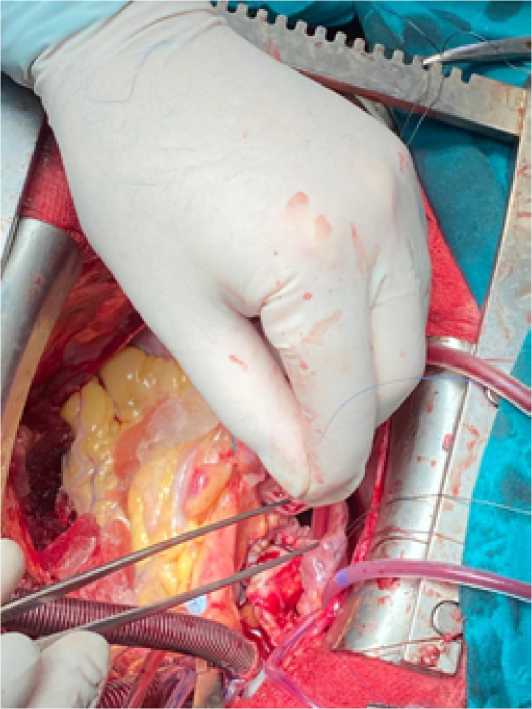
Рис. 8. Заплата на крышу ЛП
При гистологическом исследовании — опухоль сердца солидно-альвеолярного строения с очагами некроза, гиалиноза, отека, состоящая из крупных клеток с округло-овальными, местами уродливыми ядрами, заметными ядрышками и мелкодисперсным распределением хроматина, с широким ободком слабо эозинофильной, пузырьковидной и оптически пустой цитоплазмы. Митозов 1 в 10 РПЗ (при ув. × 400). Отмечаются очаговые диапедезные кровоизлияния, полнокровие сосудов, в просветах сосудов крупного калибра — смешанные тромбы с округлыми плотными аморфными базофильными массами. В прилежащем миокарде — очаги склероза, липоматоза, слабо-выраженной лимфо-плазмоклеточной инфильтрации.
Для дифференциального диагноза между параганглиомой и крупноклеточной нейроэндокринной опухолью было проведено ИГХ-исследование. Результаты ИГХ исследования: клетки опухоли экспрессируют нейроэндокринные маркеры — синптофизин и хромогранин А в отдельных очагах — ви-ментин, и не экспрессируют цитокератины широкого спектра (клон АЕ1/АЕ3), а также рецепторы к соматостатину 2 и 5 типа. Пролиферативная активность клеток в ткани опухоли выражена неравномерно: средний индекс Ki 67 участках максимальной пролиферативной активности равен 9,8%, в участках минимальной пролиферативной активности равен 2–3%. Заключение: особенности гистологического строения и иммунофенотипа клеток опухоли соответствуют параганглиоме.
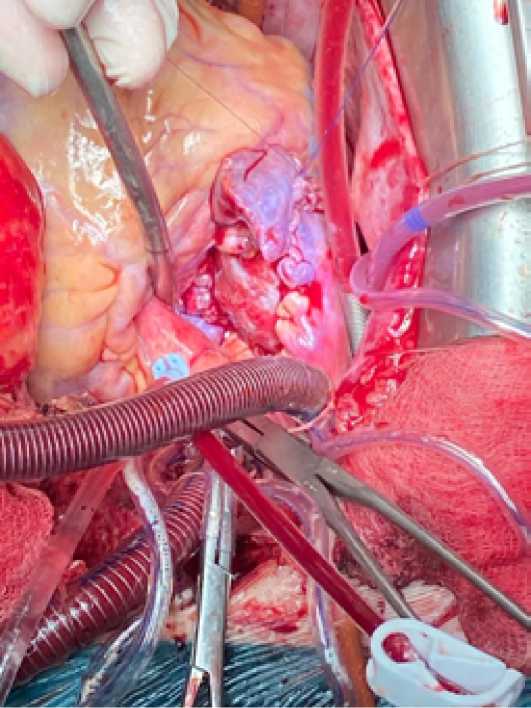
Рис. 9. Реконструкция правого предсердия
Обсуждение
Клиническая картина параганглиом сердца варьирует в зависимости от локализации и секреторного статуса. Например, опухоль может препятствовать кровотоку к сердцу, что приводит к обморокам, одышке и боли в груди, сердечной недостаточности [1, 2]. Функционально параганлиомы производят избыток катехоламинов, которые могут вызывать множество симптомов, включая гипертонию, головную боль, наджелудочковую тахикардию, тревогу [1, 2]. Также может развиться сердечная недостаточность из-за секреции опухолью катехоламинов [1]. Обычно параганглиомы проявляются триадой из гипертонии, головной боли и сердцебиения [5].
В нашем случае, учитывая секрецию катехоламинов, синдром слабости синусового узла, высокий риск кровотечения, а также фрагментацию опухоли, первым этапом планировалось достичь обратного развития опухоли при помощи эмболизации спиралями афферента, питающего опухоль сердца. Однако ввиду нескольких источников кровоснабжения образования данная методика лечения не привела к должному эффекту. В связи с этим была выбрана тактика открытого хирургического удаления образования с реконструкцией камер сердца. По заключению послеоперационной биопсии были получены данные о параганглиоме. Была проведена позитронно-эмиссионная компьютерной томография, при которой не было обнаружено остатков злокачественного образования, а также метастазов в других органах. В этой связи от химиотерапии было решено воздержаться, однако пациент состоит на учете в онкологическом диспансере.
Заключение
Данное наблюдение демонстрирует значимость муль-тидисциплинарного и персонифицированного подхода к лечению пациентов в условиях многопрофильного стационара.
Список литературы Мультидисциплинарный подход к лечению злокачественной опухоли сердца
- Alakeel F., Al Sannaa G., Ibarra-Cortez S.H., Reardon M.J., Czerniak B., Chan E.Y., Ro J. Cardiac paragangliomas: A case series with clinic pathologic features and succinate dehydrogenase B immunostaining. Annals of Diagnostic Pathology, 2020, No. 45, р. 151477. DOI: 10.1016/j.anndiagpath.2020.151477
- Alam A., Dib E., Hall S., Gonzales G., Guerrero-Miranda C. Heart failure resulting from highly invasive primary cardiac paraganglioma. JACC, 2020, March, No. 24, Volume 75, р. 11.
- Wcislak S.M., King W.S., Waller B.R., Goins N., Dickson P.V. Multifocal pheochromocytoma-paraganglioma in a 29-year-old woman with cyanotic congenital heart disease. Surgery, 2019, No. 16, 165(1), рр. 228-231. DOI: 10.1016/j.surg.2018.08.033
- Chang S.H., Yapar I., Kozower B.D. Aorticopulmonary paraganglioma with symptomatic postoperative bradycardia. The Annals of Thoracic Surgery, 2020, May, No. 109, Issue 5, рр. 367-369. DOI: 10.1016/j.athoracsur.2019.08.046
- Berona K., Joshi R., Woo Y.J., Shrager J. Postpartum diagnosis of cardiac paraganglioma: a case report. The Journal of Emergency Medicine, 2018, October, No. 55, Issue 4, рр. 101-105. DOI: 10.1016/j.jemermed.2018.05.034


