Наблюдение особенностей температурного поведения спектральных линий ЯМР 13C как метод изучения полигидроксилированного фуллерена C6O(OH)W
Автор: Карпунин А.Е., Мазур А.С., Проскурина О.В., Герасимов В.И., Плешаков И.В., Фофанов Яков Андреевич, Кузьмин Ю.И.
Журнал: Научное приборостроение @nauchnoe-priborostroenie
Рубрика: Физика приборостроения
Статья в выпуске: 2 т.28, 2018 года.
Бесплатный доступ
В работе показано, что в спектрах ядерного магнитного резонанса 13С, наблюдавшегося в полигидроксилированном фуллерене С60(ОН)п (фуллереноле), регистрируются особенности, отражающие существование изомеров данного соединения, а исследование температурного поведения пиков, соответствующих этим особенностям, может рассматриваться как метод качественного определения соотношения, в котором изомеры присутствуют в составе фуллеренола. Установлено, что в определенном режиме изменяя температуру, можно управлять изомерным составом образцов.
Ядерный магнитный резонанс, фуллеренол, спектры ямр углерода
Короткий адрес: https://sciup.org/142214855
IDR: 142214855 | УДК: 548.736.1:
Observation of temperature behavior of peculiarities of 13C NMR spectrum lines as a method for the investigation of polyhydroxylated fullerene C60(OH)W
It is shown in the work, that in spectra of nuclear magnetic resonance of 13C in polyhydroxylated fullerene (fullerenol) peculiarities are registered, which reflects the existence of isomers in the substance. The study of temperature behavior of corresponding peaks can be regarded as a qualitative method for specification of the isomers proportion in fullerenol composition. It was found out, that by changing of the temperature in a certain regime it is possible to control the isomer speciation of samples.
Текст научной статьи Наблюдение особенностей температурного поведения спектральных линий ЯМР 13C как метод изучения полигидроксилированного фуллерена C6O(OH)W
ВВЕДЕНИЕ полученного фуллеренола, и выяснения того, ка кие данные могут быть извлечены из температур-
Изучение водорастворимых форм углеродных материалов привлекает внимание исследователей в связи с тем, что эти соединения обладают необычными и с точки зрения многих возможных применений полезными свойствами. К числу таких соединений следует отнести и т. н. фуллере-нолы, для которых существуют различные предложения по их биомедицинскому использованию. Кроме этого, они имеют характеристики, интересные для целого ряда других областей [1, 2].
Полигидроксилированные фуллерены (фулле-ренолы) имеют общую формулу С 60 (ОН) n , в структурном отношении они представляют собой углеродный каркас в виде молекулы фуллерена С 60 , окруженный оболочкой из OH-групп, обеспечивающих высокую растворимость вещества. Величина n зависит от того, каким образом вещество было синтезировано, причем известно, что технология может определять и более тонкие особенности строения, связанные с распределением гидроксильных групп на поверхности каркаса. Для изучения деталей формирования рассматриваемой системы требуется привлечение различных физических и физико-химических методов, среди которых важное место занимает ядерный магнитный резонанс (ЯМР), дающий полезную информацию о расположении молекулярных функциональных групп.
В настоящей работе рассмотрено применение ЯМР для характеризации специальным образом ного поведения его спектра.
ОБРАЗЦЫ
Материал был синтезирован по рассмотренной в [3, 4] схеме. Из сажи, полученной в электрической дуге эрозией графитовых электродов, выделялась смесь фуллеренов, из которой на хроматографической колонке отделялось соединение С 60 . Затем выполнялась его многоступенчатая очистка с использованием углеродного сорбента, причем состав необходимого продукта на каждом этапе контролировался методом жидкостной хроматографии. В итоге был получен фуллерен С 60 с чистотой 99.9 масс. % без примесей высших фуллеренов и содержанием С 60 О не более 0.1 %. Далее синтезировался фуллеренол, для чего в отфильтрованный бензольный раствор С60 при интенсивном перемешивании добавлялся концентрированный раствор NaOH, и в качестве катализатора раствор гидроксида тетрабутиламмония. После прохождения реакции щелочь удалялась, и образец высушивался в вакууме.
Качественный анализ, проведенный методами рентгеновской фотоэлектронной и инфракрасной спектроскопии, подтвердил получение соединения C 60 (OH) n , которому по результатам комплексного термического и элементного анализа наилучшим образом соответствует значение n ≈ 46–50.
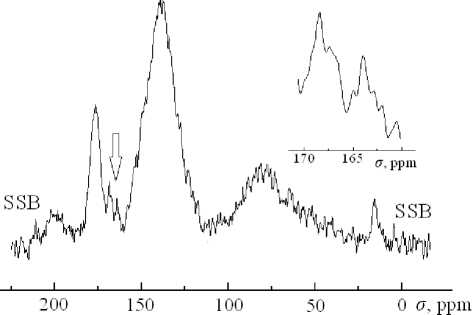
Рис. 1. Спектр ЯМР 13С при T = 50 ºC.
Стрелкой отмечен расщепленный пик; SSB — вращательные артефакты; на вставке — область расщепления в увеличенном масштабе
МЕТОДИКА ИЗМЕРЕНИЙ
На синтезированных описанным выше способом образцах был изучен ЯМР 13C. Сигналы наблюдались на радиоспектрометре Bruker Avance III 400 WB по методике твердотельного ЯМР с использованием вращения образцов под магическим углом. Частота вращения составляла 20 кГц. При определении химических сдвигов σ в качестве стандарта использовался тетраметилси-лан. Для регистрации спектров применялась одно-импульсная возбуждающая последовательность с периодом повторения 5 с, длительностью импульса 2.6 мкс и несущей частотой 100.613 МГц. Кроме того, использовалась последовательность с кросс-поляризацией (CP), имеющая период повторения 5 с, с длительностью контакта 2 мс. Измерительная система позволяла проводить эксперименты с изменением температуры образца T от комнатной до 90 ºC.
РЕЗУЛЬТАТЫ ЭКСПЕРИМЕНТОВ И ОБСУЖДЕНИЕ
Полученные нами спектры ЯМР в основных чертах не отличались от обычных для данного соединения [5–7]. Рис. 1 демонстрирует один из них (поскольку в работе использовался нагрев образцов, для примера приведен результат измерения при температуре выше комнатной). Главные резонансные линии, отнесение которых к различным атомным группам можно найти, например, в [6], были воспроизведены и у нас, однако, кроме этого, была обнаружена ранее не отмечавшаяся особенность: пик, соответствующий одновалентной карбоксильной группе О=С–О с σ ≈ 165 ppm, оказался расщепленным на два, расположенных друг относительно друга с небольшим сдвигом (4– 6 ppm). Она сохранялась практически при всех Т (только при Т = 70 K сигнал был соизмерим с шумами), причем положение пиков оставалось неизменным. Такой эффект характерен для изомеров, наличие которых мы и предполагаем в нашем образце.
Спектры ЯМР были сняты при температурах от комнатной до 90 ºС. Их участки, относящиеся к карбоксильной группе (интервал 162 < σ < 171 ppm), приведены на рис. 2, 3. При обработке экспериментальных данных предполагалось, что форма резонансных кривых описывается функцией Гаусса
f(°)=^expC-(° °0), p^2n L 2P _ где σ0 — центральное значение (математическое ожидание) химического сдвига, p — параметр
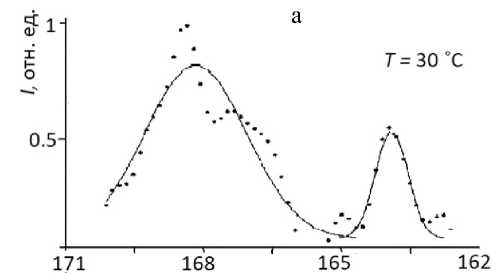
σ , ppm
Рис. 2. Участки спектров ЯМР 13С при нагреве T = 30 (а) и T = 50 ºС (б) и последующем охлаждении образца. На рисунке — экспериментальные точки и линии аппроксимации пиков функцией Гаусса
б
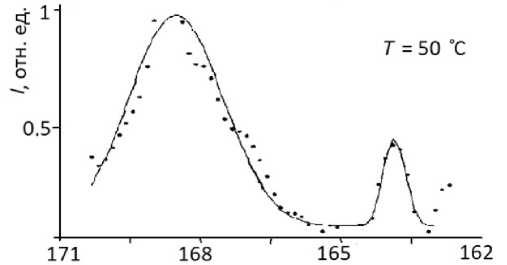
σ , ppm
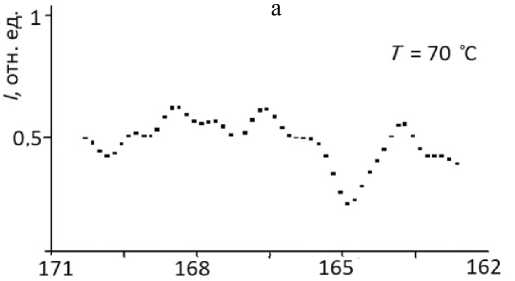
σ , ppm
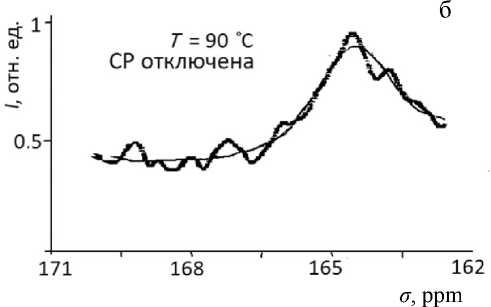
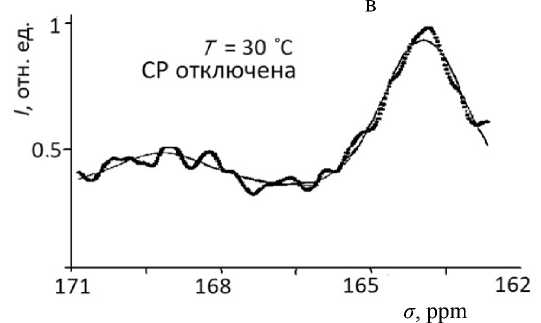
Рис. 3. Участки спектров ЯМР 13С при нагреве T = 70 (а), T = 90 (б) и T = = 30 ºС (в) и последующем охлаждении образца.
На рисунке — экспериментальные точки и линии аппроксимации пиков функцией Гаусса ширины пика (среднеквадратичное отклонение). Подгоночные функции на рис. 2, 3 показаны сплошными линиями. Видно, что избранная функция, характерная для неоднородно уширенного спектра, вполне удовлетворительно описывает резонансы.
Известно [8], что углеродный каркас фуллере-нола (т. е. молекула фуллерена C 60 ) может образовывать изомеры, и возможно, что некоторый вклад в наблюдавшееся расщепление связан с существованием разных форм этой части структуры. Нами, однако, обнаружена сильная зависимость компонентов расщепленного пика от температуры (см. рис. 2, 3), что более типично для изменчивой гидратной оболочки. Можно предположить, что в эксперименте в основном регистрируются изомеры, отвечающие разным способам присоединения OH-групп к каркасу C 60 с формированием карбоксильного фрагмента. Исследование температурного поведения спектров выявляет еще одно свойство резонанса в этой частотной области, заключающееся в том, что при нагреве и последующем охлаждении образца происходит противоположным образом направленное изменение интенсивностей компонент расщепленного пика. Это
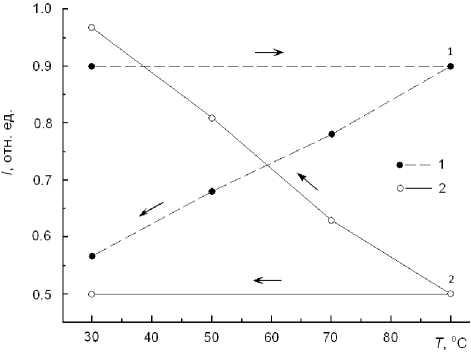
Рис. 4. Изменение относительных интенсивностей компонентов расщепленного пика в зависимости от температуры (1 — σ ≈ 164 ppm, 2 — σ ≈ 169 ppm)
показано на рис. 4, где приводятся зависимости амплитуд сигналов ЯМР (определенных из под-
гонки гауссовой функции к экспериментальным данным) от T . Видно, что в конце цикла "нагрев— охлаждение" отношение интенсивностей пиков с σ ≈ 169 ppm и σ ≈ 164 ppm изменилось более, чем в 3 раза. Следовательно, то, в какой пропорции содержатся в веществе предполагаемые изомеры, зависит от предварительной температурной обработки вещества, причем это соотношение достаточно точно устанавливается методом ЯМР.
ЗАКЛЮЧЕНИЕ
При исследовании спектров ЯМР фуллеренола методом твердотельного ЯМР обнаружена особенность в области пика, отвечающего карбоксильной группе. Высказано предположение, что она связана с существованием изомеров данного соединения, присутствие которых обеспечено, по всей видимости, применением описанной в работе технологии. Показано, что ЯМР может использоваться как метод определения соотношения, в котором изомеры присутствуют в веществе, причем это соотношение регулируется нагревом образцов.
Авторы благодарят ресурсный центр СПбГУ за предоставление возможности для проведения экспериментов и Ю.М. Жукова за характеризацию образцов методом рентгеновской фотоэлектронной спектроскопии.
Работа выполнена при поддержке ФАНО России по теме ИАП РАН гос. рег. № АААА-А16-116041110125-9 и при частичной поддержке Программы повышения конкурентоспособности ФГАОУ ВО СПбПУ № 5-1002020.
Список литературы Наблюдение особенностей температурного поведения спектральных линий ЯМР 13C как метод изучения полигидроксилированного фуллерена C6O(OH)W
- Андреев С.М., Башкатова Е.Н., Пургина Д.Д., Шершакова Н.Н., Хаитов М.Р. Фуллерены: биомедицинский аспект//Иммунология. 2015. Т. 36, № 1. С. 5761.
- Andrievsky G.V., Klochkov V.K., Bordyuh A.B., Dovbeshko G.I. Comparative analysis of two aqueous-colloidal solutions of C60 fullerene with help of FTIR reflectance and UV-Vis spectroscopy//Chemical Physics Letters. 2002. Vol. 364, no. 1-2. P. 8-17.
- Li J., Takeuchi A., Ozawa M., Li X., Saigo K., Kitazawa K.J. C60 fullerol formation catalysed by quaternary ammonium hydroxides//Chem. Soc., Chem. Commun. 1993. Vol. 23. P. 1784-1785.
- Семенов К.Н., Летенко Д.Г., Чарыков Н.А., Никитин В.А., Матузенко М.Ю., Кескинов В.А., Постнов В.Н., Копырин А.А. Синтез и идентификация фуллеренола, полученного методом прямого окисления//Журнал прикладной химии. 2010. Т. 83, № 12. С. 1948-1952.
- Chiang L.Y., Upasani R.B., Swirczewski J.W. Evidence of hemiketals incorporated in the structure of fullerols derived from aqueous acid chemistry//J. Am. Chem. Soc. 1993. Vol. 115, no. 13. P. 5453-5457.
- Wang Z., Chang X., Lu Z., Gu M., Zhao Y., Gao X. A precision structural model for fullerenols//Chemical Science. 2014. Vol. 5, no. 8. P. 2940-2948.
- Andreeva D.V., Ratnikova O.V., Melenevskaya E.Yu., Gribanov A.V. The regioselectivity of fullerenols C60(OH)x determined by high-resolution solid-state 13C and ^H NMR analysis//International Journal of Polymer Analysis and Characterization. 2007. Vol. 12. P. 105-113.
- Gerasimov V.I., Trofimov A., Proskurina O. Isomers of fullerene C60//Materials Physics and Mechanics. 2014. Vol. 20, no. 1. P. 25-32.


