Нарушения циркадианного ритма и нейродегенерация: современный обзор проблемы
Автор: Громова Д.С.
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Обзоры
Статья в выпуске: 1, 2026 года.
Бесплатный доступ
Цель работы проанализировать современные данные, освещающие механизмы развития отдельных нейродегенеративных патологий при нарушениях циркадианного ритма. Материалы и методы. Поиск литературных источников проводился по базам данных PubMed, CyberLeninka, Google Scholar и РИНЦ. Временной горизонт поиска охватывал 2015–2024 гг. Результаты. Нарушения цикла «сон – бодрствование» у пациентов с нейродегенеративными заболеваниями встречаются в несколько раз чаще, чем при других хронических заболеваниях. Механизм возникновения нарушений сна и бодрствования при болезни Паркинсона связан со множеством факторов: повреждением структур, входящих в фотопериодическую систему мозга, недостаточностью функции орексинергической системы, патологической импульсацией от базальных ганглиев и даже десинхронозом на молекулярном уровне. Пациенты с болезнью Альцгеймера демонстрируют десинхроноз в различных проявлениях физиологических и поведенческих реакций. У них нарушен паттерн секреции мелатонина, снижено содержание рецепторов к нему в супрахиазматических ядрах гипоталамуса. Циркадианная дисфункция при болезни Гентингтона связана с патологией гипоталамуса, где расположены как супрахиазматические ядра, так и нейроны орексина. Однако имеются данные и о вовлечении нейронов ствола мозга, что также объясняет дисфункцию норадренергической системы при регуляции бодрствования. Выводы. Нарушения циркадианного ритма наблюдаются при многих нейродегенеративных заболеваниях, однако в большинстве своем они требуют более пристального изучения, что может способствовать повышению эффективности терапии и улучшению качества жизни пациентов.
Циркадианная система, нейродегенерация, болезнь Альцгеймера, болезнь Паркинсона, болезнь Гентингтона
Короткий адрес: https://sciup.org/14134849
IDR: 14134849 | УДК: 612 | DOI: 10.34014/2227-1848-2026-1-6-17
Circadian rhythm dysregulation and neurodegeneration: a contemporary review
The aim of the study is to analyze current data on the mechanisms underlying specific neurodegenerative pathologies in the context of circadian rhythm dysregulation. Materials and Methods. A literature search was conducted using the PubMed, CyberLeninka, Google Scholar, and RSCI (Russian Science Citation Index) databases. The search period spanned from 2015 to 2024. Results. The incidence of sleep-wake cycle disorders in patients with neurodegenerative diseases is several times higher compared to those with other chronic pathologies. The mechanism underlying the onset of sleep-wake dysregulation in Parkinson's disease is associated with many factors: damage to structures within the brain's photoperiodic system, dysregulation of the orexinergic system, pathological impulses from the basal ganglia, and even desynchronization of the molecular clock. Patients with Alzheimer's disease demonstrate desynchronization in various physiological and behavioral responses. These patients exhibit a disrupted melatonin secretion pattern and reduced melatonin receptor levels in the suprachiasmatic nuclei of the hypothalamus. Circadian dysfunction in Huntington's disease is associated with pathology of the hypothalamus, where both the suprachiasmatic nuclei and orexin neurons are located. However, there is evidence of involvement of brainstem neurons, which also explains the dysfunction of the noradrenergic system in regulating wakefulness. Conclusion. Circadian rhythm dysregulation is observed in mane neurodegenerative diseases. However, for the most part, these dysfunctions require further investigation to improve therapeutic efficacy and patients' quality of life.
Текст научной статьи Нарушения циркадианного ритма и нейродегенерация: современный обзор проблемы
Введение. Нейродегенеративные заболевания представляют собой одну из самых распространенных групп расстройств, частым проявлением которых являются нарушения циркадианных ритмов [1]. Накапливающиеся данные свидетельствуют о двунаправленной взаимосвязи между нарушениями циклов сна и нейродегенеративными заболеваниями [2, 3].
Расстройства цикла «сон – бодрствование» у пациентов с нейродегенеративными заболеваниями встречаются в 1,5–3,5 раза чаще, чем при других хронических заболеваниях. Распространенность нарушений циркадианного ритма и дисфункции сна при различных нейродегенеративных заболеваниях сильно варьирует, что играет важную роль в дифференциальной диагностике [4, 5].
Цель исследования. Анализ современных опубликованных данных, освещающих механизмы развития отдельных нейродегене-ративных патологий при нарушениях циркадианного ритма.
Материалы и методы. Поиск источников осуществляли в базах данных PubMed, CyberLeninka, Google Scholar и РИНЦ по следующим словарным запросам: «болезнь Альцгеймера», «когнитивные нарушения», «деменция», «болезнь Паркинсона», «болезнь Гентингтона»,
«нейродегенеративные заболевания», «циркадианные нарушения», «Alzheimer's disease», «Parkinson's disease» и др. Временной горизонт поиска охватывал 2015–2024 гг. Были отобраны наиболее актуальные публикации, дублирующие и малоинформативные статьи отсеивались.
Результаты и обсуждение. Основы циркадианных дисфункций. В целом все циркадианные дисфункции можно поделить на три категории: поведенческие, физиологические и молекулярные (рис. 1).
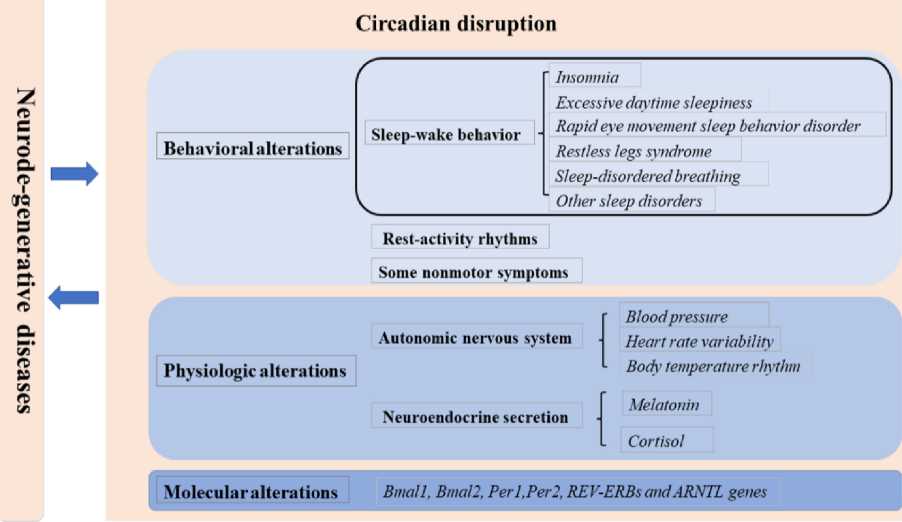
Рис. 1. Циркадианные дисфункции при нейродегенерации [6]
Fig. 1. Circadian dysfunction in neurodegeneration [6]
Поведенческие изменения чаще всего связаны с нарушением цикла «сон – бодрствование», возникновением дневной сонливости, фрагментацией сна и т.д.
Физиологические изменения связаны с теми процессами, которые регулируются су-прахиазматическими ядрами и другими структурами циркадианной системы. В различных исследованиях, включающих пациентов с нейродегенеративными патологиями, были выявлены изменения околосуточной амплитуды ритма секреции кортизола, суточного диуреза, нарушения цикла высвобождения ме- латонина и регуляции температуры тела [6, 7]. В совокупности все это демонстрирует, что у пациентов с нейродегенеративными заболеваниями наблюдается глобальная циркадианная дисфункция.
Молекулярная основа регуляции циркадианных ритмов в норме обеспечивается часовыми генами, работа которых осуществляется по принципу петель положительной и отрицательной обратной связи [9, 10]. Любые эпигенетические отклонения в работе этих связей способны повлечь за собой циркадианные нарушения.
Болезнь Паркинсона . Одной из наиболее распространенных среди всех нейродегенера-тивных патологий является болезнь Паркинсона. Нарушения циркадианных ритмов при данном заболевании встречаются у 75 % пациентов и являются вторым по распространенности немоторным симптомом, часто опережающим многие моторные проявления болезни на несколько лет [11]. Расстройства сна и бодрствования при данной патологии могут быть очень разнообразны и представлены изменением структуры сна, его фрагментаций, инсомнией, сонливостью в дневное время, нарушением поведения в фазе быстрого сна и т.д. [12]. Но наиболее часто они носят характер хронической инсомнии. Причиной ночных пробуждений у людей могут стать усиление ригидности и дрожания, нередко возникающие при переходе от глубоких к поверхностным фазам сна, лекарственные дискинезии, ночная миоклония, боли в конечностях. Фрагментация сна при болезни Паркинсона может быть связана с урологическими проблемами, например нейрогенными нарушениями мочеиспускания [13]. Раннее утреннее пробуждение часто вызвано депрессией, приемом на ночь нейрофармакологических препаратов, нарушениями циркадианных ритмов, а также усилением симптоматики на фоне ослабления действия вечерней дозы противопаркинсони-ческих средств [14].
Механизм возникновения нарушений сна и бодрствования при болезни Паркинсона является достаточно сложным и связан со множеством факторов.
Во-первых, отмечается повреждение структур, входящих в фотопериодическую систему мозга и принимающих участие в регуляции сна и бодрствования. Характер повреждений связан в первую очередь с нарушением межнейронального взаимодействия в этих структурах. Кроме того, дисфункция элементов фотопериодической системы связана с повреждением дофаминергической и других нейромедиаторных систем. Известно, что ГАМК-ергические нейроны вентролатеральных преоптических ядер переднего гипоталамуса вовлечены в регуляцию сна [15]. Эти нейроны в период бодрствования ингибируются гистаминергическими нейронами тубе-ромамиллярных ядер заднего гипоталамуса. Также к восходящей активирующей системе мозга, участвующей в поддержании бодрствования, относятся серотонинергические нейроны шва, норадренергические нейроны голубого пятна, холинергические нейроны педун-кулопонтинного ядра и ядра покрышки, а также дофаминергические нейроны черных ядер и вентральной покрышки. При болезни Паркинсона еще на ранней стадии при отсутствии моторных нарушений наблюдается дегенерация дорсальных ядер шва, голубого пятна, педункулопонтинного ядра ствола мозга, что приводит к соответствующим нейромедиаторным дисфункциям, связанным с нарушениями сна [16].
Патоморфологическим субстратом заболевания является гибель нейронов вследствие избыточного накопления в них белка α-си-нуклеина [17, 18] и телец Леви [19]. Измененные нейроны еще на ранних стадиях патологии обнаруживаются в регуляторных центрах сна и бодрствования: ядрах ствола мозга, гипоталамусе и переднем мозге [14].
Основной причиной дневной сонливости у людей, страдающих болезнью Паркинсона, является повреждение орексинергических нейронов в латеральном гипоталамусе. Орек-синергическая система является главным центром бодрствования и обеспечивает активацию других нейромедиаторных систем, а затем коры головного мозга. R. Fronczek et al. показали, что количество орексинергических нейронов в гипоталамусе пациентов с болезнью Паркинсона снижено почти в 2 раза по сравнению с контрольной группой, а содержание орексина в префронтальной коре и вентрикулярной цереброспинальной жидкости соответственно на 40 % и 25 % ниже. Также установлено, что степень потери нейронов коррелирует со стадией заболевания.
Во-вторых, большое значение при нарушении цикла «сон – бодрствование» имеют возрастные изменения в центральной нервной системе, затрагивающие основные компоненты циркадианной системы. Известно, что при нормальном старении происходит уменьшение объема функционально активной шишковидной железы в связи с ее кальцифициро-ванием, что приводит к снижению мелатонина. У пациентов с болезнью Паркинсона выявляется смещение ночного пика выделения мелатонина, усиливающееся при прогрессировании болезни [20].
В работах Э.Б. Арушаняна и соавт. продемонстрировано, что супрахиазматические ядра гипоталамуса (основной циркадианный пейсмейкер) имеют прямые и опосредованные связи со стриатумом. Таким образом, полосатое тело, супрахиазматические ядра и эпифиз представляют единый функциональный хронобиологический блок. Нарушение же отдельных компонентов данного блока, в т.ч. и при недостаточности дофамина, является причиной циркадианной дизритмии [21].
Важную роль в развитии нарушений циркадианной системы может играть патологическая импульсация от базальных ганглиев, вызванная дефицитом дофамина в стриатуме [22]. Направляясь к ретикулярному ядру таламуса и педункулопонтинному ядру, она способна изменять их функциональное состояние.
В модельных исследованиях на животных было показано, что введение веществ, повреждающих дофаминергические нейроны, приводит к развитию нарушений сна и бодрствования.
Большое значение для регуляции цикла «сон – бодрствование» имеют противопаркин-сонические препараты, главным образом модулирующие работу дофаминергической системы. Низкие дозы дофаминергических средств оказывают седативное действие, более высокие – затрудняют засыпание, могут вызывать ночные кошмары, галлюцинации, фрагментацию сна, дневную сонливость.
Физиологические аспекты циркадианных дисфункций при болезни Паркинсона связаны с нарушениями вегетативной нервной системы и изменениями нейроэндокринной регуляции. Вегетативные нарушения при болезни Паркинсона подробно описаны и включают в себя нарушение гемодинамики, низкий уровень вариабельности сердечного ритма, изменения циркадианного ритма температуры тела [23, 24].
Практически у всех больных с синдромом Паркинсона отмечается ночная гипертензия. Для многих отмечено снижение вариабельности сердечного ритма в ночное время по сравнению со здоровыми людьми того же возраста. При этом снижение вариабельности ритма связано с тяжестью заболевания, длительностью двигательных симптомов и дозой дофаминергических препаратов [25, 26].
Установлено, что пациенты с болезнью Паркинсона демонстрируют десинхроноз и на молекулярном уровне. У человека найден целый ряд генов, прямо или косвенно связанных с циркадными ритмами. К ним относятся гены Bmal1 и Clock , образующие гетеродимеры и запускающие транскрипцию; гены транскрипционных факторов period ( Per1, Per2, Per3 ); ген Timeless ; ген Npas2 ; гены белков криптохромов [27]. Кодируемые этими генами факторы транскрипции, ферменты, транспортеры, прогормоны, сигнальные и другие белки вовлечены в регуляцию суточной периодичности. Кроме этого, внимания заслуживают гены, связанные с синтезом и действием мелатонина, например ген Aanat , регулирующий суточный ритм [28].
В лейкоцитах крови пациентов с болезнью Паркинсона обнаруживается снижение уровня экспрессии гена Bmal1 в вечернее время по сравнению со здоровыми людьми. Кроме того, уменьшается экспрессия гена Bmal2 . Изменения в работе часовых генов показаны и на животных моделях болезни Паркинсона. Так, у животных, которым вводили инъекции 6-гидроксидопамина, снижалась дневная экспрессия гена Per2 в клетках стриатума [29].
Болезнь Альцгеймера. Пациенты с болезнью Альцгеймера также демонстрируют нарушения циркадианного ритма на разных уровнях функциональных систем. Для таких людей характерны фрагментация сна, повышенная дневная сонливость и императивные засыпания [11, 12]. Важно отметить, что многие больные недооценивают выраженность нарушений сна в связи со снижением когнитивных функций и снижением критики к своему состоянию. У пациентов с синдромом Альцгеймера наблюдаются изменения продолжительности различных стадий сна и их качественных характеристик: снижение длительности глубоких стадий сна и фазы быстрого сна, удлинение стадий поверхностного сна. Укорочение фазы быстрого сна, увеличение представленности Δ- и θ-активности, снижение α- и β-активности связаны с поражением холинергических нейронов ствола головного мозга и теменно-височных долей. По мере развития заболевания прослеживается тенденция к усилению нарушений ритма сна и бодрствования.
Пациенты с болезнью Альцгеймера демонстрируют десинхроноз в различных проявлениях физиологических и поведенческих реакций. В вечернее и ночное время наблюдаются изменения суточной физической активности, сумеречный синдром – дезориентация и психомоторное возбуждение. Нарушения регуляции вегетативной функции в первую очередь проявляются в виде ортостатической гипотензии и флуктуации суточной температуры тела. У больных нарушен паттерн секреции мелатонина, снижено содержание рецепторов к нему в супрахиазматических ядрах гипоталамуса.
Более того, по данным патоморфологиче-ских исследований, уровень мелатонина в ликворе при болезни Альцгеймера обратно коррелирует со степенью распространенности нейродегенеративного процесса.
Появляется все больше данных, указывающих на двунаправленную связь между циркадианными ритмами, сном и болезнью Альцгеймера. Многочисленные исследования показывают, что циркадианные дисфункции усугубляют нейродегенерацию при болезни Альцгеймера за счет холинергических нарушений и снижения продукции мелатонина [30, 31].
Аутопсийные исследования выявили у пациентов гибель нейронов в супрахиазматиче-ских ядрах, особенно нейронов, синтезирующих вазопрессин. Нейродегенеративный процесс при болезни Альцгеймера приводит к зна- чительной дисфункции различных нейромедиаторных систем. На экспериментальных моделях было показано, что холинергические нейроны в большей степени, чем другие, чувствительны к нейротоксическому эффекту β-амилоида, вследствие чего наблюдается их гибель. Значительный дефицит наблюдается в функционировании серотонинергической и норадренергической системах, что в первую очередь связано с дегенерацией нейронов ядер шва и голубого пятна. Недостаток катехоламинов ведет к более частым аффективным расстройствам [32], а также значительным нарушениям сна и поддержанию функционального состояния бодрствования [21].
По данным патологоанатомических исследований, при болезни Альцгеймера, как и при болезни Паркинсона, происходит снижение численности орексинергических нейронов. β-амилоид и τ-протеин при болезни Альцгеймера выявляются в супрахиазмальном ядре еще на преклинической стадии болезни. Вследствие этого довольно рано происходит изменение профиля секреции мелатонина. Мелатонин в свою очередь подавляет генерацию β-амилоида и образование амилоидных фибрилл.
Нарушения циркадианных ритмов при болезни Альцгеймера способствуют нейродегенерации, что запускает порочный круг. Отсутствие или нарушение сна значительно увеличивает нейровоспаление и последующую продукцию β-амилоида в спинномозговой жидкости. Повышение уровней β-амилоида и фосфорилированного τ-протеина продемонстрировано на моделях трансгенных мышей с болезнью Альцгеймера [33]. Интересно, что хроническое нарушение сна может усиливать распространение τ-белка в нейронных сетях [34]. Вероятно, нарушение нейротоксического клиренса связано с активностью глимфатической системы. Известна преобладающая активность этого пути в медленноволновом сне. Соответственно, отсутствие сна вызывает заметное и быстрое увеличение количества патогенных видов белков [35, 36].
Musiek et al. описали тяжелый астроглиоз, окислительное повреждение и синаптическую дегенерацию у мышей после удаления гена Bmal1, что указывает на то, что циркадианная дисрегуляция окислительно-восстановительного гомеостаза нейронов также может способствовать нейродегенерации при болезни Альцгеймера.
Также могут быть обнаружены ритмы метилирования ДНК всего генома, которые, по-видимому, становятся менее устойчивыми с возрастом или в связи с развитием болезни Альцгеймера. Циркадные колебания часовых генов в шишковидной железе человека нарушаются даже на очень ранних стадиях заболевания, отражая потерю ритмичной секреции мелатонина у больных.
Как и при болезни Паркинсона, у пациентов с болезнью Альцгеймера нарушается экспрессия часовых генов в периферических клетках, в т.ч. Bmal1 . Y. Wu et al. описали нарушение ритмичности транскрипции Bmal1, Per1 и Cry1 у пациентов на клинических и даже пре-клинических стадиях рассматриваемой патологии [37–39].
Болезнь Гентингтона. Болезнь Гентингтона, в отличие от болезни Альцгеймера и болезни Паркинсона, является аутосомным заболеванием, вызываемым экспансией тринуклеотидов в гене хантингтина. Дисфункция сна и циркадного ритма при данной патологии встречается часто, хотя исследований экспрессии и функций отдельных циркадианных генов у людей с болезнью Гентингтона недостаточно. Хотя нарушение сна коррелирует с тяжестью и продолжительностью заболевания, имеются сообщения о плохом сне уже на ранних стадиях и даже среди бессимптомных носителей мутации. Полисомнография при заболевании выявляет фрагментированный сон с повышенной плотностью сонных веретен. Продолжительность быстрой фазы сна снижается, хотя это наблюдается не у всех пациентов. Низкое качество сна также может быть связано с депрессией и другими психоневрологическими проявлениями заболевания [40, 41]. Несмотря на распространенность нарушений сна при болезни Гентингтона, они не были так тщательно исследованы, как при других нейродегенеративных расстройствах [42].
Однако биомедицинские исследования с участием животных демонстрируют определенные закономерности. У мышиных моделей болезни Гентингтона, в которых экспрессировался повышенный уровень человеческого хантингтина, наблюдались выраженные нарушения циркадианных ритмов поведения. Так, у трансгенных мышей R6/2 дневная активность была повышена, а ночная – снижена. Нарушения ночной и дневной активности усугублялись по мере прогрессирования заболевания, что в конечном итоге приводило к полному расстройству поведения.
Механизм развития нарушений циркадианного цикла может быть связан с его регуляцией с помощью супрахиазматических ядер. Было установлено, что у мутантных животных снижается их пейсмейкерная активность, хотя молекулярный механизм при этом в большинстве случаев не нарушается [43]. Имеются данные о том, что у мышей R6/2 наблюдалась аномальная экспрессия часовых генов Period2 ( mPer2 ). Механизм, лежащий в основе функционального дефицита, пока неизвестен, но, вероятно, определенную роль в нем играют митохондриальная дисфункция и окислительный стресс. Возможно, циркадианная дисфункция при болезни Гентингтона обусловлена такими общесистемными влияниями на экспрессию часовых генов, как изменение уровней мелатонина, кортизола или циркадианных ритмов поведения, а не прямым влиянием на них мутантного белка хан-тингтина [44].
Вывод о нарушении секреции мелатонина у больных с синдромом Гентингтона можно сделать на основании данных, которые демонстрируют снижение его концентрации в плазме на разных этапах заболевания. По мере прогрессирования заболевания уменьшается как акрофаза мелатонина, так и амплитуда его секреции [45].
В патогенез болезни Гентингтона вовлечен гипоталамус, где находятся не только су-прахиазматические ядра, но и нейроны орек-сина, ответственные за управление состояниями сна и бодрствования [46]. Именно это в настоящее время принимается за ключевой механизм, с помощью которого заболевание вызывает циркадианную дисфункцию [47]. Однако многие исследования не выявили корреляций между степенью поражения гипоталамуса и выраженностью десинхронозов. Предполагается также, что болезнь Гентингтона может вызывать дисфункцию сна за счет влияния на другие области мозга. Например, известно, что патология приводит к атрофии структур ствола мозга, таких как голубое пятно, которое обеспечивает переход между стадиями сна [48]. Недавние данные выявили возможную роль полосатого тела в управлении пробуждением во время сна и генерации периодических движений конечностей [45]. Поскольку полосатое тело является основным ранним и стойким очагом патологии при болезни Гентингтона, это указывает на еще одну возможную связь между патологией и нарушением сна. Однако прямых доказательств в поддержку таких гипотез нет.
Заключение. Анализ современных опубликованных в отечественной и зарубежной литературе данных позволяет говорить о многочисленных механизмах, лежащих в основе возникновения нейродегенеративных заболеваний при нарушениях циркадианного ритма. Однако в большинстве случаев требуется более детальное изучение молекулярных, эпигенетических, биохимических и физиологических основ развития патологии. Описанные в обзоре механизмы могут помочь в поиске мишеней для создания лекарственных препаратов, способных корректировать нарушения циркадианного ритма и снижать риск развития нейродегенеративных заболеваний.


