Неалкогольная жировая болезнь печени: патогенез, диагностика, лечение
Автор: Черкашина Елена Алексеевна, Петренко Людмила Васильевна, Евстигнеева Алина Юрьевна
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Внутренние болезни
Статья в выпуске: 1, 2014 года.
Бесплатный доступ
Неалкогольная жировая болезнь печени (НАЖБП) является распространенным хроническим заболеванием, объединяющим клинико-морфологические изменения в печени: стеатоз, неалкогольный стеатогепатит, фиброз и цирроз. НАЖБП тесно ассоциирована с ожирением, особенно абдоминальным и метаболическим синдромом, что повышает кардиометаболический риск и отражается на заболеваемости, прогнозе и продолжительности жизни больных. В обзоре изложены основные механизмы развития НАЖБП, клинические проявления, диагностика и лечение заболевания.
Неалкогольная жировая болезнь печени, стеатоз, стеатогепатит, ожирение, сахарный диабет
Короткий адрес: https://sciup.org/14112966
IDR: 14112966 | УДК: 616.36-002
Non-alcoholic fatty liver disease: pathogenesis, diagnostics, treatment
Insulinoresistance is a risk point of non-alcochol fatty degenerative disease of the liver that is a constituent component of metabolic syndrome. High-calorie diet sedentary lifestyle (physical inactivity) redundant bacterial processes in the intestine genetic predisposition are the main risk factors of non-alcohol liver disease development. Clinical symptoms laboratory test diagnostic criteria were defined modern treatment methods of non alcohol fatty degenerative disease of the liver were discussed from the point of view of metabolic disorders treatment The problem of non alcohol fatty disease of the liver was assessed.
Текст научной статьи Неалкогольная жировая болезнь печени: патогенез, диагностика, лечение
Неалкогольная жировая болезнь печени (НАЖБП) – распространенное хроническое заболевание печени, характеризующееся патологическим накоплением жировых капель, не связанное с употреблением алкоголя. Имеет три формы, отражающие стадии патологического процесса. Неалкогольный стеатоз (НАС) – избыточное накопление жира с развитием дистрофии гепатоцитов. Неалкогольный стеатогепатит (НАСГ) – воспалительная инфильтрация с очагами некроза ткани печени. Неалкогольный цирроз – нарушение архитектоники вследствие некроза и образования узлов регенерации соединительной ткани.
В настоящее время заболеваемость НАЖБП достигает эпидемических размеров. 20–30 % взрослого населения западных стран страдает этой патологией [29, 32]. Установлен неуклонный рост заболеваемости [5]. По данным большинства авторов, НАЖБП чаще страдают женщины [40], другие авторы считают, что заболеваемость НАСГ увеличивается с возрастом у мужчин. Частота встречаемости у детей – 3 % в общей популяции и 53 % среди детей, страдающих ожирением.
Данная проблема чрезвычайно актуальна и для России. Каждый третий пациент терапевта нуждается в лечении как метаболического синдрома (МС), так и НАЖБП [13]. В России, по данным скрининговой программы, проведенной в 2007 г. и охватившей 30 754 чел., НАЖБП выявлена у 27 % обсле- дованных, причем 80,3 % из них имели стеатоз, 16,8 % – стеатогепатит и 2,9 % – цирроз печени [23]. Согласно литературным данным, до 80 % случаев криптогенных циррозов являются исходом НАЖБП. Распространенность дислипидемии среди пациентов с НАЖБП достигает 75 %, и эти показатели в 2 раза выше, чем в популяции [21].
В 1884 г. Frerichs описал изменения в печени у больных «сахарной болезнью». Понятие «неалкогольный стеатогепатит» впервые сформулировал Ludwig с соавт. в 1980 г. при изучении характера изменений печени у больных с ожирением и сахарным диабетом (СД) 2 типа, у которых в анамнезе не было указаний на прием алкоголя в гепатотоксич-ных дозах. M. Thaler установил возможность развития цирроза вследствие жировой болезни печени.
В 2003 г. на I Всемирном конгрессе по инсулинорезистентности (ИР) в Лос-Анджелесе было принято, что НАЖБП, наряду с ожирением, СД 2 типа, дислипидемией, артериальной гипертензией, является составляющим компонентом метаболического синдрома.
Печени отводится важная роль в метаболизме липидов. Находясь на пути транспорта потока пищевых компонентов – жирных кислот, приносимых из тонкой кишки по воротной вене, печень регулирует их поступление в системную циркуляцию. В печени здорового человека присутствует 0,8–1,5 % от ее массы липидов различных типов, преимущественно триглицериды, холестерин, фосфолипиды. При чрезмерном накоплении липидов развивается жировая болезнь печени.
Причины развития НАЖБП разнообразны, и чаще имеется их сочетание [12]. Наиболее распространены факторы приобретенного характера: повышенное питание, нарушения кишечного пищеварения и всасывания, длительное парентеральное питание, метаболические расстройства типа сахарного диабета, подагры, инфекции, хирургические вмешательства, воздействия лекарственных препаратов. В результате происходит повреждение митохондрий, нарушаются процессы окисления жирных кислот. Особенности питания современного человека с дефицитом пищевых волокон, резкое снижение веса также являются факторами развития НАЖБП.
Бессимптомное течение заболевания, трудности его диагностики, отсутствие единой концепции лечения НАЖБП – актуальные проблемы, требующие изучения и заслуживающие внимания специалистов [20]. НАЖБП является составляющей МС [22], который представляет собой комплекс взаимосвязанных нарушений углеводного и жирового обмена, а также механизмов регуляции артериального давления (АД) и функции эндотелия сосудов. Пациенты с МС имеют максимальный риск развития НАЖБП и, как следствие, неалкогольного гепатита, который при МС выявляется в 37,5 % случаев [21].
У пациентов с СД 2 типа и ожирением НАЖБП встречается от 70 до 100 % случаев, у данной группы больных стеатогепатит встречается в 50 % случаев, а у каждого шестого в сочетании с СД 2 типа выявлен цирроз печени [5]. В основе этих процессов лежит ИР – снижение чувствительности тканей к инсулину. В развитии ИР имеют значение особенности образа жизни: избыточное питание, снижение физической активности, а также генетическая предрасположенность – нарушение рецепторных механизмов передачи сигнала инсулина, нарушения регуляции процесса окисления жирных кислот, транспорта триглицеридов из гепатоцитов.
В результате снижения чувствительности клеток-мишеней к действию инсулина нару- шается усвоение глюкозы инсулинзависимыми тканями (печенью, мышцами, жировой тканью), компенсаторно увеличивается секреция инсулина b-клетками, уровень глюкозы в сыворотке длительное время остается нормальным. Гиперинсулинемия (ГИ) является наиболее ранним и постоянным маркером ИР. Обладая мощным липотропным действием, ГИ способствует увеличению массы тела вследствие накопления жировой ткани преимущественно в области верхней половины туловища и в брюшной полости (сальнике и брыжейке).
Основные этиологические факторы
НАЖБП :
-
- употребление пищи с высоким содержанием насыщенных жиров;
-
- низкая физическая активность;
-
- гормональные нарушения;
-
- первичная и вторичная инсулиноре-зистентность;
-
- ожирение.
Жировая ткань является своеобразным эндокринным органом. Высокая плотность кортикостероидных и андрогенных рецепторов и низкая плотность рецепторов к инсулину создает особые условия ее функционирования. Высокая чувствительность к липолитическому действию катехоламинов и низкая чувствительность к антилиполитическому действию инсулина приводят к гормональным нарушениям у пациентов с ожирением и способствует ИР. В жировой висцеральной ткани происходят метаболические процессы, она имеет обширную сеть капилляров, сообщается с портальной системой. Жиры сальника легко липолизируются и приводят к выбросу свободных жирных кислот в портальную вену. Избыток свободных жирных кислот перемещается в гепатоциты, образуются триглицериды, липопротеины низкой плотности, это способствует гиперлипидемии. Часть свободных жирных кислот вовлекается в глюконеогенез и приводит к избыточной секреции печенью глюкозы в кровоток. Повышенный захват жирных кислот гепатоцитами в сочетании с повышенным образованием подавляет поглощение инсулина печенью, что усиливает ИР, которая в свою очередь поддерживает гипе-ринсулинемию, увеличивает липолиз с высво- бождением свободных жирных кислот, стимулируя печеночный липогенез – формируется жировая дистрофия гепатоцитов.
Гормоном, регулирующим гомеостаз жирных кислот, является лептин, который секретируется преимущественно адипоцитами белой жировой ткани, является продуктом экспрессии гена ожирения, участвует в регуляции энергетического обмена, массы тела, влияет на процессы ангиогенеза, фиброгене-за, воспаление, иммунные реакции. По данным ряда авторов, гиперлептинемия участвует в развитии и прогрессировании НАЖБП.
При ожирении уровень лептина повышен, но в условиях лептинорезистентности, характерной для ожирения, не происходит усиления компенсаторного окисления жирных кислот, в ответ на их избыточное поступление в ткани, увеличивается образование триглицеридов, активируется перекисное окисление липидов. Накопление метаболитов свободных жирных кислот (СЖК) приводит к развитию липотоксичности, метаболическим нарушениям.
Лептин обладает профиброгенным действием: способствует усилению выработки проколлагена I типа, трансформирующего фактора роста-β (TGF-β), усиливает фагоцитарную активность и выработку цитокинов купферовскими клетками, макрофагами, стимулирует пролиферацию эндотелиоцитов и продукцию ими активных форм кислорода.
В развитии ИР важная роль отводится адипонектину – гормону жировой ткани, обладающему антиатерогенным действием, уменьшающему продукцию свободных жирных кислот жировой тканью, стимулирующему гликогенообразование, предотвращающему апоптоз гепатоцитов за счет снижения уровня фактора некроза опухоли (ФНО). У пациентов с НАЖБП и ожирением уровень адипонектина значительно ниже, чем у обследованных с аналогичным ИМТ без НАЖБП, и отрицательно коррелирует с содержанием жира в печени [28, 38, 39]. Низкий уровень адипонектина рассматривается как один из предикторов развития СД 2 типа и сердечно-сосудистых заболеваний.
12-перстной кишке, являющегося стимулятором аппетита. Обнаружены генные мутации, связанные с предрасположенностью к ИР и НАЖБП.
Причины перегрузки жирными кислотами: избыточное поступление СЖК после приема пищи (гидролиз пищевых триглицеридов вследствие активного липолиза в жировой ткани), снижение активности бета-окисления жирных кислот в гепатоцитах при инсулино-резистентности, нарушение экспорта липопротеидов очень низкой плотности из гепатоцитов при нарушении синтеза апопротеинов.
Уровень жирных кислот при НАЖБП повышен и коррелирует с тяжестью. Перенос жирных кислот в гепатоциты осуществляется путем пассивной диффузии, а также специфическими транспортерами внутри клеток. СЖК переносятся белками-транспортерами, при НАЖБП активность мембранных транспортеров повышена [27].
В гепатоцитах СЖК подвергаются эсте-рифицированию с образованием метаболически нейтральных триглицеридов – буферный механизм предохранения клетки от перегрузки жирными кислотами. При избыточном поступлении в гепатоциты СЖК проявляют цитотоксическое действие (это происходит через эндоплазматический ретикулум), повышаются уровни продуктов перекисного окисления липидов, активные формы кислорода повреждают ферменты дыхательной цепи митохондрий. Нарушение целостности митохондрий и утечка цитохрома в цитоплазму запускают каскад программированной гибели клеток. В зависимости от энергетического статуса клетки дисфункция митохондрий может привести к гибели клетки по механизму апоптоза или некроза [27].
По данным литературы [31], в крови и ткани печени больных НАЖБП наблюдается существенное повышение содержания продуктов перекисного окисления липидов. Окислительный стресс провоцирует активацию клеток иммунной системы и аутоагрессию к собственным белкам.
Определенное значение в трансформации стеатоза в стеатогепатит имеет наличие избыточного бактериального роста в кишечнике. Максимальная выраженность роста бак- терий отмечена при НАСГ с трансформацией в цирроз [15].
Свободные радикалы запускают секрецию цитокинов, включая ФНО, интерлейкин-6, интерлейкин-8. Гибель гепатоцитов опосредована цитотоксическими эффектами ФНО. Повышение образования ФНО в жировой ткани связано с уменьшением синтеза адипонектина при ожирении.
Продукты перекисного окисления липидов и воспалительные субстанции стимулируют звездчатые клетки и синтез коллагена. При этом велика роль трансформирующего фактора роста, усиливающего синтез проколлагена клетками Ито. Образуются металлопротеиназы, ингибиторы расщепления коллагена.
Существует модель патогенеза НАЖБП – теория двух толчков. При нарастании ожирения на фоне ИР увеличивается поступление в печень СЖК, развивается дисбаланс между усиленным синтезом триглицеридов в печени и снижением их поступления в кровь – первый толчок, результат – стеатоз, печень становится более чувствительной к агрессивным факторам. В процессе реакций окисления СЖК образуются реактивные формы кислорода, продукты перекисного окисления липидов, провоспалительные цитокины – окси-дативный стресс – второй толчок. Хроническое персистирующее воспаление, приводящее к апоптозу и некрозу гептоцитов, трансформирует стеатоз в стеатогепатит с последующим развитием фиброза печеночной ткани. Фиброз выявляется у 20–37 % пациентов с НАЖБП. В прогрессировании НАЖБП и развитии фиброза печени участвуют различные факторы роста, стимулирующие хроническое воспаление и фиброгенез путем усиления образования коллагена и соединительной ткани в печени: трансформирующий фактор роста- β , инсулиноподобный фактор роста-1 (IGF-1), тромбоцитарный фактор роста (PDGF).
В патогенезе НАЖБП могут принимать участие гены, отвечающие за метаболизм глюкозы, липидов, воспаление и развитие фиброза [37].
Длительная гипертриглицеридемия в условиях ИР нарушает эндотелийзависимую вазодилатацию, вызывает оксидативный стресс и является важнейшим фактором риска раннего атеросклероза. В связи с тем что смертность от сердечно-сосудистых заболеваний занимает 1 место в мире, НАЖБП приобретает еще большее значение.
При НАЖБП повышен риск тромбообра-зования за счет увеличения пула провоспали-тельных цитокинов, проатерогенной дислипидемии, гиперкоагуляции и гипофибринолиза [36]. Кроме того, выявлена взаимосвязь между выраженностью стеатоза печени и ИР миокарда. У пациентов с СД 2 типа накопление жира в печени, содержание которого было измерено с помощью протонной магнитно-резонансной спектроскопии, в наибольшей степени было связано с инсулинстиму-лированным захватом глюкозы миокардио-цитами по сравнению с другими показателями, такими как масса висцеральной жировой ткани или общий уровень захвата глюкозы в организме.
Таким образом, генез НАЖБП является многофакторным процессом [3]. НАЖБП может быть как отдельной нозологической единицей, так и компонентом других заболеваний, ассоциированных с ИР [17]. Эти заболевания имеют общие патогенетические факторы, определяющие их прогрессирование, они могут сочетаться, потенцировать развитие друг друга.
Главная особенность форм НАЖБП – это частое отсутствие симптомов: болезнь выявляется случайно, на основании лабораторных или инструментальных тестов, проводимых пациентам с метаболическим синдромом. Симптомы НАСГ неспецифичны и отражают сам факт поражения печени, но не коррелируют со степенью его тяжести. Астеновегета-тивный синдром является характерным признаком и обнаруживается у большей части пациентов с НАСГ; реже отмечается не связанный с чем-либо дискомфорт в правом верхнем квадранте живота в виде тяжести кратковременного или длительного характера – дискинетический синдром. Появление жалоб на кожный зуд, анорексию, диспепти-ческий синдром наряду с развитием желтухи и симптомов портальной гипертензии свидетельствует о трансформации НАСГ в цир- роз [16].
При физикальном обследовании у 50– 75 % больных с НАЖБП обнаруживают гепатомегалию [5]. Диагностический поиск проводится при наличии следующих признаков:
-
- бессимптомное повышение уровней аминотрансфераз;
-
- необъяснимое существование постоянной гепатомегалии;
-
- гепатомегалия при радиологическом исследовании;
-
- исключение всех других причин, приводящих к гепатомегалии.
Редко у пациентов с НАСГ отмечаются такие признаки хронического заболевания печени, как телеангиоэктазии и пальмарная эритема. Признаки НАЖБП выявляются у 10–15 % людей без клинических проявлений МС.
Важным моментом в диагностическом поиске НАЖБП является сбор анамнеза с оценкой факторов риска. Исключить необходимо алкогольное поражение печени, что возможно на основании изучения анамнеза, проведения специальных тестов. Критерием является количество употребляемого алкоголя в сутки: для женщин – менее 10 г, мужчин – менее 20 г алкоголя в сут. Диагноз хронических вирусных гепатитов В и С исключается при изучении маркеров вирусного поражения печени. Исследование ферритина, насыщение железом трансферрина позволяют дифференцировать наследственный гемохроматоз, а уровень церрулоплазмина, наличие кольца Кайзера–Флейшнера – болезнь Вильсона. Диагностика аутоиммунных заболеваний печени проводится по клиническим симптомам и уровню антител – антинуклеар-ных, антимитохондриальных.
Существуют предикторы, позволяющие предположить высокий риск прогрессирования НАЖБП с развитием стеатогепатита и фиброза, которые были установлены при проведении статистической обработки результатов большого количества наблюдений:
-
- возраст старше 45 лет;
-
- женский пол;
-
- ИМТ более 28 кг/м2;
-
- увеличение активности АЛТ в два раза и более;
-
- уровень ТГ более 1,7 ммоль/л;
-
- наличие артериальной гипертензии;
-
- СД 2 типа;
-
- индекс ИР (НОМА-Ш) более 5.
Выявление более двух критериев свидетельствует о высоком риске фиброза печени. Необходимо отметить возможность обратного развития НАС, НАСГ на фоне постепенного снижения массы тела. Быстрая потеря массы способствует прогрессированию одной стадии в другую.
Лабораторные и инструментальные методы диагностики НАЖБП: повышение активности АЛТ и АСТ аминотрансфераз не более чем в 4–5 раз, индекс АСТ/АЛТ – не более 1, чаще повышена активность АЛТ; повышение активности щелочной фосфотазы и ГГТП обычно не более чем до 2 норм, встречается в 40–60 % случаев; гипертриглицеридемия, гиперхолестеринемия; гипергликемия (НТГ или СД 2 типа) – повышение уровня глюкозы натощак более 6,1 ммоль/л, изменение глюкозотолерантного теста, повышение С-пептида; гипоальбуминемия; повышение уровня билирубина (в пределах 30–35 ммоль/л); тромбоцитопения, увеличение протромбинового времени.
У 10–25 % больных выявляются гипер-гаммаглобулинемия и антинуклеарные антитела, значение которых неясно. Основным дифференциальным отличием жирового ге-патоза (ЖГ) от НАСГ, доступным в клинической практике, может быть выраженность биохимического синдрома цитолиза. При анализе лабораторных данных, полученных в специализированных клиниках, цитолиз описывается у 50–90 % больных НАСГ. Чаще активность АЛТ выше, нежели АСТ, но иногда, особенно у больных с трансформацией в цирроз печени, активность АСТ преобладает. По данным некоторых исследований, величина АЛТ, наряду с другими метаболическими факторами, является показателем ИР, что предполагает возможность использования этого показателя в качестве дополнительного маркера у пациентов с ИР. Низкий уровень АЛТ в сыворотке крови в сочетании с высоким ИМТ может свидетельствовать о вероятном наличии тяжелого фиброза при НАСГ. Маркером НАЖБП может являться содержа- ние в сыворотке крови фрагментов белка – филамента цитокератина-18 (CK18-Asp396), образующихся при его расщеплении активированными каспазами из гепатоцитов при апоптозе. Повышение уровней фрагментов цитокератина-18 является специфичным для стеатогепатита и позволяет дифференцировать его от стеатоза. Специфичность и чувствительность данного метода составляют 99,9 и 85,7 % соответственно [33].
В последние годы для диагностики НАЖБП используются фибротесты, позволяющие оценить степень выраженности повреждения печени. Чувствительность и специфичность фибротестов составляют 70– 90 %. Однако в связи с отсутствием в настоящее время достоверных данных по сопоставлению тестов с клинико-морфологическими изменениями в печени у пациентов с НАЖБП при пункционной биопсии фиброте-сты не являются основным методом диагностики НАЖБП. Так как основные печеночные тесты, используемые в клинической практике, не специфичны и не всегда коррелируют с гистологическими изменениями (повреждение, воспаление, фиброз), биопсия печени является «золотым стандартом» в диагностике, определении стадии развития, эффективности терапевтического воздействия при НАЖБП.
Показаниями для биопсии являются: возраст старше 45 лет и хронический цитолиз неустановленной этиологии; сочетание хронического цитолиза неустановленной этиологии по крайней мере с двумя проявлениями МС, независимо от возраста. Биопсия печени не показана в тех случаях, когда уровень аминотрансфераз в норме. Морфологическое исследование позволяет определить степень активности НАСГ и стадию фиброза.
На основе существующей классификации была разработана и предложена Шкала активности НАЖБП (NAFLD activity score – NAS), представляющая комплексную оценку морфологических изменений в баллах и объединяющая такие критерии, как стеатоз (0–3), лобулярное воспаление (0–2) и баллонную дистрофию гепатоцитов (0–2). Сумма баллов менее 3 позволяет исключить НАСГ, а более 5 свидетельствует о наличии стеатогепатита. Такая шкала также незаменима для оценки динамики НАЖБП.
Brunt предложил классифицировать стеа-тогепатиты по морфологическим признакам. Степень поражения печени определяется по выраженности некроза и воспалительного процесса (табл. 1), стадия – по интенсивности развития фиброза (табл. 2).
Таблица 1
Критерии оценки гистологической активности неалкогольного стеатогепатита
|
Степень |
Стеатоз |
Баллонная дистрофия |
Воспаление |
|
1 (мягкий НАСГ) |
Крупнокапельный (≤33–66 %) |
Минимальная, в 3-й зоне ацинуса |
Лобулярное – рассеянная или минимальная инфильтрация полиморфноядерными лейкоцитами (ПМЯЛ) и мо-нонуклеарами, портальное – отсутствует или минимальное |
|
2 (умеренный НАСГ) |
Крупно-и мелкокапельный (>33–66 %) |
Умеренная, в 3-й зоне ацинуса |
Лобулярное – умеренная инфильтрация ПМЯЛ и мононуклеарами*, портальное – отсутствует или мягкое, умеренное |
|
3 (тяжелый НАСГ) |
Крупно-и мелкокапельный (>66 %), 3-я зона или панацинарно |
Доминирует в 3-й зоне ацинуса, представлена панацинарно |
Лобулярное – выраженная рассеянная инфильтрация ПМЯЛ и мононуклеара-ми**, портальное – мягкое, умеренное, не активнее лобулярного |
Примечание. * – может не быть ассоциировано с баллонной дистрофией гепатоцитов и/или перицеллюлярным фиброзом; ** – максимально выражено в 3-й зоне ацинуса наряду с баллонной дистрофией и перисинусоидальным фиброзом.
Таблица 2
Стадии фиброза печени при НАСГ
|
1-я стадия |
Перисинусоидальный/перицеллюлярный фиброз в 3-й зоне ацинуса, очаговый или распространенный |
|
2-я стадия |
1-я стадия + очаговый или распространенный перипортальный фиброз |
|
3-я стадия |
Мостовидный фиброз, очаговый или распространенный |
|
4-я стадия |
Цирроз печени |
При отсутствии у пациента клинической симптоматики, выявлении отклонений функциональных печеночных тестов и при невозможности проведения гистологического исследования ткани печени УЗИ может служить объективным методом для распознавания стеатоза печени, особенно при наличии у больного одного или более факторов риска развития НАСГ, а также позволяет следить за динамикой заболевания.
Выделяют 4 основных ультразвуковых признака стеатоза печени:
-
- дистальное затухание эхосигнала;
-
- диффузная гиперэхогенность паренхимы печени («яркая печень»);
-
- увеличение эхогенности печени по сравнению с почками;
-
- нечеткость сосудистого рисунка.
Однако иногда изменения на УЗИ бывает трудно отличить от фиброза и даже цирроза печени. В ряде случаев выявить жировую инфильтрацию печени позволяют компьютерная и магнитно-резонансная томография. Основным КТ-симптомом жировой инфильтрации печени является снижение денсито-метрического показателя паренхимы. Преимуществами современного МР-исследова-ния являются высокая тканевая контрастность, возможность получить целостное изображение органа в любой проекции.
К настоящему времени в перечне заболеваний МКБ-10 отсутствует единый код, отражающий полноту диагноза НАЖБП. Целесообразно использовать один из нижеприведенных кодов: К 73.0 – хронический персистирующий гепатит, не классифицированный в других рубриках; К 73.9 – хронический гепатит неуточненный; К 76.0 – жировая дегенерация печени, не классифицированная в других руб- риках; К 74.6 – неуточненный цирроз печени.
Нами исследована эпидемиология и клинико-лабораторные особенности НАЖБП у больных СД, находящихся на стационарном лечении в эндокринологическом отделении ГУЗ ЦК МСЧ. Оказалось, что среди поступающих в течение месяца в эндокринологический стационар 73–86 % – больные с СД, причем у 87 % – СД 2 типа, при этом избыточная масса тела и ожирение выявлены у 82 % обследованных.
Пациенты были разделены на 3 группы. 1 группа – больные СД 1 типа (35 чел.: 15 мужчин, 20 женщин), средний возраст – 24±3 года, давность заболевания – 8±2 года. 2 группа – больные СД 2 типа с ожирением (32 чел.: 12 мужчин, 20 женщин), средний возраст – 56±4 года, давность заболевания – 10±4 года. 3 группа – больные СД 2 типа с избыточной массой тела (35 чел.: 15 мужчин, 20 женщин), средний возраст – 60,0±5,6 года, давность анамнеза заболевания – 10±2 года. Клиническое обследование больных содержало изучение образа жизни, наличия сопутствующей патологии, наследственной отяго-щенности по СД, патологии печени, исключение алкогольного поражения печени. Лабораторная диагностика исключала поражение печени вирусной этиологии.
Ведущими были 3 синдрома, представленные на рис. 1. Пациенты 1 группы в основном предъявляли жалобы на слабость, дискомфорт в правом подреберье наблюдался лишь в 12 % случаев, отсутствовал болевой синдром. Во 2 группе дискомфорт и тяжесть в правом подреберье выявлена в 88 % случаев, боли в правом подреберье – в 12 %. В 3 группе дискомфорт выявлен в 56 % случаев, боли в правом подреберье – в 15 %.
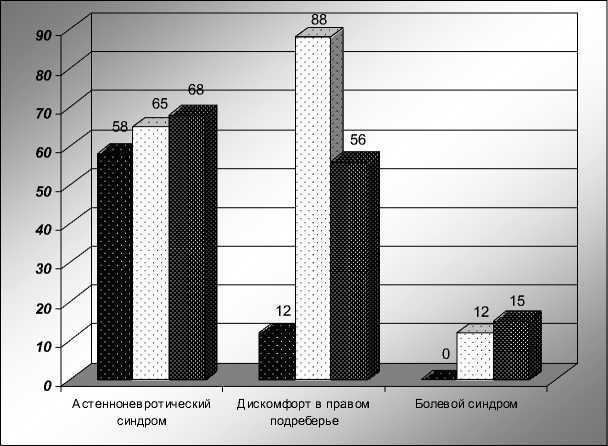
Рис. 1. Клинические проявления НАЖБП у больных сахарным диабетом
Отягощенная наследственность по сахарному диабету отмечена у 32 % больных 1 группы, 56 % больных 2 группы и в 58 % случаев в 3 группе. Артериальная гипертензия выявлена у 86 % пациентов 2 группы и 92 % больных 3 группы, т.е. при СД 2 типа и наличии избыточной массы тела и ожирении.
Контроль биохимических показателей сыворотки крови с помощью общепринятых методик позволил выявить отсутствие отклонения от нормы показателей трансаминаз (АЛТ и АСТ), билирубина, холестерина, триглицеридов в 1 группе больных, т.е. при СД 1 типа. В отличие от 2 группы, где уровень АЛТ в 42 % случаев составил 3 нормы, у 45 % больных – 2 нормы, АСТ в 15% случаев – 2 нормы; в 3 группе в 39 % случаев АЛТ увеличено до 3,5 норм, АСТ в 14 % – до 2 норм.
Содержание общего холестерина в среднем составило 7,4±0,8 и 6,9±1,5 ммоль/л, уровень триглицеридов – 1,9±0,3 и 2,1±0,3 ммоль/л соответственно во 2 и 3 группах наблюдаемых больных.
По данным УЗИ органов брюшной полости (рис. 2), увеличение печени, чаще обеих долей, выявлено у 78 % пациентов 2 группы и 81 % – 3 группы, обеднение сосудистого рисунка печени отмечено в 82 % случаев во 2 группе и 84 % – в 3 группе, повышение эхогенности печеночной ткани – в 96 % случаев во 2 группе и 93 % – в 3 группе больных.
Таким образом, наши наблюдения выявили, что среди больных эндокринологического отделения превалирующим является диагноз СД 2 типа на фоне ожирения и избыточной массы тела у лиц женского пола с давностью анамнеза более 10 лет, часто с отягощенной наследственностью и артериальной гипертензией. Согласно данным литературы, наличие сочетания СД 2 типа с ожирением увеличивает риск развития гепатоцеллюлярной карциномы в 2 раза, особенно у мужчин. Кроме того, женский пол, СД 2 типа, отягощенная наследственность, ожирение, возраст более 50 лет – это факторы риска прогрессирования и трансформации жирового гепатоза в НАСГ. Высокие показатели цитолиза свидетельствуют об этой трансформации. Полиморбидность у пациентов с СД требует комплексного подхода к диагностике и лечению, несмотря на отсутствие стандартов лечения НАЖБП у этой группы больных. Лечение должно быть направлено в т.ч. на предупреждение прогрессирования НАЖБП от стеатоза в цирроз печени.
Современное лечение НАЖБП имеет цель устранить или ослабить воздействие основных факторов ее развития [7, 21].
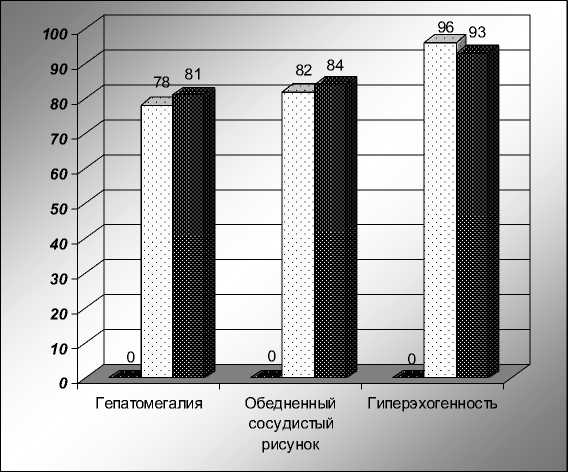
Рис 2. УЗИ-симптомы НАЖБП у больных сахарным диабетом 2, 3 групп, %
У большинства пациентов НАЖБП характеризуется длительным, стабильным бессимптомным течением. По современным представлениям, специальная фармакотерапия показана только больным с прогрессирующим течением этого заболевания или высоким риском его прогрессии. Ожирение, СД 2 типа, гиперлипидемия – основные состояния, связанные с развитием НАСГ. При отсутствии лечения и диетической коррекции в 12–14 % случаев жировой гепатоз трансформируется в НАСГ, в 5–10 % – в цирроз печени.
Пациентам с избыточной массой тела необходимо соблюдать диету с калорийностью суточного рациона до 1500–1700 ккал, со снижением насыщенных жиров в пище и повышением пищевых волокон, растительной клетчатки. При этом сочетание диетических рекомендаций с физической активностью умеренной интенсивности минимум 30 мин в день дает больший эффект, чем только соблюдение диеты. Многочисленные данные о влиянии снижения массы тела на состояние печени весьма противоречивы. Показано, что быстрая потеря массы тела закономерно приводит к нарастанию активности воспаления и прогрессии фиброза. Эффективным и безопасным признано уменьшение массы тела не более чем на 1,6 кг в нед., которое достига- ется при энергетической ценности пищи 25 кал/кг/сут и выполнении физических упражнений. Немаловажную роль играет исключение употребления продуктов «быстрого питания» [6].
Бариатрические операции – бандажиро-вание, желудочное шунтирование, установление внутрижелудочного баллона – используются редко.
НАЖБП тесно ассоциируется с дислипидемией, поэтому показано назначение статинов – препаратов, снижающих печеночный синтез и секрецию липопротеинов с высоким содержанием триглицеридов, общего холестерина, повышающих уровень липидов высокой плотности. Большинство авторов признают, что отклонение уровня печеночных трансаминаз – нечастый эпизод лечения статинами.
Официальной классификации гепатопро-тективных препаратов нет. Наиболее близко подошли к систематизации и решению этого вопроса С.В. Оковитый и соавт. [24]. Гепато-протективные препараты должны обеспечить антиоксидативную защиту гепатоцитов, сосудов и стромы печени, репарацию и улучшение всех функций, тормозить фибротиче-ские изменения в печени [10]. Препараты ур-содезоксихолиевой кислоты, особенно в сочетании со статинами, подавляют всасывание холестерина в кишечнике, снижают синтез в гепатоцитах, являются средствами, воздействующими на патогенез НАЖБП. Они также способствуют снижению выраженности воспалительной инфильтрации, подавляют апоптоз, замедляют фиброгенез в печени, уменьшают продукцию аутоантител. Цитопротек-тивный эффект препаратов показан при стеатозе и наличии факторов риска трансформации в НАСГ, особенно в сочетании с дислипидемией [22]. Адеметионин (гептрал) представляет собой S-аденозил-L-метионин, имеющий основное значение в биохимических реакциях трансметилирования (биосинтез фосфолипидов), транссульфатирования (синтез и оборот глутатиона и таурина, конъюгация и детоксикация желчных кислот, аминопропилирование) [2]. Эссенциальные фосфолипиды (ЭФЛ) представляют высокоочищен-ный экстракт из бобов сои и содержат преимущественно фосфатидилхолин с высокой концентрацией полиненасыщенных жирных кислот. Гепатотропное действие достигается встраиванием молекул ЭФЛ в поврежденные мембранные структуры печеночных клеток, ингибированием процессов ПОЛ, включением в состав апопротеинов осуществляющих транспорт триглицеридов в составе липидов очень низкой плотности из гепатоцита [1]. В настоящее время представлены эссенциа-ле-Н, резалют ПРО, эссливер и ливолин. Эс-сенциале-Н характеризуется наиболее высоким содержанием активного компонента ПФХ: 93 % в ампульной форме и 70 % в капсулах [14, 22, 25]. Препарат фосфоглив, имеющий в своем составе фосфолипиды и натрия глицирризинат, оказывает мембраностабилизирующее, гепатопротективное действие. Гепатопротектор метадоксил способствует снижению жировой инфильтрации печени, выраженности фиброза, нормализует липидный спектр крови, снижает показатели цитолиза и холестаза, активирует процессы окисления свободных жирных кислот в митохондриях гепатоцитов [18]. Препарат ли-поевой кислоты (липамид, тиоктацид) являются коферментом, участвующим в окислительном декарбоксилировании пировиноградной кислоты и кетокислот, оказывают липотропное действие, кроме того, выявлена их антиоксидативная активность [24]. Препарат гепагард-актив состоит из ЭФЛ (222 мг), L-карнитина (93 мг) и витамина Е (1,23 мг). L-карнитин приводит к уменьшению липидов, повышению мобилизации жирных кислот из жировой ткани, снижению веса. Эс-лидин, по данным ряда авторов [1], способствует улучшению как жирового, так и углеводного обмена веществ в организме. Реза-лют – фосфолипидный препарат нового поколения – показан пациентам с НАЖБП в сочетании с сердечно-сосудистыми заболеваниями, ИР для уменьшения негативного влияния статинов. Ремаксол – препарат, имеющий свойства полиионного раствора, в состав которого введены метионин, рибоксин, никотинамид и янтарная кислота; под его влиянием увеличивается эндогенный S-аденозил-L-метионина в печени [18].
У больных НАЖБП нарушения биоцино-за выявлены в 70–90 % случаев. Максимально выраженный рост бактерий отмечен при НАСГ и циррозе [6, 15]. Связывание и снижение реабсорбции в подвздошной кишке желчных кислот приводит к снижению холестерина и уменьшению его внутриклеточного содержания под воздействием препарата му-кофальк (псиллиум). Снижение уровня глюкозы, ИР является положительным фактором при назначении этого препарата [9]. Одним из средств коррекции эндотоксемии с пре-биотическим действием является лактулоза (дюфалак) [5].
Накоплен большой опыт применения би-гуанидов при НАЖБП в сочетании с СД [8]. Эффекты бигуанидов обусловлены уменьшением глюконеогенеза и синтеза липидов в печени, реализуемого через активацию цАМФ-зависимой протеинкиназы печени, что приводит к снижению синтеза триглицеридов из жирных кислот и митохондриального перекисного окисления. Кроме того, би-гуаниды подавляют экспрессию ФНО-α в печени и индуцирование этим цитокином стеатоза. Исследования показали, что назначение инсулинсенситайзеров больным с НАСГ, в частности метформина в дозе 1500 мг/сут в течение 12 мес., позволило снизить степень ИР у 86,6 % пациентов, активность аминотрансфераз – у 80 % пациентов, нормали- зовать АД, снизить и коррегировать дислипидемию – у 46,6 % [4]. Описан центральный аноректический эффект метформина, который способствует снижению потребности в пище и уменьшению массы тела.
Использование группы глитазонов позволило путем подавления синтеза СЖК в печени, повышения активности транспорта глюкозы снизить триглицеридемию и СЖК в крови. Тиазолидиндионы (глитазоны) селективно улучшают чувствительность к инсулину, стимулируя активность клеточного транспорта глюкозы, улучшается усвоение глюкозы периферическими тканями. Глита-зоны второго поколения – пиоглитазон – способствуют перераспределению жировой ткани за счет центрального ожирения [4].
Сложность верификации диагноза, поиск достоверных и высокоинформативных маркеров заболевания и новых неинвазивных методов диагностики делает необходимым проведение дальнейших исследований.
-
1. Балукова Е. В. Эссенциальные фосфолипиды в комплексной терапии неалкогольной жировой болезни печени / Е. В. Балукова, Ю. П. Успенский // Русский медицинский журнал. – URL: http://www.rmj.ru/articles_7995.htm .
-
2. Барановский А. Ю. Применение S-адено-зилметионина (гептрала) в терапии НАСГ / А. Ю. Барановский, К. Райхельсон, Н. В. Марченко // Клинические перспективы гастроэнтерологии. – 2010. – № 1. – С. 1–8.
-
3. Богомолов П. О. Многофакторный генез жировой болезни печени / П. О. Богомолов, А. О. Буеверов // Гепатологический форум. – 2006. – № 3. – С. 4–10.
-
4. Богомолов П. О. НАЖБП: стеатоз и НАСГ / П. О. Богомолов, Ю. О. Шульпекова // Клинические перспективы гастроэнтерологии, гепатологии. – 2004. – № 3. – С. 20–27.
-
5. Богомолов П. О. Неалкогольный стеатоге-патит: патофизиология, патоморфология, клиника и подходы к лечению / П. О. Богомолов, Т. В. Павлова // Фарматека. – 2003. – № 10. – С. 31–39.
-
6. Болезни печени и желчевыводящих путей : руководство для врачей / под ред. В. Т. Ивашкина. – 2–е изд. – М. : ООО Изд. дом «М–Вести». – 2005. – С. 536.
-
7. Буеверов А. О. Патогенетическое лечение НАСГ: обоснование, эффективность, безопасность / А. О. Буеверов, П. О. Богомолов, М. В. Маевская // Тер. архив. – 2007. – Т. 7, № 8. – С. 68.
-
8. Бутрова С. А. Эффективность метформина и больных с метаболическим синдромом и неалкогольной жировой болезнью печени / С. А. Бут-рова, А. Ю. Елисеева, А. В. Ильин // Ожирение и метаболизм. – 2008. – № 2 (15). – С. 17–21.
-
9. Возможность применения синбиотиков у пациентов с ХЗП / В. Г. Радченко [и др.]. – СПб., 2010. – С. 25.
-
10. Голофеевский В. Важнейшие вопросы патоморфогенеза и лечения НАЖБП у больных СД / В. Голофеевский // Врач. – 2012. – № 7. – С. 8–11.
-
11. Драпкина О. М. Влияние инсулинорези-стентности на развитие НАЖБП и артериальной гипертензии у пациентов с ожирением / О. М. Драп-кина, И. Попова, В. Т. Ивашкин // Врач. – 2012. – № 8. – С. 19–22.
-
12. Драпкина О. М. НАЖБП. Современный взгляд на проблему / О. В. Драпкина, В. И. Сми-рин, В. Т. Ивашкин // Лечащий врач. – 2010. – Т. 5, № 5. – С. 57–61.
-
13. Драпкина О. М. Неалкогольная жировая болезнь печени как компонент метаболического синдрома / О. М. Драпкина, Д. С. Гацолаева, В. Т. Ивашкин // Российские медицинские вести. – 2010. – № 2. – URL: http://www.m–vesti.ru/rmv/ rmv210.htm11.
-
14. Драпкина О. М. Терапия НАСГ при метаболическом синдроме: фокус на эссенциальные фосфолипиды / О. Н. Драпкина, В. Т. Корнеева, В. Т. Ивашкин // Лечащий врач. – 2010. – № 2. – С. 43–45.
-
15. Ивашкин В. Т. Болезни печени и желчевыводящих путей : руководство для врачей / В. Т. Ивашкин. – URL: http://www.twirpx.com/ file/958192.
-
16. Ивашкин В. Т. Диагностика и лечение неалкогольной жировой болезни печени : методические рекомендации / В. Т. Ивашкин, О. М. Драп-кина, Ю. О. Шульпекова // Российские медицинские вести. – 2009. – Т. XIV, № 3. – С. 71–72.
-
17. Калинин А. В. Метаболический синдром и НАЖБП / А. В. Калинин, Г. М. Такмулина // Научные ведомости Белгородского гос. ун-та. – 2009. – Т. 67, № 8. – С. 53.
-
18. Клиническая и экспериментальная гастроэнтерология / Т. Ф. Федотова [и др.]. – 2009. – № 3. – С. 2.
-
19. Корнеева О. Н. Возможность применения УД ХК и статинов для уменьшения сердечнососудистого риска у больных МС и НАЖБП / О. Н. Корнеева, О. М. Драпкина // Российские медицинские вести. – 2011. – № 3. – С. 57–63.
-
20. Махов В. М. Жировая болезнь печени: клиническое значение / В. М. Махов // Врач. – 2011. – № 10. – С. 14–19.
-
21. Мехтиев С. Н. Современный взгляд на перспективы терапии неалкогольной болезни печени / С. Н. Мехтиев, О. А. Мехтиева // Эффективная фармакотерапия. – 2011. – № 2. – С. 50.
-
22. Неалкогольный стеатогепатит при метаболическом синдроме / О. Н. Корнеева [и др.] // Consilium medicum. – 2007. – № 2. – С. 18–21.
-
23. Никитин И. Г. Скрининговая программа по выявлению распространенности неалкогольной жировой болезни печени и определению факторов риска развития заболевания / И. Г. Никитин // Российские медицинские вести. – 2010. – № XV (1). – С. 41–46.
-
24. Оковитый С. В. Гепаторпротекторы / С. В. Оковитый, Н. Н. Безбородкина, М. Улей-чик. – М. : ГЭОТАР-Медиа, 2010. – С. 56.
-
25. Полунина Т. Е. Неалкогольный стеатоз печени в практике интерниста / Т. Е. Полунина, И. В. Маев // Эффективная фармакотерапия в гастроэнтерологии. – 2009. – № 1. – С. 14–19.
-
26. Сологуб Т. В. Гепатопротективная активность ремаксола при хронических поражениях печени (материалы многоцентрового рандомизированного плацебо-контролируемого исследования) / Т. В. Сологуб, Л. Г. Горячева, Д. С. Суханов // Клин. медицина. – 2010. – № 47. – С. 262–269.
-
27. Шульпекова Ю. О. Патогенетическое значение липидов при неалкогольной жировой болезни печени / Ю. О. Шульпекова // Российский журн. гастроэнтерологии, гепатологии, колопрок-тологии. – 2012. – Т. ХХII, № 1. – С. 46.
-
28. Adipocyte fatty acid binding protein levels relate to inflammation and fibrosis in nonalcoholic fatty liver disease / K. Milner [et al.] // Hepatology. – 2009. – № 49 (6). – Р. 1926–1934.
-
29. Behavior therapy for nonalcoholic fatty liver disease: the need for a multidisciplinary approach / S. Bellentani [et al.] // Hepatology. – 2008. – № 47. – Р. 746–754.
-
30. Betain resolves severe alcohol-induced hepatitis and steatosis following liver transplantation / K. Samara [et al.] // Dig. Dis. Sci. – 2006. – Vol. 51. – P. 1226–1229.
-
31. Clinicopathological significance of oxidative cellular damage in non-alcoholic fatty liver diseases / S. Seki [et al.] // Hepatol. Res. – 2005. –
-
32. Current concepts in the pathogenesis of nonalcoholic fatty liver disease / Nahum [et al.] // Liver Int. – 2007. – 27 (4). – Р. 432–433.
-
33. Cytokeratin-18 fragment levels as noninva-sive biomarkers for nonalcoholic steatohepatitis: a multicenter validation study steatohepatitis / A. E. Feldstein [et al.] // Hepatology. – 2004. – № 39 (1). – Р. 188–196.
-
34. Cytokines and the pathogenesis of nonalcoholic steatohepatitis / H. Tilg [et al.] // Gut. – 2005. – № 54. – Р. 303–306.
-
35. Epidemiology of nonalcoholic fatty liver disease Dig / S. Bellantani [et al.] // Dis. – 2010. – № 28. – Р. 155–161.
-
36. Gamma–glutamyltransferase is associated with incident vascular events independently of alcohol intake: analysis of the British Women's Heart and Health Study and meta–analysis / A. Fraser [et al.] // Arterioscler Thromb Vasc Biol. – 2007. – Vol. 27. – Р. 2729–2735 [Erratum, Arterioscler Thromb Vasc Biol. – 2008. – Vol. 28 (2)].
-
37. Genetic variants regulating insulin receptor signalling are associated with the severity of liver damage in patients with non-alcoholic fatty liver disease / P. Dongiovanni [et al.] // Gut. – 2010. – № 59. – Р. 267–273.
-
38. Mofrad P. Clinical and histologic spectrum of nonalcoholicfatty liver disease associated with normal ALT values / P. Mofrad, M. Contos, M. Haque // Hepatology. – 2003. – № 37. – Р. 1286–1292.
-
39. Musso G. Non-alcoholic fatty liver disease from pathogenesisto management: an update / G. Musso, R. Gambino, M. Cassader // Obesity Reviews. – 2010. – № 11 (6). – Р. 430–445.
-
40. Stefan N. Causes and Metabolic Consequences of Fatty Liver / N. Stefan, K. Kantartzis, H. Häring // Endocrine Reviews. – 2008. – № 29 (7). – Р. 939–960.
-
41. The ins and auts of mitochondrial dysfunction in NASH / B. Fromenty [et al.] // Diabetes Metab. – 2004. – № 30 (2). – Р. 121–138.
Vol. 33 (2). – Р. 132–134.
NON-ALCOHOLIC FATTY LIVER DISEASE:PATHOGENESIS, DIAGNOSTICS, TREATMENT
Е.А. Chercashina1, L.V. Petrenco2, A.Yu. Evstigneeva1
Список литературы Неалкогольная жировая болезнь печени: патогенез, диагностика, лечение
- Балукова Е. В. Эссенциальные фосфолипиды в комплексной терапии неалкогольной жировой болезни печени/Е. В. Балукова, Ю. П. Успенский//Русский медицинский журнал. -URL: http://www.rmj.ru/articles_7995.htm.
- Барановский А. Ю. Применение S-аденозилметионина (гептрала) в терапии НАСГ/А. Ю. Барановский, К. Райхельсон, Н. В. Марченко//Клинические перспективы гастроэнтерологии. -2010. -№ 1. -С. 1-8.
- Богомолов П. О. Многофакторный генез жировой болезни печени/П. О. Богомолов, А. О. Буеверов//Гепатологический форум. -2006. -№ 3. -С. 4-10.
- Богомолов П. О. НАЖБП: стеатоз и НАСГ/П. О. Богомолов, Ю. О. Шульпекова//Клинические перспективы гастроэнтерологии, гепатологии. -2004. -№ 3. -С. 20-27.
- Богомолов П. О. Неалкогольный стеатогепатит: патофизиология, патоморфология, клиника и подходы к лечению/П. О. Богомолов, Т. В. Павлова//Фарматека. -2003. -№ 10. -С. 31-39.
- Болезни печени и желчевыводящих путей: руководство для врачей/под ред. В. Т. Ивашкина. -2-е изд. -М.: ООО Изд. дом «М-Вести». -2005. -С. 536.
- Буеверов А. О. Патогенетическое лечение НАСГ: обоснование, эффективность, безопасность/А. О. Буеверов, П. О. Богомолов, М. В. Маевская//Тер. архив. -2007. -Т. 7, № 8. -С. 68.
- Бутрова С. А. Эффективность метформина и больных с метаболическим синдромом и неалкогольной жировой болезнью печени/С. А. Бутрова, А. Ю. Елисеева, А. В. Ильин//Ожирение и метаболизм. -2008. -№ 2 (15). -С. 17-21.
- Возможность применения синбиотиков у пациентов с ХЗП/В. Г. Радченко [и др.]. -СПб., 2010. -С. 25.
- Голофеевский В. Важнейшие вопросы патоморфогенеза и лечения НАЖБП у больных СД/В. Голофеевский//Врач. -2012. -№ 7. -С. 8-11.
- Драпкина О. М. Влияние инсулинорезистентности на развитие НАЖБП и артериальной гипертензии у пациентов с ожирением/О. М. Драпкина, И. Попова, В. Т. Ивашкин//Врач. -2012. -№ 8. -С. 19-22.
- Драпкина О. М. НАЖБП. Современный взгляд на проблему/О. В. Драпкина, В. И. Смирин, В. Т. Ивашкин//Лечащий врач. -2010. -Т. 5, № 5. -С. 57-61.
- Драпкина О. М. Неалкогольная жировая болезнь печени как компонент метаболического синдрома/О. М. Драпкина, Д. С. Гацолаева, В. Т. Ивашкин//Российские медицинские вести. -2010. -№ 2. -URL: http://www.m-vesti.ru/rmv/rmv210.htm11.
- Драпкина О. М. Терапия НАСГ при метаболическом синдроме: фокус на эссенциальные фосфолипиды/О. Н. Драпкина, В. Т. Корнеева, В. Т. Ивашкин//Лечащий врач. -2010. -№ 2. -С. 43-45.
- Ивашкин В. Т. Болезни печени и желче-выводящих путей: руководство для врачей/В. Т. Ивашкин. -URL: http://www.twirpx.com/file/958192.
- Ивашкин В. Т. Диагностика и лечение неалкогольной жировой болезни печени: методические рекомендации/В. Т. Ивашкин, О. М. Драпкина, Ю. О. Шульпекова//Российские медицинские вести. -2009. -Т. XIV, № 3. -С. 71-72.
- Калинин А. В. Метаболический синдром и НАЖБП/А. В. Калинин, Г. М. Такмулина//Научные ведомости Белгородского гос. ун-та. -2009. -Т. 67, № 8. -С. 53.
- Клиническая и экспериментальная гастроэнтерология/Т. Ф. Федотова [и др.]. -2009. -№ 3. -С. 2.
- Корнеева О. Н. Возможность применения УД ХК и статинов для уменьшения сердечно-сосудистого риска у больных МС и НАЖБП/О. Н. Корнеева, О. М. Драпкина//Российские медицинские вести. -2011. -№ 3. -С. 57-63.
- Махов В. М. Жировая болезнь печени: клиническое значение/В. М. Махов//Врач. -2011. -№ 10. -С. 14-19.
- Мехтиев С. Н. Современный взгляд на перспективы терапии неалкогольной болезни печени/С. Н. Мехтиев, О. А. Мехтиева//Эффективная фармакотерапия. -2011. -№ 2. -С. 50.
- Неалкогольный стеатогепатит при метаболическом синдроме/О. Н. Корнеева [и др.]//Consilium medicum. -2007. -№ 2. -С. 18-21.
- Никитин И. Г. Скрининговая программа по выявлению распространенности неалкогольной жировой болезни печени и определению факторов риска развития заболевания/И. Г. Никитин//Российские медицинские вести. -2010. -№ XV (1). -С. 41-46.
- Оковитый С. В. Гепаторпротекторы/С. В. Оковитый, Н. Н. Безбородкина, М. Улейчик. -М.: ГЭОТАР-Медиа, 2010. -С. 56.
- Полунина Т. Е. Неалкогольный стеатоз печени в практике интерниста/Т. Е. Полунина, И. В. Маев//Эффективная фармакотерапия в гастроэнтерологии. -2009. -№ 1. -С. 14-19.
- Сологуб Т. В. Гепатопротективная активность ремаксола при хронических поражениях печени (материалы многоцентрового рандомизированного плацебо-контролируемого исследования)/Т. В. Сологуб, Л. Г. Горячева, Д. С. Суханов//Клин. медицина. -2010. -№ 47. -С. 262-269.
- Шульпекова Ю. О. Патогенетическое значение липидов при неалкогольной жировой болезни печени/Ю. О. Шульпекова//Российский журн. гастроэнтерологии, гепатологии, колопроктологии. -2012. -Т. ХХII, № 1. -С. 46.
- Adipocyte fatty acid binding protein levels relate to inflammation and fibrosis in nonalcoholic fatty liver disease/K. Milner [et al.]//Hepatology. -2009. -№ 49 (6). -Р. 1926-1934.
- Behavior therapy for nonalcoholic fatty liver disease: the need for a multidisciplinary approach/S. Bellentani [et al.]//Hepatology. -2008. -№ 47. -Р. 746-754.
- Betain resolves severe alcohol-induced hepatitis and steatosis following liver transplantation/K. Samara [et al.]//Dig. Dis. Sci. -2006. -Vol. 51. -P. 1226-1229.
- Clinicopathological significance of oxidative cellular damage in non-alcoholic fatty liver diseases/S. Seki [et al.]//Hepatol. Res. -2005. -Vol. 33 (2). -Р. 132-134.
- Current concepts in the pathogenesis of nonalcoholic fatty liver disease/Nahum [et al.]//Liver Int. -2007. -27 (4). -Р. 432-433.
- Cytokeratin-18 fragment levels as noninva-sive biomarkers for nonalcoholic steatohepatitis: a multicenter validation study steatohepatitis/A. E. Feldstein [et al.]//Hepatology. -2004. -№ 39 (1). -Р. 188-196.
- Cytokines and the pathogenesis of nonalcoholic steatohepatitis/H. Tilg [et al.]//Gut. -2005. -№ 54. -Р. 303-306.
- Epidemiology of nonalcoholic fatty liver disease Dig/S. Bellantani [et al.]//Dis. -2010. -№ 28. -Р. 155-161.
- Gamma-glutamyltransferase is associated with incident vascular events independently of alcohol intake: analysis of the British Women's Heart and Health Study and meta-analysis/A. Fraser [et al.]//Arterioscler Thromb Vasc Biol. -2007. -Vol. 27. -Р. 2729-2735 [Erratum, Arterioscler Thromb Vasc Biol. -2008. -Vol. 28 (2)].
- Genetic variants regulating insulin receptor signalling are associated with the severity of liver damage in patients with non-alcoholic fatty liver disease/P. Dongiovanni [et al.]//Gut. -2010. -№ 59. -Р. 267-273.
- Mofrad P. Clinical and histologic spectrum of nonalcoholicfatty liver disease associated with normal ALT values/P. Mofrad, M. Contos, M. Haque//Hepatology. -2003. -№ 37. -Р. 1286-1292.
- Musso G. Non-alcoholic fatty liver disease from pathogenesisto management: an update/G. Musso, R. Gambino, M. Cassader//Obesity Reviews. -2010. -№ 11 (6). -Р. 430-445.
- Stefan N. Causes and Metabolic Consequences of Fatty Liver/N. Stefan, K. Kantartzis, H. Häring//Endocrine Reviews. -2008. -№ 29 (7). -Р. 939-960.
- The ins and auts of mitochondrial dys-function in NASH/B. Fromenty [et al.]//Diabetes Metab. -2004. -№ 30 (2). -Р. 121-138.


