Нейробластический резерв энтеральной нервной системы человека
Автор: Марков И.И., Низаметдинова Д.Р.
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 1 т.34, 2026 года.
Бесплатный доступ
ВВЕДЕНИЕ. В соответствии с отечественной классификацией энтеральная нервная система (ЭНС) входит в состав метасимпатической системы, объединяющей интрамуральные нервные ганглии различных органов [1]. При этом, нет ни одного положения, касающегося ее морфологии, которое не являлось бы спорным. Прежде всего, это отсутствие достоверной информации о физиологической и репаративной регенерации ЭНС, об участии в ней стволовых клеток, митотически или амитотически делящихся нейробластов, нейробластического резерва и дикарионов или гетерокарионов, образовавшихся путем слияния нейронов и олигодендроцитов. ЦЕЛЬ: доказать наличие нейробластического резерва в ЭНС в постнатальном онтогенезе человека. МАТЕРИАЛЫ И МЕТОДЫ. Изучены классическими и оригинальными импрегнационными методами аутопсийные фрагменты кишечника новорожденных детей (n=3) и людей I зрелого возраста (n=12). РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ. Полученные данные свидетельствуют о том, что дифференцировка чрезмерно избыточной и чрезвычайно гетерогенной популяции нейробластов ЭНС человека продолжается и в постнатальном периоде онтогенеза. В связи с этим в ней формируется резерв, за счет которого постоянно пополняется популяция дифференцированных нейроцитов.
Энтеральная нервная система, нейробласты, нейроны, нервные ганглии
Короткий адрес: https://sciup.org/143185635
IDR: 143185635 | УДК: 591.818.2 | DOI: 10.20340/mv-mn.2026.34(1).1014
Neuroblastic reserve of the human enteric nervous system
INTRODUCTION. According to the Russian classification, the enteric nervous system (ENS) is part of the metasympathetic system that unites the intramural nerve ganglia of various organs [1]. At the same time, there is not a single provision concerning its morphology that would not be controversial. First of all, this is the lack of reliable information about the physiological and reparative regeneration of the ENS, about the participation in it of stem cells, mitotically or amitotically dividing neuroblasts, neuroblastic reserve and dicaryons or heterokaryons formed by the fusion of neurons and oligodendrocytes. AIM of the study is to prove the presence of neuroblastic reserve in the ENS in human postnatal ontogenesis. MATERIALS AND METHODS. Autopsy fragments of the intestines of newborns (n=3) and people of mature age I (n=12) were studied using classical and original impregnation methods. RESULTS AND DISCUSSION. The data obtained indicate that the differentiation of an markedly abundant and extremely heterogeneous population of human ENS neuroblasts continues in the postnatal period of ontogenesis. In this regard, a reserve is formed in it, due to which the population of differentiated neurocytes is constantly replenished.
Текст научной статьи Нейробластический резерв энтеральной нервной системы человека
(1).1014
Марков И.И., Низаметдинова Д.Р. Нейробластический резерв энтеральной нервной системы человека. Морфологические ведомости. 2026;34(1):1014. (1).1014
(1).1014
Markov II, Nizametdinova DR. Neuroblastic reserve of the human enteric nervous system. Morfologicheskie Vedomosti – Morphological newsletter. 2026;34(1):1014. (1).1014
Огромное число публикаций, посвященных ЭНС [2–11] содержит и огромное число противоречий. Причем, создается впечатление, что они не решаются и даже не обсуждаются, а только созерцаются. Совершенно очевидно, что «среди всего, что есть в природе и изучается наукой, мозг человека был и долго еще будет оставаться самым интригующим органом (цит. по [12], с. 47).
В свою очередь, ЭНС – энтеральный мозг [7, 12] подобен центральной нервной системе [13]: в ней есть афферентные и эфферентные элементы, а ее рефлекторная деятельность осуществляется без участия ЦНС [14]. Более того, энтеральный мозг - носитель генетической памяти, а головной мозг - только приобретенной [8, 15]. При этом, при болезни Паркинсона наблюдаются желудочно-кишечная симптоматика [16, 17]. «Нейрон, не способный к регенерации, быстро и необратимо погибающий при повреждении аксона и аноксии / ишемии - такой нейрон стал достоянием прошлого» (цит. по [17], с. 13). Повреждению и гибели нейроцитов противостоят два фактора: их пролиферация и обширные возможности репарации. Открытие нейрональной стволовой клетки хотя и стимулировало изучение нейрогенеза, но факт образования новых нейронов в головном мозге так и не был установлен [18]. Поэтому, с одной стороны «нервные клетки не восстанавливаются», а с другой стороны – способность головного мозга к реабилитации после различных повреждений, в том числе и после инсульта, хорошо известна. Поскольку для нейронов характерны две особенности: 1) сверхсложная структурная организация и 2) сверхпродолжительная функция хранения приобретенной памяти [18], то и способ регенерации у них оригинальный: образование путем слияния дикарионов и гетерокарионов [18–24]. Несмотря на то, что такой способ регенерации «воспринимается учеными с недоверием» (цит. по [18], с. 21), он для нейроцитов является наиболее рациональным с биологической точки зрения [25]. Но если он не способен увеличить число нейронов, то это означает, что масса головного мозга и количество нейроцитов в ЭНС увеличивается в постнатальном онтогенезе за счет других механизмов. Так, в головном мозге щенков «в состоянии деления находится большое количество нервных клеток: больших, средних и малых пирамидных, клеток полиморфного типа, а также клеток – зерен, находящихся преимущественно в слое IV (цит. по [26], с. 135). В ЭНС в постнатальном онтогенезе происходит увеличение числа нейронов и отходящих от них отростков. Так, если у новорожденного в ганглиях ауэрбаховского сплетения определяется от 3 до 45 клеток, то у детей 4–6 лет – от 40 до 150 [27]. То есть число нейроцитов увеличивается от 3 до 50 раз? За счет чего это увеличение происходит? Разные авторы предлагают различные пути решения, часто диаметрально противоположные. Так, начиная с конца XIX века и до настоящего времени значительное число авторов [25, 27–34] являются активными сторонниками амитоза. Они считают, что «если нервные клетки вообще не способны размножаться путем деления (или каким-либо другим путем), то, конечно, никакого увеличения их количества в любой части животного в течение его жизни произойти не может» (цит. по [26], с. 123).
Однако, никто из этих авторов, кроме [26, 34] процесса амитотического деления нейрона не наблюдал, они лишь констатировали конечный его этап – наличие в гистологических препаратах дикарионов. Лишь [35, 36] наблюдали единичные случаи митотически делящихся нейробластов в межмышечном сплетении кишечника эмбриона человека. Но признали их за случайно «заблудившихся» в потоке мигрантов стволовые клетки. Так, стволовые клетки или нейробласты? И в то же время, по мнению [36] существуют два генетически детерминированных варианта репаративной регенерации в нервной системе. Первый - только компенсаторный, за счет увеличения числа и мощности сохранившихся дифференцированных нейроцитов, второй – за счет нейробластического резерва, потенциального источника вновь дифференцированных нейроцитов. При этом, общее число нейроцитов в постнатальном онтогенезе остается постоянным, а их дифференцировка в тонкой кишке заканчивается примерно к 30 годам [27]. Считается, что для определенных нервных структур количество нейроцитов наследуется как доминантный признак: это установлено для голубого пятна головного мозга мыши [37].
В ЭНС основная масса нервных клеток – это нейробласты, их число во много раз превышает число дифференцированных нейроцитов, выявленных импрегнацией серебром [10, 38–45]. Именно эти нейробласты растущего и взрослого организма наиболее резистентные к экстремальным факторам [6, 11, 13], дифференцируясь затем в нейроциты, сохраняют, тем самым, численность популяции [46, 47].
Данные, полученные [41], отрицают представления о нейробластическом резерве, заложенном в эмбриогенезе, мотивируя тем, что число нейробластов возрастает при аппендиците [25, 43, 44]. Эти данные, по мнению [41], позволяют считать, что нейробласты могут образовываться и в постнатальном онтогенезе, хотя это отрицают многие другие авторы [2, 11, 48–52]. Эти разногласия о оценке количества нейробластов и нейроцитов в ЭНС, связаны, в первую очередь, с методикой импрегнации серебром [45], когда технические возможности оказались неадекватными для решения поставленных задач. Всегда же, «научные открытия являются функцией использованных методов» (цит. по [53], с. 177). Действительно, поскольку нейробласты лишены нейрофибрилл, то их нейроплазма практически не выявляется методами Бильшовского – Грос, Гольджи и Кампоса. Интенсивно импрегнируют только ядра нейробластов, которые признаются ядрами нейроглиоцитов. По мере дифференцировки нейробластов, у них постепенно идентифицируется нейроплазма и отростки, и они, приобретая статус нейроцитов, увеличивают численность популяции.
Таким образом, существуют многочисленные противоречия в работах, посвященных проблеме физиологической и репаративной регенерации ЭНС. Значительная их часть, вероятно, устранена благодаря универсальному методу импрегнации, применению цито- и кариометрии нейробластов на различных стадиях их дифференцировки и вычислению информационных показателей их энтропии и избыточности.
ЦЕЛЬ : доказать наличие нейробластического резерва в ЭНС в постнатальном онтогенезе человека.
МАТЕРИАЛЫ И МЕТОДЫ
Аутопсийный материал получен в 2019–2022 годы из патологоанатомических отделений лечебных учреждений г. Самары. При отборе материала были исключены случаи с морфологической картиной повреждений кишечника.
Фрагменты аутопсийного материала (кишечника) после тщательной предварительной подготовки (освобождения от слизистых наслоений, промывания водопроводной водой) подвергались гидропрепарированию под стереомикроскопом и разделялись на слизистую, мышечную оболочки и подслизистую основу. Каждая из оболочек (мышечная и слизистая) и подслизистая основа фиксировались в 10% аметанольном формалине в отдельных флаконах.
Гистологическая обработка материала для окраски по Ван-Гизону, гематоксилином и эозином, парарозанилином проводилась по стандартным методам. Готовились парафиновые блоки, из них получали срезы толщиной 5–7 мкм, которые после завершения окраски заключались в канадский бальзам.
Для одновременного выявления нервных и сосудистых элементов энтеральный нервной си- стемы был модифицирован универсальный метод импрегнации аргирофильных структур [54]. Использовались тотальные препараты стенки кишечника (мышечная оболочка и подслизистая основа) толщиной 40,0–100,0 мкм и площадью до 24 см2 (4,0×6,0 см). После завершения процедуры импрегнации препараты заключались в канадский бальзам для максимального просветления.
Морфометрические исследования
На серийных гистологических срезах, окрашенных классическими способами, и на тотальных препаратах, импрегнированных универсальным методом, проводится цито- и кариометрия дифференцирующихся и сформировавшихся нейроцитов: измеряются большие и малые оси перикарионов и ядер. На основании средних значений ядерно-цитоплазматических отношений вычисляются информационные показатели энтропии (P) и избыточности (R) [55, 56].
Используются формулы:
-
1. H = -^1Pi^2pi;2)R = (l--^-)-100, max
-
2. Отношение площади ( S ) перикариона к его Is
-
3. Определяется объем нейробластов и малодифференцированных нейроцитов по формуле: V = 4/3 πa2b, где a – малый и b – большой радиус их перикарионов.
-
4. Впервые была использована собственная методика расчета объема ядра и перикариона клетки II типа Догеля с целью сравнения полученных результатов с данными, полученными по формуле элипсоида вращения.
где pi – частность элемента системы, Hmax =1.
Площадь перикариона нейроцита – чрезвычайно важная его характеристика. На ее поверхности совершаются все процессы обмена, действуют внешние регулирующие и повреждающие агенты, осуществляются межнейронные взаимодействия.
у – дисперсность – самостоятельный термодинамический параметр, демонстрирующий морфологический и функциональный статус нейроцита.
^^Ш1(у. + 1_уд.(1.1)
s w = Ai ^Уд = ^+^ _ y^.(1.2)
7^ = A---- л ----=---о---(№+y-bjw+i+ yJ ; (i-3)
A^^w^i^^Ciw-yi);(1-5)
Sx^s^Z^^^^U^^^(1.6)
Jx - l^J® = Z?.i^(y.+1 - yiXyl+1 + y.)2;(1.7)
Ixy^iZ^^i^^1^(1-8)
Sy^M^Z^^^t^i-xf);(1-9)
к Ем/^^м^^^к- ■y)(^i+-y)2. (i-10)
Статистическая обработка морфометрических параметров проведена современными био-статистическими методами. Статистический анализ в программах MS Excel - 2019 и JBM Statistic SPSS-26 с использованием вариационного и дисперсного методов.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В стенке кишечника новорожденных часть ганглиев ЭНС находится в просвете лимфатических микрососудов (рис. 1). Это соответствует филогенетически более раннему диффузному способу трофики нервных структур, характерному для рептилий и земноводных [57, 58].
В этих ганглиях доминируют нейробласты, находящиеся на различных стадиях дифференцировки.
Они отличаются друг от друга размерами перикарионов и ядер, а также наличием или отсутствием тончайших отростков. При этом, в одних ганглиях идентифицируются только много-отросчатые нейробласты, связанные между собой цитоплазматическим синцитием. В других ганглиях – только безотросчатые, плотно упакованные нейробласты, с дополнительным источником трофики – кровеносными микрососудами (рис. 2).
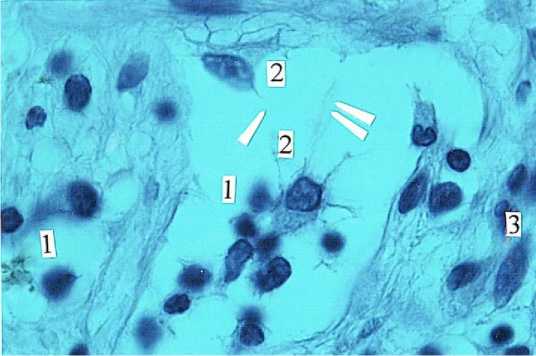
Рисунок 1. Нейробласты (2) в лимфатическом микрососуде (1) стенки тонкой кишки (3) новорожденного. Окраска парарозанилином. Ув. 400
Figure 1. Neuroblasts (2) in a lymphatic microvessel (1) of the small intestinal wall (3) of a newborn. Stained with pararosaniline. Mag. 400
я

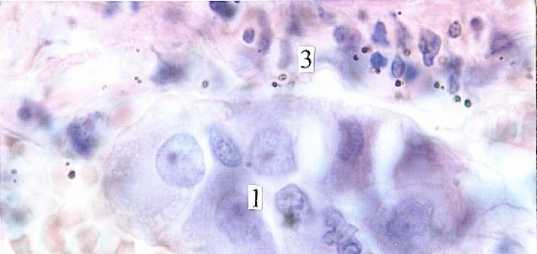
Рисунок 2. Нейробласты (1) в ганглии межмышечного сплетения тонкой кишки (3) новорожденного. 2) венула. Окраска гематоксилином и эозином. Ув. 400
Figure 2. Neuroblasts (1) in the ganglion of the intermuscular plexus of the small intestine (3) of a newborn. 2) venule. Stained with hematoxylin and eosin. Mag. 400
Информационный анализ нейробластов на основе энтропии и избыточности информации позволяет выделить четыре стадии их дифференцировки: 1) стадию нейробласта; 2) стадию роста нейробласта; 3) стадию созревания нейробласта; 4) стадию малодифференцированного нейроцита. Процесс дифференцировки нейробластов характеризуется закономерным увели- чением перикариона и ядра, а также возрастанием цитоплазменно-ядерных отношений. Так, энтропия (H) нейробластов снижается от 0,6536 бит (I стадия), 0,5664 бит (II стадия), 0,4275 бит (III стадия) до 3989 бит (IV стадия). При этом, избыточность информации (R) медленно возрастает: от 35,54% (I стадия), 41,08% (II стадия), 48,72% (III стадия) до 54,10% (IV стадия). Цитоплазменно-ядерные отношения возрастают: от 2,2 (I стадия) до 2,9 (II стадия), до 4,3 (III стадия) и до 5,7 (IV стадия).
В ЭНС людей I зрелого возраста ганглии межмышечного и подслизистого сплетений также содержат значительное число нейробластов, находящихся на различных стадиях дифференцировки. Они еще не имеют нейрофибрилл, поэтому цитоплазма импрегнируется чрезвычайно слабо, даже при использовании универсального метода импрегнации. При импрегнации же по Бильшовскому – Грос цитоплазма нейробластов вообще не воспринимает серебро, идентифицируются только ядра. Поэтому на иллюстрациях в работах авторов [13, 59, 60], в ганглиях нейробласты отсутствуют, а их многочисленные ядра обозначаются как элементы нейроглии.
Отдельные нейробласты ЭНС людей I зрелого возраста были идентифицированы на стадии аргирофильных включений в нейроплазме (рис. 3). У них отсутствуют отростки, они имеют крупное прозрачное ядро с одним светлым ядрышком и многочисленные аргирофильные зерна, занимающие всю нейроплазму и проникающие даже в ядро.
Глиальная защита у таких нейробластов не сформирована, лишь единичные, но активные глиоциты с крупными ядрами и двумя–тремя ядрышками находятся вблизи их перикарионов.
Процесс формирования истинной нейрофиб-риллярной сети происходит на всех стадиях дифференцировки нейробластов, и у новорожденных, и у людей I зрелого возраста. На препаратах, им-прегнированных универсальным методом, это проявляется образованием в нейроплазме аргирофильной зернистости, затем более интенсивной, но не гомогенной импрегнацией всей нейроплазмы, и завершается идентификацией в ней нейрофибриллярной сети, продолжающейся во все отростки дефинитивных нейроцитов (рис. 4).
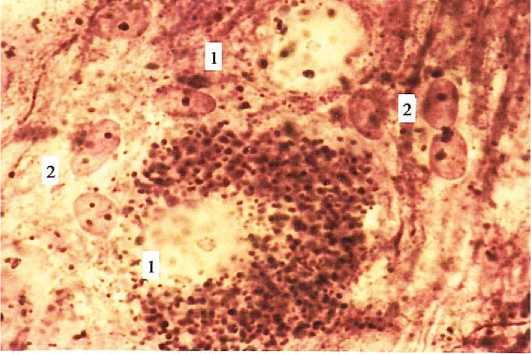
Рисунок 3. Нейрофильная зернистость в нейроплазме нейробластов (1) межмышечного сплетения толстой кишки мужчины I зрелого возраста. 2) сателлитные глиоциты Универсальный метод импрегнации. Ув. 600
Figure 3. Neurophilic granularity in the neuroplasm of neuroblasts (1) from the intermuscular plexus of the colon of a mature man. 2) satellite gliocytes. Universal impregnation method. Mag. 600
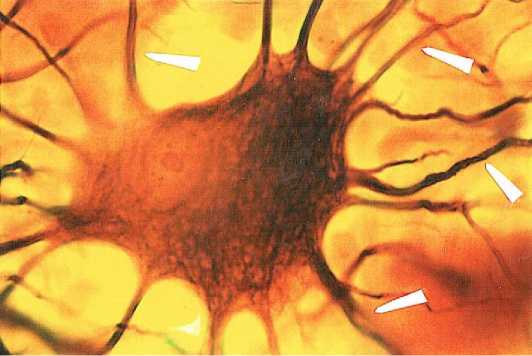
Рисунок 4. Нейрофибриллярная сеть в нейроплазме нейро-цита подслизистого сплетения тонкой кишки женщины I зрелого возраста. ↑) нейрофибриллы в отростках. Универсальный метод импрегнации. Ув. 900
Figure 4. Neurofibrillary network in the neuroplasm of a neurocyte of the submucosal plexus of the small intestine of a mature woman. ↑) neurofibrils in processes. Universal impregnation method. Mag. 900
Изучение нейрофибриллярной сети в нейро-цитах имеет длительную историю. Еще [37, 57, 58] «наблюдали внутри тел нервных клеток загадочную сеть, состоящую из тонкогранулярных фибрилл, продолжающихся в протоплазматические отростки (цит. по [53], с. 171).
Для решения главного вопроса: «имеются ли основания считать их внутриклеточными путями, специально дифференцированными для распространения нервного импульса?» (цит. по [53], с. 176) методы Гольджи, Бильшовского – Грос и Эрлиха оказались неадекватными. Поэтому в 1903 году S. Ramon y Cajal [59] разработал метод импрегнации с помощью восстановления нитрата серебра, позволивший представить «истинную организацию нейрофибрилляр-ного скелета в нервной протоплазме и в периферических разветвлениях» (цит. по [15], с. 177). При интенсивной импрегнации перикариона нейроцитов, нейрофибриллы «великолепно им-прегнировались в коричневый, черный или кирпично-красный цвет и были совершенно прозрачны» (цит. по [53], с. 175). В основе метода [65] – простая, но чрезвычайно плодотворная идея: 1) использовать для импрегнации не сре- зы, а фрагменты нервной ткани; 2) подогревать погруженные в крепкий раствор азотнокислого серебра фрагменты в течение нескольких суток; 3) восстанавливать серебро до металла пирогал-ловой кислотой или гидрохиноном. Вскоре после публикации этого метода, в 1904 году M.Bielschowsky [66] предложил свой метод выявления нейрофибрилл в гистологических срезах. Но двойной импрегнацией – раствором нитрата серебра и раствором аммиачного серебра. Затем в 1930 году А.В. Фаворский [67] модифицировал метод Кахаля, добавляя в фиксирующий раствор муравьиную или ледяную уксусную кислоты.
Таким образом, в распоряжении нейрогистологов есть три метода, «в равной степени легких и плодотворных» (цит. по [53], с. 176) для исследования нервной системы. Однако, до настоящего времени во многих современных нейроги-стологических монографиях [13, 59, 60, 63] и публикациях [6, 50, 64] отсутствуют микрофотографии, «основное достоинство которых – точность и объективность даваемых ими изображений» (цит. по [65], с. 284). Замена их рисунками свидетельствует о том, что микрофотографии, сделанные с препаратов, импрегнированных по
Бильшовскому – Грос, Кампосу и другими методами не отличаются высокими информативными качествами. При этом, чрезвычайно гомогенная импрегнация нейроплазмы и ядра нейроцита («темный» нейрон) считается результатом его функциональной активности [66].
Это означает, что только нейроциты, при наличии нейрофибрилл, способны выполнять нервную функцию – проведения нервного импульса. А какую функцию выполняют нейробласты? Считается, что нейробласты – это «лишь переходная форма эмбрионального и раннего постэмбрионального этапов развития нервной ткани» (цит. по [13], с. 125) и до преобразования в нейроны нервной функции не выполняют. Другая точка зрения – нейробласты могут долго сохраняться во взрослом организме и, после завершения дифференцировки в нейроциты, способны участвовать в репаративной регенерации поврежденных нервных структур [14, 35, 38, 55, 67]. То есть, согласно теории тканевой камби-альности [68], нейробласты являются камбиальными элементами нервной ткани, ее нейробла-стическим резервом. Но и нейробласты, и нейроциты не способны ни к митозу, ни к амитозу [7, 48, 19, 51, 68, 69]. Хотя, в многочисленных работах [25–29, 31, 32, 36, 45, 70–72] авторы указывают на возможность амитотического деления нейронов в вегетативных ганглиях и в центральной нервной системе. При этом, они считают, что только амитоз является механизмом феномена двуядерности нейроцитов. И только в отдельных работах двуядерность нейроцитов признается результатом их синцитиального слияния [18–21].
ЭНС содержит более 200,0 млн нейроцитов [3, 7, 8, 12, 58], значительно больше, чем спиной мозг [73]. Эти данные оказались неожиданными, поскольку они во много раз превышают число нейроцитов, идентифицированных в стенке кишечника [5, 74]. Так, на 1,0 см², межмышечного сплетения в тощей кишке было обнаружено лишь 619±20 афферентных нейронов, в подвздошной кишке – 665±59, в слепой кишке – 365±52 [27]. Если же ориентироваться на эти данные, то у но- ворожденных детей во всем межмышечном сплетении тонкой кишки окажется не более 55000 афферентных нейроцитов. Это при площади ее поверхности в среднем 85 см² (от 40 до 144 см²) и при постоянном количестве нейроцитов и у новорожденных, и у взрослых [75].
В подслизистой основе и мышечной оболочке стенки кишечника, кроме «классических» плоскостных ганглиев, идентифицированы и локальных ганглии с компактным расположением нейробластов.
Вероятно, что только определенная часть нервных ганглиев ЭНС, заложенных еще на 12–14 неделе эмбрионального развития, трансформируются в постнатальном онтогенезе в дефинитивные ганглии основных плоскостных сплетений – межмышечное и подслизистое. Другая часть ганглиев трансформируется в дефинитивные локальные ганглии с плотной упаковкой нейроцитов. Нейроциты, локализованные в первой группе ганглиев, получают питание из кровеносной системы, нейроциты второй группы ганглиев - из интерстициальной жидкости и лимфы. Площади локальных ганглиев в 2–3 раза меньше площади плоскостных ганглиев, в них нет нейропиля и глиоцитов. Число нейробластов варьирует в них от 12 до 56. Это крупные клетки с большим интенсивно импрегнированным ядром овальной формы, содержащим многочисленные (от 5 до 10) крупных глыбок хроматина. Нейроплазма – светлая, лишена нейрофибрилл, граница между ней и ядром четкая. Нейробласты упакованы так компактно, что между ними сформированы плотные контакты. Каждый нейробласт контактирует с 4–6 нейробластами. Ядерно-цитоплазматическое отношение – 0,25, информационные показатели: энтропии (H) – 0,5688 бит, избыточность (R) – 30,52%. Это стадия индифферентного нейробласта, вступающего в стадию роста (рис. 5).
Расположенные на периферии ганглиев нейробласты имеют короткие и широкие в основании конусы роста. Это униполярные нейробласты уже в стадии роста. У них нет плотных контактов с остальными нейробластами, тем самым, они обособляются от общей структуры ганглия. Ядра в растущих нейробластах принимают форму вытянутого овала и смещаются в самую вершину перикариона. Ядерно-цитоплазматические отношения в них становятся равными 0,6, информационные показатели ядра: энтропия (H) – 0,2792 бит, избыточность (R) – 5,36%. Информационные показатели нейроплазмы: энтропия (H) – 0,1680 бит, избыточность (R) – 35,96%. Эти данные свидетельствуют о том, что униполярные нейробласты вступили в стадию специфической дифференцировки. В нее последовательно вступают и другие нейробласты локальных ганглиев. Их перикарионы и ядра принимают округлую форму, интенсивность импрегнации становится слабее, а структура апикальных нейритов усложняется. В них идентифицируются нейрофибриллы, и они сопровождаются нейролеммоцитами. Более того, наблюдается слияние нейробластов, нередко среди них определялись дикарионы с характерными перехватами 8-образного профиля. Ядерно-цитоплазматическое отношение в таких нейробластах изменяется и становится равным 0,45.
Соотношение числа нейробластов к числу отходящих от ганглиев отростков находится в пределах от 15:1 до 25:1. Это означает, что лишь незначительная часть нейробластов локальных ганглиев приобретает статус дифференцированных униполярных нейроцитов. В глубине же ганглиев между нейробластами сохраняются плотные контакты, которые объединяют их единый синцитиальный кластер.
Значительное число нейробластов и малодифференцированных нейроцитов обнаружено в пучках нервных волокон: межузловых тяжей и внутриорганных нервов, в подслизистой основе тонкой и толстой кишки лиц I зрелого возраста. Они располагаются небольшими группами, включающими от 2 до 4–6 нейробластов и от 3 до 16 малодифференцированных нейроци-тов. Это эктопированные нервные элементы, поскольку они идентифицированы на путях естественной миграции пронейробластов. Нейробласты прилежат непосредственно к одной из сторон нервного пучка, имеющего в своем составе несколько тонких миелиновых волокон, или находятся непосредственно в его толще. Лишь несколько глиоцитов расположены вблизи от нейробластов, но контакт между ними отсутствует (рис. 6).
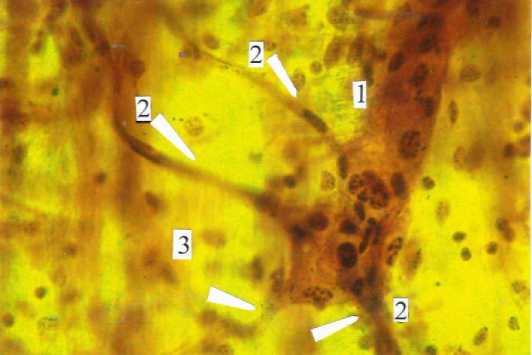
Рисунок 5. Локальный ганглий с компактным расположением нейробластов (1) в подслизистой основе (3) тонкой кишки женщины I зрелого возраста. 2↑) нейриты. Универсальный метод импрегнации. Ув. 200
Figure 5. Local ganglion with a compact arrangement of neuroblasts (1) in the submucosa (3) of the small intestine of a mature woman. 2↑) neurites. Universal impregnation method. Mag. 200
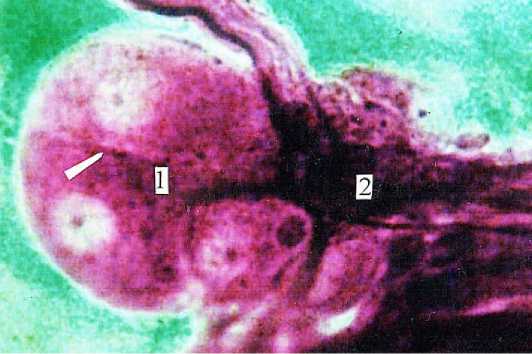
Рисунок 6. Эктопированные нейробласты (2↑) в составе нервного пучка (2) в подслизистой основе тонкой кишки женщины I зрелого возраста. Универсальный методы импрегнации. Ув. 600
Figure 6. Ectopic neuroblasts (2↑) within the nerve bundle (2) in the submucosa of the small intestine of a mature woman. Universal impregnation method. Mag. 600
Нейробласты имеют крупные, интенсивно импрегнированные, овальной формы ядра с одним, смещенным к периферии ядрышком. Вокруг ядрышка – «шапочка» перинуклеарного хроматина, а вокруг ядра – тонкий ободок нейроплазмы. Ядерно-цитоплазматическое отношение – 0,45, информационные показатели: энтропии (H) – 0,5975 бит, избыточности (R) – 12,01%. Столь высокие информационные показатели энтропии и достаточно низкие – информационной избыточности характерны для стадии индифферентного нейробласта. При этом, процент избыточной информации в ядре (R = 21,15%) в 5 раз превышает процент избыточной информации (R=4,23%) в нейроплазме. В то же время, информационные показатели энтропии в ядре (H=0,1914 бит) в 1,96 раза ниже информационного показателя энтропии (H=0,3752 бит) в нейроплазме.
Нейробласты практически «замурованы» в нервных пучках: они не имеют прямого контакта с кровеносными микрососудами и, вероятно, источником их питания является периневральная жидкость. В связи с этим, нейробласты устойчивы к гипоксии, они не участвуют в проведении нервных импульсов, поскольку у них отсутствуют нейрофибриллы, дендриты и нейрит. Более крупные скопления нейробластов обнаружены в участках разветвлений внутриор-ганных пучков кишечных нервов. Здесь, нейробласты, располагаясь по обеим сторонам нервных пучков, образуют изолированные от окружающей ткани, локальные нервные ганглии. Они не входят в состав подслизистого сплетения, поскольку не имеют отростков, вступающих в состав межузловых тяжей, и не входят в состав пучков нервных волокон кишечных нервов. Нейробласты не имеют глиальной защиты, а контактируют только с нейролеммоцитами миелиновых нервных волокон (рис. 7). Они по морфологическим признакам значительно отличаются от индифферентных нейробластов: у них небольшое светлое ядро, светлое ядрышко и отсутствуют нейрофибриллы и отростки. Перикарионы плотно прилегают друг к другу, между ними нет ни тел, ни отростков глиоцитов. Ядер-но-цитоплазматическое отношение низкое – 0,28. Информационные показатели: энтропии (H) – 0,5539 бит, избыточности (R) – 36,05%.
Эти показатели, в сочетании со значительным увеличением объема перикариона и резким снижением ядерно-цитоплазматического отношения характерны для нейробластов в стадии роста.
Происходит переход синтетических процессов в нейробласте от ядерного типа к нейропла-стическому. Избыточная информация в ядре (R=5,31%) становится в 6,2 раза меньше избыточной информации в нейроплазме (R=32,96%). Нейробласты в стадии роста – это соматохром-ные, а индифферентные нейробласты – это цитохромные нейробласты.
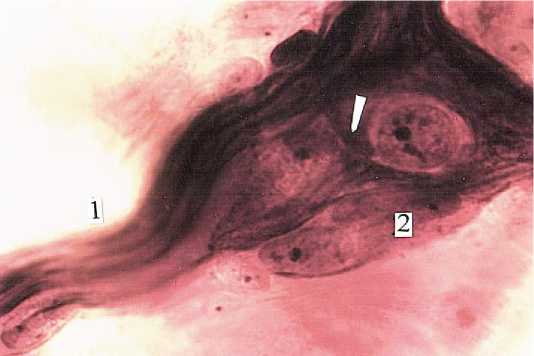
Рисунок 7. Эктопированные нейробласты (1↑) в составе нервного пучка кишечного нерва (2). Подслизистая основа тонкой кишки у мужчины I зрелого возраста. Универсальный метод импрегнации. Ув. 900
Figure 7. Ectopic neuroblasts (1↑) within the enteric nerve bundle (2). Submucosa of the small intestine in a mature man. Universal impregnation method. Mag. 900
ЗАКЛЮЧЕНИЕ
Полученные в работе данные позволяют считать, что:
-
1) универсальный метод импрегнации и ци-то- и кариометрия нейробластов позволяют идентифицировать их на различных стадиях
дифференцировки и включать в общую популяцию нейроцитов как нейробластический резерв;
-
2) дифференцировка нейробластов продолжается в постнатальном периоде человека, в результате формируется чрезмерно избыточная и чрезвычайно гетерогенная популяция нейроцитов;
-
3) митозы и амитозы нейробластов и нейро-цитов в популяции нервных клеток ЭНС новорожденных и людей I зрелого возраста отсутствуют. Двуядерные нейроциты (дикарионы) образуются в результате слияния двух нейроци-тов, связанных межнейронной цитоплазматической комиссурой (рис. 8).
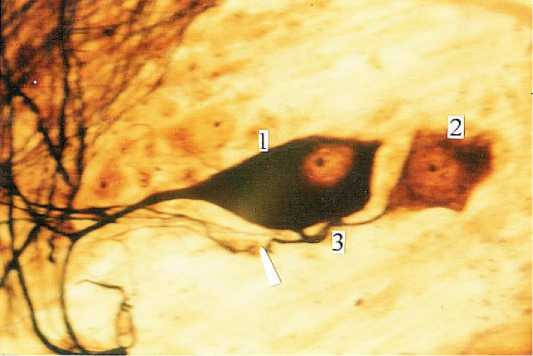
Рисунок 8. Межнейронный комиссуральный анастомоз (3) в межмышечном нервном сплетении тонкой кишки мужчины I зрелого возраста. 1) псевдо-униполярный нейроцит; 2) униполярный нейробласт. Универсальный метод импрегнации. Ув. 600 Figure 8. Interneuronal commissural anastomosis (3) in the intermuscular plexus of the small intestine in a mature man. 1) pseudo-unipolar neurocyte; 2) unipolar neuroblast. Universal impregnation method. Mag. 600


