Нейрохимические механизмы действия производного аденина
Автор: Мохаммад Амин Н.А., Авилова Т.М.
Журнал: Волгоградский научно-медицинский журнал @bulletin-volgmed
Статья в выпуске: 2 (66), 2020 года.
Бесплатный доступ
Проведено изучение нейрохимических механизмов антидепрессивного действия производного аденина VMA-99-82 с использованием метода высокоэффективной жидкостной хроматографии с электрохимической детекцией. Антидепрессивная активность производного аденина вероятно обусловлена активирующим влиянием на норадренергическую и серотонинергическую системы мозга.
Антидепрессивная активность, производные аденина, нейрохимические механизмы, моноамины, крысы
Короткий адрес: https://sciup.org/142225954
IDR: 142225954 | УДК: 615.214.32:616.895.4
Neurochemical of the mechanism of action of the adenine derivative
The neurochemical mechanisms of the antidepressant action of the adenine derivative VMA-99-82 was studied using the method of high-yield liquid chromatography with electrochemical detection. Antidepressant action of adenine derivative is possible caused of promoting effect on the noradrenergic and serotonergic systems of brain.
Текст научной статьи Нейрохимические механизмы действия производного аденина
За последнее десятилетие значительно возрос интерес к проблеме депрессивных расстройств, что обусловлено их высокой распространенностью в обществе [1]. У 7–12 % мужчин и 25 % женщин встречается не менее одного клинического депрессиовного эпизода на протяжении всей жизни. Повторные случаи встречаются в 60 % случаев, высокий риск их возникновения коррелирует с терапевтическим эффектом от лечения предыдущего эпизода депрессии [2].
Современные психические расстройства имеют тенденцию к изменению, усложнению, полиморфизму и сочетаемости. При практическом выборе антидепрессантов ориентируются на длительность пребывания пациентов в стационаре из-за необходимости подбора наиболее эффективного и безопасного лекарственного средства. Согласно литературным источникам [3] при применении антидепрессантов определяется высокая частота неблагоприятных побочных реакций (17 %). Выявленные особенности вынуждают искать новые пути терапии, определяют необходимость сочетания психотерапии и фармакотерапии, применения препаратов, сочетающих в себе различные эффекты и имеющих минимум побочных действий [4].
ЦЕЛЬ РАБОТЫ
Изучить нейрохимические механизмы действия нового производного аденина VMA-99-82, совместно с теоретическим обоснованием применения данного соединения для коррекции депрессивных расстройств.
МЕТОДИКА ИССЛЕДОВАНИЯ
Экспериментальное исследование было выполнено на линии крыс Wistar обоего пола массой 190–250 г. Все животные содержались в стандартных условиях вивария с естественным световым режимом на полнорационной сбалансированной диете. В настоящем исследовании было изучено соединение 9-[2-(4-изопропилфенокси)-этил]аденина (лаб. шифр VMA-99-82), синтезированное д. хим. наук проф. А. А. Озеровым (ФГБОУ ВО ВолГМУ Минздрава России). Проводилось изучение нейрохимических механизмов антидепрессивного эффекта VMA – 99-82.
Изучаемое соединение вводилось животным внутрибрюшинно. В качестве препаратов сравнения использовались антидепрессанты: циталопрам (Cipramil, «H. Lundbeck, Дания) в дозе 10 мг/кг, мапротилин (Ludiomil, «Ciba-Geigy», Швейцария) в дозе 10 мг/кг.
Из мозга крыс определяли прилежащее ядро, стриатум и фронтальная кора.
В работе использовали стандарты («Sigma», США): норадреналина (НА), дофамина (ДА), серотонина (5-ОТ), дигидроксифенилуксусной кислоты (ДОФУК), 5-оксииндолуксусной кислоты (5-ОИУК). Количественное определение проводили на жидкостном хроматографе с флуоресцентным детектором RF 10-Axl («Shimadzu», Япония), на колонке Supelcosil LC-18.
Мобильная фаза содержала 95 % буферной системы (однозамещенный фосфат калия 50мМ, рН 3.0) и 5 % ацетонитрила для ВЭЖХ (УФ 210 нм) (Россия).
Хроматографирование проводили на скорости потока 1 мл/мин, при температуре 30° по Цельсию. В качестве анализатора использовали 20 % гомогенаты структур головного мозга в 0,1 н HCIO4, получаемые в гомогенизаторе Crusher (Германия).
Статистическую обработку полученных данных проводили с использованием критерия Фишера [5, 6].
Содержание моноаминов и их метаболитов в тканях мозга определялось методом вы- сокоэффективной жидкостной хроматографии с электрохимической детекцией [6].
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯИ ИХ ОБСУЖДЕНИЕ
При изучении нейрохимических изменений, выявленных при некоторых патологических состояниях, нами было определено, что состояние стресс-индуцированной депрессии сопровождалось незначительным снижением метаболизма серотонина и норадреналина в прилежащем ядре и стриатуме [7].
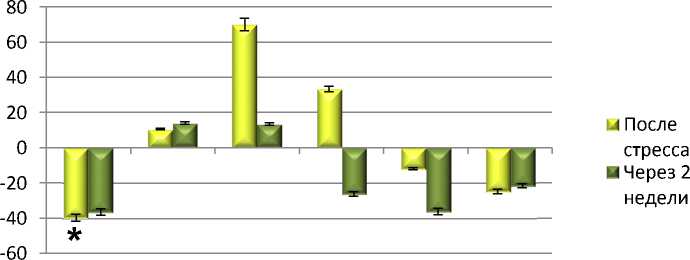
Полученные данные подтвердили ранее выявленные изменения и позволили определить нейрохимическую «мишень» для коррекции депрессивноподобных изменений поведения животных (рис. 1, 2).
Стриатум
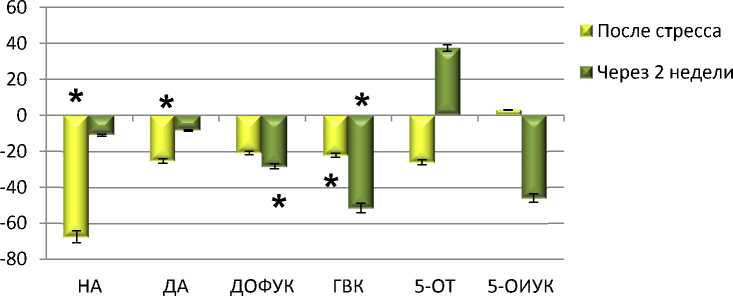
Рис. 1. Содержание моноаминов и их метаболитов в структурах мозга крыс при экспериментальной депрессии по сравнению с контролем: по оси ординат: ∆ % по отношению к контролю;
* – достоверные различия с контрольной группой интактных животных (р < 0,05)
I После стресса и Через 2 недели
I После стресса и Через 2 недели
Гиппоталамус
НА ДА ДОФУК ГВК 5-ОТ 5-ОИУК
Рис. 2. Содержание моноаминов и их метаболитов в структурах мозга крыс при экспериментальной депрессии по сравнению с контролем:
по оси ординат: ∆ % по отношению к контролю;
* – достоверные различия с контрольной группой интактных животных (р < 0,05)
Кроме того, были изучены нейрохимические механизмы антидепрессивной активности исследуемого соединения в сочетании с препаратами сравнения.
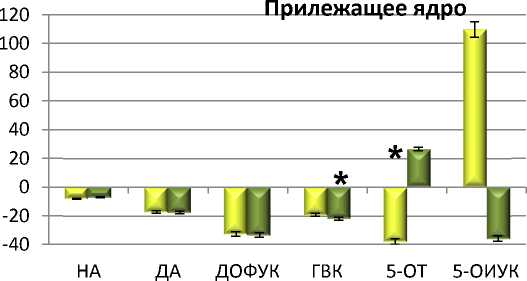
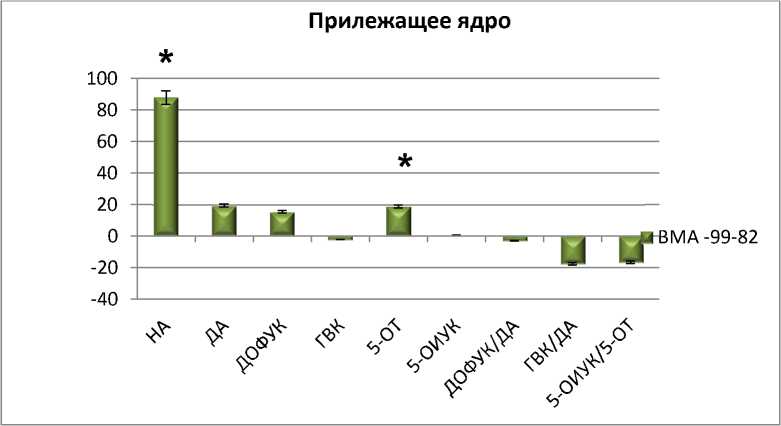
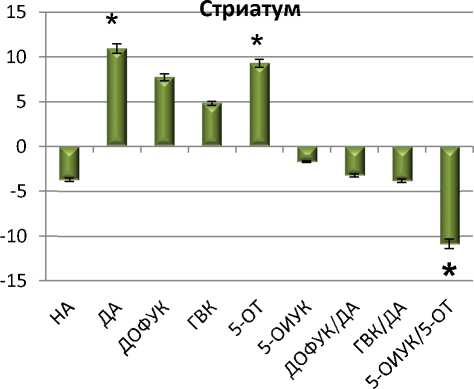
Производное аденина VMA-99-82 (10 мг/кг) оказывало влияние как на серотонинергическую систему так и на содержание НА. При одно- кратном введении наблюдалось достоверное увеличение 5-ОТ и НА в прилежащем ядре. Под действием VMA-99-82 уменьшалось соотношение 5-ОИУК/5-ОТ в гипоталамусе и стриатуме, что свидетельствует об усилении метаболизма серотонина и косвенно об усилении синтеза 5-ОТ (рис. 3).
м ВМА -99-82
Рис. 3. Влияние соединения VMA-99-82 10 мг/кг на содержание моноаминов и их метаболитов в структурах мозга по сравнению с контролем: по оси ординат: ∆ % по отношению к контролю;
* – достоверные различия с контрольной группой (физ. р-р) (р < 0,05)
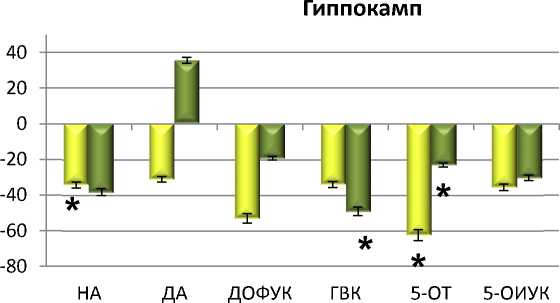
При двухнедельном введении препарата сравнения циталопрама (10 мг/кг) нарастало содержание серотонина и его метаболита 5-ОИУК в гиппокампе. Введение препарата сравнения мапротилина приводило к достоверному повышению содержания норадреналина в гиппокампе и во фронтальной коре.
Таким образом, данные наших экспериментов подтвердили особенности нейрохимического профиля известных антидепрессантов.
При двухнедельном введении VMA-99-82 (10 мг/кг) достоверно увеличивалось содержание, НА и ДОФУК в прилежащем ядре НА и
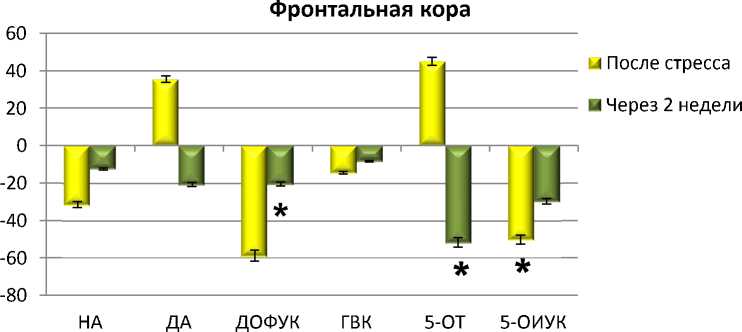
ДОФУК, ГВК и НА во фронтальной коре. Наблюдалось увеличение 5-ОТ и ДА в прилежащем ядре. Увеличение содержания дофамина в стриатуме и прилежащем ядре отмечалось после введения циталопрама, что можно расценивать как возможность межмедиаторных взаимодействий при действии антидепрессантов. В итоге соединение VMA-99-82, предположительно, оказывает модулирующее влияние на серотонин – и норадренергические системы мозга (рис. 4, 5).
Выявленные нейрохимические изменения коррелировали с антидепрессивной активностью в тестах «выученной беспомощности».
^Фронтальная кора
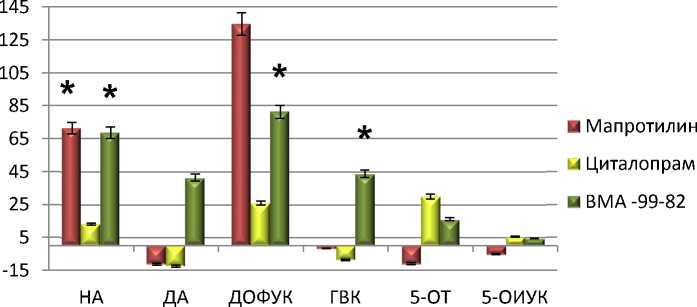
Рис. 4. Содержание моноаминов и их метаболитов в ткани мозга крыс при хроническом (14 дней) введении соединений VМА-99-82 (10 мг/кг), мапротилина (10 мг/кг) и циталопрама (10 мг/кг):
по оси ординат: ∆ % по отношеию к контролю; * – достоверные различия с контрольной группой (физ. р-р) (р < 0,05)
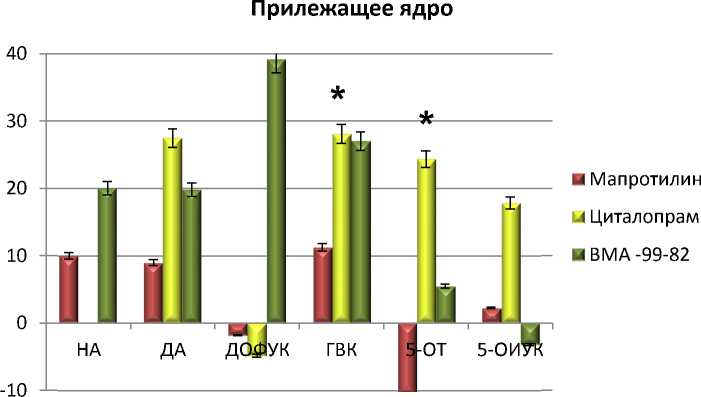
Рис. 5. Содержание моноаминов и их метаболитов в ткани мозга крыс при хроническом (14 дней) введении соединений VМА-99-82 (10 мг/кг), мапротилина (10 мг/кг) и циталопрама (10 мг/кг):
по оси ординат: ∆ % по отношеию к контролю; * – достоверные различия с контрольной группой (физ. р-р) (р < 0,05)
На сегодняшний день, в практической медицине, среди критериев эффективности анти-депрессивных средств, также выделяют их влияние на моноаминергическую систему мозга [9]. Помимо этого, модуляция активности этих систем, начиная от стимуляторов метаболического типа и заканчивая рецепторными модуляторами, может дать не меньший, а, вполне возможно, и больший фармакологический эффект [8]. С нашей точки зрения, перспективным в этом направлении является изучение механизмов модуляции активности моноаминерги-ческой и серотонинергической, передачи в мозге, препаратами – производными аденина.
ЗАКЛЮЧЕНИЕ
Антидепрессивная активность VMA-99-82 вероятно обусловлена его активирующим влиянием на серотонинергическую и норадренергическую системы мозга.
Список литературы Нейрохимические механизмы действия производного аденина
- Арушанян, Э. Б. Стриатные дофаминергические механизмы и специфическая активность антидепрессантов / Э. Б. Арушанян, Е. В. Щетинин // Экспериментальная и клиническая фармакология. - 2014. - Т. 57, № 3. - С. 60-64.
- Влияние противопаркинсонического препарата гимантана на содержание и метаболизм нейро-медиаторных моноаминов в структурах головного мозга мышей линии C57BL/6 / Г. И. Ковалев [и др.] // Экспериментальная и клиническая фармакология. - 2009. - № 1. - С. 64-67.
- Гпани, С. Медико-биологическая статистика [пер. с англ.] / С. Гланц. - М.: Практика, 1998. - 459 с.
- Григорьян, Г. А. Стресс-реактивность и стресс-устойчивость в патогенезе депрессивных расстройств: роль эпигенетических механизмов / Г. А. Григорьян, Н. В. Гуляева // Журнал высшей нервной деятельности. - 2015. - Т. 65, № 1. - С. 1-14.
- Клиническая фармакогенетика антидепрессантов / М. Ю. Герасимчук [и др.] // Клиническая фармакология. - 2013. - № 2. - С. 15-20.
- Пакриев, С. Г. Экспресс-диагностика депрессий / С. Г. Пакриев, Ю. В. Ковалев // Медицинская психология в России: электрон. науч. журн. - 2011. - № 3.
- Смупевич, А. Б. Депрессии при психических и соматических заболеваниях / А. Б. Смулевич. -М.: Медицинское информационное агентство, 2015. - 640 с.
- Узбеков, М. Г. О состоянии моноаминергического и гормонального обменов у больных тревожной депрессией и антиглюкокортикоидная терапия депрессий / М. Г. Узбеков, Н. М. Максимова // Междисциплинарные подходы к изучению психического здоровья человека и общества: матер. науч.-практич. конф. - 2019. - С. 237-243.
- Фармакотерапия депрессии с позиции персонализированной медицины / Н. А. Псарева [и др.] // Клиническая фармакология и терапия. - 2015. -Т. 24, № 3. - С. 62-65.


