Нейтронная терапия в лечении радиорезистентных злокачественных новообразований
Автор: Мусабаева Людмила Ивановна, Чойнзонов Евгений Лхамацыренович, Грибова Ольга Вячеславовна, Старцева Жанна Александровна, Великая Виктория Валерьевна, Лисин Валерий Андреевич
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Опыт работы онкологических учреждений
Статья в выпуске: 3 (75), 2016 года.
Бесплатный доступ
Представлены результаты комплексного и комбинированного лечения с применением быстрых нейтронов у больных с резистентными формами злокачественных новообразований различных локализаций. Оценка эффективности нейтронной терапии на циклотроне У-120 проведена по критериям резорбции опухоли, продолжительности безрецидивного периода и пятилетней выживаемости. При применении нейтронной и нейтронно-фотонной терапии как при комбинированном лечении, так в виде самостоятельного метода лучевого лечения показана ее большая эффективность по сравнению с фотонной терапией. Разработана комплексная программа по предупреждению и лечению острых лучевых повреждений, возникающих при нейтронной и нейтронно-фотонной терапии.
Нейтронная терапия, рецидив рака молочной железы, злокачественные новообразования головы и шеи, лучевые реакции
Короткий адрес: https://sciup.org/14056688
IDR: 14056688 | УДК: 616-006.04-08:615.849.12 | DOI: 10.21294/1814-4861-2016-15-3-67-71
Neutron therapy in the treatment of radioresistant malignant tumors
The results of the combined modality treatment including neutron therapy for patients with resistant malignant tumors were presented. Efficacy of neutron therapy was assessed using disease-free and 5-year survival rates. Neutron therapy used alone or as a combination therapy was shown to be more effective than photon therapy. A comprehensive program for the prevention and treatment of acute radiation-induced damages was devised.
Текст научной статьи Нейтронная терапия в лечении радиорезистентных злокачественных новообразований
Проблема преодоления радиорезистентности в лечении онкологических больных занимает умы ведущих ученых не один десяток лет. Создание в первой половине прошлого столетия первого циклотрона положило начало эпохе развития совершенно иного направления в радиационной онкологии – нейтронной терапии [12, 15]. Быстрые нейтроны относятся к плотноионизирующим видам радиации. Экспериментальные исследования выявили значимые преимущества нейтронной терапии перед стандартным облучением: сравнительно более высокое значение линейной передачи энергии (ЛПЭ); меньшая зависимость от кислородного эффекта; более выраженное подавление репарационных способностей облученных опухолевых клеток; нивелировка различий в радиочувствительности отдельных стадий клеточного цикла.
При оценке эффективности нейтронной терапии в клинической практике доказано преимущество применения данного вида ионизирующего излучения при различных видах сарком, раке молочной железы (РМЖ), щитовидной железы (РЩЖ), опухолях головы и шеи и др. [6, 8, 12, 14]. В Томске работы по созданию медико-биологического комплекса на базе циклотронной лаборатории Томского политехнического университета велись с 1980 по 1983 г. Становление нейтронной терапии на первом этапе включало создание терапевтического канала быстрых нейтронов средней энергии 6,3 МэВ, проведение дозиметрических и радиобиологических исследований, пробных клинических испытаний. Тогда же впервые в России на циклотроне У-120 сотрудники Томского НИИ онкологии начали проводить терапию быстрыми нейтронами больным со злокачественными новообразованиями (ЗНО). К настоящему времени накоплен значительный опыт лечения опухолей различных локализаций и морфологического генеза.
Материал и методы
Терапевтический пучок нейтронов со сплошным энергетическим спектром был получен на циклотроне У-120 при бомбардировке бериллиевой мишени дейтронами с энергией 13,5 МэВ. При этом средняя энергия нейтронов составила 6,3 МэВ. Облучение проводили горизонтальным фиксированным пучком при силе тока в пучке 30 мкА, мощности дозы – 0,15 Гр/мин, на расстоянии от мишени 110 см. Вклад гамма-излучения в суммарную поглощенную дозу на входе в облучаемую ткань составляет ~10 %. На предкли-ническом этапе были изучены дозиметрические характеристики полученного терапевтического пучка нейтронов [9]. Уменьшение поглощенной
дозы по оси терапевтического пучка нейтронов в водном фантоме на 50 % для поля 6x8 см 2 происходит на глубине 6 см, для поля 10×10 см2 – на глубине 7 см. Найдены зависимости относительной биологической эффективности (ОБЭ) нейтронов терапевтического пучка от дозы. Впервые для нейтронной терапии разработана модель время – доза – фракционирование (ВДФ) [4], принципы которой к тому времени уже были широко применены в фотонной терапии. На основе данных, полученных при изучении закономерностей распределения дозы нейтронов в тканеэквивалентной среде, зависимости ОБЭ нейтронов от дозы и модели ВДФ, была создана компьютерная программа, с помощью которой осуществлялось дозиметрическое и радиобиологическое планирование нейтронной и нейтронно-фотонной терапии [11, 13].
Расчет курсовой дозы, исключающей высокую частоту появления выраженных лучевых реакций, проводился по модели ВДФ для двух режимов нейтронной терапии:
I режим: РОД 1,2–1,4 Гр (ОБЭ 3,2–3,1), ФЭД 3,8-4,3 Гр, СОД 40-60 изоГр за курс, длительность – 4–6 нед;
II режим: РОД 1,8–2,4 Гр (ОБЭ 2,8–2,6), ФЭД 5–6,2 Гр, СОД 38–40 изоГр, длительность – 8–12 дней.
В статье представлены результаты лечения больных с 1998 по 2008 г. В исследование включены 165 больных ЗНО головы и шеи (из них 46 пациентов с ЗНО верхнечелюстной пазухи и полости носа, 74 больных с ЗНО слюнных желез, 45 больных с раком щитовидной железы), 116 больных с местными рецидивами РМЖ T2-4N0-2M0, которым в план комплексного, комбинированного и лучевого лечения были включены быстрые нейтроны.
Результаты
Злокачественные новообразования головы и шеи (n=165)
Комбинированное лечение с предоперационной нейтронной терапией получили 46 пациентов с ЗНО верхнечелюстной пазухи и полости носа. Показатели 5-летней общей выживаемости составили 62 ± 9,6 %, безрецидивной – 68 ± 8,2 %, в контрольной группе – 42 ± 9,2 % и 40 ± 9,2 % соответственно. У 39,4 % наблюдались поздние лучевые изменения кожи в виде атрофического дерматита, телеангиоэктазии и фиброза подкожной клетчатки. В группе больных, получивших нейтронную терапию, десятилетний срок наблюдения пережили 11 больных. В контрольной группе ни один больной не пережил десятилетний срок [14].
Показатели 5-летней общей выживаемости у больных раком слюнных желез, получивших комбинированное лечение с послеоперационным курсом нейтронной терапии, составили 64,5 ± 9,1 %, безрецидивной – 72,4 ± 9,8 %. В контрольной группе такие же показатели составили 25,6 ± 19,1 и 42,4 ± 18,6% соответственно. Общая 5-летняя выживаемость пациентов, получивших радикальный курс нейтронной терапии, составила 60,6 ± 13,6 %, в контрольной группе пятилетний рубеж не пережил ни одни пациент. Качество жизни больных после комбинированного и радикального лечения быстрыми нейтронами вполне удовлетворительное [12].
Было изучено влияние нейтронной терапии на функциональную активность ферментов слюны (альфа-амилазы, калликреина и калликреиноге-на) у 30 больных с опухолями головы и шеи для контроля развития тяжелых лучевых реакций со стороны слюнных желез и предупреждения ксеростомии в отдаленный период. Полученные показатели использовали в качестве критерия переносимости курса облучения и толерантности нормальных тканей. Значительные изменения ферментативной активности слюны отмечены при использовании быстрых нейтронов по сравнению с гамма-терапией, что послужило основанием для разработки методики смешанной нейтроннофотонной терапии [5].
Проведен сравнительный анализ эффективности комбинированного и лучевого лечения рака щитовидной железы с применением быстрых нейтронов у 34 больных, нейтронно-фотонная терапия ЗНО щитовидной железы по радикальной программе у 11 больных. Лечение получали пациенты с неблагоприятными факторами прогноза (медуллярный и анапластический РЩЖ). Общая 5-летняя выживаемость больных с анапластическим РЩЖ составила 32,8 ± 15,1 %, больных с медуллярным раком щитовидной железы – 63,4 ± 7,8 % [7, 12].
Нейтронная и смешанная нейтронно-фотонная терапия рецидивов РМЖ (n=116)
В исследование было включено 116 больных с местными рецидивами РМЖ T2-4N0-2M 0 , получавших комплексное лечение. Первая группа (n=71) – после нейтронной или смешанной нейтронно-фотонной терапии при этом 63 (89 %) имели первичный, 8 (11 %) больных – повторный рецидив после ранее проведенной электронной терапии (ЭТ) по радикальному курсу. В 8 (11 %) случаях местный рецидив РМЖ был диагностирован в течение первых двух лет после комбинированного лечения первичной опухоли с предоперационной дистанционной гамматерапией (ДГТ) крупными фракциями на область молочной железы.
В зависимости от распространенности местного рецидива РМЖ: множественные опухолевые образования от 0,5 до 4,5 см в области послеоперационного рубца, на коже грудной клетки или в мягких тканях, площадь облучения быстрыми нейтронами составляла от 96 до 248 см2. Разовая очаговая доза (РОД) быстрых нейтронов на местный рецидив составляла 1,6–2,0 Гр (ОБЭ 2,91–2,79), на кожу – 2,0-2,2 Гр (ОБЭ 2,79-2,73). Проводилось 3-5 сеансов нейтронной терапии.
Из-за горизонтального направления пучка быстрых нейтронов при лечении местнораспространенных рецидивов РМЖ имеется опасность повреждения прилежащей легочной ткани. Обязательным являлся расчет дозы на легкое в зоне облучения быстрыми нейтронами с учетом его гетерогенности (рис. 1). При РОД 1,6–1,76 Гр входная разовая доза быстрых нейтронов в легком на глубине 4 см от поверхности передней грудной стенки (по данным КТ ОГК при планировании) составляла 1,4–1,54 Гр. Суммарная фотонэквива-лентная доза (ФЭД) быстрых нейтронов в легочной ткани (с учетом ее гетерогенности) составила 16,5–27 Гр, что находится в пределах толерантной дозы (30–40 Гр) для одного легкого. Однако при проведении смешанного облучения, когда к нейтронной терапии дополнительно применяется гамма-терапия, лучевая нагрузка на легкое увеличивается, и у больных в некоторых случаях наблюдается лучевой пневмофиброз [3].
По разработанному способу лечения нейтронную терапию в дозе 30–40 изоГр получили 19 больных с местными рецидивами РМЖ, нейтронно-фотонную терапию в дозе 60 изоГр – 52 пациентки [3]. В контрольной группе (n=45) проведен радикальный курс электронной терапии: РОД 3,0 Гр, суммарная доза – 48 Гр (60 изоГр). Сравниваемые группы были сопоставимы по числу курсов (4–6) и схемам проводимой химиотерапии (CMF или CAF/FAC). Медиана наблюдения – 58 ± 5,5 мес.
Общая переносимость нейтронной терапии больными с местными рецидивами РМЖ была вполне удовлетворительной. С профилактической целью и для купирования острых лучевых реакций назначалась лазерная терапия на парах меди, гель «Тизоль» и магнитолазерная терапия. Впервые при нейтронной терапии была показана возможность не только эффективного лечения, но и предупреждения радиационных повреждений кожи излучением лазера на парах меди. За 6-летний период наблюдения выживаемость больных без повторных рецидивов в зоне облучения местного рецидива быстрыми нейтронами в основной группе составила 92,2 ± 5,7 %, в контрольной группе (ЭТ) – 51,5 ± 9,1 % (p=0,0001) [2].
В сроки наблюдения от одного до трех лет после нейтронной и нейтронно-фотонной терапии на полях облучения у 16 (23 %) больных наблюдались поздние лучевые повреждения кожи и подкожной клетчатки. Из них у 7 (10 %) – очаговая атрофия кожи и телеангиоэктазии, у 5 (7 %) – выраженный фиброз кожи, у 4 (6 %) пациенток – лучевая язва. Причинами лучевых повреждений явились: выраженная атрофия кожи после радикальной мастэктомии; у отдельных больных вклад быстрых нейтронов составлял свыше 56 % в курсовую дозу смешанного облучения. Совместно с кафедрой
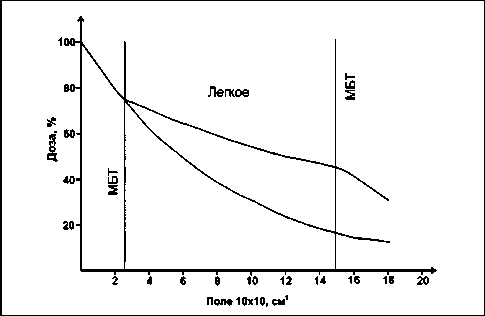
Рис. 1. Распределение поглощенной дозы быстрых нейтронов 6,3 МэВ (верхняя кривая с учетом гетерогенности легочной ткани, МБТ – мягкая биологическая ткань)
прикладной физики Томского политехнического университета была разработана программа лечения лучевых язв кожи с применением озоновых технологий. Клиническая апробация применения озонотерапии у больных с лучевыми язвами показала безвредность разработанного метода и хороший эффект [1, 10]. Проведенные исследования продемонстрировали, что применение быстрых нейтронов 6,3 МэВ у больных с местными рецидивами РМЖ обладает выраженным эффектом, что позволило увеличить продолжительность жизни больным.
Таким образом, проведенные клинические исследования показали возможность применения лучевой терапии быстрыми нейтронами по разработанным режимам и в сочетании с фотонной терапией у больных с различными локализациями злокачественных новообразований. Эффективность предоперационного курса нейтронного облучения подтверждается выраженными признаками лучевого патоморфоза опухолевой ткани. Получены вполне удовлетворительные результаты в сравнении с контрольными группами. В наиболее сложных случаях, при местных рецидивах рака молочной железы, необходимо соблюдение точного расчета величины дозовой нагрузки на кожу грудной стенки в области рецидива, что позволит предупредить появление лучевых повреждений у больных в отдаленные сроки наблюдения. Разработаны новые методы лечения лучевых реакций и повреждений кожи с применением лазера на парах меди и озонотерапии.
Заключение
Проведенная оценка эффективности нейтронной терапии на циклотроне У-120 по критерию достигаемой резорбции опухоли, продолжительности безрецидивного периода и 5-летней выживаемости пациентов свидетельствует о ее преимуществе в сравнении с воздействием на опухоль стандартной фотонной терапии.
Список литературы Нейтронная терапия в лечении радиорезистентных злокачественных новообразований
- Великая В.В., Мусабаева Л.И., Алейник А.Н., Грибова О.В., Старцева Ж.А., Симонов К.А., Лисин В.А. Применение озонотерапии у больных при местных рецидивах рака молочной железы после нейтронной и нейтронно-фотонной терапии//Медицинская радиология и радиационная безопасность. 2015. Т. 60, № 3. С. 61-64
- Великая В.В., Мусабаева Л.И., Старцева Ж.А. Клинические модели рака молочной железы для проведения нейтронной терапии//Тюменский медицинский журнал. 2010. № 3-4. С. 39-40
- Великая В.В., Мусабаева Л.И., Старцева Ж.А, Лисин В.А. Быстрые нейтроны 6,3 МЭВ в комплексном лечении больных местными рецидивами рака молочной железы//Вопросы онкологии. 2015. Т. 61, № 4. С. 583-585
- Головков В.М., Лисин В.А., Мусабаева Л.И., Старцева Ж.А., Великая В.В. 30 лет нейтронной терапии на циклотроне U-120 Томского политехнического университета//Известия высших учебных заведений. Физика. 2013. Т. 56, № 11-3. С. 173-179
- Грибова О.В., Мусабаева Л.И., Кайгородова Е.В., Суханова Г.А., Дюкова Е.В. Влияние нейтронной и фотонной терапии на активность протеолитических ферментов слюны у больных злокачественными опухолями области головы и шеи//Сибирский онкологический журнал. 2007. № 4. С. 101-104
- Грибова О.В., Мусабаева Л.И., Чойнзонов Е.Л., Лисин В.А. Нейтронно-фотонная терапия в комбинированном и лучевом лечении больных прогностически неблагоприятным раком щитовидной железы//Медицинская физика. 2009. № 2. С. 41-46
- Грибова О.В., Мусабаева Л.И., Чойнзонов Е.Л., Мухамедов М.Р. Клиническое течение рака щитовидной железы после комбинированного лечения с применением быстрых нейтронов у больных с высоким риском рецидива//Вестник оториноларингологии. 2012. № 5. С. 91-92
- Кандакова Е.Ю., Важенин А.В., Кузнецова А.И., Важенин И.А., Паньшин Г.А., Цалланова З.С. Результаты сочетанной фотонно-нейтронной терапии в условиях эскалации дозы нейтронов в общем курсе сочетанной фотонно-нейтронной терапии//Вестник Российского научного центра рентгенорадиологии Минздрава России. 2014. № 4. С. 7
- Лисин В.А., Горбатенко А.И. Дозиметрические характеристики пучка быстрых нейтронов циклотрона У-120, применяемого для лечения онкологических больных в г. Томске//Медицинская радиология. 1986. № 5. С. 94
- Мусабаева Л.И., Великая В.В., Грибова О.В., Старцева Ж.А., Алейник А.Н. Профилактика и лечение лучевых поражений кожи//Онкохирургия. 2013. Т. 5, № 2. С. 76-81
- Мусабаева Л.И., Жогина Ж.А., Слонимская Е.М., Лисин В.А. Современные методы лучевой терапии рака молочной железы. Томск, 2003. 199 с
- Мусабаева Л.И., Лисин В.А., Жогина Ж.А., Великая В.В. Нейтронная и нейтронно-фотонная терапия в лечении местно-распространенных форм рака молочной железы и местных рецидивов//Практическая медицина. 2009. № 4 (36). С. 45-46
- Мусабаева Л.И., Лисин В.А., Старцева Ж.А., Грибова О.В., Великая В.В., Мельников А.А. Нейтронная терапия на циклотроне U-120. К 30-летию применения нейтронной терапии -обзор результатов научных исследований//Медицинская радиология и радиационная безопасность. 2013. Т. 58, № 2. С. 53-61
- Новиков В.А., Мусабаева Л.И., Кицманюк З.Д., Лисин В.А. Опухоли полости носа и околоносовых пазух (Новые технологии в лечении и реабилитации). Томск, 2002. 202 с
- Stone R.S. Neutron therapy and specific ionization//Am. J. Roent-genol. Radium. Ther. 1948. Vol. 59 (6). P. 771-785


