Некомпактность миокарда. Насколько это серьезно?
Автор: Нарциссова Галина Петровна, Прохорова Дарья Станиславовна, Курыгина Светлана Васильевна
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Врожденные пороки сердца
Статья в выпуске: 4 т.13, 2009 года.
Бесплатный доступ
Данная статья посвящена редкой патологии сердца - неуплотнению миокарда. Это генетическая кардиомиопатия, которая диагностируется с помощью эхокардиографии. Анализ выполнен на основании 52 случаев некомпактного миокарда у детей (14 случаев изолированного неуплотнения желудочков, 38 случаев сочетания некомпактного миокарда с врожденными пороками сердца). Авторы проанализировали влияние данной патологии на функцию миокарда и клиническое состояние больных. В дискуссии авторы высказывают мнение относительно того, когда это явление является заболеванием.
Некомпактность миокарда, генетическая кардиомиопатия, эхокардиографические критерии, дисфункция миокарда, сердечная недостаточность
Короткий адрес: https://sciup.org/142233517
IDR: 142233517 | УДК: 616.127-005.2-073.48
Noncompaction of the myocardium. How much is it serious?
This article is devoted a rare pathology of heart - noncompaction of the myocardium. This is genetic cardiomyopathy, which is diagnosed by an echocar-diography. The analysis is made on the basis of 52 cases of noncompaction of the myocardium in children (14 cases of isolated ventricular non-compaction, 38 cases of a combination of a noncompaction of myocardium with congenital heart diseases). The authors analysed of influence of this pathology on myocardial function and the clinical status of the patients. In discussion authors express opinion concerning when this phenomenon is disease.
Текст научной статьи Некомпактность миокарда. Насколько это серьезно?
Выполняя ультразвуковые исследования у детей с кардиальной патологией, мы обращали внимание на состояние миокарда. У ряда пациентов нами обнаружены характерные эхокардиографические признаки некомпактности миокарда одного из желудочков. Некомпактность, или неуплотнение, миокарда представляет собой редкий вид кардиомиопатии, характеризующейся присутствием многочисленных, чрезмерно выраженных трабекул и наличием глубоких межтрабекулярных перерывов, которые сообщаются с полостью левого желудочка (ЛЖ). Этот феномен диагностируется методом эхокардиографии (ЭхоКГ). Частота данной кардиальной аномалии точно не известна, по данным разных авторов, она составляет не более 0,05% у взросл ых [13].
A. Nava и его коллеги (1988) сообщают о первом описании некомпактного миокарда ЛЖ еще в 1926 г. Однако интерес к этой патологии наблюдается с конца 1980-х гг. В 1995 г. описаны ангио- и эхокардиографические характеристики как первый шаг в изучении и идентификации диагноза новой болезни . В прошлом десятилетии некомпактный миокард ЛЖ рассматривался как особая форма кардиомиопатии с отличительной основной причиной и прогнозом [1].
В 1995 году некомпактный миокард был включен в классификацию кардиомиопатий ВОЗ, отнесен к категории «неклассифицируемых кардиомиопатий». Это название – свидетельство того, что в то время не были известны этиология и патогенез забол евания. Позднее, в 2006 году, в связи с получением новых данных об этиопатогенезе заболевания, некомпактный миокард был включен в классификацию кардиомиопатий ВОЗ как генетическая кардиомиопатия.
На сегодняшний день происхождение некомпактного миокарда связывают с дисморфогенезом миокарда во внутриутробном периоде, предполагая его генетическую природу [1, 6]. В ранний эмбриональный период человеческое сердце состоит из губчатых мышечных волокон и трабекул, сообщающихся через перерывы с желудочковой полостью. На 6–8-й неделе внутриутробного развития сердца начинается процесс уплотнения миокарда, нарушение которого приводит к постоянству трабекулярности и сохранению глубоких перерывов.
Механизмы наследственной передачи при не-компактности миокарда могут варьировать. Семейные случаи составляют от 18 до 50%, по данным разл ичных авторов. Семейный скрининг поможет выявить затронутых членов семьи, что позволит провести первичную профилактику, включая антикоагуляцию и вживление кардиовертора-дефибрилля-тора [1].
Болезнь существует в двух формах: изолированная некомпактность и, реже, сочетание некомпактного миокарда с ВПС. Данная патология непредсказуема. Одни пациенты развивают прогрессирующую сердеч ную недостаточность и нуждаются в пересадке сердца, а другие – «волнообразный фенотип», при котором эхокардиографические данные кол еблются между признаками дилатационной и гипертрофической кардиомиопатии, иные пациенты – первичную д иастолическую дисфункцию. В некоторых случаях некомпакт-ность миокарда сочетается с такими системными заболеваниям, как синдром Барта, митохондриальными или метаболическими расстройствами [1, 3, 10]. Общие проявления – сердечная недостаточность (53%), желудочковая тахикардия (41%), внезапная сердечная смерть (35%), кардиоэмболические события (24%) и обморок (18%). Желудочковые аритмии являются главными и иногда фатальными осложнениями. Предсердные аритмии, синдром WPW также встречаются при этой патологии. Высокая распространенность кардиоэмболических событий, как предполагают, происходит из-за образования тромбов в пределах глубоких межтрабекулярных впадин [8]. Хотя некомпакт-ность миокарда – врожденное нарушение структуры миокарда и типично диагностируется у педиатрических пациентов, начало кл и н ич еских проявлений кардиомиопатии может быть отсрочено во взрослую жизнь. Большинство детей с изолированной некомпактностью являются бессимптомными на начальном представлении и с возрастом показывают постепенное ухудшение функции ЛЖ. В сообщениях о симптоматических детях превалируют сердечная недостаточность и аритмия. Пациенты с некомпактностью миокарда ЛЖ имеют плохой прогноз: смертность составила около 35% у взросл ых и более 22% у детей в 7летнем наблюдении. Основные причины летальности – тяжелая сердечная недостаточность и внезапная сердечная смерть [4, 5].
Так как признаки некомпактности миокарда у детей, особенно младенцев, с ВПС не редкость, нами была поставлена цель – изучить, влияет ли этот феномен некомпактности миокарда на функциональное состояние желудочков у данной категории пациентов.
МАТЕРИАЛ И МЕТОДЫ
В исследование включено 52 пациента в возрасте от 4 мес. до 18 лет. Из них с ВПС – 38 чел . (73%), с изолированной некомпактностью миокарда – 14 чел . (27%). Преобладали пациенты женского пола (57%). Среди ВПС были септальные дефекты, открытый артериальный проток, аортальные пороки, аномалия Эбштейна, мембрана левого предсердия, цианотические пороки типа единственного желудочка и другие.
Выполнялись ЭхоКГ в двух- и четырехмерном режимах, ЭКГ. Для диагностики некомпактного миокарда мы использовали основные эхокардио-гра-фические критерии, принятые на сегодняшний день [5, 7].
-
1. Критерии Jenni и др. [2001].
-
1) Двухслойная структура с тонким уплотненным (компактным) слоем и толстым неуплотненным (некомпактным) слоем. Измерения проводятся в конце систолы в парастернальном сечении по короткой оси. Некомпактность ЛЖ определяется при отношении N / C >2, где N – non-compacted layer of myocardium – некомпактный слой миокарда; C – compacted layer of myocardium – компактный слой миокарда.
-
2) Отсутствие сопутствующих сердечных структурных аномалий.
-
3) Многочисленные, чрезмерно видимые трабекулы и глубокие межтрабекулярные перерывы.
-
4) Перерывы, заполненные кровью внутри желудочка при цветном допплере.
-
2. Критерии Chin и др. [1990].
У детей отношение неуплотнения к уплотнению может быть менее 2,0.
Некомпактность миокарда, определенная при отношении X/Y ≤ 0,5, где X – расстоян ие от эпикардиальной поверхности через трабекулярные перерывы (толщина истинного плотного слоя миокарда); Y – расстояние от эпикардиальной поверхности до пика трабекулярности (толщина всей стенки миокарда).
РЕЗУЛЬТАТЫ
Следует отметить, что в норме миокард у младенцев отличается от миокарда взрослых меньшей плотностью, большей разреженностью, наличием трабекул. В большинстве случаев в школьном и подростковом возрасте отсутствуют визуальные отличия от миокарда взрослых. Поэтому мы рассматривали лишь те случаи, когда имелись характерные признаки некомпактности с учетом эхокардиографических критериев. По данным ЭКГ были выявлены признаки гипертрофии миокарда, неполная блокада правой ножки пучка Гиса, диффузные изменения миокарда, депрессия ST и отрицательный T (3), синдром WPW (1).
При стандартном эхокардиографическом исследовании нами обнаружена некомпактность миокарда ЛЖ при разл ичных ВПС. Чаще всего это были септальные дефекты – 27,7% (10 чел.), реже двустворчатый аортальный клапан (3), аортальный стеноз (1), коарктация аорты (1), ОАП (1), аномалия Эбштейна (2), мембрана левого предсердия (1), цианотические пороки типа единственного желудочка – 21% (8 чел.) и другие.
Преобладала локализация некомпактного миокарда в обл асти боковой стенки (95%), а также у верхушки ЛЖ. У большинства пациентов функциональные показатели были в пределах нормы. Однако у 7 чел. (18,4% случаев) диагностирована систолическая и диастолическая дисфункция миокарда. ФВ ЛЖ была от 25 до 52%. Отношение N/C составило от 1,5 до 2,2. ХСН II А–Б (рис. 1). После хирургической коррекции ВПС у пациентов с систол ической дисфункцией наблюдалось улучшение функции сердца.
Поскольку правый желудочек (ПЖ) отличается от левого выраженной трабекулярностью, выявление некомпактного миокарда здесь наблюдается редко. Некомпактность миокарда правого желудочка с систолической дисфункцией обнаружена нами у двух пациентов. В первом случае у пациента с диагнозом тотальный аномальный дренаж легочных вен с ДМПП, некомпактный миокард свободной стенки правого желудочка выявлен на фоне объемной перегрузки с дилатацией полости (КДР 3,9 см). При этом набл юдалось снижение фракции выброса ПЖ до 29%. После хирургической коррекции и уменьшения дилатации ФВ ПЖ повысилась до 46%. Во втором случае у пациента с диагнозом клапанный стеноз легочной артерии, некомпактность миокарда в нижнем отделе свободной стенки и у верхушки обнаружена на фоне гипертрофии миокарда правого желудочка. ФВ ПЖ составила 45%.
Особую группу представляют пациенты со сложными цианотическими пороками – 8 (21%). По нашим наблюдениям, при сложных цианотических пороках с единственным желудочком серд ца не-компактность миокарда встречается в большинстве случаев. Некомпактность присутствовала, как правило, в области верхушки и свободной стенки. При этом ФВ желудочка была в пределах 50–53%, однако у одного пациента составила 38% (рис. 2).
В одном случае 9-летней пациентке с единственным желудочком, ФВ 52%, выполнена эмиссионная сцинтиграфия миокарда с технетрилом, выявившая нарушение перфузии миокарда.
По данным литературы, некомпактность миокарда не связана с аномалиями коронарных артерий. Однако мы решили продемонстрировать один случай из практики. У ребенка в возрасте 1 г. 1 мес. с синдромом Бланда-Уайта-Гарланда (отхождение левой коронарной артерии от легочного ствола) с исходом в дилатационную кардиомиопатию наблюдалась резко выраженная дилатация и сферификация ЛЖ (КДО 156 мл, индекс сферичности 0,88), диффузный гипокинез миокарда, ФВ 25–28%, митральная регургитация II ст. После хирургической коррекции порока сохранялись дилатация ЛЖ (КДО 150–140 мл), сферификация, диффузный гипокинез, ФВ 20–25%, д иастолическая дисфункция, клинически – сердечная недостаточность II Б ст. Через 2 недели после операции на фоне незначительного уменьшения КДО, улучшения кинеза миокарда в базал ьном отд еле и увеличения ФВ до 40% обнаружены признаки неком-пактности миокарда в области боковой стенки. На ЭКГ сохранялись депрессия сегмента ST, отрицательный зубец T в V4–V6. Дисфункция миокарда (ФВ 40%) сохранялась в течение 1,5 мес. наблюдения после операции до выписки ребенка из клиники. Обычно после хирургической коррекции такого порока происходит улучшение коронарной перфузии и постепенное восстановление функции миокарда. У данного пациента, несмотря на адекватную коррекцию, сохраняются признаки выраженной дисфункции, сердечной недостаточности. Мы не можем объяснить причину тяжелой дисфункции миокарда у данного пациента и не можем пока связать ее с некомпактностью миокарда. Требуется дальнейшее наблюдение, чтобы ответить на этот вопрос.
На сегодняшний день установлена генетическая природа некомпактности миокарда и сообщается о семейных случаях этой патологии. Нами обнаружено два семейных случая некомпактного миокарда у детей с ВПС и один случай при изолированной некомпактности. У разнополых детей из двойни с двустворчатым аортальным клапаном выявлена некомпактность миокарда боковой стенки ЛЖ. В другом случае мы наблюдали двоих детей с цианотическими пороками сердца, родившихся в одной семье с разницей в возрасте 3 года. У старшей девочки был единственный желудочек сердца, транспозиция магистральных артерий, обструкция левого выводного тракта. Младший ребенок (мальчик) род ился с атрезией легочной артерии с ДМЖП, гипоплазией правого желудочка. На фоне цианотических пороков сердца у обоих детей набл юдалась некомпактность миокарда в области боковой стенки и верхушки.
В одном случае мы выявили семейный характер изолированной некомпактности миокарда. У девочки 16 лет с нарушением ритма при эхокардиографическом исследовании обнаружена неком-пактность миокарда в области боковой стенки с признаками систолической и диастолической дисфункции. У ее 40-летней матери, по данным ЭхоКГ, также обнаружен некомпактный миокард боковой стенки, клинически наблюдалась экстрасистолия.
Мы обследовали 14 детей с изолированной не-компактностью миокарда ЛЖ. Основные диагнозы у этих пациентов: дилатационная кардиомиопатия (3), нарушения ритма сердца (3), открытое овальное окно (5), пролапс митрального клапана, синдром дисплазии соединительной ткани (1). Клинические проявления наблюдались в 6 случаях (42,8%): нарушения ритма и проводимости, сердечная недостаточность, тромбообразование. ФВ колебалась от 44 до 67%. На ЭКГ наблюдались неполная блокада правой ножки пучка Гиса, нарушения ритма в виде экстрасистолии, синоатриальная блокада, синусовая тахикардия, синдром WPW. Клинические признаки сердечной недостаточности присутствовали у двух детей (14,3%).
Остановимся на этих двух случаях изолированной некомпактности миокарда, протекающей с ХСН II А–Б стадии. Пациентка В. наблюдается нами на протяжении 3 лет с 3-месячного возраста с диагнозом дилатационная кардиомиопатия, ХСН II А стадии. По данным эхокардиографии отмечается дилатация ЛЖ, митральная недостаточность II степени. За период наблюдения ФВ колебалась от 57 до 63%, сохранялись признаки легочной гипертензии, расчетное систол ическое давление в ПЖ 56 мм рт. ст. Обнаружена некомпактность миокарда в области боковой стенки с признаками гипокинеза, компенсаторный гиперкинез межжелудочковой перегородки (рис. 3, 4). На фоне медикаментозного лечения существенного улучшения не наблюдалось.
Показательна история болезни пациента Ш., 16 лет. У мальчика после переохлаждения возникла температура 39 °С, одышка, сердцебиение, отеки ног, сердечная недостаточность. После лечения выставлен диагноз подострого миокардита. ХСН II Б стадии. Наблюдалось волнообразное течение с незначительным кратковременным улучшением с последующим нарастанием симптомов сердечной недостаточности. В НИИ патологии кровообращения пациент был направлен через 4 мес. от начала заболевания. При выполнении ЭхоКГ нами обнаружена дилатация всех отделов сердца, в большей степени левых, диффузный гипо-, акинез миокарда. КДО ЛЖ 195 мл. Индекс сферичности 0,9. ФВ 21–28%. Диастолическая дисфункция ЛЖ I типа. Некомпактность миокарда верхушки, нижних отделов боковой стенки. N/C=2. У верхушки в глубоком межтрабекулярном пространстве визуализируется организованный тромб 1,0 х1,0 см, вероятны мелкие тромбы в прилежащем губчатом миокарде. Гипо-, акинез миокарда в сегментах с некомпактным миокардом и в прилежащих сегментах. Митральная и трикуспидальная регургитация III степени, умеренная (площадь струи составила 33 и 35% от площади предсердия). Пациент поставлен в лист ожидания на трансплантацию сердца (рис. 5).
Таким образом, некомпактный миокард у детей в сочетании с ВПС в 18,4% случаев сопровождался систолической и диастолической дисфункцией миокарда, снижением ФВ. После хирургической коррекции порока наблюдалось улучшение функциональных показателей, уменьшение признаков систолической дисфункции.
Изолированная некомпактность ЛЖ в наших наблюдениях протекала с клиническими проявлениями у 42,8%, сопровождалась тенденцией к снижению ФВ, нарушениями ритма, редко - признаками дилатационной кардиомиопатии, а у 14,3% - сердечной недостаточности.
ОБСУЖДЕНИЕ
Неуплотненный желудочковый миокард характеризуется чрезмерно выраженной трабекулярной сетью и глубокими межтрабекулярными перерывам, однако диагноз некомпактного миокарда может быть затруднен. При бессимптомном течении диагноз может быть установлен лишь при многократных исследованиях или не установлен вообще. Дифференциальный эхокардиографический диагноз включает видимые нормальные миокардиальные трабекулы, ложные сухожилия и отклонения при сердечных опухолях и апикал ьном тромбе. В этих случаях некомпактность миокарда подтверждают глубокие межтрабекулярные перерывы и кровоток в них, сообщающийся с желудочковой полостью при цветном допплеровском анализе. В дифференциальной диагностике следует обратить внимание на особенности визуализации миокарда у младенцев, поскольку их миокард отличается от миокарда взрослых: он имеет некомпактное строение в норме, хорошо визуализируемые нормальные 3 трабекулы [1, 12, 13].
Хотя эхокардиографические критерии некомпактного миокарда предполагают отсутствие другой кардиальной патологии, большинство авторов отмечает характерные признаки некомпакного миокарда у больных ВПС. Поэтому присутствие ВПС не исключает данного диагноза. В нашем исследовании у 38 детей с ВПС мы наблюдали характерные признаки некомпактности миокарда. Отношение неуплотнения к уплотнению у этих детей было от 1,4 до 2,0. При этом, учитывая отсутствие каких-либо нарушений функции миокарда у 81,6% больных, вероятно, можно рассматривать эту патологию как синдром некомпактности миокарда при ВПС. Так как процесс уплотнения миокарда в морфогенезе сердца начинается на 6-8-й неделе гестации, когда заканчивается формирование сердца, а, следовательно, и формирование ВПС, то можно предположить, что это звенья одной цепи. Об этом же свидетельствует присутствие некомпакт-ности миокарда у большинства пациентов с единственным желудочком. Обратив внимание на то, что сложные ВПС типа единственного желудочка, как правило, сопровождаются некомпактностью миокарда, мы можем предположить связь дисморфо-генеза миокарда с дисэмбриогенезом сердца в целом, который происходит на более ранних сроках внутриутробного развития. То, что, по нашим данным, у 18,4% пациентов с ВПС и признаками некомпактности миокарда имеются признаки дисфункции миокарда, которая уменьшается после хирургической коррекции, позволяет предположить влияние гемодинамического фактора на функцию неуплотненного миокарда. Следует отметить, что иногда затронутые некомпактностью миокардиальные сегменты гипокинетичны, наблюдается дисфункция миокарда. Причина угнетения желудочковой функции не ясна. Систолическая дисфункция - наиболее вероятно, результат относительной ишемии миокарда из-за несоответствия миокардиальной кислородной поставки и требования [4]. Мы также наблюдали нарушение перфузии миокарда с помощью сцинтиграфии у пациентки с некомпактностью миокарда единственного желудочка сердца.
По-видимому, лишь у отдельных пациентов с ВПС при наличии четких эхокардиографических критериев некомпактный миокард может быть признан кардиомиопатией, у остальных должен рассматриваться как синдром. С другой стороны, поскольку описаны отсроченные во взрослую жизнь клинические проявления некомпактности миокарда, мы не можем знать, каковы последствия не-уплотнения миокарда у больных ВПС в отдаленном периоде даже при нормальной исходной функции желудочка и адекватной хирургической коррекции. Поэтому мы считаем, что необходимо наблюдение за этими пациентами на протяжении жизни.
Что касается изолированной некомпактности, то для установления диагноза у детей необходимо учитывать все эхокардиографические критерии. Клинические проявления чаще всего связаны с нарушениями ритма и проводимости (у 42,8%), а сердечная недостаточность в нашем исследовании манифестировала у 14,3%, сопровождаясь систолической и диастолической дисфункцией миокарда. При этом пациентам часто выставляется другой диагноз, как правило, это диагноз дилатационной кардиомиопатии.
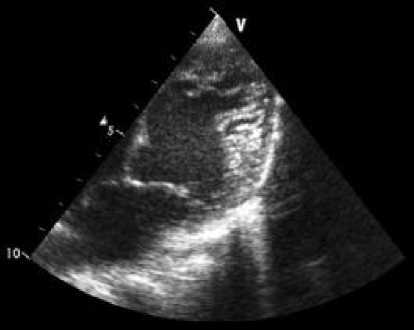
Рис. 3. Изолированная некомпактность миокарда ЛЖ. ФВ 63%. ХСН II А ст. Легочная гипертензия (пациент В., 3 лет).
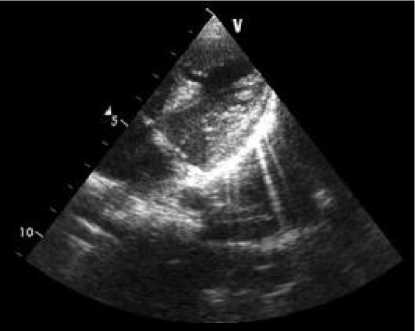
Рис. 1. ДМЖП. Некомпактность миокарда боковой стенки ЛЖ (пациент К.).
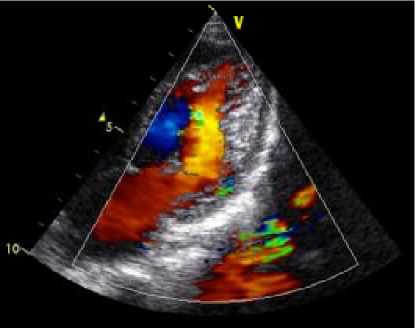
Рис. 4. Изолированная некомпактность миокарда ЛЖ. ФВ 63%. ХСН II А ст. Легочная гипертензия. Характерная картина при цветном допплеровском картировании (пациент В., 3 лет).
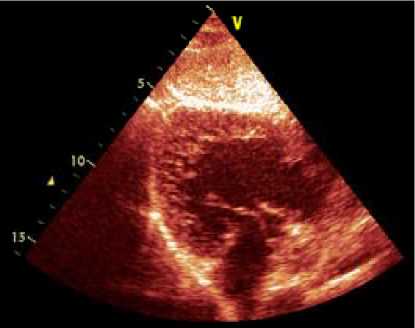
Рис. 2. Единственный желудочек сердца. Некомпак-тность миокарда в области верхушки, нижних отделов желудочка (пациент В., 10 лет).
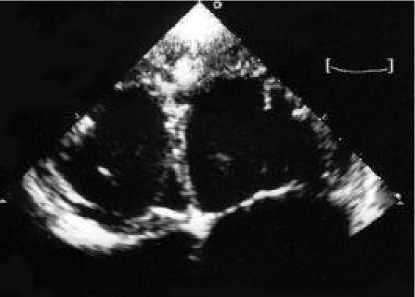
Рис. 5. Некомпактность миокарда верхушки, боковой стенки. Тромб 1,0 х 1,0 см в межтрабекулярном пространстве у верхушки (пациент Ш., 16 лет).
Кроме того, не следует забывать, что в норме миокард детей, особенно раннего возраста, отличается от миокарда взрослых меньшей плотностью. Процесс уплотнения миокарда происходит по мере роста ребенка и постепенно приобретает чер- ты «взрослого». Поэтому следует избегать гипердиагностики синдрома некомпактности миокарда у детей, для чего нужно использовать описанные выше эхокардиографические критерии.
ЗАКЛЮЧЕНИЕ
Таким образом, ЭхоКГ – основной метод для установления диагноза и определения плана наблюдения и лечения пациентов с некомпактным миокардом. Однако, несмотря на широко распространенное использование ЭхоКГ, некомпактность миокарда желудочков обычно неправильно диагностируется из-за нехватки знания этой патологии и недооценки существенного негативного воздействия на прогноз этих пациентов. Нередко болезнь диагностируется лишь после неоднократного проведения эхокардиографических исследований. Бывают случаи, когда эхокардиографист устанавл ивает наличие некомпактного миокарда при отсутствии других структурных аномалий сердца у пациентов или отмечает этот признак при ВПС, но кардиолог не придает значения данному заключению, и пациенты либо остаются без наблюдения, либо при наличии симптомов сердечной недостаточности наблюдаются с диагнозами дилатационной кардиомиопатии, кардита, аритмий. Поэтому мы попытались ознакомить эхокардиографи-стов и кардиологов с признаками и проявлениями некомпактности миокарда. Это, по нашему мнению, улучшило бы не только знание, но также и понимание данной патологии и, таким образом, облегчило бы диагностику, поскольку даже глаз квалифицированного специалиста-эхокардиографиста видит лучше, зная, что искать.
Список литературы Некомпактность миокарда. Насколько это серьезно?
- Осовская Н.Ю., Серкова В.К., Иванив Ю.А. Изолированная некомпактность миокарда левого желудочка. http://www.ukrcardio.org/journal.php/>.
- Острожаков Г.И., Тронина О.А., Мелехов А.В. и др. // Журнал сердечная недостаточность. 2004. Т. 5. № 4. С. 159-162.
- EDN: RVIJZJ
- Шлевков Н.Б., Харлап М.С., Бакалов С.А., и др. // Журнал Сердечная недостаточность. 2004. Т. 5. № 3. С. 157-162.
- EDN: TOYIZJ
- Barbosa N.D., Azeka E., Estela A.E. et al. // Clinics. V. 63. № 1. 2008. P. 136-139.
- Chin T.K., Perloff J.K., Williams R.G. et al. // Circulation. 1990. V. 82. P. 507-513.


