Непосредственные результаты применения неоадъювантной химиотерапии по схеме mFOLFIRINOX у больных резектабельным раком поджелудочной железы
Автор: Вервекин И.В., Захаренко А.А.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 4 т.24, 2025 года.
Бесплатный доступ
Цель исследования – оценка эффективности и безопасности применения неоадъювантной химиотерапии (НАХТ) по схеме mFOLFIRINOX в лечении больных резектабельным раком поджелудочной железы. Материал и методы. С 2020 г. по настоящее время в ПСПБГМУ им. акад. И.П. Павлова проводится проспективное исследование II фазы, в котором изучается эффективность НАХТ по схеме mFOLFIRINOX с последующей радикальной операцией при резектабельном РПЖ по сравнению с радикальной операцией на первом этапе. В статье представлен предварительный анализ непосредственных результатов лечения. На сентябрь 2024 г. в исследование было включено 80 пациентов (группа стандартного лечения – n=41, группа НАХТ – n=39). В группе стандартного лечения проводилась радикальная операция с адъювантной полихимиотерапией (АПХТ) по схеме mFOLFIRINOX (оксалиплатин 85 мг/м2, внутривенно 120 мин; иринотекан 150 мг/м2, внутривенно 90 мин; кальция фолинат 400 мг/м2, внутривенно 120 мин; 5-фторурацил 2 400 мг/м2, внутривенная инфузия в течение 46 ч, каждые 2 нед) в объеме 12 циклов, в группе экспериментального лечения первым этапом выполнялась верификация опухоли (тонкоигольная аспирационная биопсия под контролем эндосонографии с последующим цитологическим исследованием или чрескожная трепанационная биопсия), после которой проводилось 6 циклов НАХТ по схеме mFOLFIRINOX, радикальная операция с АПХТ по схеме mFOLFIRINOX в объеме 6 циклов. В рамках данной статьи оценивались непосредственные хирургические результаты лечения, осложнения и летальность. Результаты. Выявлено значимое превосходство группы НАХТ над группой стандартного лечения по показателям: частота резекций воротной и/или верхней брыжеечной вены – 10,2 vs 21,9 % (ОР 0,44, 95 % ДИ [0,149–1,329] p=0,04), R0-резекция – 88,5 vs 73,2 % (ОР 0,6, 95 % ДИ [0,118–0,909], p=0,03), наличие лимфоваскулярной инвазии – 52,6 vs 14,8 % (ОР 0,28, 95 % ДИ [0,108–0,730] p=0,05), микроваскулярной инвазии – 55,2 vs 11,1 % (ОР 0,26, 95 % ДИ [0,1–0,669] p=0,01), периневральной инвазии – 65,7 vs 37 % (ОР 0,56, 95 % ДИ [0,327–0,969] p=0,01), частота отрицательного статуса лимфоузлов (pN0) – 73,1 vs 41,5 % (ОР 0,61, 95 % ДИ [0,331–0,969] p=0,009). Заключение. Неоадъювантная химиотерапия – перспективный и безопасный метод, способный улучшить непосредственные результаты лечения пациентов с резектабельным РПЖ.
Рак поджелудочной железы, неоадъювантная химиотерапия, резектабельность, R0-резекция, хирургическое лечение, послеоперационные осложнения
Короткий адрес: https://sciup.org/140312271
IDR: 140312271 | УДК: 616.37-006.6-08:615.28 | DOI: 10.21294/1814-4861-2025-24-4-43-53
Immediate results of neoadjuvant chemotherapy with mFOLFIRINOX regimen in patients with resectable pancreatic cancer
The aim of the study was to evaluate of the efficacy and safety of neoadjuvant chemotherapy (nCT) with mFOLFIRINOX regimen for treating patients with resectable pancreatic cancer. Material and Methods. Since 2020, a prospective phase II clinical trial that tests the effectiveness of mFOLFIRINOX chemotherapy followed by radical surgery compared to surgery followed by chemotherapy has been conducted at Pavlov First Saint Petersburg State Medical University for patients with resectable pancreatic cancer. A preliminary analysis of the immediate treatment outcomes has been presented. As of September 2024, 80 patients were included in the study (standard treatment group: n=41, nCT group: n=39). Patients in the standard treatment group underwent radical surgery followed by mFOLFIRINOX aCT (oxaliplatin 85 mg/m2 IV for 120 min, irinotecan 150 mg/m2 IV for 90 min, calcium folinate 400 mg/m2 IV for 120 min, 5-fluorouracil 2400 mg/m2 IV infusion for 46 hours every 2 weeks) for 12 cycles; patients in the experimental treatment group underwent tumor verification at the first stage (endosonography-guided fine-needle aspiration biopsy with subsequent cytological examination or percutaneous biopsy), after which 6 cycles of mFOLFIRINOX nCT and radical surgery followed by mFOLFIRINOX aCT were performed for 6 cycles. The immediate surgical outcomes, complications and mortality rates were assessed. Results. A statistically significant superiority of the nCT group over the standard treatment group was revealed in the following indicators: frequency of portal and/or superior mesenteric vein resections – 10.2 vs 21.9 % (OR 0.44, 95 % CI [0.149–1.329] p=0.04), R0 resections – 88.5 vs 73.2 % (OR 0.6, 95 % CI [0.118–0.909], p=0.03), lymphovascular invasion – 52.6 vs 14.8 % (OR 0.28, 95 % CI [0.108–0.730] p=0.05), microvascular invasion – 55.2 vs 11.1 % (OR 0.26, 95 % CI [0.1–0.669] p=0.01), perineural invasion – 65.7 vs 37 % (OR 0.56, 95 % CI [0.327–0.969] p=0.01), frequency of negative lymph node status (pN0) – 73.1 vs 41.5 % (OR 0.61, 95 % CI [0.331–0.969] p=0.009). Conclusion. nCT is a promising and safe method that can improve immediate treatment outcomes in patients with resectable pancreatic cancer.
Текст научной статьи Непосредственные результаты применения неоадъювантной химиотерапии по схеме mFOLFIRINOX у больных резектабельным раком поджелудочной железы
Протоковый рак поджелудочной железы (РПЖ) – агрессивная злокачественная опухоль со стремительным течением болезни [1]. Заболеваемость РПЖ неуклонно растет, несмотря на успехи в диагностике и доступности медицинской помощи. По данным GLOBOCAN, количество случаев РПЖ возросло с 458 918 в 2018 г. до 495 773 в 2020 г. [2]. Несмотря на значительный прогресс в хирургическом и лекарственном лечении, прогноз для пациентов с РПЖ остается негативным. В США 5-летняя выживаемость составляет 10 %, 80–85 % пациентов на момент диагностики имеют либо неоперабельную, либо метастатическую опухоль [3]. Даже для небольшой подгруппы пациентов, у которых диагностирована резектабель-ная опухоль, прогноз остается неблагоприятным: только 20 % больных переживают 5-летний рубеж после операции. На данный момент оценка резек-табельности (согласно рекомендациям NCCN, МЗ РФ, ESMO) основывается на рентгенологических критериях MD Anderson [4]. Согласно этим критериям, резектабельной является опухоль, у которой имеются следующие взаимоотношения с сосудами: верхняя брыжеечная артерия – не вовлечена, имеется нормальная жировая прослойка между опухолью и артерией, чревный ствол, общая/собственная печеночная артерии – не вовлечены, воротная/ верхняя брыжеечная вены. Стандартом лечения резектабельного заболевания является радикальная резекция и адъювантная химиотерапия (АХТ) в течение 6 мес. В исследовании ESPAC-4 показано, что АХТ по схеме гемцитабин + капецитабин улучшает 5-летнюю общую выживаемость (ОВ) до 28,8 % в сравнении с гемцитабином в монотерапии [4]. В исследовании PRODIGE24 продемонстрировано увеличение 5-летней ОВ до 43,2 % у пациентов, получавших АХТ по схеме mFOLFIRINOX [5].
Достижения в хирургическом и лекарственном лечении привели к затяжной дискуссии по поводу оптимального метода лечения резектабельного РПЖ. «Ахиллесовой пятой» оперативного лечения РПЖ является развитие отдаленных метастазов после удаления первичной опухоли. Все больше авторов поддерживают гипотезу о том, что метастатическое распространение происходит на ранних стадиях канцерогенеза РПЖ, а диссеминированные опухолевые клетки, скорее всего, присутствуют в отдаленных органах на момент постановки диагноза [6]. Дальнейший рост диссеминированных опухолевых клеток приводит к появлению клинически детектируемых метастазов и является основным фактором смертности, связанной с РПЖ.
Неоадъювантная химиотерапия (НАХТ) активно применяется при ряде других солидных опухолей для снижения локальной стадии и лечения клинически не обнаруживаемых микрометастазов [7–9]. Одним из преимуществ НАХТ является большая вероятность завершения полного предусмотренного объема терапии в условиях неоадъювантного лечения по сравнению с адъювантными режимами химиотерапии. Это особенно актуально при раке поджелудочной железы, учитывая, что при этом заболевании частота завершения адъювантного лечения в полном объеме составляет не более 60 % [10]. C другой стороны, принимая во внимание, что рак поджелудочной железы является системным заболеванием даже на ранних стадиях, НАХТ может рассматриваться как метод отбора пациентов с более агрессивным типом течения болезни, у которых локальное (хирургическое) лечение будет неэффективным [11]. По данным ранее проведенных исследований, НАХТ у пациентов с резектабельным РПЖ достоверно позволяет улучшить непосредственные хирургические результаты, а именно: увеличить частоту R0-резекций, рN0-статуса лимфатических узлов, снизить частоту периневральной, лимфоваскулярной инвазии, резекции воротной/ верхней брыжеечной вены, без увеличения количества осложнений, длительности операции и кровопотери по сравнению с группой хирургического лечения «up-front». Однако влияние НАХТ на показатели выживаемости остается неясным, имеющиеся данные клинических исследований являются неоднозначными [12]. Кроме того, во всех ранее проведенных исследованиях различается как конкретный тип неоадъювантного лечения (хи-миотерапия/химиолучевая терапия – PREOPANC, Casadei, Jang) [13–15], так и смешиваются 2 различные прогностические группы (резектабельный и погранично-резектабельный РПЖ), не говоря уже о различиях в используемых режимах неоадъювантной химиотерапии (NEONAX – Gem+NabP, S1 – Prep-02/JSAP-05, капецитабин – ESPAC-5, PEXG – PACT-15, mFOLFIRINOX/ FOLFIRINOX – NORPACT-1, ESPAC-5) [16–19]. Таким образом, вопрос об эффективности НАХТ по схеме mFOLFIRINOX у больных резектабельным РПЖ по-прежнему сохраняет свою актуальность.
Цель исследования – оценка эффективности и безопасности применения неоадъювантной химиотерапии по схеме mFOLFIRINOX в лечении резектабельного рака поджелудочной железы.
Материал и методы
С 2020 г. по настоящее время в ПСПБГМУ им. академика И.П. Павлова проводится проспективное исследование II фазы, в котором изучается эффективность НАХТ по схеме mFOLFIRINOX с последующей радикальной операцией у пациентов с резектабельным РПЖ в сравнении с радикальной операцией на первом этапе. Критерии включения: наличие резектабельной опухоли поджелудочной железы (сT1–3N0–2M0), подтвержденное данными инструментальных исследований (МСКТ органов брюшной полости, грудной клетки и малого таза, выполненная в срок не более 21 дня на момент рандомизации), морфологическая верификация для рандомизации не является необходимой, отсутствие противопоказаний к запланированной терапии (тяжелая соматическая патология, ургент-ные осложнения первичной опухоли); адекватная функция основных органов и систем.
При наличии критериев включения больные рандомизировались в одну из групп в отношении 1:1, при отсутствии противопоказаний пациенты получали предписанное согласно группе рандомизации лечение, при наличии механической желтухи выполнялось дренирование желчных протоков (наружное дренирование или эндоскопическое стентирование – на усмотрение врача). После купирования осложнений и при отсутствии противопоказаний к радикальному хирургическому лечению или химиотерапии – пациентам выполнялось лечение согласно их группе рандомизации.
Пациентам группы стандартного лечения проводилась радикальная операция с последующей АХТ mFOLFIRINOX (оксалиплатин 85 мг/м2, внутривенно 120 мин; иринотекан 150 мг/м2, внутривенно 90 мин; кальция фолинат 400 мг/м2, внутривенно 120 мин; 5‐фторурацил 2 400 мг/м2, внутривенная инфузия в течение 46 ч, каждые 2 нед) в объеме 12 циклов. Пациентам группы экспериментального лечения первым этапом выполнялась верификация опухоли (тонкоигольная аспирационная биопсия под контролем эндосонографии с последующим цитологическим исследованием или чрескожная трепанационная биопсия), после которой проводилось 6 циклов НАХТ по схеме mFOLFIRINOX, радикальное хирургическое лечение с последующей АХТ по схеме mFOLFIRINOX в объеме 6 циклов.
Данные пациентов были консолидированы в виде электронных таблиц и анализировались с помощью программы SPSS Statistics v. 17.0. Оценка нормальности распределения проводилась с применением теста Шапиро–Уилка. Количественные показатели, имеющие нормальное распределение, описывались с помощью средних арифметических величин (M) и стандартных отклонений (SD), границ 95 % доверительного интервала (95 % ДИ). В случае отсутствия нормального распределения количественные данные описывались с помощью медианы (Me) и нижнего и верхнего квартилей (Q1–Q3). Категориальные данные описывались с указанием абсолютных значений и процентных долей. Сравнение двух групп по количественному показателю, имеющему нормальное распределение, при условии равенства дисперсий выполнялось с помощью t-критерия Стьюдента. Сравнение двух групп по количественному показателю, распределение которого отличалось от нормального, выполнялось с помощью U-критерия Манна–Уитни. Сравнение процентных долей при анализе четырехпольных таблиц сопряженности выполнялось с помощью точного критерия Фишера (при значениях ожидаемого явления менее 10). Сравнение процентных долей при анализе многопольных таблиц сопряженности выполнялось с помощью критерия χ2 Пирсона. Различия считались статистически значимыми при p<0,05.
Результаты
В статье представлен предварительный анализ непосредственных результатов лечения, на сентябрь 2024 г. в исследование включено 80 пациентов (группа стандартного лечения – n=41, группа НАХТ – n=39). При анализе клиникодемографических показателей (табл. 1) не обнаружено значимых различий по большинству показателей. Статистически значимые, но клинически не значимые различия обнаружены по сле- дующим показателям: медиана возраста в группе стандартного лечения составила 64 года (IQR – 61–72) vs 62 лет (IQR – 53–66) в группе НАХТ (p=0,001), медиана ИМТ в группе стандартного лечения – 25,2 кг/м2 (IQR – 23,3–28,5) vs 24,1 кг/м2 (IQR – 20,4–26,2) в группе НАХТ (p=0,011). Статистически и клинически значимые различия между группами обнаружены в следующих характеристиках: медиана максимального размера опухоли в группе стандартного лечения составила 3,2 см (IQR – 2,5–3,7) vs 3,8 см (IQR – 3,0–4,4) в группе НАХТ (p=0,001). Кроме того, сТ3 и cN+ опухоли чаще встречались в группе НАХТ по сравнению с группой стандартного лечения: для сТ3 – 19 (48,7 %) vs 9 (21,9 %) (p=0,001), для сN+ – 17 (43,6 %) vs 9 (21,9 %) (p=0,01) соответственно.
При анализе периоперационных результатов лечения обнаружены статистически и клинически значимые различия в частоте радикальных хирургических резекций и сроке начала АПХТ (табл. 2). Резектабельность в группе стандартного хирургического лечения составила 92,7 vs 68,4 % в группе НАХТ (ОР 4,2, 95 % ДИ [1,283–13,778], p=0,01) (рис. 1), в группе стандартного лечения пациенты позже начинали АПХТ по сравнению с группой НАХТ, медиана времени начала составила 7 нед (IQR – 5–9) vs 5 нед (IQR –4–6) (p=0,044).
При оценке непосредственных хирургических результатов лечения (табл. 3) обнаружено значи-
Частота радикальных резекций (структурирование по типу операции)/ Frequency of radical resections (structured by type
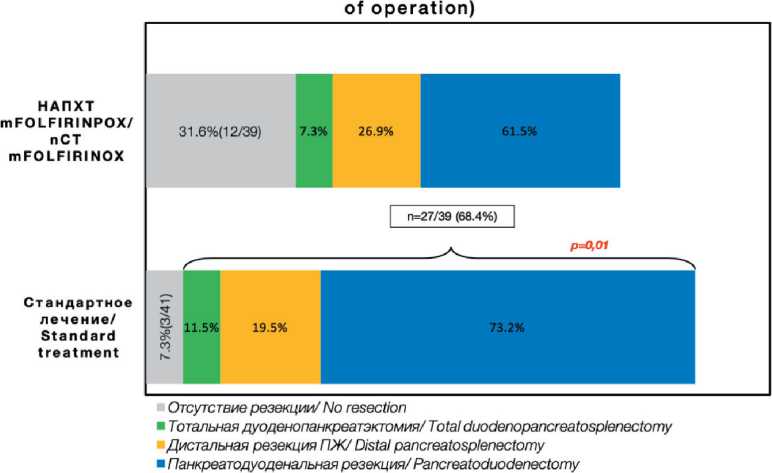
Рис. 1. Частота радикальных резекций. Примечание: рисунок выполнен авторами Fig. 1. Frequency of radical resections.
Note: created by the authors
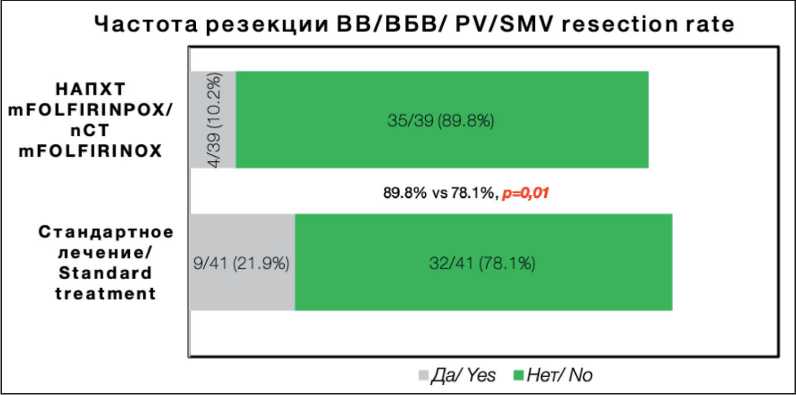
Рис. 2. Частота резекции воротной и/или верхней брыжеечной вены.
Примечание: рисунок выполнен авторами Fig. 2. Frequency of portal and/or superior mesenteric vein resection. Note: created by the authors
Таблица 1/table 1
|
Параметры/Parameteres |
Стандартное лечение/ Standard treatment (n=41) |
НАХТ/ nCT (n=39) |
p-value |
|
Пол/Gender |
|||
|
Муж/Male |
18 (43,9 %) |
16 (41 %) |
0,82 |
|
Жен/Female |
46 (56,1 %) |
23 (59 %) |
|
|
Возраст (лет), медиана (IQR)/Age (years), median (IQR) |
64 (61–72) |
62 (53–66) |
0,001 |
|
Функциональный статус ECOG/Functional status ECOG |
|||
|
0 |
29 (70,7 %) |
28 (71,8 %) |
0,46 |
|
1 |
12 (29,3 %) |
11 (28,2 %) |
|
|
ИМТ (кг/м2), медиана (IQR)/BMI (kg/m2), median (IQR) |
25,2 (23,3–28,5) |
24,1 (20,4–26,2) |
0,011 |
|
Степень отклонения массы тела/Degree of deviation of body weight |
|||
|
<18,5 кг/м2/kg/m2 |
1 (2,4 %) |
4 (10,3 %) |
|
|
18,5–25 кг/м2/kg/m2 |
18 (43,9 %) |
22 (56,4 %) |
0,053 |
|
25–30 кг/м2/kg/m2 |
17 (41,5 %) |
11 (28,2 %) |
|
|
>30 кг/м2/kg/m2 |
5 (12,2 %) |
2 (5,1 %) |
|
|
Макс размер опухоли (см), медиана (IQR)/ Max tumor size (cm), median (IQR) |
3,2 (2,5–3,7) |
3,8 (3,0–4,4) |
0,001 |
|
Локализация опухоли/Tumor localization |
|||
|
Головка/Head |
32 (78 %) |
29 (74,4 %) |
|
|
Тело/Body |
4 (9,7 %) |
6 (15,4 %) |
0,46 |
|
Хвост/Tail |
5 (12,2 %) |
4 (10,3 %) |
|
|
Критерий сT/cT criterion |
|||
|
сT1 |
5 (12,2 %) |
0 (0,0 %) |
|
|
сT2 |
27 (65,9 %) |
20 (51,3 %) |
0,001 |
|
сT3 |
9 (21,9 %) |
19 (48,7 %) |
|
|
Критерий сN/cN criterion |
|||
|
сN0 |
32 (78,1 %) |
22 (56,4 %) |
0,01 |
|
сN+ |
9 (21,9 %) |
17 (43,6 %) |
|
|
СА 19–9 крови (ЕД/мл), median (IQR)/ CA19–9 (U/ml), median (IQR) |
74,2 (12,75–424,6) |
213,8 (30,6–609,1) |
0,081 |
|
СА 19–9 крови/СA 19–9 blood level |
|||
|
0–37 ЕД/мл/U/ml |
15 (36,6 %) |
12 (30,8 %) |
|
|
37–400 ЕД/мл/U/ml |
15 (36,6 %) |
11 (28,2 %) |
0,241 |
|
>400 ЕД/мл/U/ml |
21 (26,8 %) |
16 (41 %) |
|
|
Рентгенологический ответ RECIST/RECIST radiographic response |
|||
|
PD |
NA |
14 (36,8 %) |
|
|
SD |
NA |
13 (34,2 %) |
|
|
PR |
NA |
11 (28,9 %) |
|


