Невус Ядассона: редкие варианты течения, особенности диагностики и подходы к терапии (клинические случаи)
Автор: Платонова А.В., Пономаренко И.Г., Рассказов Я.А., Кашутин С.Л., Шапчиц Н.Л.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Дерматовенерология
Статья в выпуске: 1 т.21, 2025 года.
Бесплатный доступ
Невус сальных желез Ядассона - врожденная гамартома, представляющая интерес для дерматологов возможностью добро- и злокачественного перерождения в течение жизни пациента. В статье описаны редкие проявления невуса: случай краниального невуса с поздним его дебютом во взрослом возрасте, внекраниального невуса с большой площадью распространения, клиническое и дерматоскопическое описание запущенного малигнизированного краниального невуса. Дано подробное описание стадийности течения невуса, его дерматоскопические и патоморфологические характеристики, подходы к терапии.
Невус сальных желез, невус ядассона, дерматоскопия, малигнизация
Короткий адрес: https://sciup.org/149148674
IDR: 149148674 | УДК: 616.53-006.55 | DOI: 10.15275/ssmj2101057
Jadassohn’s nevus: rare course variants, diagnosis features and approaches to therapy (clinical cases)
Nevus of the sebaceous glands of Jadassohn is a congenital hamartoma, which is of interest to dermatologists with the possibility of benign and malignant degeneration during the patient's life. The article describes rare manifestations of nevus: a case of a cranial nevus with a late onset in adulthood, an extracranial nevus with a large area of distribution, a clinical and dermoscopic description of an advanced malignant cranial nevus. A detailed description of the stages of the course of the nevus, its dermoscopic and pathomorphological characteristics, and approaches to therapy are also given.
Текст научной статьи Невус Ядассона: редкие варианты течения, особенности диагностики и подходы к терапии (клинические случаи)
EDN: MJTMBA
происхождения [1, 4]. У 62,5% пациентов формируются очаги на волосистой части головы, у 24,5% — на других участках головы, у 4,7% — на туловище, у 4,2% — на шее [5]. В случае внекраниальной локализации невус обычно располагается в соответствии с ориентацией по линиям Блашко [1, 2].
Себорейный невус наследуется преимущественно по аутосомно-доминантному типу, реже — в результате мозаицизма генов [6, 7]. В последних исследованиях описана ассоциация с постзиготной соматической мутацией, связанной с генами KRAS (хромосомой 12p12), NRAS (хромосомой 1p13) и HRAS (хромосомой 11p15) [8–10]. Мутации в этих
генах приводят к увеличению пролиферации эпителиальных клеток и развитию вторичной добро- и злокачественной неоплазии, синдрома Мьюира — Торре (описанного E. Muir и соавт. в 1967 г. и D. Torre в 1968 г.), характеризующегося наличием как новообразований сальных желез, так и висцеральных злокачественных новообразований, а также синдрома Шиммельпеннинга — Фейерштейна — Мимса [7]. При этом последний представляет собой мультиси-стемное заболевание, называемое также синдромом линейного невуса [2, 9], включающим поражение органов зрения и слуха, вовлечение нервной, сердечнососудистой, мышечной, мочеполовой систем, а также связочно-суставного аппарата [11, 12]. Наиболее часто синдром Шиммельпеннинга — Фейерштейна — Мимса подразумевает наличие таких заболеваний, как гипофосфатемический рахит, умственная отсталость и другие когнитивные нарушения, колобома и косоглазие [12].
Длительно существующие невусы [13–20] в 10– 20% случаев способны перерождаться в другие доброкачественные новообразования, такие как аденома сальных желез, пигментная эккринная порома, сирингиома, себорейная эпителиома, сирингиоци-стаденома, трихобластома и трихолеммома, а также во вторичные злокачественные новообразования [4, 10]. На долю злокачественных образований приходится примерно 3% случаев. Наиболее часто развиваются базальноклеточная карцинома (1,1%) [20] и плоскоклеточная карцинома (0,57%), крайне редко — карцинома сальных и апокринных желез, микро-кистозная карцинома [12]. Кроме того, существование невуса сальных желез может быть ассоциировано с формированием коллизионных опухолей кожи внутри новообразования, например меланомы [19].
Клиническая манифестация невуса подразделяется на три стадии [11, 18]. Так, I стадия начинается после рождения и длится все детство. В это время выявляются округлые высыпания в виде небольших точечных папул, практически лишенных волос, цвета кожи или нежно-желтого, желтовато-розового и коричневого оттенков. Патоморфологически на ранней стадии наблюдают акантоз, гипоплазию сальных желез и волосяных фолликулов с поражением протоков эккринных и апокринных потовых желез [6, 7, 13–15].
Во время пубертата развивается II стадия, характеризующаяся формированием более крупных папул и бляшек, полностью лишенных волос. В ходе исследований были обнаружены андрогенные рецепторы в себорейных невусах [3]. Благодаря их активности во II стадию высыпания становятся более интенсивно окрашенными, развивается акантоз с папилломатозом, гиперплазия сальных желез, эктопия апокриновых желез и клеток, гиперплазия эккринных желез [16].
На III стадии во взрослом возрасте возрастает риск развития вторичной неоплазии имеющихся образований [8, 16]. С целью раннего выявления малигнизации невусов применяют видеодерматоскопию и ультразвуковой метод визуализации [16, 17]. Дерматоскопические паттерны зависят от стадии течения. Первично выявляются желтоватые или коричневатые глобулы, собранные в кластеры на общем бесструктурном желтоватом и беловатом фоне; в стадию бородавчатых бляшек они приобретают беловато-желтый дольчатый вид или сероватый папиллярный вид на желто-беловатом однородном фоне [17].
Цель — представить редкие клинические случаи невуса Ядассона, обсудить дермоскопические и па-томорфологические критерии подтверждения диагноза, подходы к терапии.
От всех пациентов получены письменные согласия на публикацию материалов.
Описание клинических случаев. Клинические случаи краниальной локализации новообразования. Пациент М. 22 лет: дебют высыпаний — в 20-летнем возрасте. Обращался к нескольким дерматологам, диагноз долго не был поставлен, проводилось пробное лечение топическими глюкокортикоидами более 6 мес назад — без эффекта. При обращении в нашу клинику — процесс поражения кожи носит ограниченный характер с локализацией в правой скуловой области. Представлен сгруппированными милиарными папулами розовато-желтоватого цвета, расположенными линейно, очаг поражения размером 25×80 мм (рис. 1, а ).
При дермоскопическом осмотре выявлены множественные желтые и оранжевые точки на фоне светло-желтой и розоватой бесструктурных областей (рис. 1, б ). Пациент был направлен на гистологическое исследование с предварительным диагнозом невуса Ядассона. Выявлены акантоз, папилломатоз, гиперплазия сальных желез, редукция и эктопия апокринных желез, гиперплазия эккринных желез, предварительный диагноз подтвержден.
В связи с локализацией на лице, нежеланием пациента радикально удалять образование, рекомендовано динамическое наблюдение, фотодокументация, видеодермаскопия не реже 1 раза в 6 мес.
На рис. 1 ( в ) представлен подобный по клиническим проявлениям невус сальных желез. Однако в данном случае он развивался классически, дебютировал в 8–9-летнем возрасте. Проявлялся
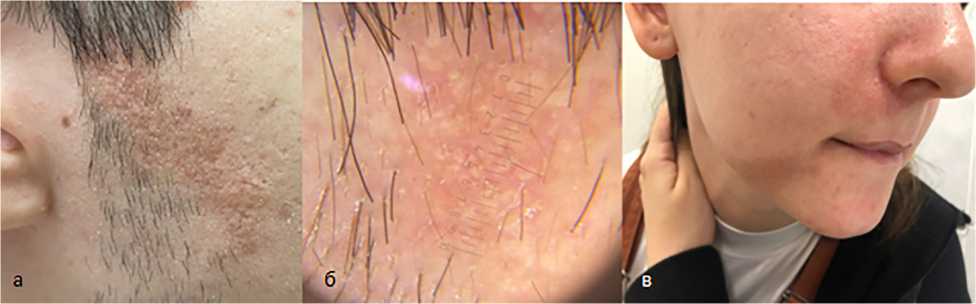
Рис. 1. Папулы желтовато-розового цвета ( а — в )
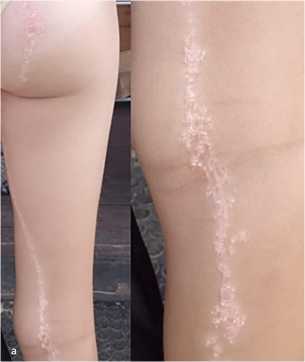
Рис. 2. Линейно расположенные сгруппированные папулы ( а , б )
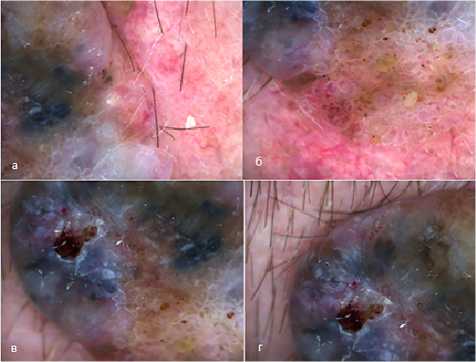
Рис. 3. Дерматоскопическое изображение образования: бело-голубая вуаль, атипичная сосУдистая сеть, асимметричные пигментные точки и глобулы ( а , б ), папула фиолетовокоричневого цвета с эрозивным дефектом ( в , г )
одиночной папулой желтовато-розоватого цвета в области подбородка. Активно увеличивался в размерах в пубертатном возрасте (11–12 лет), в настоящее время пациентке 24 года, образование стабильно, от удаления отказывается, находится под динамическим наблюдением.
Цель демонстрации этих клинических случаев — напомнить практикующим дерматологам, что невус Ядассона иногда может развиваться во взрослом возрасте, но при этом выглядит классически, и клиническая постановка диагноза в совокупности с данными дерматоскопии не должна вызывать затруднений. Тем не менее рекомендовано проведение гистологического исследования всем пациентам с подозрением на невус сальных желез вне зависимости от возраста дебюта.
Клинический случай внекраниальной локализации новообразования. Пациентка Н. 11 лет: дебют высыпаний — в 2-летнем возрасте (рис. 2). Процесс начинался с появления нескольким папул в области правой ягодицы, в течение года распространился на всю заднебоковую поверхность правого бедра, верхнюю треть голени, с тех пор рост незначительный. Пациентка обследована, соматически здорова, находится под динамическим наблюдением.
В настоящее время патологический процесс представлен сгруппированными беловато-желтоватыми милиарными папулами, расположенными по заднебоковой поверхности правой ягодицы, бедра и голени, ориентирован по линии Блашко.
Встречаемость подобных невусов внекраниаль-ной локализации не превышает 5% по популяции, случай демонстрируется как редкая клиническая форма образования.
Клинический случай озлокачествления новообразования. Пациент М. 56 лет: невус существовал в области волосистой части головы с детского возраста, не беспокоил, иногда травмировался во время стрижки и расчесывания. К дерматологу ранее пациент никогда по поводу образования не обращался; впоследствии в связи с изменением цвета, кровоточивостью, которые заметила супруга больного, был консультирован (рис. 3).
На момент осмотра патологический процесс представлен папулой фиолетово-коричневого цвета, размером 10^15 мм, расположенной на фоне бляшки желтоватого цвета, преимущественно округлой формы диаметром 40 мм. На поверхности папулы имеется единичный эрозивный дефект округлой формы диаметром 3 мм. При дерматоскопическом осмотре определяются бело-голубая вуаль, атипичная сосудистая сеть, асимметричные пигментные точки и глобулы.
Пациент направлен к врачу-онкологу с целью радикального иссечения невуса.
Случай демонстрируется с целью напомнить практикующим врачам важность осмотра всех кожных покровов пациентов для своевременного выявления новообразований кожи и определения тактики их ведения.
Обсуждение. Невус сальных желез, как правило, существует с периода новорожденности, и постановка диагноза в этом случае не вызывает затруднений. Особенностью клинического примера на рис. 1 ( а , б ) является дебют невуса во взрослом возрасте, что характерно менее чем для 10% всех сальных невусов [1, 13]. В практике авторов встречаемость невуса Ядассона с первыми проявлениями во взрослом возрасте ниже, чем описанная по данным литературы, на такие образования приходится примерно 2-3% пациентов от всех обращений по поводу данного вида образования.
Выявление невуса в раннем возрасте требует углубленного обследования пациентов для исключения синдрома Шиммельпеннинга — Фейерштей-на — Мимса. При дебюте во взрослом возрасте, когда соматический статус пациента уже определен, или при схожем с другими врожденными эктопиями кожном процессе важно проведение гистологического исследования с целью подтверждения диагноза и определения дальнейшей тактики его ведéния в условиях наличия рисков добро- и злокачественной неоплазии. Период наблюдения за пациентами из клинических примеров (см. рис. 1) составляет приблизительно 1,5 года. За это время не отмечено какой-либо клинической и дерматоскопической динамики невусов.
Выявление крупных образований в детском возрасте (см. рис. 2) является показанием для динамического наблюдения за такими больными, сроки и возможность иссечения образования определяются с учетом особенностей клинической картины и динамики изменения образований с ростом ребенка. Динамическое наблюдение за девочкой осуществляется в течение 3 лет, образование клинически и дерматоскопически стабильно. Родители ориентированы провести хирургическое удаление образования в несколько этапов в ближайший год.
Отсутствие надлежащего наблюдения за невусом (см. рис. 3), локализация в области волосистой части головы, затрудняющая самостоятельный осмотр, а также способствующая повышенному риску трав-матизации, может приводить к малигнизации невусов, что ухудшает общий прогноз по качеству жизни.
В случае иссечения новообразования классически гистологическая картина невуса Ядассона представляет собой папилломатоз и гиперкератоз, выраженную гиперплазию сальных желез с отсутствием волосяных фолликулов, присутствие апокринных желез. Морфология и распределение сальных желез при этом аномальны, они локализуются высоко в дерме, их протоки непосредственно сообщаются с поверхностью эпидермиса. В ряде случаев проводятся специальные окрашивания срезов. Так, экспрессия антигена эпителиальной мембраны (ЕМА) в цитоплазме характерна для 100% случаев. Выявление экспрессии цитокератина 7 (СК) и рецептора андрогена (AR) не является специфичным признаком, может быть характерно и для других опухолей придатков кожи. Более специфичным является обнаружение адипофилина и фактора XIIIа (клона АС-1А1). Применение специальных методов окрашивания перспективно в плане диагностики синдрома Мьюира — Торре с целью выявления клинически не-диагностированных микросателлитных нестабильностей, выявления висцеральных новообразований, прежде всего толстой кишки.
Превентивное иссечение невусов не противопоказано, но мнения об оптимальных для удаления сроках противоречивы: часть авторов рекомендуют проведение удаления до пубертата, а часть — после такового периода [8, 14]. Необходимость иссечения себорейных невусов в профилактических целях до сих пор является дискутабельным вопросом [14, 15]. Эталонным способом удаления данных невусов в настоящее время признаны физические методы деструкции, такие как криодеструкция, радиохирургическое лечение, высокоинтенсивная лазеротерапия: деструкция аргоновым и углекислотным (CO2) лазерами [20]. Они дают наиболее предсказуемый и стабильный результат. Однако при большой площади поражения одномоментное радикальное иссечение невуса таким способом затруднительно, чаще проводится в несколько этапов, что повышает риски развития осложнений, прежде всего рубцевания. В научном сообществе рассматривается вопрос применения трихлоруксусной кислоты с целью удаления этих невусов, а также ароматических ретиноидов (изотретиноина) в качестве кератолитического и обладающего угнетающим действием на сальные железы агента, но они имеют низкий уровень доказательности [20].
Заключение. Невус Ядассона является редкой, но сложной в плане прогноза гамартомой, дебют заболевания возможен не только в детском возрасте, что требует особой внимательности от практикующих врачей на приеме. При выявлении данного образования важно проведение регулярного динамического наблюдения, а также своевременного радикального иссечения в пределах здоровых тканей в случае обнаружения признаков малигнизации.
Вклад авторов. Все авторы сделали эквивалентный вклад в подготовку публикации.


