Нитрат 4,4’-дипиридил меди(II) - 2D металл-органический каркас
Автор: Осипов А.А., Найферт С.А., Раджакумар К., Дороватовский П.В., Ефремов А.Н., Жеребцов Д.А.
Журнал: Вестник Южно-Уральского государственного университета. Серия: Химия @vestnik-susu-chemistry
Рубрика: Физическая химия
Статья в выпуске: 2 т.16, 2024 года.
Бесплатный доступ
Описана кристаллическая структура металл-органического каркаса - нитрата 4,4’-дипиридил меди(II) с молекулой ДМСО в координационной сфере меди, детали строения установлены методом РСА. Кристаллографические данные: брутто-формула C55H93Cu2N12O23S7, М 1641,91; моноклинная сингония, пространственная группа P 1 21/n 1; параметры ячейки: a = 15,490(3), b = 14,760(3), c = 15,980(3); a = 90, β = 90,10(3), g = 90 град; V = 3653,5(13) Å3, Z = 2, ρрасч = 1,493 г/см3. Бидентатным лигандом в исследуемом МОК является 4,4’-бипиридил; медь образует координационный полиэдр - октаэдр, в четырех экваториальных положениях которого находятся атомы азота бипиридиновых фрагментов, а в двух аксиальных положениях - атомы кислорода в нитрат-иона и диметилсульфоксида. Длины связей Cu-N в экваториальном положении лежат в диапазоне 2,014-2,031 Å, а длины связи Cu-O составляют 2,297 Å и 2,515 Å. Занятость экваториальных положений 4,4’-дипиридилом приводит к образованию сетчатой слоистой 2D-структуры. Отдельные слои в полученном нитрате 4,4’-дипиридил меди(II) не связаны между собой и сдвинуты относительно друг друга. Ароматические кольца 4,4’-дипиридила повернуты на угол 5,77(2) град. относительно друг друга.
Металл-органические каркасы, структура, рентгеноструктурный анализ
Короткий адрес: https://sciup.org/147244630
IDR: 147244630 | УДК: 546.02 | DOI: 10.14529/chem240220
4,4’-dipyridylcopper(II) nitrate as a 2D organometallic framework
The crystal structure of the organometallic framework, namely, 4,4’-dipyridylcopper(II) nitrate with the DMSO molecule in the copper coordination sphere, has been described, the structural features have been established by the X-ray method. Crystallographic data: C55H93Cu2N12O23S7, M 1641.91; monoclinic syngony, space group P 1 21/n 1; cell parameters: a = 15.490(3), b = 14.760(3), c = 15.980(3); a = 90, β = 90.10(3), g = 90 deg.; V = 3653.5(13) Å3, Z = 2, ρcalc = 1.493 g/cm3. The bidental ligand in the organometallic framework is 4,4’-bipyridyl; copper, being a complexing ion, forms a coordination octahedron, the nitrogen atoms of bipyridine fragments are in four equatorial positions, the oxygen atoms of nitrate ion and dimethyl sulfoxide are in two axial positions. The Cu-N bond lengths in the equatorial position are in the range of 2.014-2.031 Å, and the Cu-O bond lengths are 2.297 Å and 2.515 Å. The occupation of the equatorial positions by 4,4’-dipyridyl leads to formation of a layered structure, which distinguishes the resulting compound from another MOF based on copper(II), nitrate ions and 4,4’-dipyridyl, in which all the equatorial positions are occupied by NO3-groups. The individual layers in the obtained 4,4’-dipyridylcopper(II) nitrate are not crosslinked; they are shifted relative to neighboring layers. The pyridyl rings of 4,4’-dipyridyl are rotated at an angle of 5.77(2) degrees. relative to each other.
Текст научной статьи Нитрат 4,4’-дипиридил меди(II) - 2D металл-органический каркас
Металл-органические каркасы (МОК, metal-organic frameworks, MOF) – координационные полимерные материалы, которые состоят из ионов металлов и мостиковых лигандов. МОК могут образовывать одно- [1–3], дву- [4–6] или трехмерные структуры [7–10]. Металл-органические каркасы применяются в адсорбции, хранении и разделении газов, а также в газовых сенсорах. Например, МОК используются для разделения смесей органических соединений: было показано, что каркасы серии MIL перспективны для разделения смесей ксилолов, соединения серии SIFSIX [11], а также UTSA-100, NOTT-300 [12] – для разделения ацетилена и этилена. Трансформации структуры при определенных физических или химических воздействиях – это важная особенность группы так называемых «гибких» МОК, которая активно применяется для разделения веществ [13].
Важная область применения МОК – катализ. Медь-содержащий МОК, имеющий формулу [Cu 3 (btc) 2 (H 2 O)] (btc – бензол-1,3,5-трикарбоксилат), является кислотой Льюиса [14]. Координированная вода может быть легко удалена нагреванием до 383 К, что делает кислотный центр Льюиса доступным для реагента. Примеры гетерогенного катализа на МОК: соединения Zn 3 (chirbtb-1) 2 (chirbtb-1 – 1,3,5-три(4-[2-(4-изопропил-2-оксооксазолидин-3-ил)]бензоат)бензол) и Zn 3 (chirbtb-2) 2 (chirbtb-2 – 1,3,5-три(4-[2-(4-бензил-2-оксооксазолидин-3-ил)]бензоат)бензол) катализируют альдольную реакцию Мукаямы с хорошими выходами и умеренными значениями энантиомерного избытка [15]; соединение Cu(2-pymo) 2 (2-pymo – 2-гидроксипиримидинолат) проявляет каталитическую активность в реакциях 1,3-диполярного циклоприсоединения [16].
Используемый в данной работе линкер 4,4’-дипиридил (4,4’-bipy) – бидентатный лиганд, который широко используется для получения металл-органических каркасов, например, координационных полимеров {[Cu(AF 6 )(4,4′-bipy) 2 ] · 8H 2 O} n , где А – Si, Ge [17], транс-[Cu(NCS) 2 (4,4’-bipy)] [18].
Экспериментальная часть
Синтез нитрата 4,4’-дипиридила меди(II) (1). В стеклянную ампулу поместили навеску ди-ацетилендибензойной кислоты (0,015 г, 0,052 ммоль), 4,4’-дипиридила (0,018 г, 0,11 ммоль), нитрата меди (II) (0,010 г, 0,054 ммоль), 1 мл диметилсульфоксида и 0,2 мл 1,4-диоксана. Ампулу запаяли и поместили в муфельную печь со следующей программой: нагрев от 25 до 100 °С со скоростью 100 °С/ч, выдержка при 100 °С 48 ч, охлаждение до 25 °С со скоростью 1 °С/ч. По окончании программы в ампуле выросло 2–3 мг мелких голубых кристаллов соединения 1 , пригодных для структурных исследований.
Рентгеноструктурное исследование кристаллов выполнено на канале «Белок/РСА» Курчатовского источника синхротронного излучения [19, 20]. Эксперимент на монокристалле проводили на дифрактометре Mardtb с ПЗС-детектором Rayonix SX165 (λ = 0,745 Å, φ-сканирование с шагом 1,0°) в прямой геометрии с плоскостью детектора, перпендикулярной лучу, при температуре 100 K, которая поддерживалась с помощью системы Oxford Cryostream 700Plus. Данные бы- ли проиндицированы и интегрированы программным пакетом XDS [21]. Структура была решена прямыми методами с помощью программы SHELXT [22]. Модель структуры была исследована и уточнена в программе OLEX2 [23] полноматричным методом наименьших квадратов с анизотропными тепловыми параметрами. Положения атомов водорода уточняли с использованием модели «наездника».
Таблицы координат атомов, длин связей и валентных углов депонированы в Кембриджский банк структурных данных (№ 2285923 для 1; ; . Кристаллографические параметры структур и данные дифракционного эксперимента приведены в таблице.
Кристаллографические данные, параметры эксперимента и уточнения структуры 1
|
Брутто-формула |
C 55 H 93 Cu 2 N 12 O 23 S 7 |
|
Молекулярная масса |
1641,91 |
|
Температура, K |
100(2) |
|
Сингония |
моноклинная |
|
Пр. гр. |
P 1 21/n 1 |
|
a , Å |
15,490(3) |
|
b , Å |
14,760(3) |
|
c , Å |
15,980(3) |
|
α, град. |
90 |
|
β, град. |
90,10(3) |
|
γ, град. |
90 |
|
Объем ячейки V , Å3 |
3653,5(13) |
|
Z |
2 |
|
ρрасч, г/см |
1,493 |
|
Коэффициент поглощения μ, мм–1 |
1,001 |
|
F (000) |
1722 |
|
Размер кристалла, мм |
0,1×0,04×0,01 |
|
Излучение |
синхротрон ( λ =0,7527) |
|
Диапазоны индексов |
–21 ≤ h ≤ 16, –17 ≤ k ≤ 20, –21 ≤ l ≤ 21 |
|
Общее количество рефлексов |
26563 |
|
Независимые рефлексы |
9670 [ R int = 0,0707, R sigma = 0,0726] |
|
Данные / ограничения / параметры |
9670/40/489 |
|
F 2 |
1,110 |
|
R -факторы по I ≥ 2σ(I) |
R 1 = 0,0990, wR 2 = 0,2217 |
|
R -факторы по всем отражениям |
R 1 = 0,1327, wR 2 = 0,2376 |
|
Остаточная электронная плотность, э·Å–3 |
1,178/–1,042 |
Обсуждение результатов
Целью работы являлось получение металл-органического каркаса на основе комплекса 4,4’-(бута-1,3-диин-1,4-диил)бис(бензоата) меди (диацетилендибензоата меди) с 4,4’-бипиридилом. В составе же полученных кристаллов диацетилендибензоат-ион отсутствует. Синтезируемое вещество является двумерным координационным полимером, связанным бипиридильными мостиками в плоские сетки. Медь, являясь комплексообразователем, имеет координационное окружение в форме октаэдра, в четырех экваториальных положениях которого находятся атомы азота молекул бипиридина, а в двух аксиальных положениях – атомы кислорода нитрат-иона и диметилсульфоксида (рис. 1). Длины связей Cu–N в экваториальном положении лежат в диапазоне 2,014–2,031 Å, а длины связи Cu–O составляют 2,297 Å и 2,515 Å. Молекула диметилсульфоксида, как и один из нитрат-ионов, занимает аксиальное положение и обуславливает отсутствие координационных связей с соседним слоем (рис. 2). Второй нитрат-ион располагается во внешней координационной сфере и служит ионной составляющей связи между соседними положительно заряженными 2D-сетками.
В полостях сетки соединения ( 1 ) присутствует некоторое количество адсорбированной воды и диметилсульфоксида. Положение молекул воды из-за наличия значительного свободного пространства разупорядочено (см. рис. 1).
Координационную сферу меди помимо атомов азота бипиридинового фрагмента занимают нитрат-ион и растворитель – диметилсульфоксид, причем указанные лиганды чередуются местами в аксиальных пол ожениях у соседних атомов меди. Известен нитрат 4,4’-бипиридил меди [24], однако строение данно го соединения отличается от полученного н ами продукта. В ук а занной работе катион меди та кже имеет октаэдрическое окружение, в кот ором атомы азота л иганда 4,4’-bipy занимают два аксиальных положения, а все экваториальны е положения коорд инируются атомами кислорода нитрат-ионов, причем атомы кислорода одной NO 3– группы участ вуют в координации соседних атомов меди. Ввиду этого образуются пол имерные ленты с м аленьким размером пор.
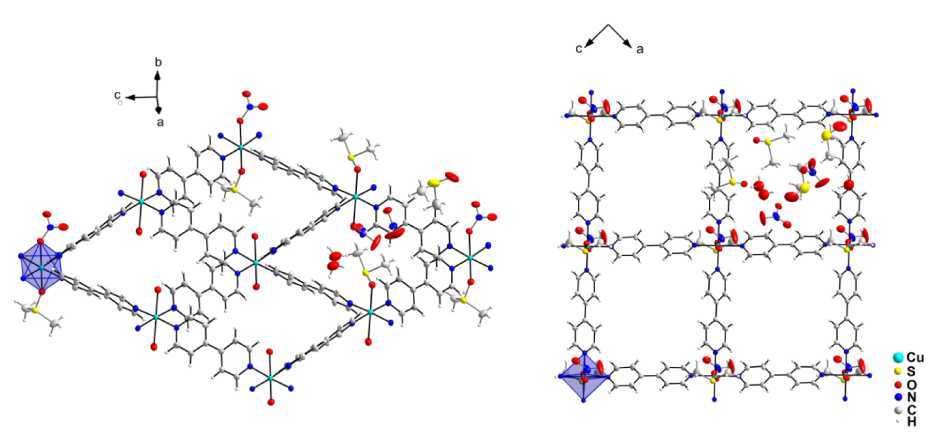
а)
б)
Рис. 1. Строение упаковки одного слоя соединения 1. В трех из четырех ячеек некоординированные с ионом меди частицы опущены для ясности. Для одного иона меди показан его координационный полиэдр;
а, б – вид с разных ракурсов
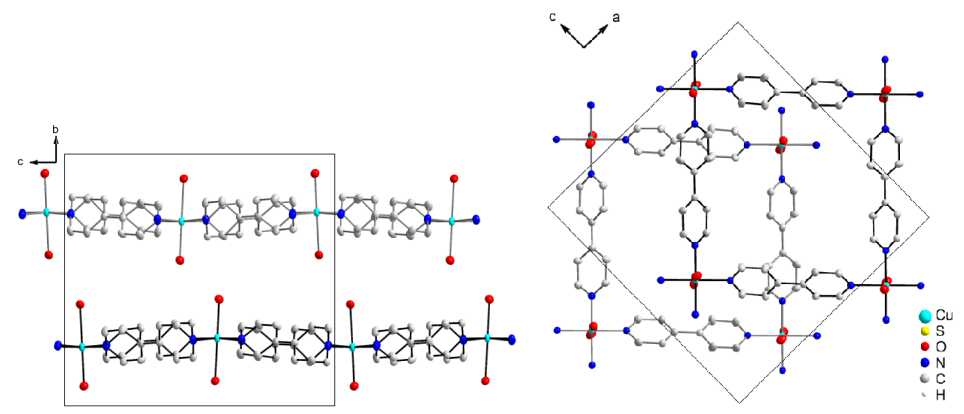
а)
б)
Рис. 2. Строение соединения 1: а, б – относительное расположение соседних слоев
Координация воды с ионом меди может влиять на пористость структуры МОК: например, металл-органический каркас [25] пористый и является эффективным селективным сорбентом, способным обратимо связывать TcO4-/ReO4-; соединение [Cu(4,4’-bipy)2(H2O)2](NO3)2⋅4,5C2H5OH в аксиальных положениях относительно атома меди координируется двумя молекулами воды с образованием трехмерной пористой структуры [26, 27]. При использовании одновалентной меди [28] образуются структуры с каналами прямоугольной формы.
Заключение
Синтезирован металл-органический каркас – нитрат 4,4’-дипиридила меди(II) – сольвотермальным способом. Кристаллическая структура МОК отличается от ранее полученных соединений благодаря координации с ионом меди молекулы ДМСО и образованию слоистой 2D-структуры.
Список литературы Нитрат 4,4’-дипиридил меди(II) - 2D металл-органический каркас
- Derakhshandeh P.G., Abednatanzi S., Leus K. et al. // Cryst. Growth Des. 2019. V. 19, No. 12. P. 7096. DOI: 10.1021/acs.cgd.9b00949.
- Yang D., Liang Z., Tang P. et al. // Adv. Mater. 2022. V. 34, No. 10. P. 2108835. DOI: 10.1002/adma.202108835.
- Saad A., Biswas S., Gksniatsou E. et al. // Chem. Mater. 2021. V. 34, No. 15. P. 5825. DOI: 10.1021/acs.chemmater.1c01034.
- Khan U., Nairan A., Gao J. et al. // Small Structures. 2022. V. 4, No. 6. P. 2200109. DOI: 10.1002/sstr.202200109.
- Wang M., Dong R., Feng X. // Chem. Soc. Rev. 2021. V. 50. P. 2764. DOI: 10.1039/D0CS01160F.
- Zheng Y., Sun F., Han X. et al. // Adv. Opt. Mater.. 2020. V. 8, No. 13. P. 2000110. DOI: 0.1002/adom.202000110.
- Chen G., Gee L.B., Xu W. et al. // J. Am. Chem. Soc. 2020. V. 142, No. 51. P. 21243. DOI: 10.1021/jacs.0c09379.
- Zou R.Q., Sakuari H., Xu Q. // Angew. Chem. 2022. V. 118, No. 48. P. 8264. DOI: 10.1002/ange.200690169.
- Gomez-Lor B., Gutierrez-Puebla E., Iglesias M. et al. // Chem. Mater. 2005. V. 17, No. 10. P. 2568. DOI: 10.1021/cm047748r.
- Nagarkar S.S., Unni S.M., Sharma A. et al. // Angew. Chem. Int. Ed. 2013. V. 53, No. 10. P. 2638. DOI: 10.1002/anie.201309077.
- Cui X., Chen K., Xing H. et al. // Science. 2016. V. 353, No. 6295. P. 141. DOI: 10.1126/science.aaf2458.
- Bao Z., Chang G., Xing H. et al. // Energy Environ. Sci. 2016. V. 9, No. 12. P. 3612. DOI: 10.1039/C6EE01886F.
- Shneemann A., Bon V., Schwedler I. et al. // Chem. Soc. Rev. 2014. V. 43. P. 6062. DOI: 10.1039/C4CS00101J.
- Farrusseng D., Aguado S., Pinel C. // Angew. Chem. Int. Ed. 2009. V. 48, No. 41. P. 7502. DOI: 10.1002/anie.200806063.
- Gedrich K., Heitbaum M., Notzon A. et al. // Chem. Eur. J. 2011. V. 17, No. 7. P. 2099. DOI: 10.1002/chem.201002568.
- Luz I., Labres i Xamena F. et al. // Catal. 2010. V. 276, No. 1. P. 134. DOI: https://doi.org/10.1016/j.jcat.2010.09.010.
- Noro S.I., Kitaura R., Kondo M. et al. // J. Am. Chem. Soc. 2002. V. 124, No. 11. P. 2568. DOI: 10.1021/ja0113192.
- Handy J.V., Ayala G., Pike R.D. // Inorg. Chim. Acta. 2017. V. 456. P. 64. DOI: 10.1016/j.ica.2016.11.013.
- Lazarenko V.A., Dorovatovskii P.V., Zubavichus Y.V. et al. // Crystals. 2017. V. 7, No. 11. P. 325. DOI: 10.3390/cryst7110325.
- Svetogorov R.D., Dorovatovskii P.V., Lazarenko V.A. // Cryst. Res. Technol. 2020. V. 55, No. 5. P. 1900184. DOI: 10.1002/crat.201900184.
- Kabsch W. // Acta Crystallogr., Sect. D: Biol. Crystallogr. 2010. V. 66, No. 2. P. 125.
- Sheldrick G.M. // SHELXT–Integrated space-group and crystal-structure determination. Acta Crystallographica Section A: Foundations and Advances. 2015. V. 71, No. 1. P. 3.
- Dolomanov O.V., Bourhis L.J., Gildea R.J. et al. // J. App. Crystallogr. 2009. V. 42. P. 339. DOI: 10.1107/S0021889808042726.
- Rubio-Martinez M., Imaz I., Domingo N. et al. // Adv. Mater. 2016. V. 28, No. 37. P. 8150. DOI: 10.1002/adma.201506462.
- Mei L., Li F., Lan J. et al. // Nat. Commun. 2019. V. 10, No. 1. DOI: 10.1038/s41467-019-09504-3.
- Yutkin M.P., Zavakhina M.S., Samsonenko D.G. et al. // J. Struct. Chem. 2011. V. 52, No. 2. P. 365. DOI: 10.1134/s002247661102017x.
- Lin X.C., Yin H., Lin Y. // Acta Crystallogr. Sect. E: Struct. Rep. Online. 2007. V. 63, No. 5. P. 1467. DOI: 10.1107/S1600536807019551.
- Yaghi O.M., Li H. // J. Am. Chem. Soc. 1995. V. 117, No. 41. P. 10401. DOI: 10.1021/ja00146a033.


