Низкочастотная индуктивная диэлькометрия - информативный метод для изучения структурирования воды в водных растворах
Автор: Галль Лидия Николаевна, Максимов С.И., Скуридина Т.С., Галль Н.Р.
Журнал: Научное приборостроение @nauchnoe-priborostroenie
Рубрика: Приборостроение физико-химической биологии
Статья в выпуске: 1 т.26, 2016 года.
Бесплатный доступ
Рассмотрена возможность изучения внутренней структуры воды по зависимости тангенса диэлектрических потерь от частоты с использованием метода низкочастотной индуктивной диэлькометрии. Экспериментальная установка для проведения измерений в диапазоне частот 40-800 кГц построена на основе стандартного куметра, модернизированного путем разработки набора специализированных катушек индуктивности. Возможности метода и экспериментальной установки продемонстрированы на примере исследования воды в водных растворах электролитов и биологически активных веществ различных концентраций, меняющихся в широких пределах. Показано, что бидистиллированная вода характеризуется падающей частотной зависимостью тангенса диэлектрической проницаемости, причем для обеспечения хорошей воспроизводимости требуется использование свежих растворов. Растворы солей щелочных металлов демонстрируют наличие сильной и немонотонной дисперсии тангенса диэлектрических потерь в интервале концентраций 10-4- 10-6 М, приводящей к формированию линейчатых спектров, причем внутри этого интервала характер кривых существенно меняется с концентраций. При концентрациях ниже 10-6 М растворы всех солей демонстрируют поведение, близкое к бидистилляту. Наоборот, растворы биоактивных молекул, таких как фенозан калия, сохраняют практические одинаковые спектры дисперсии в очень широком диапазоне концентраций от 10-5 до 10-16 М. Предложено интерпретировать измеряемую низкочастотную область спектра тангенса диэлектрических потерь как следствие внутренней структуры воды, возникающей в контакте с ионами и органическими молекулами.
Структурирование воды, электролиты, радиоспектрометрия, диэлькометрия
Короткий адрес: https://sciup.org/14265005
IDR: 14265005 | УДК: 546.212;
Low frequency inductive dielcometry - informative method for the study of the structuring of water in aqueous solutions
Possibility to study inner water structure using frequency dependence of dielectric loss tangent by low-frequency inductive dielcometry has been considered. Experimental setup at the range 40-800 kHz was based on a standard Q-meter with specialized inductance coils. Features of the method and setup have been demonstrated using bi-distilled water, and solutions of non-organic electrolytes and biologically active molecules with concentrations varied in a wide range. It has been shown that bi-distillate water presents decreased frequency dependences of dielectric loss tangent; one should use fresh samples to provide good reproducibility. LiNO3 solutions shows strong and non-monotonic dispersion of dielectric loss tangent for the concentration range of 10-4-10-6 M; this results in formation of discrete spectra, strongly variable with concentration within the range. At a concentration -6 M, lithium salts present curves similar to those for bi-distilate. On the contrary, bio-active molecular solutions, like potassium phenozan, show nearly similar dispersion spectra for a very wide concentration range at least from 10-5 to 10-16 M. We propose to interpret the low frequency range of the dielectric loss tangent spectrum as a result of inner water structure originated in contact with the ions and organic molecules.
Текст научной статьи Низкочастотная индуктивная диэлькометрия - информативный метод для изучения структурирования воды в водных растворах
На современном уровне развития науки особенно востребованными оказываются методы, позволяющие получать информацию о надмолекулярной, наноразмерной структуре вещества. Особое значение имеют возможности осуществления такой диагностики в отношении жидкой фазы, где субмолекулярные ассоциаты являются неустойчивыми, а современные методы электронной микроскопии — неэффективными. При этом именно надмолекулярные объекты в воде и водных растворах ответственны за характер процессов, протекающих в живых системах, и есть все основания полагать, что многие процессы в неживых системах также определяются наноразмерной структурой растворителя. В настоящее время объем знаний о таких структурах в биологических жидкостях, да и в неорганических системах, весьма мал. Это, безусловно, связано не только с невероятной сложностью процессов, протекающих в жидкостях, но и с отсутствием экспериментальных методов, позволяющих надежно интерпретировать внутреннюю структуру жидкостей и растворов. До настоящего времени не существует общепри- знанных универсальных экспериментальных способов определения состава, структуры и концентраций ассоциатов и комплексов, возникающих в водных растворах. Для получения такой информации обычно используются традиционные физические методы молекулярных исследований, в которых интерпретируются те или иные минорные характеристики метода, а именно уширение и тонкие сдвиги линий в ИК-спектроскопии, уширение рефлексов в дифракционных методах и т. д. Наиболее информативным методом до последнего времени оставалась ИК-спектроскопия, с использованием которой были получены уникальные результаты, демонстрирующие образование структур в растворах [1]. С развитием новых возможностей лазерной техники ее методы также стали активно привлекаться к исследованию водных растворов. Так, метод лазерного светорассеяния позволил не только визуализировать образование ассоциатов в водных растворах, но и определить их распределение по размерам в предположении об их простейших геометрических формах [2].
Экспериментальные исследования последних двадцати лет принципиально поколебали принятую в традиционной химии концепцию бесконеч- но разбавленных растворов, согласно которой при разбавлении растворы достаточно быстро приобретают свойства чистых растворителей. В экспериментах с растворами целого ряда органических и биоорганических молекул в [1] и в [2] было показано, что многие биоактивные вещества в водных растворах ведут себя "неклассическим" образом, т. е. образуют с растворителем-водой структуры (ассоциаты) достаточно больших размеров, в десятки и даже сотни нанометров. Они были названы А.И. Коноваловым наноассоциатами [2], и выявляются вплоть до очень высоких степеней разбавления. Наноассоциаты, образующиеся вокруг "неклассических" молекул, имеют широкое распределение по размерам, немонотонно изменяющееся со степенью разбавления, и метод динамического лазерного светорассеяния позволяет оценить их средний размер как 200–400 нм. Однако этот метод не дает информации об энергиях, необходимых для образования структур и их поддержания, а, кроме того, структуры меньших размеров им уже не визуализируются.
В связи с этим представляется весьма полезным развитие и совершенствование еще одного физического метода, дающего косвенную, но весьма надежную информацию о наличии надмолекулярных структур в воде, а именно метода низкочастотной индуктивной диэлькометрии (L-диэль-кометрии), развитого в 80-х годах в МГУ школой В.Ф. Киселева [3] и усовершенствованного Л.П. Семихиной [4]. Этот метод, основанный на измерении спектральных зависимостей диэлектрических потерь от частоты электромагнитного поля в низкочастотном, недоступном другим методам диапазоне, позволяет наблюдать результаты структурообразования воды, находящейся в контакте с инициатором этого процесса (ионом, молекулой, поверхностью твердого тела ("стенки") и т. д.), и может дать обширную информацию об энергетических характеристиках водных ассоциатов.
ОПИСАНИЕ МЕТОДА L-ДИЭЛЬКОМЕТРИИ
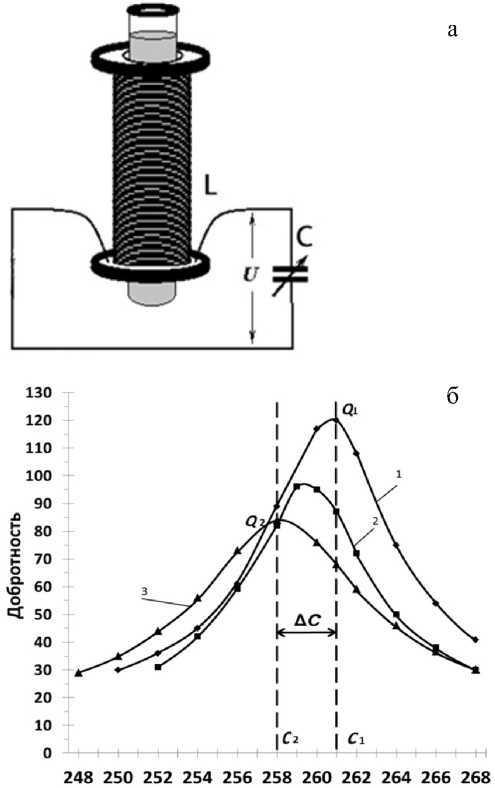
Метод L-диэлькометрии — это метод, в котором диэлектрические жидкости помещаются в слабое вихревое электрическое поле соленоидальной катушки индуктивности (L-ячейки), входящей в последовательный колебательный LC-контур измерителя добротности (куметра), вторым элементом которого является образцовый конденсатор переменной емкости, обеспечивающий настройку контура в резонанс на частоте питающего напряжения. В свою очередь, катушка индуктивности выполняется в виде соленоида с отверстием по оси, в который
(рис. 1, а) вставляется стеклянная пробирка с исследуемым раствором (пробой) [4].
Емкость, пФ
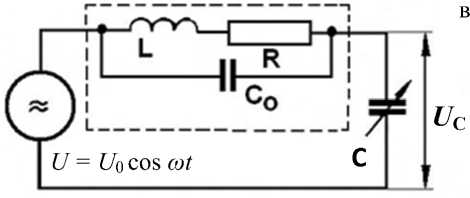
Рис. 1. Схема и основные характеристики экспериментальной установки.
а — упрощенная конфигурация куметра с измерительной L-ячейкой и введенной в нее пробиркой с жидкостью; б — резонансные кривые колебательного контура куметра с L-ячейкой на частоте 100 кГц без пробы (1), после внесения пробирки с бидистиллятом (2), после внесения пробирки с раствором LiNO 3 в концентрации 1·10–5 М (3); в — эквивалентная схема измерений
Суть метода демонстрирует рис. 1, б, согласно которому ввод сосуда с жидкостью внутрь L-ячейки, подключенной к колебательному контуру куметра, приводит к уменьшению добротности Q и емкости С контура при резонансе, что свидетельствует об изменении как активного, так и реактивного сопротивления ячейки.
Как показано в [4], при достаточно больших величинах добротности Q > 20 смещение резонансной емкости определяется только изменением реактивных параметров ячейки, и изменение реактивной части диэлектрической константы прямо пропорционально величине Δ С . Активная часть диэлектрической константы может быть вычислена из изменения добротности катушки. С целью избежать проблем абсолютной калибровки измерений в [4] предложено использовать величину тангенса угла диэлектрических потерь, представляющего собой отношение активной части диэлектрической константы для раствора, помещенного в катушку индуктивности, к ее реактивной части, tg 5 = е "/ е '. Для любой из катушек индуктивности в интервале частот, в котором для нее может наблюдаться резонанс, эта величина может быть найдена по формуле
С Q f 1 ( 1 + C о / C ) 2 - C 2 Q f 2 ( 1 + С о / C 2 ) 2 ( C - C 2 ) Q f 1 Q f 2 ( 1 + C 0/ C )( 1 + C 0/ C 2 )
, (1)
где Qf1 И C1 — добротность контура без пробы и емкость подстроечного конденсатора в момент резонанса, а Qf2 и C2 — те же параметры контура в резонансе при наличии пробы. Поскольку собственная емкость катушек составляет несколько пФ (см. таблицу), а емкость подстроечного конденсатора лежит в интервале 40–450 пФ, для расчета tgδ можно использовать упрощенную формулу tgδ = (Q1C1 – Q2C2)/(Q1Q2 (C1 – C2)). (2)
При величинах Q ≥ 20 и имеющихся значениях C 0 ошибка в определении tg δ , вычисляемого по формуле (2), не превышает 1 % по сравнению с ее величиной, вычисляемой по формуле (1).
РАЗРАБОТКА ЭКСПЕРИМЕНТАЛЬНОЙ УСТАНОВКИ
Поскольку с каждой измерительной катушкой условие резонанса фиксируется лишь в относительно узком диапазоне частот порядка нескольких десятков или сотен килогерц, для измерения частотных зависимостей tg δ и ε L растворов в рабочем диапазоне 40–800 кГц необходим комплект измерительных катушек индуктивности одинакового геометрического размера со значениями индуктивности, обеспечивающими перекрывание их частотных диапазонов. Катушки наматывались медной проволокой на диэлектрический каркас из материала с минимальной величиной собственной диэлектрической проницаемости ε к . В качестве материала каркаса был использован фторопласт-4, для которого ε к близка к 2 практически во всем диапазоне изменения частотного диапазона измерений (40–800 кГц) [5]. Как показали тестовые измерения, это позволило практически полностью устранить собственные артефакты катушек. Диаметр каркаса 30 мм, его длина 200 мм для всех катушек. Для таких размеров, как было показано в [4], реализуется наилучший по интенсивности сигнала режим измерения Q и С , необходимых для расчета величины tg δ . Внутренний диаметр отверстия в каркасе 26 мм, что позволяет использовать для исследования растворов стандартные пробирки, плотно фиксированные в катушке. Поскольку точность измерений, основанная на изменении как активной, так и реактивной составляющих импеданса катушки, напрямую зависит от ее паразитных параметров — сопротивления R и собственной емкости C 0 , — они при изготовлении катушек минимизировались при одновременной максимизации индуктивности L .
Параметры катушек, изготовленных для комплекса изучения структурирования воды, представлены в таблице.
Параметры катушек индуктивности
|
Параметры |
Номер катушки |
|||
|
1 |
2 |
3 |
4 |
|
|
Число витков, n |
3450 |
1585 |
1110 |
580 |
|
Число слоев |
23 |
11 |
7 |
3 |
|
Сопротивление R , Ом |
36.6 |
25.7 |
14.1 |
5.1 |
|
Индуктивность L , мГн |
51 |
32 |
9.6 |
1.03 |
|
Собственная емкость C 0 , пФ |
16 |
8.5 |
7.8 |
6 |
|
Частотные пределы, кГц |
31–106 |
43–155 |
77–270 |
240–810 |
Если зависимость tg δ измеряется в большом частотном диапазоне и для этого требуется использовать более одной катушки, то на границе диапазона несколько экспериментальных точек определяются на двух катушках для корректного сшивания данных. Во всех случаях разница в экспериментальных данных для соседних катушек не превышает 5 %.
ПРИМЕРЫ ЭКСПЕРИМЕНТАЛЬНЫХ ИЗМЕРЕНИЙ И ИХ ОБСУЖДЕНИЕ
Условия и материалы экспериментов
Для определения возможностей метода и реализующей его экспериментальной установки при исследовании процессов структурирования воды в водных растворах веществ с различными свойствами были проведены измерения tg δ для чистой бидистиллированной воды в стеклянных пробирках, растворов электролитов — солей LiNO 3 , NaCl, KCl и CsCl, — растворов двух биологически активных веществ — трипептида глутатиона и фенозана калия. Измерения проводились в диапазоне частот от 45 до 800 кГц при изменении концентраций растворенных веществ в диапазоне от 10–2 до 10–16 М. Во всех случаях дисперсия tg δ в диапазоне измерений по частоте, а также при изменении концентраций растворов представляла собой хорошо воспроизводимые спектральные характеристики, позволяющие наблюдать процессы структурирования в растворах исследуемых веществ, в том числе и изменение этих структур во времени.
Бидистиллированная вода в стеклянной пробирке
Для бидистиллированной воды зависимость tg δ от частоты f в диапазоне измерений от 45 до 800 кГц не демонстрирует структурных пиков и в логарифмическом масштабе представляет собой гладкую кривую, близкую к экспоненте. Типичная кривая, полученная для "свежего" бидистиллята, представлена на рис. 2 (кривая 1). На рисунке представлена также типичная зависимость tg δ ( f ) для бидистиллята, постоявшего 3 дня в стеклянной бутыли с притертой пробкой (кривая 2), а кривая 3 — зависимость для "свежего" бидистиллята в пробирке, имеющей не наблюдаемый глазом дефект поверхности (дефект при изготовлении). В обоих последних случаях на зависимости tg δ ( f ) наблюдаются структурные пики, причем на дефектных пробирках характерные для данной пробирки пики проявляются сразу же и всегда однозначно воспроизводятся. При хранении бидистиллята в стеклянной таре уже на второй день на за-
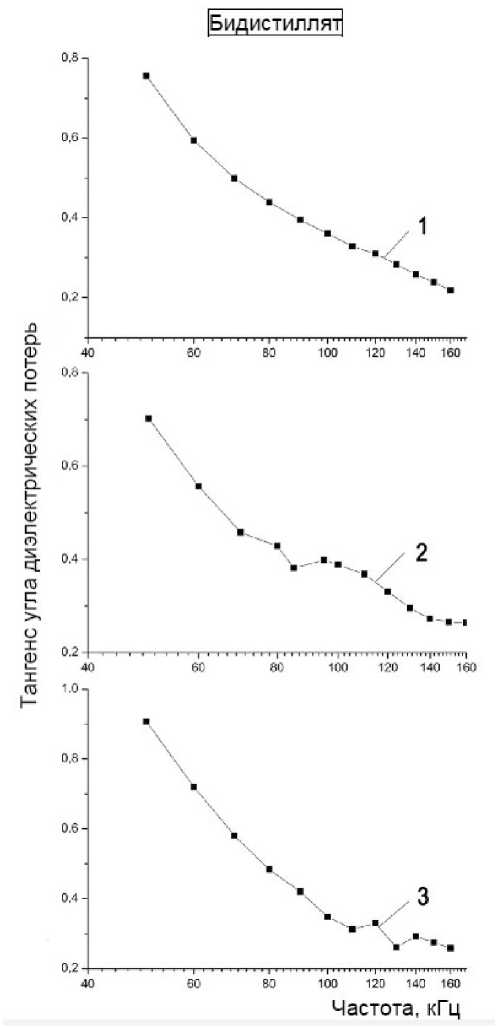
Рис. 2 . Типичные зависимости tg δ как функции частоты f для бидистиллированной воды (логарифмический масштаб):
1 — свежеприготовленный бидистиллят; 2 — бидистиллят, хранившийся в стеклянной таре; 3 — свежеприготовленный бидистиллят в "дефектной" пробирке
висимости tg δ ( f ) появляются слабые выпуклости, которые далее преобразуются во вполне четкие, хоть и очень широкие, пики. По-видимому, их можно связать с выщелачиванием катионов металлов из окислов, образующих массу легкоплав-
ких стекол стандартной химической посуды. Приведенные данные показывают, что для получения надежных результатов в диэлькометрических измерениях все коммерческие пробирки должны быть тщательно промерены с использованием свежего бидистиллята и "дефектные" отбракованы.
Отметим, что воспроизводимость кривых, представленных на рис. 2, очень хорошая: так положения максимумов на "дефектных" кривых воспроизводятся с точностью порядка 2–3 кГц, а кривые для свежеприготовленного бидистиллята ложатся одна на другую с точностью порядка 5–6 %. Это позволяет использовать свежеприготовленный бидистиллят как стандартный образец для калибровки прибора и оценки роли наводок за счет работающих поблизости радиоэлектронных устройств.
Растворы солей щелочных металлов
Известно, что кинетические свойства водных растворов электролитов во многом зависят от взаимодействия продуктов диссоциации солей — катионов и анионов — с молекулами воды раствора. Уже более 60 лет тому назад было показано [6], что в то время как ряд ионов уменьшает подвижность ближайших к ним молекул воды, около некоторых ионов молекулы воды, наоборот, становятся более подвижными, чем в чистой воде. Это явление было названо соответственно положительной и отрицательной гидратацией. Особенности гидратации характеризуются координационным числом иона, под которым понимается
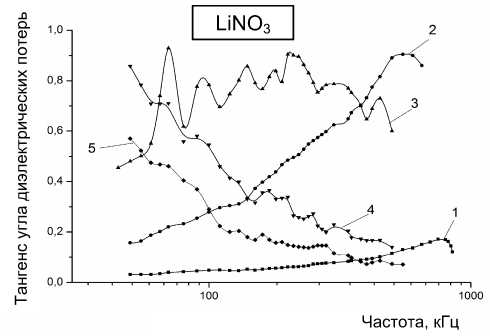
Рис. 3 . Зависимость tg δ от частоты для водных растворов LiNO3 разных концентраций.
Концентрация раствора (М): 1 — 2·10–2; 2 — 1·10–3; 3 — 2·10–4; 4 — 2·10–5; 5 — 1·10–6
среднее число постоянно сменяющихся молекул воды, составляющих в растворе его непосредственное окружение. Для изучения гидратации ионов металлов и координационных чисел ионов в химии традиционно использовался термохимический метод, основанный на измерении интегральной теплоты растворения солей в воде и в водных растворах кислот ряда концентраций. Этим методом было показано, что в ряду щелочных металлов ионы Li+ и Na+ обладают положительной гидратацией, в то время как ионы K+, Rb+, Cs+ и большинство анионов — отрицательной. Эта точка зрения в настоящее время доказана множеством экспериментов с применением весьма совершенных современных методов [7]. Считая, что ионы переориентируют только ближайшие к ним молекулы воды, основатель этих исследований О.Я. Самойлов утверждал, что "состояние исследованных ионов в разбавленных растворах в смысле окружения молекулами воды соответствует наименьшему возможному изменению структуры воды при образовании раствора". Однако термохимический метод позволяет исследовать растворы до концентраций не ниже чем 10–3 М, и указанное заключение по существу относится соответственно только к достаточно высоким концентрациям растворов электролитов [6].
На рис. 3 представлены спектральные зависимости tg δ ( f ) для водного раствора соли LiNO 3 в диапазоне концентраций от 10–2 до 10–6 М при комнатной температуре. Из рисунка видно, что уже при концентрации 2·10–4 М кривая перестает носить монотонный характер и приобретает вид линейчатого спектра, характер которого сохраняется при уменьшении концентрации вплоть до 10–6 М. Наблюдаемые пики расположены в широком интервале частот от ~40 до ~700 кГц, что позволяет предположить достаточно большой набор различных взаимодействий с водой, обусловленных наличием катионов и анионов в растворе. При более высоких разбавлениях кривые сглаживаются, и характер частотной зависимости начинает приближаться к распределению, характерному для бидистиллята. При концентрациях, близких к 10–7 М, вклад структур, создаваемых ионами, этим методом практически уже не измеряется.
Отметим, что положения всех пиков на кривых хорошо, с точностью порядка 2–3 кГц, воспроизводятся от эксперимента к эксперименту. В то же время относительные амплитуды пиков воспроизводятся хуже, и их разброс может достигать 40– 50 %. На наш взгляд, это отражает сложные с физической точки зрения процессы структурирования воды, видимо, сильно зависящие от трудно контролируемых внешних условий.
Аналогичные кривые, хотя и различающиеся многими экспериментальными деталями, получе- ны и для других щелочных металлов: Na, K и Cs. Во всех случаях при концентрациях ниже 10–6 М измеренные кривые близки к таковыми для бидистиллята, причем для каждого металла имеется своя область концентраций, где наблюдаются выраженные линейчатые спектры и своя концентрационная граница.
Растворы биоактивных молекул
Водные растворы биоактивных молекул в отличие от ионов электролитов при диэлькометри-ческих измерениях демонстрируют способность к структурированию воды в широком диапазоне концентраций, что полностью совпадает с результатами, полученными в экспериментах А.И. Коновалова [2].
На рис. 4 представлены распределения tg δ ( f ) для водного раствора фенозана калия для трех концентраций: 1·10-4, 1·10–6 и 1·10–16 М, выдержанных сутки после разведения. Структурная формула фенозана калия, представленная на рис. 4, показывает присутствие в молекуле двух гидрофильных центров, образованных протоном и калием, что предполагает возможность роста объемных протяженных водных структур. Как видно из рисунка, фенозан калия образует достаточно много различных водных структур, причем количество структурных пиков измеряемой интенсивности мало изменяется при разведении, а положение основных пиков на шкале частот практически не меняется при уменьшении концентрации растворенного фенозана калия. Эти результаты вполне укладываются в модель, предложенную нами в [8].
Метод низкочастотной индуктивной диэлько-метрии позволяет не только фиксировать изменения структур воды, образующихся на биологически активных молекулах, но и наблюдать некоторые химические процессы, происходящие с молекулами, в частности, окисление их гидрофильных групп. На рис. 5 представлено изменение распределения tg δ ( f ) со временем для глутатиона — одной из главных тиолсодержащих молекул живого организма. Рисунок показывает, что структурирование воды гидрофильной тиоловой группой глутатиона, находящегося в водном растворе, через 3 дня практически полностью прекращается, что наблюдается по исчезновению структурных пиков на частотной зависимости tg δ ( f ) и подтверждается изменением его химической активности.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Приведенные выше экспериментальные данные свидетельствуют, что сложные линейчатые спектральные зависимости, получаемые в L-ячейке, отражают реальные физические процессы в вод-
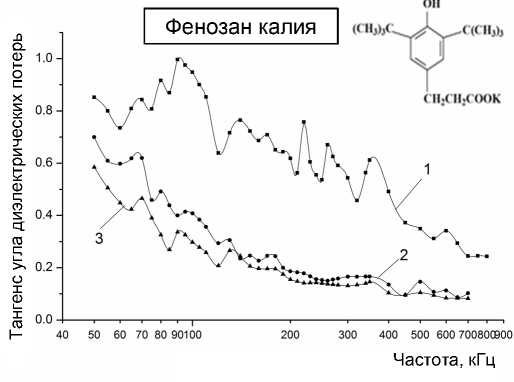
Рис. 4 Зависимость tg δ от частоты для водного раствора фенозана калия.
Концентрация раствора (М): 1 — 1·10–4; 2 — 1·10–6;
3 — 1·10–16
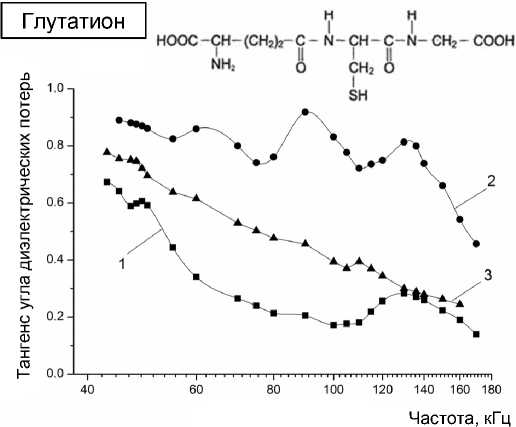
Рис. 5 . Зависимость tg δ ( f ) для водного раствора глутатиона с концентрацией 1·10–4 M от времени.
1 — свежеразведенный раствор; 2 — тот же раствор через сутки после разведения; 3 — тот же раствор через неделю после разведения ном растворе и являются их индикаторами. Сам факт немонотонных частотных зависимостей тангенса диэлектрических потерь в области частот в десятки и сотни килогерц является совершенно нетривиальным и требует развития физических моделей для объяснения наблюдаемого спектрального эффекта.
Интерпретация этого эффекта требует одновременной разработки как количественных теоре- тических представлений о структуризации молекул воды растворенными ионами и молекулами, так и корректного теоретического описания радиотехнической схемы используемой экспериментальной ячейки. На сегодняшний день теория такой ячейки отсутствует, и ее разработка остается сложной научной задачей, выходящей за пределы этой статьи. Что же касается структурирования воды, то такая модель была нами предложена [8], и факт немонотонности частотной зависимости tgδ с формированием выраженных пиков, специфичных по отношению к растворенному веществу и его концентрации, может рассматриваться как одно из ее подтверждений.
ЗАКЛЮЧЕНИЕ
Комплекс экспериментальных исследований структур воды, образующихся в водных растворах как неорганических молекул электролитов, так и молекул, обладающих высокой биологической активностью, показал, что путем правильной реализации параметров катушек в колебательном контуре куметра, исключающей вклад их артефактов, метод низкочастотной индуктивной диэлько-метрии становится эффективным новым методом для изучения явления структурирования воды. В такой реализации метод позволяет наблюдать и фиксировать реактивные и активные потери в растворе как проявление образующихся водных структур, на основании которых могут быть изучены и верифицированы модели процессов структурирования, в том числе и для живых систем.
Авторы приносят свою глубокую благодарность вед. инженеру В.А. Ледневу за изготовление катушек индуктивности и инженеру И.Р. Галлю за активное участие в проведении измерений.
Список литературы Низкочастотная индуктивная диэлькометрия - информативный метод для изучения структурирования воды в водных растворах
- Жуковский А.П., Ровнов Н.В., Жуковский М.А. Сравнительное исследование структуры микрорасслаивающихся растворов вода-диоксан и вода-диметилсульфоксид//ЖСХ. 1993. Т. 34, № 4. С. 83-88.
- Коновалов А.И. Образование наноразмерных молекулярных ансамблей в высокоразбавленных водных растворах//Вестник РАН. 2013. Т. 83, № 12. С. 1076-1082. Doi: DOI: 10.7868/S0869587313120050
- Киселев В.Ф., Салецкий А.М., Семихина Л.П. О влиянии слабых магнитных полей и СВЧ-излучения на некоторые диэлектрические и оптические свойства воды и водных растворов//Теор. и эксп. химия. 1988. № 3. С. 330-334.
- Семихина Л.П. Индуктивный метод определения диэлектрических свойств жидкостей//Научное приборостроение. 2005. Т. 15, № 3. С. 83-87. URL: http://213.170.69.26/mag/2005/full3/Art8.pdf.
- Брацыхин Е.А., Шульгина Э.С. Технология пластических масс: Учебное пособие для техникумов. 3-е изд., перераб. и доп. Л.: Химия, 1982. 121 с.
- Самойлов О.Я. Структура водных растворов электролитов и гидратация ионов. М.: Изд-во АН СССР (Ин-т общей и неорган. химии), 1957. 179 с.
- Лященко А.К., Новскова Т.А. Структурная динамика и спектры ориентационной поляризации воды и других жидкостей//Структурная самоорганизация в растворах и на границе раздела фаз. Под ред. А.Ю. Цивадзе. М.: Изд-во ЛКИ, 2008. С. 417-500 (Глава 7).
- Галль Л.Н., Галль Н.Р. К вопросу о природе аномальных физико-химических свойств сильно разбавленных водных растворов//Доклады РАН. 2015. Т. 461, № 6. С. 673-676. Doi: DOI: 10.7868/S0869565215120142


